白藜芦醇对高糖诱导足细胞损伤的改善作用及机制探讨*
李泽争,王 利,曹爱丽,彭 文
(上海中医药大学附属普陀医院肾内科,上海 200062)
糖尿病肾病(DN)是糖尿病最常见的微血管并发症,亦是导致终末期肾脏衰竭(ESRD)的重要原因[1-2]。足细胞是一种高度分化的细胞类型,在维持肾小球结构、构成肾小球滤过屏障方面发挥着重要作用。有研究证实,足细胞损伤在DN发展过程中意义重大[3-4]。越来越多的研究证明足细胞数量及形态的变化可预测DN的发生发展,抑制足细胞的损伤可能会阻止或减缓DN的疾病进程,但目前为止足细胞损伤的机制仍不明确,亦缺乏有效防治足细胞损伤的干预手段。
白藜芦醇(RSV)是一种植物抗毒素,有研究发现RSV可显著降低蛋白尿,具有明确的肾脏保护功能,此外其在保护足细胞方面也表现出巨大潜力[5],然而活化过程尚未完全明确。本研究采用体外高糖诱导足细胞损伤模型,观察RSV对足细胞损伤的保护作用及涉及的可能分子机制,以期为临床上防治DN提供理论依据。
1 材料与方法
1.1 实验主要材料 FBS、胰酶、RPMI1640培养基(美国Gibco公司);RSV(上海同田生物技术股份有限公司);二甲基亚砜(DMSO)(美国 Sigma公司);AnnexinV-FITC/PI凋亡检测试剂盒(美国BD公司);dihydroethidium(美国 Sigma公司);JC-1、MitoSOX Red(美国 Thermos Fisher Scientific公司);β-actin、含半胱氨酸的天冬氨酸蛋白水解酶(caspase)3、caspase 9(美国 Cell Signaling Technology公司)。RSV溶于DMSO(终浓度≤0.1%)中,配置成储存液,避光,4℃保存。
1.2 方法
1.2.1 足细胞培养 永生化小鼠足细胞株是从H-2Kb-tsA58转基因小鼠肾脏分离后建立的细胞系,由美国Mount Sinai医学院Mundel教授授权,上海交通大学附属第六人民医院汪年松教授转赠,传代数≤15代。
1.2.2 细胞分组及干预方法 1)对照组:5 mmol/L低糖培养液(LG);2)模型组:30 mmol/L 高糖培养液(HG);3)RSV 干预组:①HG+5 μmol/L RSV;②HG+10 μmol/L RSV,RSV提前干预2 h后高糖孵育48 h。
1.2.3 细胞凋亡检测 足细胞接种于6孔板,细胞干预结束后,消化收集细胞,磷酸盐缓冲溶液(PBS)洗2 次,加入 200 μL 1×Binding Buffer混匀,避光加入5 μL Annexin V,室温放置 15 min,加入 PI 5 μL,重悬细胞上流式细胞仪进行检测。
1.2.4 ROS检测 DHE稀释至无血清培养基,终浓度为10 μmol/L。细胞干预结束后,吸弃培养基,PBS洗涤2次,加入稀释的DHE,37℃孵育20 min,PBS洗2次,4%多聚甲醛固定10 min,即刻置荧光显微镜下观察。
1.2.5 JC-1染色 足细胞接种于内置无菌细胞爬片的6孔板,干预后吸弃培养基,PBS洗涤2次,加入 2 μmol/L JC-1,37 ℃孵育 30 min,PBS 洗 2次,4%多聚甲醛固定10 min,封片,置荧光显微镜下观察。
1.2.6 MitoSOX染色 足细胞接种于内置无菌细胞爬片的6孔板,干预后吸弃培养基,PBS洗涤2次,加入稀释的 5 μmol/L MitoSOX,37 ℃孵育 10 min,PBS洗2次,4%多聚甲醛固定10 min,封片,置荧光显微镜下观察。
1.2.7 Western blot检测 细胞干预结束后加入蛋白裂解液(含蛋白酶抑制剂)充分裂解,高速低温离心留取上清,提取蛋白并检测含量,取等量蛋白样品进行SDS-PAGE凝胶电泳,转膜,室温摇床封闭1 h,依次加入一抗(β-actin、caspase 3、caspase 9),4℃过夜,加入辣根过氧化物酶标记的二抗室温摇床1 h,在Image QuantLAS 500成像系统中进行显影。以β-actin的蛋白表达为内参照,结果以靶蛋白/内参的灰度比值表示,实验重复3次,取平均值。
1.3 统计学分析 采用SPSS 20.0统计分析软件,计量资料以均数±标准差(±s)形式表示,采用单因素方差分析,组间两两比较采用LSD-t检验。P<0.05为差异有统计学意义。
2 结果
2.1 RSV对高糖诱导足细胞的保护作用 流式细胞仪检测结果显示,高糖孵育可显著提高足细胞的早期凋亡与晚期凋亡。与HG组相比,RSV干预后,细胞凋亡出现不同程度的抑制,且随着药物浓度升高,抑制作用逐渐增强,差异均具有统计学意义(P<0.05)。见图 1,表 1。
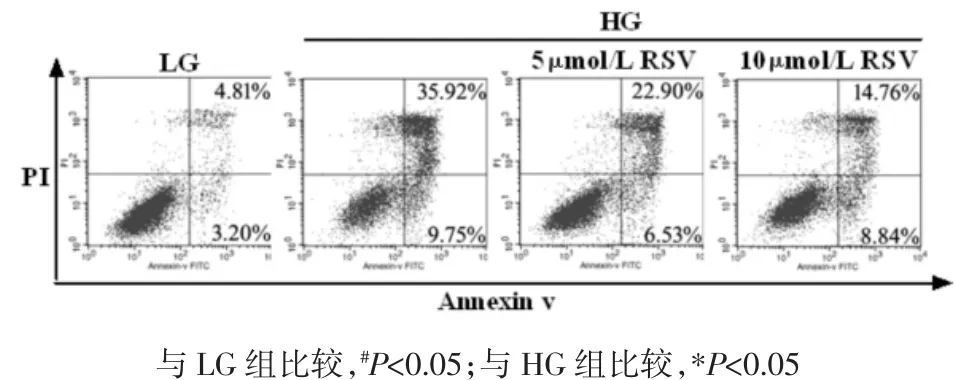
图1 RSV对足细胞凋亡的影响Fig.1 Effect of RSV on podocyte apoptosis
表1 RSV对足细胞凋亡的影响(±s)Tab.1 Effect of RSV on podocyte apoptosis(±s)

表1 RSV对足细胞凋亡的影响(±s)Tab.1 Effect of RSV on podocyte apoptosis(±s)
注:与 LG 组比较,*P<0.05;与 HG 组比较,#P<0.05。
凋亡细胞(%)8.53±1.27 47.00±7.56*28.33±2.08#21.00±3.46#组别LG组HG组HG+5 μmol/L RSV 组HG+10 μmol/L RSV 组
2.2 RSV对细胞内ROS生成的影响 ROS在足细胞损伤中发挥重要作用,本研究采用荧光探针DHE观察足细胞内ROS生成情况。结果显示,与LG组相比,高糖孵育可明显提高细胞内ROS生成,且RSV可剂量依赖性的抑制高糖诱导的ROS表达水平。见图2。
2.3 RSV对线粒体膜电位的影响 线粒体膜电位下降发生在线粒体功能障碍的早期,本研究以JC-1荧光探针检测线粒体膜电位。当线粒体膜电位较高时,JC-1聚集在线粒体基质中,以聚合体形式呈现,产生红色荧光;当线粒体膜电位较低时,JC-1不能聚集在线粒体基质中,以单体形式呈现,产生绿色荧光。激光共聚焦结果显示,RSV干预后,绿色荧光向红色荧光转变增多,提示RSV可有效抑制高糖诱导的线粒体膜电位下降。见图3。
2.4 RSV对线粒体ROS生成的影响 采用线粒体超氧阴离子染料MitoSOX检测线粒体ROS。结果提示高糖可显著提高足细胞线粒体ROS的产生,RSV可剂量依赖性的降低线粒体ROS的表达水平。见图4。
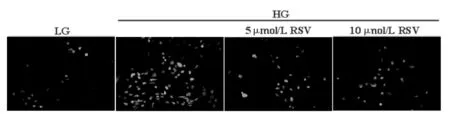
图2 RSV对细胞内ROS生成的影响(倒置荧光显微镜×200)Fig.2 Effect of RSV on the intracellular ROS generation(inverted fluorescence microscope ×200)
2.5 Western blot检测 caspase 3、caspase 9 的表达与 LG组相比,HG组 cleaved caspase 3、cleaved caspase 9表达水平显著上调;随RSV干预浓度的提高,与 HG 组相比,cleaved caspase 3、cleaved caspase 9表达水平逐渐降低,差异具有统计学意义(P<0.05)。见图 5。
3 讨论
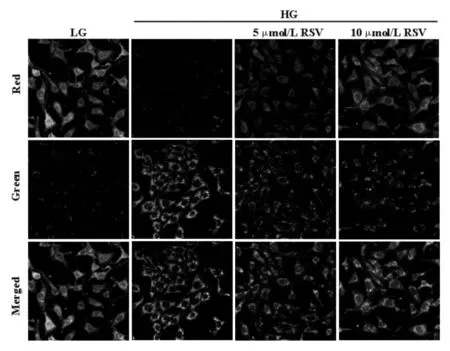
图3 RSV对线粒体膜电位的影响(激光共聚焦×400)Fig.3 Effect of RSV onmitochondrial membrane potential(laser confocal×400)
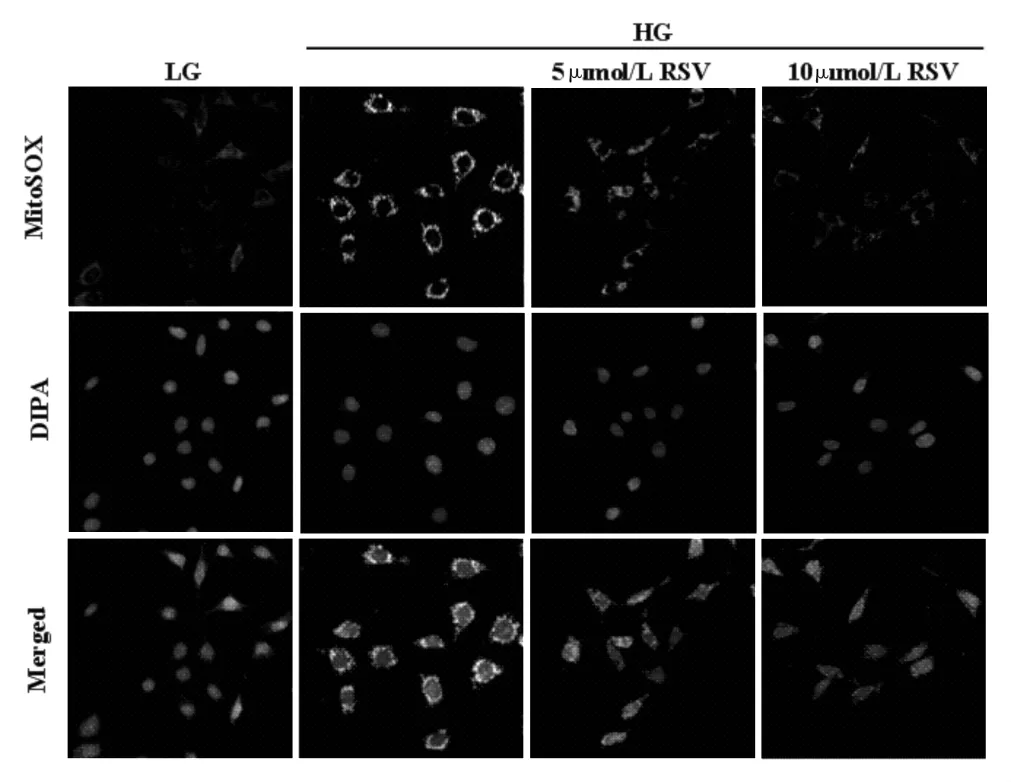
图4 RSV对线粒体ROS的影响(激光共聚焦×400)Fig.4 Effect of RSV onROS generation inmitochondrial(laser confocal×400)
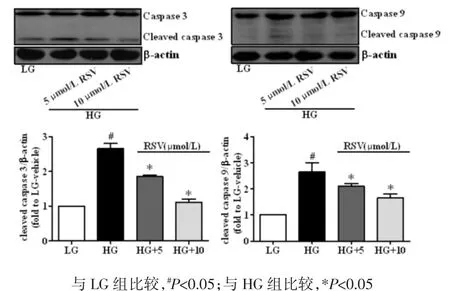
图5 RSV对线粒体凋亡途径相关蛋白的影响Fig.5 Effect of RSV on protein related to mitochondrial apoptosis pathway
DN是一种糖尿病的长期并发症,以蛋白尿和肾小球硬化为病理特征,临床中约40%的Ⅰ型及30%的Ⅱ型糖尿病患者最终会发展为DN。足细胞又称为脏层肾小球上皮细胞,与内皮细胞、肾小球基底膜共同构成肾小球滤过屏障。研究表明,DN早期便伴有足细胞损伤,表现为足细胞密度的降低和数量的减少。由于足细胞增生分化能力有限,凋亡是足细胞丢失的主要原因。至目前为止,引起足细胞凋亡的因素很多,但机制复杂,是当前肾病学科的研究热点。因此,探讨足细胞凋亡机制及有效干预手段对寻求治疗DN具有重大意义。近年来,RSV用于治疗肾脏疾病越来越受到学者们的关注。有研究证实在STZ诱导的Ⅰ型DN中,RSV可显著降低蛋白尿水平,改善肾脏病理损伤[6]。RSV可通过激活SIRT1/PGC-1α途径,改善线粒体功能障碍,从而减轻醛固酮诱导的蛋白尿及足细胞损伤[7]。探讨RSV对足细胞凋亡的保护作用及潜在分子学机制,为DN的防治研究提供了新方向。
本研究采用体外高糖孵育模拟糖尿病体内环境,结果表明RSV可显著抑制高糖诱导的足细胞凋亡,并呈量效关系,这可能是其可降低蛋白尿的机制之一。同时,实验结果显示RSV可显著降低细胞内及线粒体ROS的合成、提高线粒体膜电位、下调cleaved caspase 3及cleaved caspase 9的表达水平,提示RSV对足细胞的保护作用可能是通过抑制氧化应激,改善线粒体功能障碍实现的。
足细胞作为一种终末分化细胞,对ROS异常敏感,高糖刺激时氧化和抗氧化系统的失衡及ROS产生过多是导致足细胞损伤的主要机制之一[8-9]。ROS不仅可以直接损伤足细胞,还可激活NADPH氧化酶产生更多的ROS,从而形成恶性循环[10]。有学者更是提出在糖尿病早期,高糖即可通过ROS启动足细胞凋亡,诱导其从基底膜脱落,降低肾小球内足细胞数量,出现蛋白尿[11]。以上研究均提示氧化应激可能是DN中足细胞损伤的重要机制之一。本研究中,RSV干预可显著降低细胞内ROS生成,改善高糖诱导的细胞凋亡,表现了显著的抗氧化作用。近年来,RSV的抗氧化作用日益成为肾脏病领域的研究热点,研究显示RSV可显著降低糖尿病大鼠肾组织中ROS及MDA水平,减少细胞凋亡[12]。在高糖刺激的系膜细胞中,RSV可激活SIRT1,减少高糖诱导的氧化应激对线粒体的损伤[13]。可见,RSV作为一种具有抗氧化作用的中药单体,在转化为公认抗氧化剂发面具有巨大潜力。
线粒体是真核细胞能量供应的最重要细胞器,通过氧化磷酸化途径产生机体内大部分ATP,同时它也是ROS生成的主要来源,亦是ROS的作用靶点[14-15]。ROS可损伤线粒体的酶类、脂类和核酸,进一步导致ROS合成增加。同时,ROS还可对线粒体DNA产生氧化损伤,导致线粒体ATP合成减少、线粒体膜电位破坏等结构和功能的改变,因此ROS增多也是线粒体功能障碍的表现之一。综上,氧化应激与线粒体功能密切相关,亦有研究显示高糖诱导的氧化应激是由线粒体依赖的通路介导的。本研究发现RSV干预可显著降低足细胞线粒体内ROS的生成,提高线粒体膜电位,改善线粒体功能障碍。线粒体功能障碍可引发内源性的线粒体凋亡途径,首先表现为线粒体膜通透性转换孔道的开放,进一步引起线粒体膜去极化,凋亡前因子如细胞色素c释放入胞浆,进而激活caspase 3、caspase 9等细胞凋亡蛋白。本实验中,RSV可显著降低cleaved caspase 3及cleaved caspase 9的表达水平,改善足细胞凋亡,提示RSV可通过改善线粒体功能障碍抑制内源性的线粒体凋亡途径。综上所述,RSV可通过抑制氧化应激,改善线粒体功能障碍抑制高糖诱导的足细胞凋亡。然而,RSV如何靶向降低ROS的生成、提高线粒体膜定位、抑制线粒体依赖性的凋亡途径,值得更加深入的探索与研究。
研究结果表明RSV呈浓度依赖性的抑制高糖诱导的足细胞凋亡,其保护作用可能与抑制氧化应激,改善线粒体功能障碍相关。以此推测RSV可用于预防足细胞损伤,在DN的防治方面具有广大空间。当然,这一推论还有待于动物实验及临床研究进一步证实。

