新生儿胆红素脑病的相关危险因素及其防治措施分析
金 叶,倪 琼
(1.杭州市红十字会医院,浙江 杭州 310003;2. 浙江大学医学院附属儿童医院(滨江新院区),浙江 杭州 310052)
新生儿胆红素脑病是新生儿黄疸中最为严重的并发症,胆红素可对神经系统产生毒性,引起新生儿的神经功能损伤、听力障碍及智力发育迟缓等[1]。目前,新生儿胆红素脑病的诊断主要依据胆红素水平和临床表现,但胆红素引起的神经系统症状呈进行性发展,采用临床症状评估胆红素脑病的灵敏度偏低[2]。因此,需要筛选胆红素脑病的相关危险因素,以便早期采取预防措施,降低新生儿胆红素脑病的发生率。为此,本研究以80例新生儿胆红素脑病患儿为病例组,同期选择80例无胆红素脑病的新生儿黄疸患儿为对照组,分析可能影响新生儿胆红素脑病的危险因素,现将结果报告如下。
1 资料与方法
1.1 一般资料
选取2015年1月至2017年12月在杭州市红十字会医院、浙江大学附属儿童医院儿科收治的80例胆红素脑病患儿作为病例组,所有患儿均符合新生儿胆红素脑病的诊断标准[3],入院后12h内进行神经系统功能评估,采用胆红素脑病所致神经功能系统障碍评分法(Bind)[4],入院时Bind评分达7~9分即可诊断为急性胆红素脑病;其中男49例,女31例;胎龄32~40周,平均(35.72±3.25)周;剖宫产35例,顺产45例;体重<2500g 17例,体重≥2500g 63例。同期选择80例无胆红素脑病的新生儿黄疸患儿为对照组,其中男47例,女33例;胎龄33~40周,平均(36.39±3.08)周;剖宫产31例,顺产49例;体重<2500g 12例,体重≥2500g 68例。2组患儿的性别、胎龄、分娩方式及出生体重等基础资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法
所有患儿的胆红素值采用JH20-IB来初步测定,再使用胆红素氧化酶法(全自动生化分析仪)来检测患儿的血清总胆红素。收集可能影响新生儿胆红素脑病的相关因素[4-6],具体如下:新生儿性别、胎龄、出生体重、分娩方式、母乳喂养方式、出生后12h内黄疸、新生儿溶血、遗传性葡萄糖-6-磷酸脱氢酶(G6PD)缺乏、窒息缺氧、颅内出血、感染、低蛋白血症、低血糖、代谢性酸中毒、贫血、发热、低体温、总胆红素峰值、神经功能系统障碍评分等。患儿通过早期积极综合治疗(在警告期采用换血、光疗、输注白蛋白等措施)降低胆红素浓度,逐渐恢复至正常;均通过3个月的随访,随访方式为电话随访或门诊复诊随访,无明显后遗症。
1.3 统计学处理
数据分析应用SPSS 13.0,2组间的计数资料比较采用χ2检验,多因素分析则采用二分类非条件Logistic回归法;P<0.05为差异有统计学意义。
2 结果
2.1 影响新生儿胆红素脑病的单因素比较分析
2组患儿12h内黄疸、新生儿溶血、G6PD缺乏、感染、低蛋白血症、代谢性酸中毒、贫血、发热、低体温、总胆红素峰值等因素比较差异有统计学意义(P<0.05)。见表1。
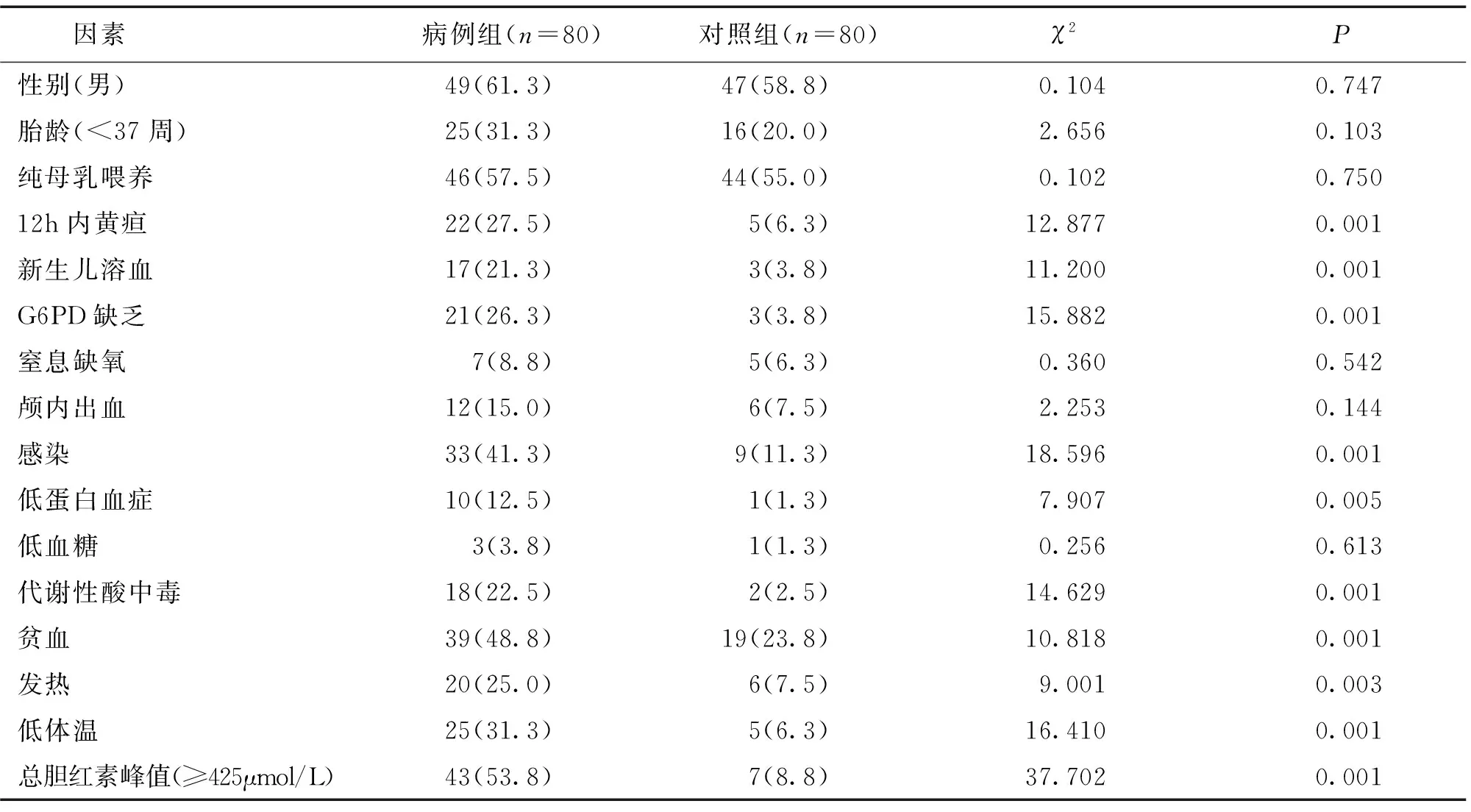
表1 2组患儿的各因素比较分析结果[n(%)]
2.2 影响新生儿胆红素脑病的多因素分析
以新生儿是否发生胆红素黄疸为因变量(对照组=0,病例组=1),将单因素比较分析有统计学意义的10个因素作为自变量纳入多因素非条件Logistic回归模型,模型筛选采用逐步回归法。最后纳入多因素模型且有统计学意义的因素包括总胆红素峰值、感染、新生儿溶血、代谢性酸中毒、12h内黄疸等,均为新生儿胆红素脑病的危险因素。见表2。

表2 影响新生儿胆红素脑病的多因素Logistic回归分析结果
3 讨论
3.1 影响新生儿胆红素脑病的危险因素
本研究显示,总胆红素峰值、感染、新生儿溶血、代谢性酸中毒、12h内黄疸等因素均为新生儿胆红素脑病的危险因素。(1)总胆红素峰值。峰值≥425μmol/L其发生胆红素脑病的风险系数为5.083。该指标可反映新生儿体内胆红素累积速度和水平,脂溶性未结合的胆红素以分子跨膜的方式扩散透过血脑屏障[5],如果胆红素水平累积过快、浓度过高,透过血脑屏障的速度就越快,诱发胆红素脑病的风险就越大;该指标是反映胆红素脑病最直接、最敏感的指标;(2)感染。其发生胆红素脑病的风险系数为4.2。胎儿宫内感染可以引起新生儿病理性黄疸,胎儿在母体内抵抗力较差,若发生严重感染,可引起胎儿代谢性酸中毒,从而产生缺氧,引起胆红素代谢酶活性下降[6];此外,感染可增加新生儿的血脑屏障通透性[7],胆红素容易通过血脑屏障从而导致胆红素脑病的发生;(3)新生儿溶血。其发生胆红素脑病的风险系数为3.452。新生儿溶血主要以ABO溶血、RH溶血为主,是导致新生儿胆红素脑病的关键因素。ABO溶血病临床上缺乏早期筛查手段,部分患者以较轻的黄疸出院,待患儿黄疸症状明显后,病情进展迅速,容易错失最佳治疗时机;(4)代谢性酸中毒。其发生胆红素脑病的风险系数为3.028。宫内窘迫、围产期窒息等均可引起胎儿代谢性酸中毒,围产期若发生代谢性酸中毒,可引起新生儿体内缺血缺氧性脑病,新生儿肝脏缺氧可导致其胆红素代谢能力下降[8],从而诱发新生儿黄疸甚至胆红素脑病;(5)12h内黄疸。其发生胆红素脑病的风险系数为2.465。12h内出现黄疸的新生儿多见于G6PD缺乏症、新生儿溶血病患儿,由于红细胞膜稳定性下降,红细胞受到破坏后引起血液中的胆红素增多,以未结合的胆红素增高为主,容易通过血脑屏障从而导致胆红素脑病[9]。
3.2 新生儿胆红素脑病的预防措施
(1)加强产前疾病筛查。包括G6PD缺乏症、母子RH血型、ABO血型不合等,对于一些抗体活性较强容易引起ABO溶血者,在孕期通过药物来控制抗体活性,具有较好的预防效果[9];(2)将宫内感染和新生儿感染作为围产期筛选的指标。定期进行产前检查,做到早发现、早评估、早治疗宫内感染,预防母婴垂直传播性疾病;产后及早发现新生儿感染,并进行治疗,减少感染引起血脑屏障通透性增加;(3)预防代谢性酸中毒,降低缺血缺氧性脑病。应通过综合疗法,如控制酸中毒、脑水肿、惊厥,对有酸中毒的新生儿进行亚低温治疗,保证稳定的脑血流灌注,预防新生儿缺血缺氧性脑病发生;(4)对于有黄疸的新生儿,定期监测总血清胆红素平均水平和峰值。对有黄疸的新生儿进行综合评估,分析引起新生儿黄疸的原因,对于有其他高危因素的患儿应进行总胆红素峰值监测,对于峰值偏高的患儿尽早采取措施降低胆红素水平,减少高胆红素通过血脑屏障损伤中枢神经系统;(5)对于有高危因素的黄疸患儿应尽早进行药物治疗或光疗。药物治疗包括苯巴比妥、微生态制剂、口服葡萄糖等,对于血清总胆红素水平超过256μmol/L的患儿,建议采用蓝光照射治疗,病情稳定后再出院。

