磁性玉米秸秆生物炭对水体中Cd的去除作用及回收利用
胡学玉,陈窈君,张沙沙,王向前,李成成,郭 晓
磁性玉米秸秆生物炭对水体中Cd的去除作用及回收利用
胡学玉,陈窈君,张沙沙,王向前,李成成,郭 晓
(中国地质大学(武汉)环境学院,武汉 430074)
以农田生态系统废弃农作物秸秆资源化利用为前提,以生物炭去除水体重金属镉(Cd)污染及其回收利用为目的,该文以500 ℃裂解的原始玉米秸秆生物炭(MSB,maize straw biochar)和磁性玉米秸秆生物炭(MMSB, magnetic maize straw biochar)试验材料,在2种生物炭的表面性状进行表征的基础上,探究了不同吸附条件下生物炭对污染水体中Cd(Ⅱ)的吸附去除作用及其回收利用的可能性。结果表明:MSB和MMSB对Cd(Ⅱ)的吸附量在pH值为5时达到最大,其最大吸附量分别为27.52和33.45 mg/g;当MSB和MMSB添加量为1.4和0.8 g/L时,对Cd(Ⅱ)的去除率分别可达85.15%和95.48%;Langmuir方程能更好地模拟等温吸附行为,MSB和MMSB达到平衡时的最大吸附容量分别为26.03和43.45 mg/g,趋近实际值;动力学数据与二级动力学方程拟合度更高,MSB和MMSB的平衡吸附量Q理论值分别为13.42和24.31 mg/g;MMSB对其表面吸附Cd(Ⅱ)的解吸率均显著低于MSB。磁性生物炭对Cd(Ⅱ)的吸附效率和固着能力增强可能与其较高的pH值、更大的比表面积、更多的极性含氧官能团有关。此外,在外部存在磁场的情况下,磁性生物炭可以通过磁力作用加以回收再利用。研究成果对促进农业废弃物的资源化利用以及水体环境中重金属净化技术的进步均有重要意义。
生物量;吸附;重金属;生物炭;磁性生物炭;重金属去除;水环境
0 引 言
水体重金属污染已经成为目前主要的环境问题之一。农村饮水安全问题更为突出,如某地农村小型水源地水体环境中镉(Cd)污染超标67倍(生活饮用水卫生标准(GB5749-2006))[1]。重金属Cd属于致癌重金属污染物,在环境介质中难以为微生物所降解,且其毒性阈值很低,并具有累积性,相比于其它非致癌重金属污染物有更大的健康风险。因此,采取相应的措施对水体环境中的Cd污染进行治理去除显得十分必要。
目前去除水体环境中重金属的方法包括化学沉淀法、氧化还原法、离子交换法、膜分离法、电化学方法、生物法、吸附法等[2-3]。相对于其他方法,吸附法具有操作简单、无需添加大量化学制剂、能量消耗少等特点。在吸附法中,吸附材料是关键因素。寻找原料广泛、价格低廉的吸附材料成为水体重金属污染修复工程领域的重要方向之一。
在众多吸附材料中,生物炭因其原料来源广、吸附容量大而受到越来越多的关注。生物炭(biochar)是生物质材料在完全缺氧或部分缺氧条件下,经低温(<700 ℃)裂解炭化产生的一类高度芳香化的、抗分解能力极强的固态物质[4-5]。生物炭在继承原有生物质良好孔隙结构特点的基础上,具有更大的孔隙度和比表面积[6]。加之其表面富含羧基、酚羟基、羰基、酸酐等官能团,具有一定的表面活性[7],可以有效吸附重金属[8]。如600 ℃空心莲子草生物炭对Pb(Ⅱ)的吸附量可高达257.12 mg/g[9]。相对低温(450 ℃)条件下制备的水葫芦生物炭对Cd(Ⅱ)的吸附量亦可达70.3 mg/g[10]。
中国是一个农业大国,农作物秸秆产量多达8亿多t,但秸秆的资源化利用技术还很短缺。玉米作为中国主要粮食作物,常年种植面积在2 333.3万 hm2左右,其秸秆产量每年约为1.8亿t,但是每年都有大量的玉米秸秆被随意弃置或露天焚烧,浪费了能量和氮素资源[11],还引起环境污染问题。因此以玉米秸秆为原料制备生物炭一方面为农业废弃物提供了资源化利用途径;另一方面,玉米秸秆生物炭可以作为一类新型的环保材料用于受污染水体的治理和修复。
为了进一步提高生物炭的表面活性和吸附能力,一些研究者将生物炭进行表面修饰和改性处理用于吸附研究或实践。如在500 ℃条件下通过热解制备的松木生物炭,经过Zn(Ⅱ)修饰后对As(Ⅲ)的吸附量由0.57增加到0.7 mg/g,提高了22%[12]。也有研究利用H2O2对水热法制备的花生壳生物炭进行化学修饰并用于对Pb(Ⅱ)的吸附,吸附量由0.88上升到了22.82 mg/g,提高近25倍[13]。还有实验以柳枝稷为原料,将其水热炭化后用KOH进行改性处理,改性后对Cd(Ⅱ)的吸附量由1.5上升到 4.0 mg/g,吸附量是改性前的2.67倍[14]。
尽管如上所述的一些研究结果显示生物炭经过氧化还原、酸碱反应等修饰改性,其吸附Cd(Ⅱ)等重金属污染物的能力有很大提高,但生物炭本身作为一种吸附材料如何将之从所处理的水环境中完全分离出来成为另外一个问题。一些研究试图通过磁化作用以生成磁性生物炭[15-16],期望不仅能够提高生物炭对水体重金属的吸附去除效率、同时亦可借助外加磁场的方式实现生物炭从水中分离并加以回收再利用。目前这方面的研究尚处于初期探索阶段,其吸附效果、吸附机理以及回收利用方式都有待于更多的研究工作去充实和印证。
为此,本研究利用玉米秸秆制备原始生物炭和磁性生物炭,探究磁性生物炭对水体环境中重金属Cd(Ⅱ)的去除固定作用及其回收再利用的可能性。研究成果对推动农业废弃物的资源化利用以及促进水体环境尤其是农村小型污染水源地水中重金属净化技术的进步均有重要意义。
1 材料与方法
1.1 生物质材料组分分析
采用美国国家可再生能源实验室(NREL, national renewable energy laboratory)方法[17],分别测定玉米秸秆纤维素和半纤维素含量,玉米秸秆取样量为0.5 g,72%浓硫酸水解1 h,4%稀硫酸水解45 min,将玉米秸秆中的纤维素和半纤维素降解为可用高效液相色谱法定量的单糖。
1.2 生物炭的制备
1.2.1 原始生物炭的制备
玉米秸秆取自湖北省武汉市洪山区。生物炭的制备方法为限氧高温热解法,将玉米秸秆用自来水清洗后再用蒸馏水清洗3次,置于80 ℃烘箱中(101,北京市永光明医疗仪器厂,北京)烘干12 h以上,直至恒质量。再将玉米秸秆放入植物粉碎机中(FW100,天津市华鑫仪器厂,天津)粉粹过20目筛,装填于瓷坩埚中压实并加盖。在室温下放入马弗炉(KSW-4b-11A,建力电炉制造有限公司,湖北)中,在500 ℃绝氧条件下加热3 h,冷却至室温后取出,研磨过60目筛,储存于自封袋中备用,记为MSB。
1.2.2 磁性生物炭的制备
将物质的量比为2∶1的FeCl3·6H2O(5.41 g)和FeSO4·7H2O(2.78 g)放入装有100 mL超纯水的烧瓶中充分溶解,加入28%的氨水溶液制得黑色Fe3O4胶体沉淀,加入6.0 g生物炭,在通氮气条件下剧烈搅拌30 min,密闭静置1 h。以上过程结束后,用磁铁对生物炭进行分离回收,用超纯水洗涤3次后于烘箱中80 ℃烘干,获得负载Fe3O4的磁性生物炭,研磨过60目筛,储存于自封袋中备用,记为MMSB。
1.3 生物炭的表征
生物炭的产率为生物炭制备前后的质量比,灰分的测定采用高温电炉灼烧法,利用马尔文纳米粒度电位仪Zetasizer测定2种生物炭的Zeta电位,利用pH计测定其pH值(生物炭:水的质量比为1∶20)。生物炭比表面积测定采用BET法测定,吸附气体采用氮气(TriStarⅡ3020,Micromeritics,美国)。生物炭表面官能团采用光谱纯KBr压片法于傅里叶变换红外光谱(FTIR)( Nicolet6700,Thermo Fisher Scientific,美国) 上分析测定,波数范围为4 000~500 cm–1,分辨率为4 cm–1,扫描次数为16。利用元素分析仪( Vario-EL-QCUBE,Elementar,德国) 测定生物炭中C、H、N和O元素的含量。在 X射线衍射仪(D8-Focus,Bruker,德国)上进行XRD分析,将供试样品粉末压片,测试条件为:Cu Kα射线,Ni滤波片,管电压40 kV,管电流40 mA,LynxEye192位阵列探测器。
1.4 生物炭的吸附
1.4.1 溶液pH值影响试验
以0.01 mol/L的Ca(NO3)2作为支持电解质,称取 0.5 g/L的生物炭于100 mL塑料离心管中,加入50 mL浓度为20 mg/L的Cd(Ⅱ)溶液,分别调节溶液pH值为3、4、5、6、7, 离心管恒温振荡24 h(25 ℃,150 r/min)。
1.4.2 吸附剂投加量的影响
以0.01 mol/L的Ca(NO3)2作为支持电解质,在pH值为5的条件下,加入50 mL浓度为20 mg/L的Cd(Ⅱ)溶液于100 mL离心管中,生物炭投加量分别为0.4、0.6、0.8、1.0、1.2、1.4、1.6、1.8 g/L,等温振荡时间为24 h(25 ℃,150 r/min)。
1.4.3 等温吸附试验
用0.01 mol/L的Ca(NO3)2作为背景电解质,设置Cd(Ⅱ)的初始质量浓度梯度为 0、5、10、20、40、60、80、100 mg/L,分别加入50 mL不同浓度Cd(Ⅱ)溶液于100 mL离心管中,溶液pH值为5,MSB和MMSB的添加量分别为1.4和0.8 g/L(均为1.4.2试验中得到的最佳投加量),在25℃、150 r/min条件下分别恒温振荡24 h。
1.4.4 吸附时间的影响
用0.01 mol/L的Ca(NO3)2作为背景电解质,加入50 mL质量浓度为20 mg/L的Cd(Ⅱ)溶液于100 mL离心管中,溶液pH值为5,MSB和MMSB的添加量分别为1.4和0.8 g/L,设置振荡时间为0、10、20、40、60 min及2、4、8、12、20、40 h,在25 ℃、150 r/min条件下分别恒温振荡。重复3次。
1.5 解吸试验
将等温吸附体系中得到的吸附了Cd(Ⅱ)的生物炭自然干燥后,用超纯水洗净,60 ℃下烘干备用。加入50 mL 0.1 mol/L的Ca(NO3)2溶液,加塞摇匀后,于25 ℃, 250 r/min条件下振荡24 h。重复3次。
1.6 Cd(Ⅱ)浓度的测定
将上述吸附试验得到的Cd(Ⅱ)溶液用0.22m的微孔滤膜过滤,用火焰原子分光光度计(Z-2000,日立株式会社日立制作所,上海)测定滤液中Cd(Ⅱ)的浓度,测定前利用镉标准溶液进行标准曲线的绘制。测定时选用Cd空心阴极灯,测定波长为228.8 nm。测定后计算生物炭对溶液中Cd(II)的平衡吸附量Q(mg/g)。
1.7 数据处理与分析
平衡时,生物炭对Cd(Ⅱ)的吸附量Q(mg/g)按公式(1)计算
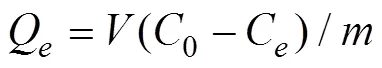
重金属去除率1公式参照公式(2)
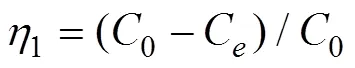
吸附等温线分别用Langmuir方程和Freundlich 模型拟合,分别得到
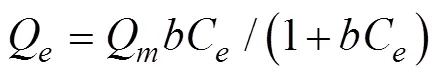
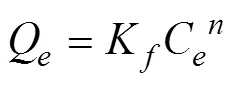
通过准一级动力学方程和准二级动力学方程研究生物炭对Cd(Ⅱ)的吸附动力学,分别得到
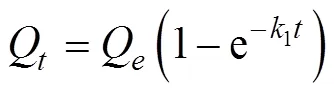
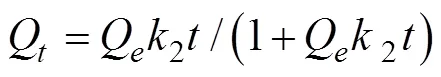
式中Q为平衡时单位质量生物炭吸附溶液中Cd(Ⅱ)的量,mg/g;0为初始溶液的Cd(Ⅱ)质量浓度,mg/L;C为平衡时溶液的Cd(Ⅱ)质量浓度,mg/L;为溶液的体积,L;为加入生物炭的质量,g;Q为生物炭的饱和吸附量,mg/g;Q为时刻的吸附量,mg/g;为Langmuir吸附特征常数,L/g;K是Freundlich模型参数,mg1-1/n·L1/n/g;为Freundlich常数;为时间,h;1为一级吸附速率常数,h–1;2为二级吸附速率常数,g/(mg·h)。
所有处理均独立重复3次,以其平均值作为测定结果,数据分析使用SPSS 18.0,作图软件为Origin 8.5。利用SPSS中单因素方差分析(One-way ANOVA)法研究处理间的差异性,多重比较采用最小显著差异法(LSD),检验显著性水平为0.05。结果以“平均值±标准差”表示。
2 结果与分析
2.1 2种生物炭对水溶液中Cd(Ⅱ)的吸附效率及其影响因素
2.1.1 2种生物炭在不同pH值下对溶液中Cd(Ⅱ)的去除作用
从图1可见,当MSB和MMSB的投加量为0.5 g/L,同时溶液中Cd(Ⅱ)的浓度为20 mg/L时,在pH值3~7之间(酸度较低,体系中不会产生Fe离子。)随着溶液初始pH值的增加,MSB和MMSB对Cd(Ⅱ)的吸附量均呈现出先增加后减少的趋势,其吸附量变化范围分别为14.15~27.52 mg/g和21.63~33.45 mg/g,在pH值为5时2种生物炭吸附量均达到最大,且在任一pH值条件下,MMSB的吸附量均高于MSB。2种生物炭对Cd(Ⅱ)的去除率范围分别为35.40%~68.80%和54.10%~83.65%,pH值为5时其去除率也达最高,MMSB对Cd(Ⅱ)的最大去除率比MSB高出14.85%,二者间差异显著(<0.05)。
2.1.2 不同添加量下2种生物炭对溶液中Cd(Ⅱ)的吸附去除影响
图2显示了不同生物炭添加量下的MSB和MMSB对Cd(Ⅱ)吸附的影响。当溶液中Cd(Ⅱ)的浓度为20 mg/L,pH值为5时,将MSB添加量从0.4 g/L增加到1.4 g/L,溶液中Cd(Ⅱ)的吸附量由33.02下降为12.16 mg/g,而去除率则从66.04%上升至85.15%。同时,将MMSB的添加量由0.4 g/L增加至0.8 g/L,其对Cd(Ⅱ)的吸附量从39.91亦下降到23.87 mg/g,而对Cd(Ⅱ)的去除率从79.81%升至95.48%。可见,MMSB在投加量更低的条件下比MSB的去除率更高,且二者在0.05水平上差异显著。当溶液中Cd(Ⅱ)的浓度一定时,随生物炭投加量的不断增加,生物炭表面的吸附位点也相应增加,大量活性位点竞争有限的重金属离子,使得单位质量生物炭吸附的重金属量减少[18],但生物炭对Cd(Ⅱ)的去除率表现为逐渐增加。
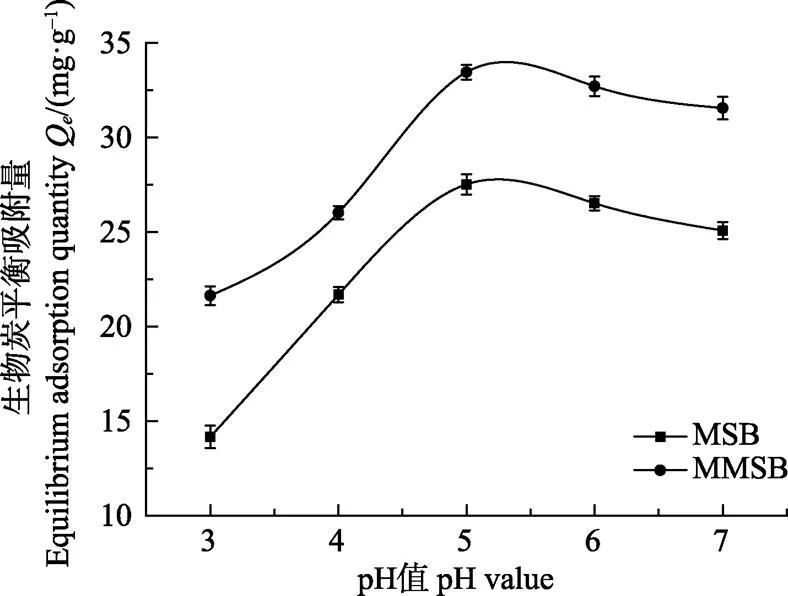
注:MSB、MMSB分别为原始生物炭、磁性生物炭,下同。
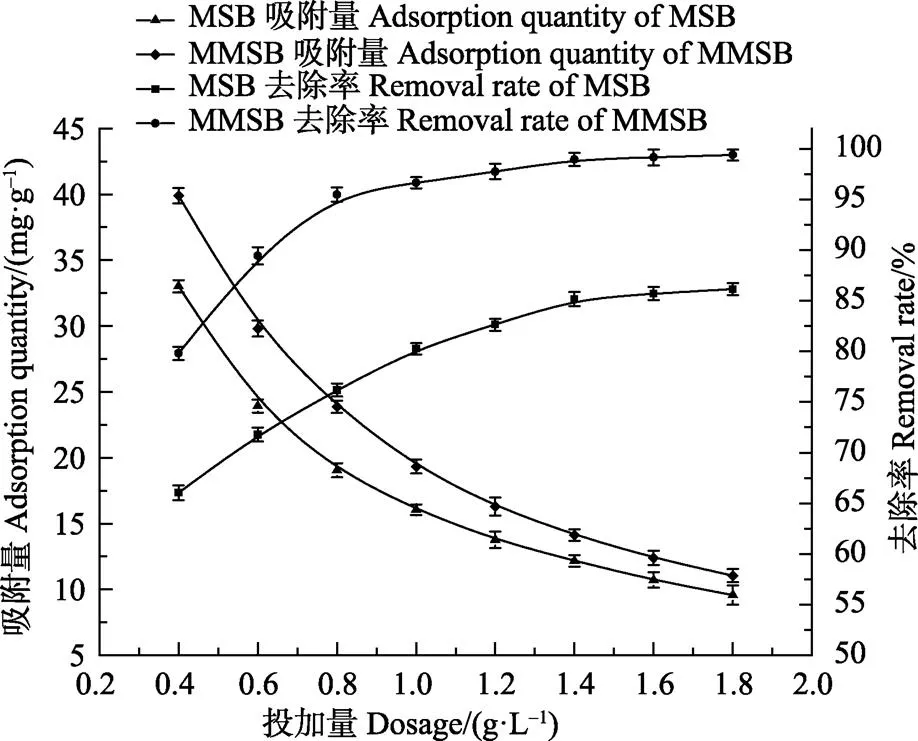
图2 MSB和MMSB的不同添加量对Cd(Ⅱ)吸附的影响
2.1.3 溶液重金属初始浓度对生物炭吸附Cd(Ⅱ)的影响
图3显示了MSB和MMSB对Cd(Ⅱ)的吸附容量和溶液中Cd(Ⅱ)的平衡浓度之间的关系。在pH值为5,MSB和MMSB添加量为1.4、0.8 g/L条件下,2种生物炭的吸附量均随着Cd(Ⅱ)浓度的增加而增加。在低浓度段,Cd(Ⅱ)的吸附平衡浓度在0~20 mg/L时,MSB和MMSB对Cd(Ⅱ)的吸附量迅速增大,由0分别增加到18.93和34.96 mg/g。但随着平衡溶液浓度从20 mg/L增大到 70 mg/L,吸附量仅从18.93和34.96 mg/g增加到25.31和43.45 mg/g,吸附量逐渐趋于平衡。
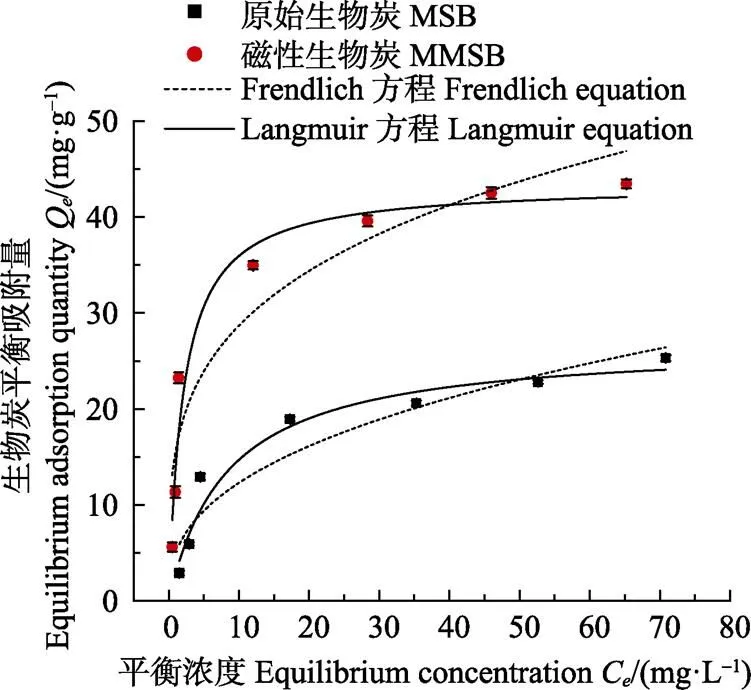
图3 MSB和 MMSB对Cd(Ⅱ)的吸附等温线
将MSB和MMSB对Cd(Ⅱ)的等温吸附数据用Langmuir和Freundlich模型进行拟合,表1中列出了相应的模型参数。由表1可知,在Langmuir模型中,MSB和MMSB的理论最大平衡吸附量Q分别为26.03和43.45 mg/g,MMSB比MSB高66.92%。尽管Langmuir方程和Freundlich方程的相关系数2均大于0.900 0,但Langmuir方程的2更大,尤其值得一提的是,Langmuir方程计算出的最大吸附量(26.03和43.45 mg/g)接近实际值(25.31和43.45 mg/g),而Freundlich模型没有饱和吸附值。从图3也可以看出,在最大平衡浓度处,Freundlich模型的吸附容量与实际值有明显偏差,进一步说明Langmuir方程的拟合效果更好。
Freundlich方程中1/和K值可以表示重金属浓度对吸附容量影响的强弱,1/值越小,K值越大,吸附性能就越好。由表1可知,与MSB相比,MMSB的1/值减小,K值升高,说明磁性生物炭对Cd(Ⅱ)的吸附能力增强。
R是一个无量纲的分离因子,表示吸附剂对吸附质的亲和力,计算公式为
R=1/(10) (7)
一般情况下,在0<R<1时,表示有利于吸附进行;R=1时表示线性吸附;R=0表示不可逆吸附;若R>1,则表示吸附性能较差[19]。由图4可见,2种生物炭均为0<R<1,说明玉米秸秆生物炭对Cd(Ⅱ)的吸附性能较好。同时,MMSB的R值均要低于MSB,因此MMSB对重金属的亲和力更强,吸附性能更优越,这可与前述的实测数据相互印证。

表1 MSB和MMSB对Cd(Ⅱ)吸附的等温线拟合参数
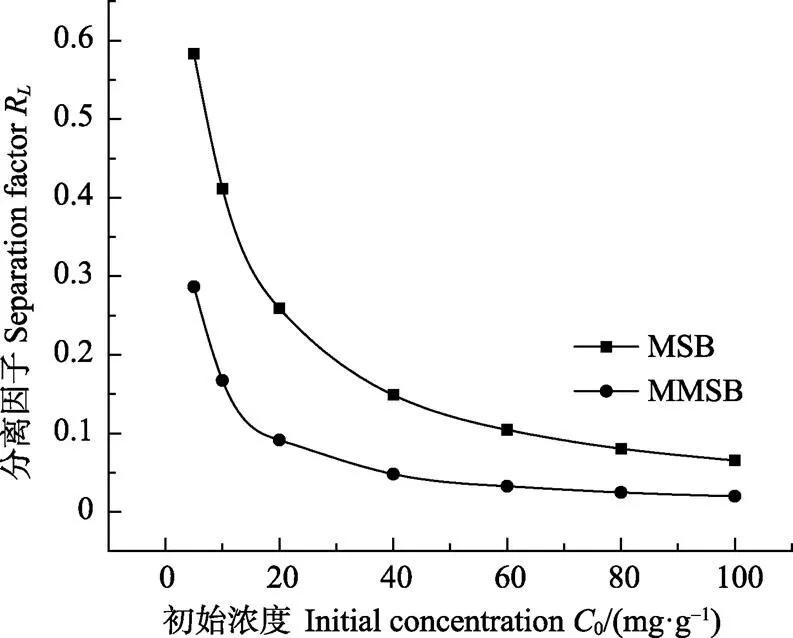
图4 分离因子与Cd(Ⅱ)初始浓度的关系曲线
2.1.4 反应时间对溶液中Cd(Ⅱ)吸附去除的影响
图5显示的是2种生物炭对Cd(Ⅱ)的吸附量随时间的变化情况。由图5可知,当溶液中Cd(Ⅱ)的浓度为 20 mg/L,pH值为5,MSB和MMSB添加量为1.4、0.8 g/L时,2种生物炭对Cd(Ⅱ)的吸附在初始阶段迅速增加,之后减缓直至吸附平衡。因此,2种生物炭对Cd(Ⅱ)的吸附可分为快吸附和慢吸附2个阶段。0~2 h为快速反应阶段,此时的MSB和MMSB对Cd(Ⅱ)的吸附量分别达到其最终吸附量的57.27%和68.13%。2 h后为慢反应阶段,吸附速率减小,吸附量的增幅降低,至12 h时吸附趋于平衡,此时吸附量分别达到实际值Q的90.06%和90.73%。
对MSB和MMSB的动力学数据进行准一级和准二级动力学模型拟合,模型参数见表2。由表2可知,2种动力学模型均可较好地模拟吸附过程。本研究中,MSB和MMSB用拟一级动力学拟合得到的Q值(12.42和22.06 mg/g)与实际值相差了5.68%和6.12%,拟二级动力学的Q值(13.42和24.31 mg/g)与实际的Q值更为接近,仅相差2.26%和3.84%。拟一级动力学能较好地反应生物炭吸附Cd(Ⅱ)的初期的过程,表明反应初期与Cd(Ⅱ)的扩散过程有关。准二级动力学模型主要与化学吸附作用有关,金属离子和吸附剂官能团之间化学键的形成是主要的影响因子[20]。可见生物炭对Cd(Ⅱ)的吸附过程是多种机制的共同作用,且主要以化学作用为主。
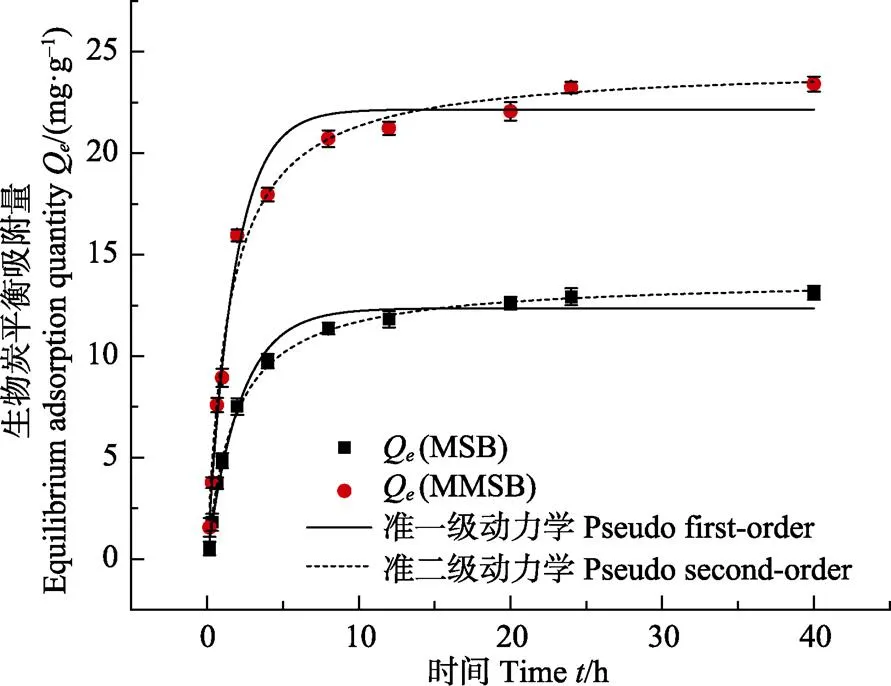
图5 MSB和MMSB对Cd(Ⅱ)吸附的动力学方程拟合
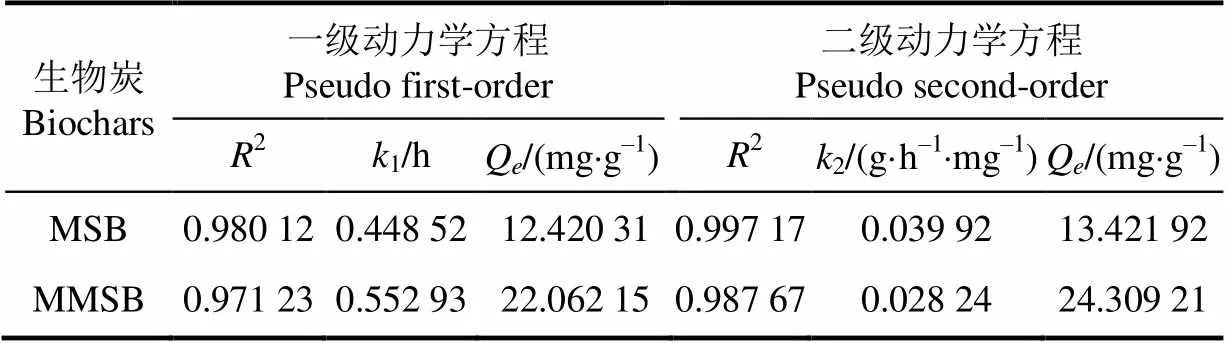
表2 MSB和MMSB对Cd(Ⅱ)吸附的动力学拟合参数
2.2 生物炭的化学特性和表面性状对其吸附能力的影响
2.2.1 生物炭的基本物理化学性质
由表3可知,与原始生物炭相比,磁性生物炭的产率上升,残留组分质量增加,灰分发生累积,MMSB含有的灰分含量比MSB增加了约3倍,由于生物炭灰分中含有钙镁钾钠等较多的盐基离子,因此pH值也相应从10.56增大到11.02,而等电点则略有降低。
磁性生物炭O元素含量上升,C、H、N、S的含量均降低,各元素降幅或升幅程度不一。元素的H/C、O/C和(O + N)/C质量比可以表征生物炭的芳香性和极性程度。改性后的生物炭H/C原子比降低,表明MMSB相对于MSB具有更强的芳香性,而O/C和(O + N)/C原子比分别由MSB的0.58和0.61增加到了MMSB的1.50和1.53,说明磁性生物炭中极性含氧官能团的数量增加。生物炭的C/N值可以反映其稳定性,由表3可以看出,磁性生物炭的C/N值增加,表明MMSB的环境稳定性更强。
生物炭吸附能力与其比表面积有关,分析生物炭比表面积的变化发现,虽然磁性生物炭表面易被负载的磁铁矿堵塞,但是其比表面积比MSB仍增加了2倍,可能是因为磁铁矿的比表面积相对较大(约65.78 m2/g[21]),从而导致磁性生物炭的比表面积显著增加。比表面积增加有利于其吸附功能的发挥,与前文的吸附结果相呼应。
MSB和MMSB的氮气吸脱附等温线如图6a所示。从图中可以看出,MSB和MMSB的氮气吸脱附等温线形状相似,都属于BDDT分类系统中的IV型,吸脱附曲线并没有重合而是都出现了明显的滞后现象,表明2种生物炭孔径以介孔为主。在低压区吸附量小,MMSB的孔容大于MSB,说明MMSB的微孔和中孔数量大于MSB[22]。在0接近于1的高压区,MMSB的吸附量显著上升,表明生物炭中含有大孔,而MSB的大孔数量则较少。
从图6b可知,MSB的孔峰分布在15~20、30和50 nm处,MMSB的孔峰在15~55 nm之间均有分布。MSB中小于2 nm的微孔分布较少,而介于2~50 nm之间的中孔分布较为丰富,但总量依然较少。MMSB与MSB相比,孔峰峰值也表现为增加,说明其中孔的孔容增加,与吸脱附等温线的测定结果一致。
MMSB的磁性特征如图7所示。MMSB在室温下表现出超顺磁行为,无矫顽力和剩磁。MMSB的饱和磁化强度是9.37 emu/g,本研究中磁性生物炭的Fe3O4含量为32.54%,Fe3O4含量的增加会促进饱和磁化强度的上升。
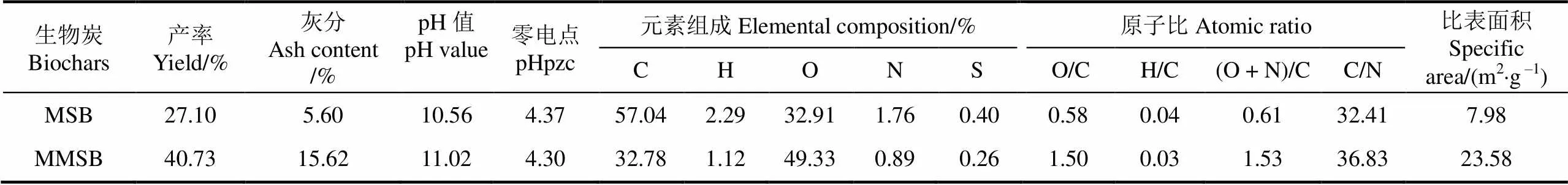
表3 MSB和MMSB的物理化学性质
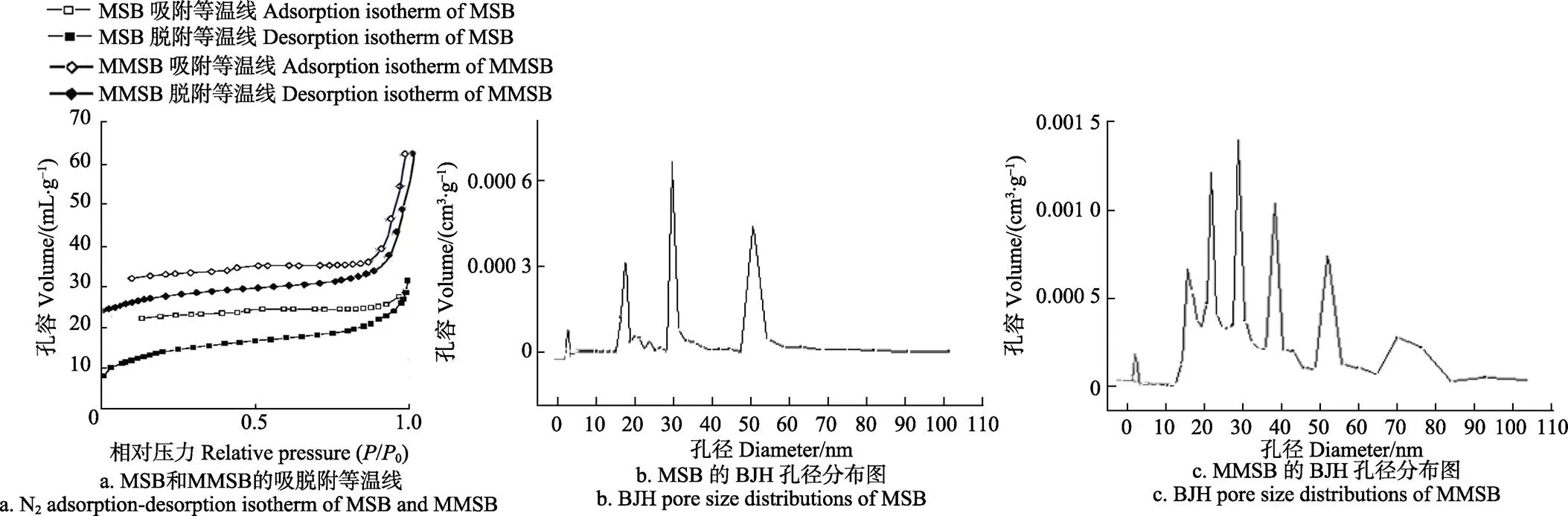
图6 MSB和MMSB的吸脱附等温线及BJH孔径分布图
2.2.2 生物炭的表面官能团种类
图8为2种生物炭吸附Cd(Ⅱ)前后的红外吸收光谱。从图中可以看出2种生物炭有相同的出峰位置。3 730~ 3 000 cm–1范围内的波峰为-OH的伸缩振动[23]。2 230 cm–1处的吸收峰为C≡C的伸缩振动[24]。波数1 580 cm–1附近的吸收峰通常是羰基C=O和芳环C=C的伸缩振动所产 生[25]。1 380 cm–1附近处的波峰是由C-H的伸缩振动产 生[26]。在1 099 cm–1和449 cm–1区域出现的波峰为Si-O-Si的特征吸收峰[27-28]。
将2种生物炭进行对比,表面官能团的种类和数量均发生了变化,其中变化较明显的有1 380、780、565 cm–1处的吸收峰。磁性生物炭在1 380 cm–1处的C-H吸收峰更加尖锐,在780~795 cm–1处增加了吡啶、呋喃等杂环化合物的振动峰,表明MMSB具有高度芳香化和杂环化的结构[29],与H/C原子比的结果一致。在565 cm–1附近处的新峰为Fe-O特征吸收峰,表明Fe3O4成功负载于生物炭中[30]。由此可知磁性生物炭特征吸收峰的数量增加,官能团更加丰富,这与O/C和(O + N)/C原子比的结果是吻合的。特征吸收峰的变化说明吸附过程中存在着化学吸附作用,吸附过程与准二级动力学模型的假设相一致。
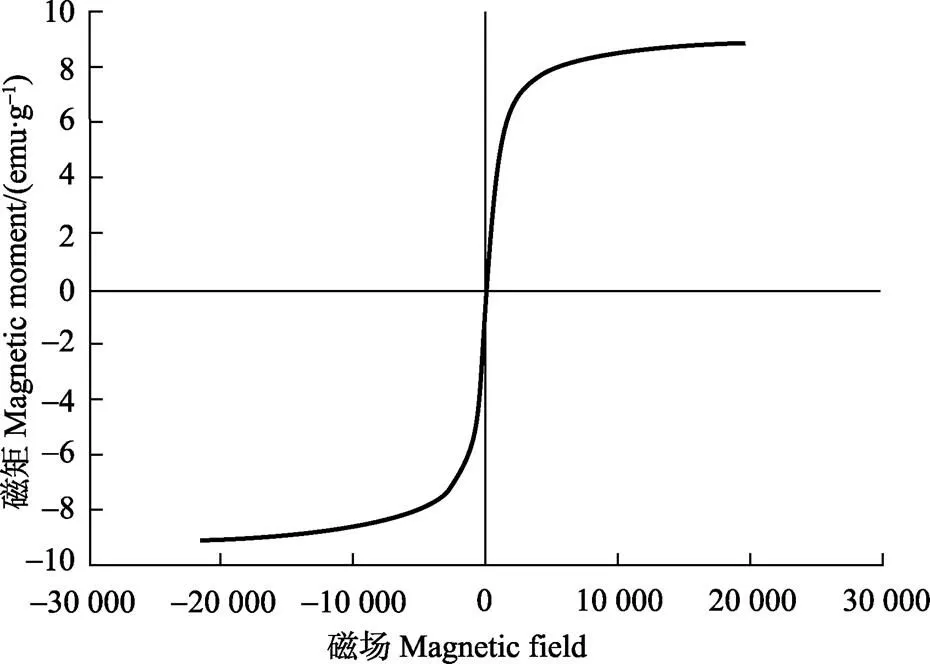
图7 300 K下MMSB的磁化曲线
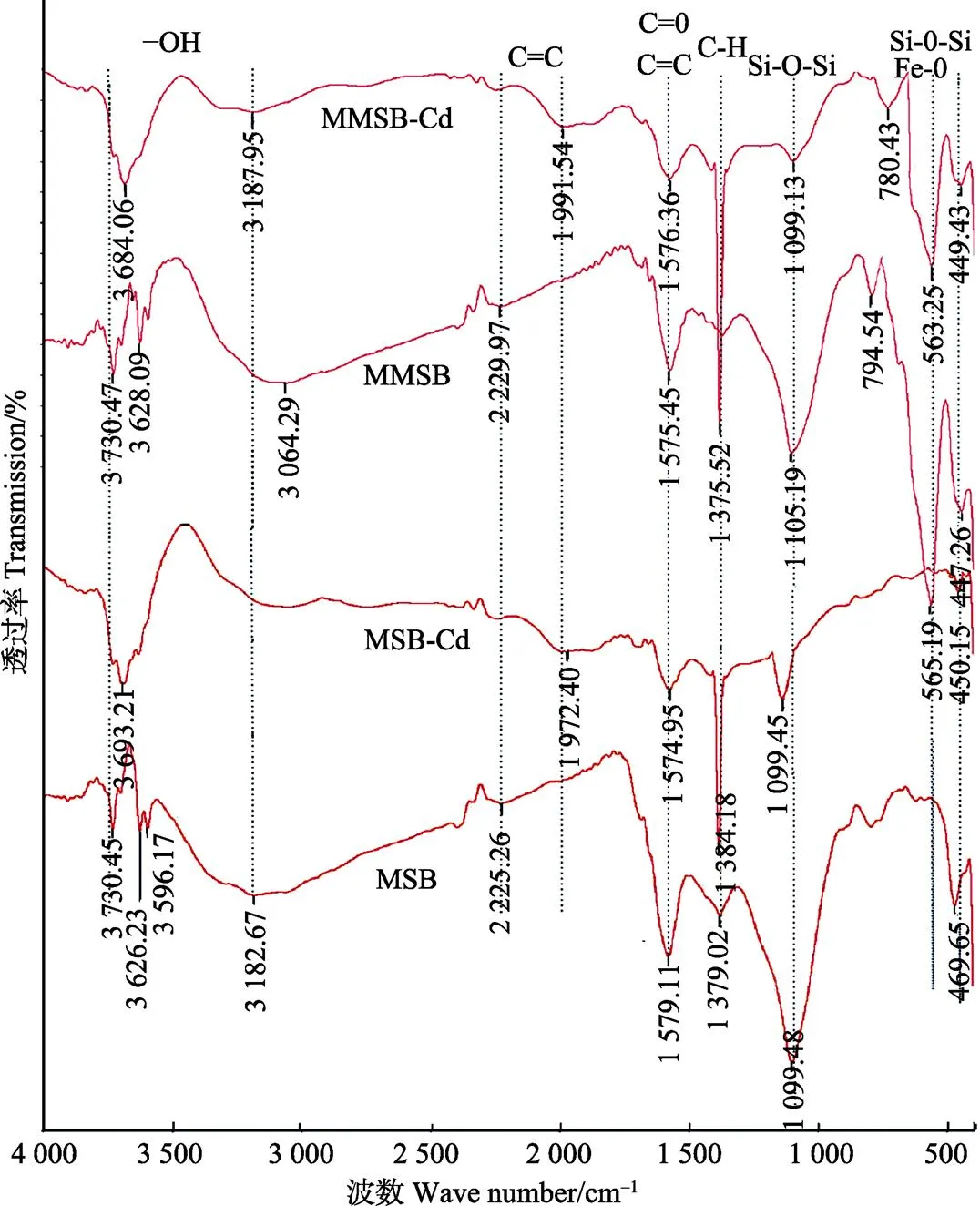
图8 MSB和MMSB吸附Cd(Ⅱ)前后的FTIR图谱
2.2.3 生物炭的矿物组成
MSB和MMSB的XRD衍射图谱如图9所示。2种生物炭在10°~50°的2范围内均存在峰值。MSB吸附Cd(Ⅱ)后在2=27°左右的强峰说明SiO2的存在[31]。MSB吸附Cd(Ⅱ)前后的XRD衍射图谱并没有明显的变化,说明其吸附Cd(Ⅱ)后并没有形成含Cd的新矿物相。MMSB吸附Cd(Ⅱ)前后峰值的位置分布是相似的,在吸附Cd(Ⅱ)后出现了多个明显的峰值,形成的Cd沉淀有CdCO3,Cd3P2以及Cd3(PO4)2等。2=36.5°处为Fe3O4特征峰,再次证实Fe3O4已负载于生物炭中,为生物炭在水体中进行磁分离提供了条件。磁性生物炭波峰的增加表明其吸附效率提高,生物炭与Cd(Ⅱ)的化学作用增强,进一步证实了准二级动力学模型的假设。

Note: D: CdCO3; Q: SiO2; C: CaCO3; O: Cd3(PO4)2; F: Fe3O4; P: Cd3P2
2.2.4 生物炭的表面形貌
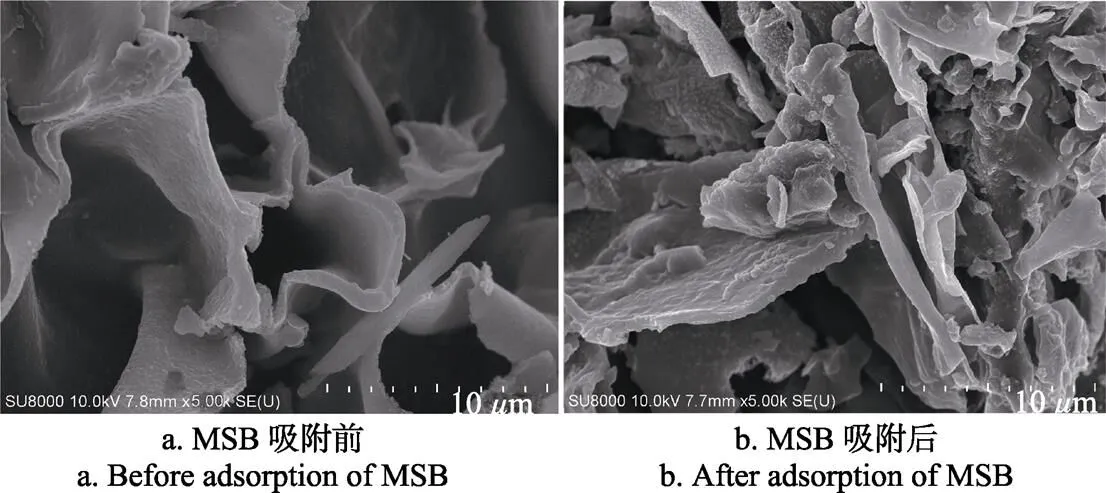
从图10a和图10b中可以看出,MSB经过灼烧后表面较为光滑,结构不完整,其对应的能谱图显示表面含有较多的SiO2、K、Ca等无机矿物。而MMSB表面粗糙不平,主要为块状结构,孔隙结构不发育,表面含有的大孔数量少,主要发育一些中孔和微孔结构。出现的光亮区域附着了一些细小的Fe3O4颗粒物,从MMSB对应的能谱图中也可以看出其表面存在Fe颗粒,与红外光谱和XRD的表征结果相吻合。
2.3 生物炭的解吸及分离回收
图11同时给出了2种生物炭在不同Cd(Ⅱ)浓度下的解吸率。随着重金属初始浓度的增加,生物炭对Cd(Ⅱ)的解吸率也表现出不同程度的增加,总体趋于稳定。MSB和MMSB对溶液中Cd(Ⅱ)的解吸率范围分别为23.60%~41.10%和14.58%~29.88%,在不同的Cd(Ⅱ)初始浓度下,磁性生物炭的解吸量均要小于原始生物炭,且均达到显著差异,说明磁性生物炭对Cd(Ⅱ)的固着能力增强,吸附性能更加优良,能够较好地防止Cd(Ⅱ)在水体环境中的迁移,与原始生物炭相比具有更高的不可逆性。

注:*表示具有统计学差异(P < 0.05)。
图12为生物炭在水体中的分离回收图。从图中可以明显看出,与原始生物炭相比,磁性生物炭可以被外部的磁场所吸引,从而更好地从水体中分离出来,促进对生物炭的回收利用。

图12 MSB和MMSB在水中的分离回收
3 讨 论
3.1 生物质原料组分对生物炭的影响
生物质热解是纤维素、半纤维素等物质热解的综合表现,玉米秸秆含有纤维素、半纤维素等多种化学成分,且纤维素含量较高,本研究中原材料玉米秸秆的纤维素和半纤维素含量分别为35.67%和22.81%。纤维素和半纤维素主要产生挥发性物质,有研究表明,由于玉米秸秆含有较多的无定型纤维素及半纤维素,因此晶面间弥散程度大,生成的生物炭微晶层数相对较少,易于形成中微孔[32]。纤维素和半纤维素在热解过程中会生成多种分解聚合的中间产物,形成多种官能团,如-OH振动峰主要来自脱水脱氧纤维素和半纤维素羟基组,羰基C=O位于纤维素结构中,芳香碳上的C=C伸缩振动峰来自纤维素结构中的芳香碳结构物质,C-H吸收峰代表的是纤维素、半纤维素上的脂肪族的伸缩振动。
3.2 pH值对生物炭吸附Cd(Ⅱ)的影响
由于溶液pH值的不同,Cd(Ⅱ)以不同的形式存在于水溶液中。在pH值较低时,超过99.9%的Cd(Ⅱ)在溶液中以自由离子形式存在[33],此时溶液中H+浓度较高,高浓度的H+会与Cd(Ⅱ)竞争生物炭表面的吸附位点,同时生物炭表面的官能团发生质子化,质子化的官能团与带正电的Cd(Ⅱ)具有静电排斥作用[34-35],因此pH值较低时生物炭对Cd(Ⅱ)的平衡吸附量也较低。随着pH逐渐增加,溶液中H+浓度降低,减弱了与Cd(Ⅱ)的竞争吸附作用。本研究中MSB和MMSB的等电点分别为4.37和4.30(表3),当溶液的pH值高于生物炭的等电点时,生物炭表面会产生带负电的官能团,带正电的Cd(Ⅱ)和带负电的官能团之间的静电作用增强,进一步促进了生物炭表面位点与Cd(Ⅱ)的结合,增加了水体中Cd(Ⅱ)的去除率[36]。有研究表明,当pH值小于5时,溶液中自由Cd(Ⅱ)离子占主导地位,之后随着pH值的进一步上升,Cd(Ⅱ)主要与氢氧根结合形成一些低可溶性氢氧化物如Cd(OH)2和Cd(OH)3沉淀[37],生物炭对Cd(Ⅱ)的吸附量随之降低。在用玉米秸秆或其它不同原材料制备生物炭吸附Cd(Ⅱ)的试验中,pH对生物炭平衡吸附量的影响与本研究所观察到的趋势一致[36,38]。
3.3 生物炭添加量对其吸附Cd(Ⅱ)的影响
在吸附发生的初始阶段,生物炭表面可供重金属占据的吸附位点数量与投加的生物炭量之间是正相关的[39],吸附位点的数量随着生物炭投加量的增加而增加[40],此时生物炭吸附率亦随之上升。随着吸附剂的进一步添加,过量的生物炭容易导致吸附剂颗粒之间因过度拥挤发生团聚作用,引起吸附位点的重叠,一些吸附点位被掩蔽,吸附剂的总比表面积也趋于减小,生物炭吸附量趋于饱和[41]。在本研究中,Cd(Ⅱ)的去除率与MSB/MMSB的添加量呈现出正相关的关系(2分别为0.9266、0.7748),这与用花生壳生物炭和玉米芯生物炭吸附溶液中Cd(Ⅱ)的实验研究结果较为一致[38-39]。
3.4 2种生物炭对Cd(Ⅱ)的吸附机制
本研究通过动力学拟合发现生物炭对Cd(Ⅱ)的吸附包含多种机制,根据2.1.4部分吸附动力学得到的分析结果,生物炭的吸附过程既有物理作用也存在化学作用。(吸附热力学用来探究吸附过程是否存在物理吸附。故在本文中省略。)从物理吸附作用来看,生物炭的比表面积较大,能够提供大量吸附点位,且其表面带有负电荷,可以与Cd(Ⅱ)发生静电吸附作用。从化学作用的角度分析,首先,对比MSB和MMSB吸附前后的FTIR谱图变化可以看出,吸附前3 731~3 590 cm–1范围内的多个-OH小峰消失,吸附后产生了一个吸收峰,表明-OH中的分子氢键作用力减弱,-OH基被Cd(Ⅱ)占据,Cd(Ⅱ)与-OH中的H+发生了离子交换[42]。有研究表明,生物炭吸附Cd(Ⅱ)的过程中,通过离子交换作用吸附的Cd(Ⅱ)占据了总吸附量的79.5%,表明离子交换对溶液中Cd(Ⅱ)的吸附具有显著作用[43]。
其次,2种生物炭的XRD衍射图和EDS能谱图中均表明生物炭表面富集了SiO2(图7、图8),在红外光谱图中1 099和450 cm–1附近处相应出现了Si-O-Si的振动吸收峰(图6),可能是因为SiO2通过羟基化作用为生物炭中的金属阳离子提供了络合位点,吸附阳离子后的Si氧化物进一步与溶液中的Cd2+/Cd(OH)+发生表面络合作用[43]。
此外,2 230 cm–1附近处的C≡C波峰明显迁移至 1 980 cm–1附近,以及在1 580~1 370 cm–1区域C-H吸收峰的位移均表明原有的π共轭芳香结构发生变化,在吸附过程中存在阳离子–π作用。在其它用玉米秸秆生物炭吸附Cd(Ⅱ)的研究中也证实阳离子– π作用是其主要的吸附机理之一[29]。因此生物炭对Cd(Ⅱ)的吸附机理主要包括静电吸附、离子交换、表面络合和阳离子–π作用。
3.5 2种生物炭对Cd(Ⅱ)的吸附效果的差异
本研究中,磁性生物炭相比原始生物炭对Cd(Ⅱ)的吸附效率更高,这一点在等温吸附时有显著表现,磁性生物炭MMSB在投加量更低的条件下,其饱和吸附量显著高于原始生物炭MSB,说明磁性生物炭能以相对低的用料成本获得更好的吸附性能。从其理化特性和表面特征分析,MMSB相比MSB具有更大的比表面积和灰分含量(表3),较大的比表面积可以提供更多的吸附位点,增加生物炭的吸附量[44]。灰分组分的增加可能会引起生物炭表面阴离子的增加,促进Cd(Ⅱ)与生物炭表面负电荷的静电作用[45]。此外,通过元素分析可以看出MMSB表面含有更为丰富的含氧官能团,有利于金属离子与生物炭的表面官能团发生一系列离子交换以及表面络合作用[46]。再则,磁性生物炭的pHpzc值减小,较低的等电点预示着磁性生物炭会解离出更多的氢离子形成负电荷表面,从而增加对水体中带有正电荷的Cd(Ⅱ)的吸附固定能力。
化学吸附作用方面,MMSB与MSB相比,MMSB的XRD图谱证实了磁性生物炭表面形成了CdCO3、Cd3(PO4)2和Cd3P2等金属沉淀(图7),表明Cd(Ⅱ)与磁性生物炭中矿物组分释放的PO34–或CO23–离子形成了Cd沉淀,从而增加了MMSB对Cd(Ⅱ)的去除率。在MMSB的FTIR光谱中,表征阳离子–π作用的1 380 cm–1处的吸收峰更加尖锐,吸收强度更大,且新增了780~795 cm–1之间的芳香化和杂环化合物振动峰,此类化合物也可以提供π电子与Cd(Ⅱ)形成稳定的结构,因此阳离子–π作用在MMSB中更加显著。最后,MMSB在565 cm–1附近处的Fe-O振动峰也发生了变化,说明对于MMSB,不仅生物炭表面对Cd(Ⅱ)有吸附作用,其负载的Fe氧化物也存在对Cd(Ⅱ)的吸附作用。Cd(Ⅱ)与磁性生物炭中的Fe氧化物有较高的亲和力,Fe氧化物的存在增强了络合吸附作用[47],这可能也是其对吸附的Cd(Ⅱ)的解吸率相对低的原因之一。
4 结 论
1)随着溶液初始pH值的增加,生物炭对Cd(Ⅱ)的吸附量呈现先增加后减少的趋势,在pH值为5时达到最大,MSB和MMSB的最大吸附量分别为27.52和 33.45 mg/g。随着生物炭投加量的增加,生物炭对溶液中Cd(Ⅱ)的单位质量吸附量呈现下降趋势,但去除率表现为逐渐增加。MSB和MMSB添加量为1.4和0.8 g/L时,对Cd(Ⅱ)的平衡去除率分别为85.15%和95.48%,二者差异显著(<0.05)。
2)Langmuir方程能更好的模拟等温吸附行为,MSB和MMSB的拟合系数均超过0.970 0,达到平衡时的最大吸附容量分别为26.03和43.45 mg/g,趋近实际值。动力学数据与二级动力学方程拟合度更高,其拟合系数值(0.997 17和0.987 67)均大于准一级动力学模型,MSB和MMSB的平衡吸附量Q理论值分别为13.42和24.31 mg/g,与实际值仅相差2.26%和3.84%。
3)MSB和MMSB的最大解吸率分别为41.10%和29.88%,MMSB的解吸量小于MSB,磁性生物炭对Cd(Ⅱ)的固着能力增强,能够较好地防止Cd(Ⅱ)在水体环境中的迁移。
4)生物炭对Cd(Ⅱ)的吸附过程是多种机制的共同作用,主要以化学作用为主,吸附机理主要包括静电吸附、离子交换、表面络合和阳离子–π作用。
[1] 陈窈君,胡学玉,王向前,等. 湖北省农村小型水源地水体环境中重金属污染状况[J]. 环境科学与技术,2017,40(3):153-160. Chen Yaojun, Hu Xueyu, Wang Xiangqian, et al. Small rural water sources’ contamination by heavy metals in Hubei Province[J]. Environmental Science and Technology, 2017, 40(3): 153-160. (in Chinese with English abstract)
[2] 谢晓君,王方园,王光军,等. 中国地表水重金属污染的进展研究[J]. 环境科学与管理,2017,42(2):31-34. Xie Xiaojun, Wang Fangyuan, Wang Guangjun, et al. Study on heavy metal pollution in surface water in China[J]. Environmental Science and Management, 2017, 42(2): 31-34. (in Chinese with English abstract)
[3] 孙维锋,肖迪. 水体重金属污染现状及治理技术[J]. 能源与节能,2012(2):49-50. Sun Weifeng, Xiao Di. Status and control technology of heavy metal pollution[J]. Energy and Energy Conservation, 2012(2): 49-50. (in Chinese with English abstract)
[4] 李音,单胜道,杨瑞芹,等. 低温水热法制备竹生物炭及其对有机物的吸附性能[J]. 农业工程学报,2016,32(24):240-247. Li Yin, Shan Shengdao, Yang Ruiqin, et al. Preparation of bamboo biochars by low-temperature hydrothermal method and its adsorption of organics[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2016, 32(24): 240-247. (in Chinese with English abstract)
[5] 董双快,徐万里,吴福飞,等. 铁改性生物炭促进土壤砷形态转化抑制植物砷吸收[J]. 农业工程学报,2016,32(15):204-212. Dong Shuangkuai, Xu Wanli, Wu Fufei, et al. Fe-modified biochar improving transformation of arsenic form in soil and inhibiting its absorption of plant[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2016, 32(15): 204-212. (in Chinese with English abstract)
[6] Méndez A, Gómez A, Paz-Ferreiro J, et al. Effects of sewage sludge biochar on plant metal availability after application to a Mediterranean soil[J]. Chemosphere, 2012, 89(11): 1354-1359.
[7] Sandeep K, Reginald E M, Lal C R, et al. Biochar preparation from parthenium hysterophorus and its potential use in soil application [J]. Ecological Engineering, 2013, 55: 67-72.
[8] 陆海楠,胡学玉,刘红伟. 不同裂解条件对生物炭稳定性的影响[J]. 环境科学与技术,2013,36(8):11-14. Lu Hainan, Hu Xueyu, Liu Hongwei. Influence of pyrolysis conditions on stability of biochar[J]. Environmental Science and Technology, 2013, 36(8): 11-14. (in Chinese with English abstract)
[9] Yang Y, Wei Z G, Zhang X L, et al. Biochar from alternanthera philoxeroides could remove Pb(II) efficiently[J]. Bioresource Technology, 2014, 171: 227-232.
[10] Zhang F, Wang X, Yin D X, et al. Efficiency and mechanisms of Cd removal from aqueous solution by biochar derived from water hyacinth (Eichorniacrassipes)[J]. Journal of Environmental Management, 2015, 153: 68-73.
[11] 闫贵龙,曹春梅,鲁琳,等. 玉米秸秆不同部位主要化学成分和活体外消化率比较[J]. 中国农业大学学报,2006,11(3):70-74. Yan Guilong, Cao Chunmei, Lu Lin, et al. Comparison of main chemical composition and in vitro digestibility in various sections of corn stalks[J]. Journal of China Agricultural University, 2006, 11(3): 70-74. (in Chinese with English abstract)
[12] Van Vinh N, Zafar M, Behera S K, et al. Arsenic(III) removal from aqueous solution by raw and zinc loaded pine cone biochar:Equilibrium, kinetics, and thermodynamics studies[J]. Environmental Science & Technologyl, 2015, 12(4): 1283-1294.
[13] Xue Y W, Gao B, Yao Y, et al. Hydrogen peroxide modification enhances the ability of biochar (hydrochar) produced from hydrothermal carbonization of peanut hull to remove aqueous heavy metals: Batch and column tests[J]. Chemical Engineering Journal, 2012 (200/201/202): 673-680.
[14] Regmi P, Garcia Moscoso J L, Kumar S, et al. Removal of copper and cadmium from aqueous solution using switchgrass biochar produced via hydrothermal carbonization process[J]. Journal of Environmental Management, 2012, 109(10): 61-69.
[15] 张如玉,刘海波,邹雪华,等. 小麦秸秆驱动菱铁矿热解制备磁性生物质碳及其吸附Cd2+活性[J]. 环境科学,2017,38(8):3519-3528. Zhang Ruyu, Liu Haibo, Zou Xuehua, et al. Preparation of magnetic biomass carbon by thermal decomposition of siderite driven by wheat straw and its adsorption on cadmium[J]. Environmental Science, 2017, 38(8): 3519-3528. (in Chinese with English abstract)
[16] 杜文琪,曹玮,周航,等. 磁性生物炭对重金属污染废水处理条件优化及机理[J/OL]. 环境科学学报,2017,1-14. Du Wenqi, Cao Wei, Zhou Hang, et al. Optimization and the mechanismin treatment of heavy metals wastewater with magnetic biochar[J/OL]. Acta Scientiae Circumstantiae, 2017, 1-14. DOI:10.13671/j.hjkxxb.2017.0355 (in Chinese with English abstract)
[17] 张红漫,郑荣平,陈敬文,等. NREL法测定木质纤维素原料组分的含量[J]. 分析试验室,2010,29(11):15-18.
[18] 马锋锋,赵保卫,钟金魁,等. 牛粪生物炭对磷的吸附特性及其影响因素研究[J]. 中国环境科学,2015,35(4): 1156-1163. Ma Fengfeng, Zhao Baowei, Zhong Jinkui, et al. Characteristics phosphate adsorption onto biochars derived from dairy manure and its influencing factors[J]. China Environmental Science, 2015, 35(4): 1156-1163. (in Chinese with English abstract)
[19] 张连科,刘心宇,王维大,等. 油料作物秸秆生物炭对水体中铅离子的吸附特性与机制[J]. 农业工程学报,2018,34(7):218-226. Zhang Lianke, Liu Xinyu, Wang Weida, et al. Characteristics and mechanism of lead adsorption from aqueous solutions by oil crops straw-derived biochar[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2018, 34(7): 218-226. (in Chinese with English abstract)
[20] Hydari S, Sharififard H, Nabavinia M, et al. A comparative investigation on removal performances of commercial activated carbon, chitosan biosorbent and chitosan/activated carbon composite for cadmium[J]. Chemical Engineering Journal, 2012 (193/194): 276-282.
[21] 赖立,谢强,方文侃,等. 水合氧化铝负载的磁性核/壳结构Fe3O4@SiO2纳米颗粒对水中磷的去除及再利用[J]. 环境科学,2016,37(4):1444-1450. Lai Li, Xie Qiang, Fang Wenkan, et al. Removal and recycle of phosphor from water using magnetic core/shell structured Fe3O4@SiO2nanoparticles functionalized with hydrous aluminum oxide[J]. Environmental Science, 2016, 37(4): 1444-1450. (in Chinese with English abstract)
[22] Arami-Niya A, Daud W M A W, Mjalli F S. Comparative study of the textural characteristics of oil palm shell activated carbon produced by chemical and physical activation for methane adsorption[J]. Chemical Engineering Research and Design, 2011, 89(6): 657-664.
[23] Sharma R K , Wooten J B, Baliga V L, et al. Characterization of chars from pyrolysis of lignin[J]. Fuel, 2004, 83(11/12): 1469-1482.
[24] LiJ, Cui L, Zhang X G, et al. Preparation and electrochemistry of one-dimensional nanostructured MnO2/PPy composite for electrochemical capacitor[J]. Applied Surface Science, 2010, 256(13): 4339-4343.
[25] Qiu Y P, Cheng H Y, Xu C, et al. Surface characteristics of crop-residue-derived black carbon and lead(Ⅱ) adsorption[J]. Water Research, 2008, 42(3): 567-574.
[26] 王震宇,刘国成,Monica Xing,等. 不同热解温度生物炭对Cd(Ⅱ)的吸附特性[J]. 环境科学,2014,35(12): 4735-4744.Wang Zhenyu, Liu Guocheng, Monica Xing, et al. Adsorption of Cd(Ⅱ) varies with biochars derived at different pyrolysis temperatures[J]. Environmental Science, 2014, 35(12): 4735-4744. (in Chinese with English abstract)
[27] 兰天,张辉,刘源,等. 玉米秸秆生物炭对Pb2+、Cu2+的吸附特征与机制[J]. 江苏农业学报,2016,32(2):368-375. Lan Tian, Zhang Hui, Liu Yuan, et al. Adsorption characteristics and mechanisms of Pb2+and Cu2+on corn straw biochar[J]. Jiangsu Journal of Agricultural Science, 2016, 32(2): 368-375. (in Chinese with English abstract)
[28] 陈再明,方远,徐义亮,等. 水稻秸秆生物碳对重金属Pb2+的吸附作用及影响因素[J]. 环境科学学报,2012,32(4):769-776. Chen Zaiming, Fang Yuan, Xu Yiliang, et al. Adsorption of Pb2+by rice straw derived-biochar and its influential factors[J]. Journal of Environmental Sciences, 2012, 32(4): 769-776. (in Chinese with English abstract)
[29] 李力,陆宇超,刘娅,等. 玉米秸秆生物炭对Cd(Ⅱ)的 吸附机理研究[J]. 农业环境科学学报,2012,31(11): 2277-2283. Li Li, Lu Yuchao, Liu Ya, et al. Adsorption mechanisms of cadmium(Ⅱ) on biochars derived from corn straws[J]. Journal of Agro-Environment Science, 2012, 31(11): 2277-2283. (in Chinese with English abstract)
[30] Lv H H, Gong Y Y, Tang J C, et al. Advances in preparation and applicaitions of biochar and its composites[J]. Journal of Agro-Environment Science, 2015, 34( 8): 1429-1440.
[31] 徐楠楠,林大松,徐应明,等. 玉米秸秆生物炭对Cd2+的吸附特性及影响因素[J]. 农业环境科学学报,2014,33(5):958-964. Xu Nannan, Lin Dasong, Xu Yingming, et al. Adsorption of aquatic Cd2+by biochar obtained from corn stover[J]. Journal of Agro-Environment Science, 2014, 33(5): 958-964. (in Chinese with English abstract)
[32] 郭平,王观竹,许梦,等. 不同热解温度下生物质废弃物制备的生物质炭组成及结构特征[J]. 吉林大学学报(理学版),2014,52(4):855-860. Guo Ping, Wang Guanzhu, Xu Meng, et al. Structure and composition characteristics of biochars derived from biomass wastes at different pyrolysis temperatures[J]. Journal of Jilin University (Science Edition), 2014, 52(4): 855-860. (in Chinese with English abstract)
[33] Lao C, Zeledon Z, Gamisans X, et al. Sorption of Cd(II) and Pb(II) from aqueous solutions by a low-rank coal (leonardite)[J]. Separation and Purification Technology, 2005, 45(2): 79-85.
[34] Liu Z, Zhang F S. Removal of copper (II) and phenol from aqueous solution using porous carbons derived from hydrothermal chars[J]. Desalination, 2010, 267(1): 101-106.
[35] Wang Y J, Bi Y Y, Gao C Y. The assessment and utilization of straw resources in China[J]. Agricultural Sciences in China, 2010, 9 (12): 1807-1815.
[36] Elaigwu S E, Rocher V, Kyriakou G, et al. Removal of Pb2+and Cd2+from aqueous solution using chars from pyrolysis and microwave-assisted hydrothermal carbonization of prosopis africana shell. Journal of Industrial and Engineering Chemistry[J]. 2014, 20: 3467-3473.
[37] Mohan D, Pittman Jr C U, Bricka M, et al. Sorption of arsenic, cadmium, and lead by chars produced from fast pyrolysis of wood and bark during bio-oil production[J]. Journal of Colloid and Interface Science, 2007, 310(1): 57-73.
[38] Mambo M, Sikwila T L, Edith S, et al. Equilibrium, kinetic, and thermodynamic studies on biosorption of Cd(II) from aqueous solution by biochar[J]. Research on Chemical Intermediates, 2016, 42(2): 1349-1362.
[39] Cheng Q M, Huang Q, Khan S, et al. Adsorption of Cd by peanut husks and peanut husk biochar from aqueous solutions[J]. Ecological Engineering, 2016, 87: 240-245.
[40] Anwar J, Shafique U, Waheeduz Z, et al. Removal of Pb(II) and Cd(II) from water by adsorption on peels of banana[J]. Bioresour. Technol, 2010, 101(6): 1752-1755.
[41] Rahmani A, Mousavi H Z, Fazli M. Effect of nanostructure alumina on adsorption of heavy metals[J]. Desalination, 2010, 253(1/2/3): 94-100.
[42] 郭文娟,梁学峰,林大松,等. 土壤重金属钝化修复剂生物炭对镉的吸附特性研究[J]. 环境科学,2013,34(9): 3716-3721. Guo Wenjuan, Liang Xuefeng, Lin Dasong, et al. Adsorption of Cd2+on biochar from aqueous solution[J]. Environmental Science, 2013, 34(9): 3716-3721. (in Chinese with English abstract)
[43] Sun J, Lian F, Liu Z, et al. Biochars derived from various crop straws: characterization and Cd(II) removal potential[J]. Environmental Ecotoxicology and Safety, 2014, 106: 226-231.
[44] Borcard N, Prost K, Kautz T, et al. Sorption of copper(Ⅱ) and sulphate to different biochars before and after compostng with farmyard manure[J]. European Journal of Soil Science, 2012, 63(3): 399-409.
[45] Oh T K, Choi B, Shinogi Y, et al. Effect of pH conditions on actual and apparent fluoride adsorption by biochar in aqueous phase[J]. Water, Air, & Soil Pollution, 2012, 223(7): 3729-3738.
[46] 王彤彤,马江波,曲东,等. 两种木材生物炭对铜离子的吸附特性及其机制[J]. 环境科学,2017,38(5):2161-2171. Wang Tongtong, Ma Jiangbo, Qu Dong, et al. Characteristics and mechanism of copper adsorption from aqueous solutions on biochar produced from sawdust and apple branch[J]. Environmental Science, 2017, 38(5): 2161-2171. (in Chinese with English abstract)
[47] Adriano D C. Trace Elements in the Terrestrial Environments: Biogeochemistry, Bioavailability, and Risks of Metals[M]. Second Edition, New York: Springer, 2001.
Cd removal from aqueous solution using magnetic biochar derived from maize straw and its recycle
Hu Xueyu, Chen Yaojun, Zhang Shasha , Wang Xiangqian, Li Chengcheng, Guo Xiao
(430074,)
China is a large agricultural country whose output of crop straw is more than 800 million tons, but the effective resource utilization technology of straw is still lacking.Heavy metal pollution in water is also one of the major environmental problems at present. Adsorption methods are widely used in removing heavy metals from water environment due to the simple operation, no need to add a large amount of chemical agents, and low energy consumption.The preparation of biochar from maize straw provides a resource utilization approach for agricultural waste. Besides, maize straw biochar can be used as a new type of environmentally friendly material for the treatment and repair of polluted water. Based on the premise of resource utilization of crop straw wastes in farmland ecosystems, the objective of this study was to remove the heavy metal cadmium (Cd) from water using biochar and realize the recycling of biochar. The original maize straw biochar (MSB) and magnetic maize straw biochar (MMSB) that cracked at 500 ℃ were used as experimental materials for this purpose. Based on the characterization of the original biochar and the magnetic biochar, the adsorption and removal effects of the 2 kinds of biochar on Cd(II) in polluted water and the possibility of recycling biochar were explored. The results showed thatthe adsorption of Cd(II) by biochar increased first and then decreased with the increase of the pH value of the solution, and the adsorption of Cd(II) by MSB and MMSB reached the maximum at the pH value of 5. The maximum adsorption capacities were 27.52 and 33.45 mg/g, respectively. When MSB and MMSB were added at 1.4 and 0.8 g/L, the removal rates of Cd(II) were up to 85.15% and 95.48% respectively,and the difference was significant (<0.05). Langmuir equation could better simulate the isothermal adsorption behavior, the fitting coefficients of MSB and MMSB were both over 0.970 0, and the maximum adsorption capacities at equilibrium reached 26.03 and 43.45 mg/g respectively, which approached the actual values. The kinetic data had a higher fitting degree with the second-order kinetics equation. The theoretical values of equilibrium adsorption capacity of MSB and MMSB were 13.42 and 24.31 mg/g respectively, which had only differences of 2.26% and 3.84% with the actual values respectively. The maximum desorption rates of MSB and MMSB were 41.10% and 29.88%, respectively, and the desorption rates of MMSB were significantly lower than that of MSB. The adsorption process of Cd(II) by biochar was a combination of various mechanisms, mainly chemical mechanism, and the adsorption mechanism mainly includes electrostatic adsorption, ion exchange, surface complexation and cation-π action. The enhancement of adsorption efficiency and fixation ability of magnetic biochar on Cd(II) might be related to its higher pH value, larger specific surface area, and more polar oxygen-containing functional groups. In addition, in the case of external magnetic fields, magnetic biochar could be recovered and reused by magnetic action.The research results are of great significance to promote the resource utilization of agricultural waste and the advancement of heavy metal purification technology in the water environment.
biomass; adsorption; heavy mental; biochar; magnetism biochar; heavy mental removal; aqueous solutions
10.11975/j.issn.1002-6819.2018.19.027
X53
A
1002-6819(2018)-19-0208-11
2018-05-10
2018-08-26
国家自然科学基金项目(41371485);湖北省自然科学基金重点项目(2014CFA116);中央高校基本科研业务费专项资金资助项目(CUG170103)
胡学玉,教授,主要研究方向为土壤环境化学。 Email:huxueyu@cug.edu.cn
胡学玉,陈窈君,张沙沙,王向前,李成成,郭 晓.磁性玉米秸秆生物炭对水体中Cd的去除作用及回收利用[J]. 农业工程学报,2018,34(19):208-218. doi:10.11975/j.issn.1002-6819.2018.19.027 http://www.tcsae.org
Hu Xueyu, Chen Yaojun, Zhang Shasha, Wang Xiangqian, Li Chengcheng, Guo Xiao.Cd removal from aqueous solution using magnetic biochar derived from maize straw and its recycle[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2018, 34(19): 208-218. (in Chinese with English abstract) doi:10.11975/j.issn.1002-6819.2018.19.027 http://www.tcsae.org

