含Sr2+和Bi3+有机杂化体的合成及其光降解罗丹明B
赵新筠, 张柳佳, 蒙俐安, 张吉辉, 蓝孟奇
(中南民族大学 化学与材料科学学院,武汉430074)
能源危机和环境污染已成为全球关注的焦点,利用廉价丰富的太阳光降解环境中的有机污染物是开发新能源及解决环境问题的重要策略. 光催化实质是在太阳光中某些波长光子能量驱动下,使光催化剂体内空穴-电子对分离,并利用空穴、电子对的强氧化还原活性引发一系列氧化还原过程. 为了充分利用太阳光的光能,出现了越来越多的光催化材料,从最早的无机材料TiO2发展到现在用途广泛的多功能材料. 但是其对太阳光的利用率较低,光生电子和空穴容易复合等,使得光催化剂发展受限. 发展廉价、高效的半导体光催化剂用于实际的光催化反应一直是科学工作者研究的重心.
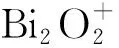
本文在前期研究的基础上通过掺入SrCl2,以期在Cl-引入能改善光催化活性的前提下,研究Sr2+对光催化活性的调控作用. 在保持硝酸铋的量不变时,调控SrCl2物质的量,在对苯二甲酸的N,N-二甲基甲酰胺溶液中,利用溶剂热法制备出不同SrCl2和Bi(NO3)3摩尔比例(分别为5%,10%,30%,50%,80%)的催化剂. 并在紫外可见光下对罗丹明B进行降解来评价催化剂的光催化活性.
1 实验部分
1.1 材料和仪器
1,4-对苯二甲酸、N,N-二甲基甲酰胺(DMF)、Bi(NO3)3·5H2O、SrCl2·6H2O、Sr(NO3)2、NaCl(国药集团化学试剂有限公司),所有试剂均为分析纯.
X射线粉末衍射仪(XRD, D8 ADVANCE型, 德国Bruker), 场发射扫描电子显微镜(SU8000,日本Hitachi),红外光谱仪(Nicloet NEXUS 4700,美国Thermo Scientific), 紫外可见分光光度计(UV-2550,日本Shimadzu),XQ 350 W可调型氙灯电源(上海天晟电子),荧光光谱仪(FL-7000,日本Hitachi).
1.2 催化剂的制备
1.2.1 不同SrCl2和Bi(NO3)3摩尔比催化剂的制备
把Bi(NO3)3·5H2O(0.645 g)超声溶解于20 mLN,N-二甲基甲酰胺中,对苯二甲酸(0.332 g)的15 mLN,N-二甲基甲酰胺进行超声溶解,两者混匀后再分别加入相对于Bi(NO3)30.018, 0.036, 0.106, 0.177, 0.284 g SrCl2·6H2O(摩尔比分别为5%, 10%, 30%, 50%, 80%). 将上述混匀溶液倒入高压反应釜中的聚四氟乙烯内衬里,120 ℃下恒温反应24 h;反应结束后,自然冷却到室温;对其进行抽滤,滤饼依次用乙醇和蒸馏水进行洗涤;100 ℃干燥过夜. 样品依次编号为:5% SrCl2doped, 10% SrCl2doped, 30% SrCl2doped, 50% SrCl2doped, 80% SrCl2doped.
1.2.2 对苯二甲酸锶和对苯二甲酸铋的制备
把SrCl2·6H2O(0.2082 g)或Bi(NO3)3·5H2O(0.645 g)超声溶解于20 mLN,N-二甲基甲酰胺中,对苯二甲酸(0.332 g)的15 mLN,N-二甲基甲酰胺进行超声溶解,将上述溶液混匀后倒入高压反应釜中的聚四氟乙烯内衬里,120 ℃下反应24 h;后处理过程同催化剂制备1.2.1部分. 样品编号为:SrBDC和BiBDC.
1.2.3 20% NaCl及10% Sr(NO3)2掺杂催化剂的制备
把Bi(NO3)3·5H2O(0.645 g)超声溶解于20 mLN,N-二甲基甲酰胺中,对苯二甲酸(0.332 g)于15 mLN,N-二甲基甲酰胺进行超声溶解,两者混匀再加入NaCl 0.016 g,相对Bi(NO3)320%摩尔比例;或者Sr(NO3)2·6H2O 0.028 g,相对Bi(NO2)310%摩尔比例. 将上述溶液倒入高压反应釜中的聚四氟乙烯内衬里,120 ℃下反应24 h;后处理过程同催化剂制备1.2.1部分.样品依次编号为: 20% NaCl doped, 10% Sr(NO3)2doped.
1.3 催化剂紫外可见光下降解RhB
将0.05 g催化剂加入含有50 mL RhB溶液(20 mg/L)的光反应器中,超声分散10 min,超声完成后暗室搅拌吸附2 h达到吸附平衡. 用循环冷凝水进行冷却维持室温条件,用紫外可见光对其进行光降解(光源为350 W的氙灯). 在指定的时间间隔内每次取样3 mL . 高速离心10 min (8000 r/min)后,上清液通过0.45 μm的有机滤膜进一步除掉残余的催化剂. 滤液用紫外可见分光光度计在553 nm波长处测量吸光度.
2 结果与讨论
2.1 红外光谱的表征
不同SrCl2摩尔比掺杂的催化剂及其对照对苯二甲酸锶(SrBDC)的红外光谱图见图1.对苯二甲酸的羰基特征吸收峰有1683,1286 cm-1,与Bi3+配位后形成对苯二甲酸铋的特征吸收峰在1532,1382 cm-1处[5]. 由图1可见:对苯二甲酸锶(SrBDC)的羰基的特征吸收峰在1532,1396 cm-1的波数处,说明已经发生了配位反应. 掺杂80% 和50% SrCl2的催化剂特征吸收峰分别是1532, 1395 cm-1和1549, 1394 cm-1,均与SrBDC的吸收峰相接近. 掺杂比例为5% 和30% 的吸收峰分别是1520, 1384 cm-1和1508, 1391 cm-1. 掺杂比例为10% 的吸收峰是1508, 1385 cm-1. 这表明在合成的催化剂中,SrCl2,Bi(NO3)3均参与和对苯二甲酸的羧基配位. 羰基的特征吸收峰变动在1384~1396 cm-1及1508~1549 cm-1之间.
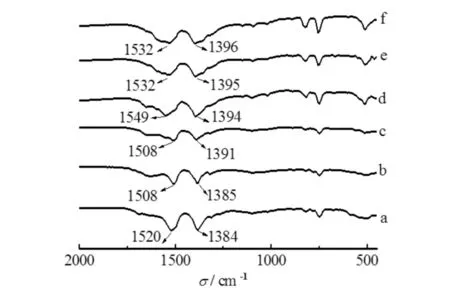
a)5% SrCl2 doped; b) 10% SrCl2 doped; c) 30% SrCl2 doped; d) 50% SrCl2 doped; e) 80% SrCl2 doped; f) BiBDC图1 不同SrCl2摩尔比掺杂催化剂的红外光谱图Fig.1 IR spectra of doped catalysts with different molar ratio of SrCl2
2.2 SEM表征
不同SrCl2摩尔比掺杂的催化剂及对苯二甲酸锶的SEM图见图2. 由图2可知:这些掺杂体均无规整形貌,但对苯二甲酸铋显示棒状[5].掺杂5% SrCl2的催化剂以棒状为主带有少量块状;掺杂10%,30%,80% SrCl2的催化剂有棒状也有块状;掺杂50% SrCl2的催化剂为块状;SrBDC催化剂为一个不规则的立体状.

a) 5% SrCl2 doped; b) 10% SrCl2 doped; c) 30% SrCl2 doped; d) 50% SrCl2 doped; e) 80% SrCl2 doped; f) SrBDC图2 不同SrCl2摩尔比掺杂催化剂SEM图Fig.2 SEM images of doped catalysts with different molar ratio of SrCl2
2.3 XRD表征
不同SrCl2摩尔比掺杂的催化剂的XRD图谱见图3. 由图3可见: 掺杂SrCl250%和80%时(见图3e和3f),明显表现为BiOCl的特征峰(PDF#01-0060),说明形成了对苯二甲酸铋或锶和BiOCl的杂合体. 对于BiBDC 和SrBDC 而言,二者显示出了明显不同的衍射峰.

a) BiBDC; b)5% SrCl2 doped; c) 10% SrCl2 doped; d) 30% SrCl2 doped;e) 50% SrCl2 doped; f) 80% SrCl2 doped; g) SrBDC图3 不同SrCl2摩尔比掺杂催化剂的XRD图Fig.3 XRD patterns of doped catalysts with different molar ratio of SrCl2
2.4 固体漫反射表征
不同摩尔比SrCl2掺杂催化剂的紫外可见固体漫反射结果如图4. 由图4可见:各个掺杂催化剂均在紫外区域有吸收,吸收边带大约在350 nm. 掺杂的催化剂可在紫外光下进行激发.
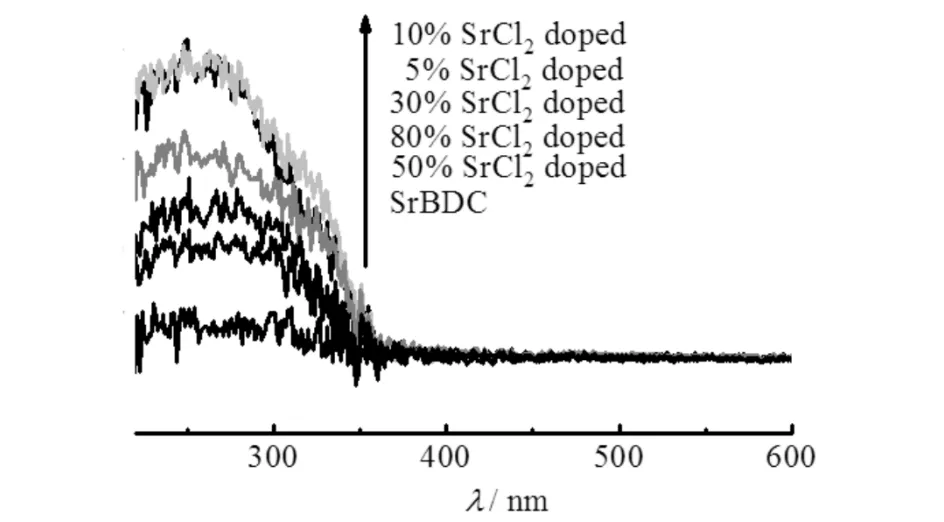
图4 不同SrCl2摩尔比掺杂催化剂的紫外-可见固体漫反射图Fig.4 UV-vis DRS of doped catalysts with different molar ratio of SrCl2
2.5 荧光光谱表征
不同SrCl2摩尔比掺杂催化剂在激发波长固定为317 nm时的荧光光谱图见图5. 由图5可见:10% SrCl2掺杂的对苯二甲酸铋的荧光丰度最小,作为参照样品BiBDC 和SrBDC均有很高的丰度(本文未列),说明光生电子和空穴在催化剂中能有效地被分离.
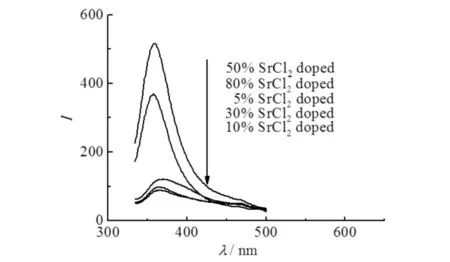
图5 不同SrCl2摩尔比掺杂催化剂的荧光光谱图Fig.5 Fluorescence (FL) spectrogram of doped catalysts with different molar ratio of SrCl2
2.6 催化剂紫外可见光降解RhB的活性研究
由于制备的催化剂在紫外区有强的吸收,而RhB是有色染料,在可见光区可被敏化,对所合成的催化剂进行了紫外可见光下降解RhB的活性评价.以RhB吸光度对浓度作图,可得到光度分析的校准曲线(见图6). 溶液中RhB浓度在0.3125~10 mg/L内符合线性关系(y= 0.178x,R2=0.9992).20 mg/L RhB在催化剂存在下经2 h暗室吸附后,溶液中留存RhB 浓度c0在该线性范围内. 故可以利用吸光度变化来衡量催化剂吸附后光催化降解时RhB的浓度变化.

图6 RhB水溶液吸光度和浓度的标准曲线Fig.6 Standard curve of RhB aqueous solution (absorbance versus concentration)
不同摩尔比SrCl2掺杂催化剂在紫外可见光下降解RhB结果见图7(c0为暗室吸附后溶液中RhB的浓度;c为光照tmin时RhB的浓度, RhB自身降解忽略不计).
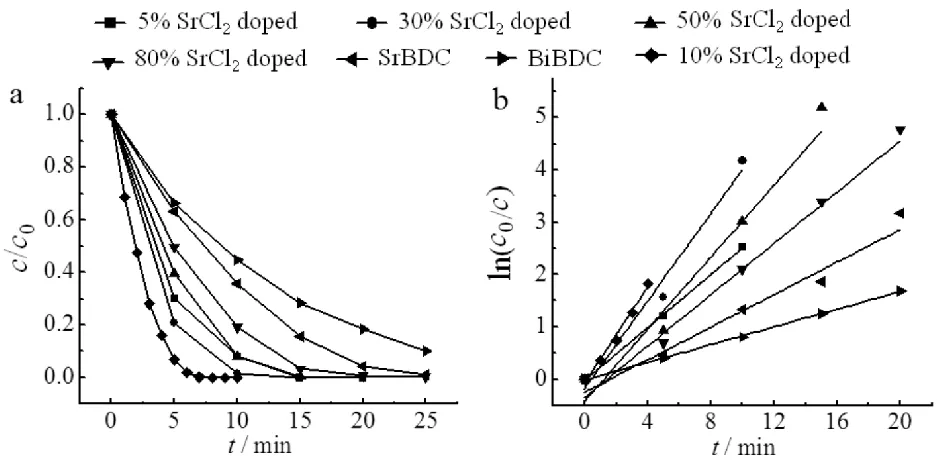
a) c/c0随时间变化曲线; b) ln(c0/c)随时间变化曲线图7 不同SrCl2摩尔比掺杂催化剂在紫外可见光下对的RhB降解Fig.7 Degradation of RhB over doped catalysts with different molar ratio of SrCl2 under UV-Vis light irradiation
由图7可见:SrCl2掺杂含量不同,催化剂的光降解活性差别很大.图7a中,10% SrCl2催化剂降解活性优异,约7 min完全降解RhB. 为定量评价催化剂活性强弱,依据其在低浓度下紫外可见光降解RhB符合准一级动力学方程ln(c0/c)=kt,作ln(c0/c)对时间t图,结果见图7b,其速率常数k见表1. 由表1可见:含10%SrCl2的催化剂降解速率常数最大,为0.46 min-1,说明SrCl2的掺入能大大增加紫外可见光下对RhB的降解.
表1 不同SrCl2摩尔比掺杂催化剂在紫外可见光下降解RhB的速率常数k
Tab.1 Rate constantsk of RhB degradation of doped catalysts with different molar ratio of SrCl2under UV-vis light irradiation
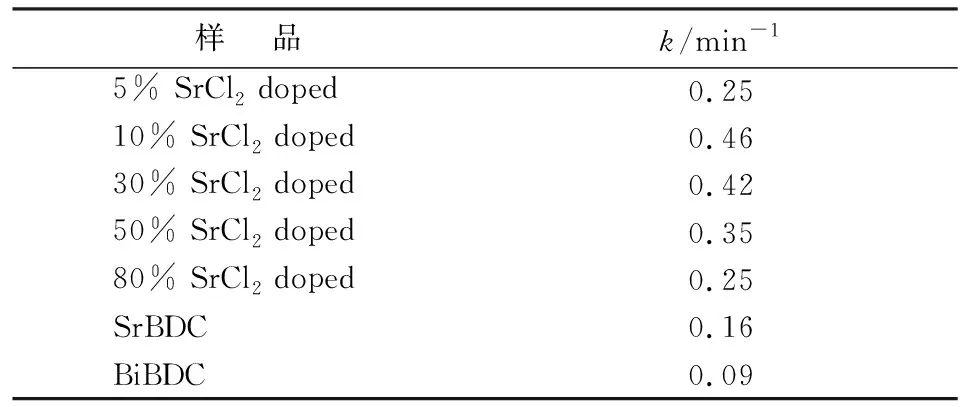
样 品k/min-15% SrCl2 doped0.2510% SrCl2 doped0.4630% SrCl2 doped0.4250% SrCl2 doped0.3580% SrCl2 doped0.25SrBDC0.16BiBDC0.09
为了粗略比较含10% SrCl2催化剂中Sr2+和Cl-对催化活性的影响,采用具有相同Cl-浓度(以20% Cl-摩尔比计)的NaCl和Sr2+浓度(以10%摩尔比计)的Sr(NO3)2进行掺杂,探讨了用20% NaCl和10% Sr(NO3)2掺杂的杂化体在同样条件下对RhB的降解,结果见图8. 由图8可见:10% Sr(NO3)2掺杂的杂化体比对苯二甲酸铋(BiBDC)的活性高,说明Sr2+的掺入能增强光降解活性;20% NaCl的掺入也能大大增强光降解活性. 说明Sr2+和Cl-均能增强光降解活性,但Cl-起主要作用,Sr2+和Cl-相比,促进作用较弱.随着Sr2+和Cl-浓度的增加,对染料的降解活性下降. 对50%和80% SrCl2掺杂的催化剂而言,尽管有光催化活性好的BiOCl的协同参与,但其光降解的活性反而下降. 因此,由于Sr2+和Cl-的协同作用,10% SrCl2掺杂的杂化体表现出较高的光催化活性,归因于催化剂在紫外区域有好的光吸收且光生电子和空穴能很好地分离.
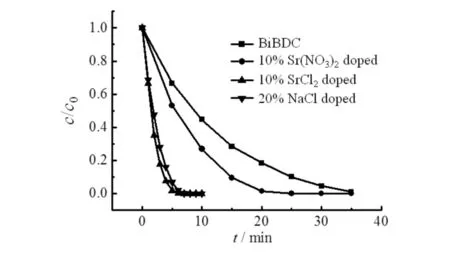
图8 Sr2+和Cl-对紫外可见光降解罗丹明B的影响 Fig.8 Effects of Sr2+ and Cl- on degradation of RhB with UV-vis light irradiation
3 结语
本文采用溶剂热法,用不同摩尔比的SrCl2和Bi(NO3)3在N,N-二甲基甲酰胺溶液中与对苯二甲酸合成了含5%,10%,30%,50%,80%的 SrCl2掺杂催化剂,并考察了其在紫外可见光下对RhB的降解活性. 结果表明:这些催化剂均显示出很好的光催化效果. 10%SrCl2掺杂的催化剂的降解活性优异,降解速率常数k为0.46 min-1,高活性归结于该催化剂在紫外光区域有好的光吸收以及有效的光生电子和空穴分离. 其中Sr2+掺杂在一定程度上增强了催化剂的光催化作用,双金属离子能调节催化剂的光催化性能. 因此SrCl2掺杂的对苯二甲酸铋催化剂在紫外可见光下可以光氧化有机染料,在废水处理及有机物的氧化制备精细化学品方面有广阔的应用前景.

