锂电池研究中的电导率测试分析方法
许洁茹,凌仕刚,王少飞,潘 都,聂凯会,张 华,邱纪亮,卢嘉泽,李 泓
锂电池研究中的电导率测试分析方法
许洁茹,凌仕刚,王少飞,潘 都,聂凯会,张 华,邱纪亮,卢嘉泽,李 泓
(中国科学院物理研究所,北京 100190)
锂电池活性电极材料的锂离子电导率、电子电导率以及电解质的锂离子电导率与锂电池的动力学行为密切相关。电导率的测试分析有助于理解材料的电化学性能,常用的方法包括直流法、交流阻抗法和直流极化法等。本文根据电解质材料和活性电极材料的不同导电特性,分类介绍了电导率测试选取的方法、原理、设备、测试流程和注意事项,并结合具体案例阐述数据的分析。
电导率;直流法;交流阻抗法;直流极化法;锂电池
1 电子输运和离子输运的基本参数和宏观传输模型
电子和离子在固体中的输运问题分别是半导体物理和固体离子学的核心研究内容,对这部分内容感兴趣的读者可以参阅相关的专著和综述类文 献[1-2]。本文对载流子输运的基本参数和宏观传输机理进行表述,以方便后文的说明。
1.1 载流子输运的基本参数[3-6]
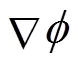
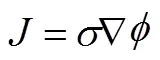
实验测量值为物体的电阻,正比于其长度,反比于其截面积
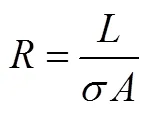
式中,为电阻,Ω;为导体长度,cm;为导体截面积,cm2。从而有
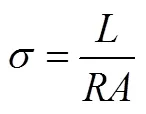
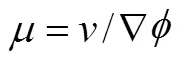
电流密度和材料的载流子的浓度、电荷量和迁移速度有关

式中,为载流子浓度,mol/cm3;为载流子所带电荷量,C。
从而得到
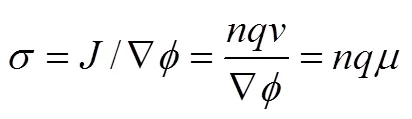
对于金属导体来说,载流子是自由电子,即为电子电量;对于离子导体,载流子是可运动的离子,为运动的离子所带的电量;而对于电子离子混合导体,其在电场中产生的总电流密度等于各种载流子所产生的分电流之和,即
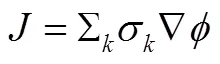
因此其总电导率等于各种载流子的电导率 之和

由此定义迁移数(transference number):某一种载流子的电导率在总电导率中所占的份额

活性电极材料希望电子和离子的输运速度都比较高,对于电子和离子迁移数的比值没有严格要求。对于电解质,要求其为电子绝缘体(电子迁移数e<0.01),以防止内部短路和自放电;此外希望电解质材料中Li+的输运对电流起主要贡献,也即Li+的迁移数尽可能的高。无机固态电解质多数情况下能够满足这些要求;而对于聚合物固态电解质或液态电解质,一般Li+的迁移数在0.2~0.4,阴离子的迁移占据较大比例,因而对离子电流产生了较大贡献,这会引起在电极侧的极化,增大了界面的传输电阻。
离子的传输特性同样可以用扩散系数来描述,对应于化学势梯度驱动的载流子扩散行为。
离子在电场下的迁移率与扩散系数遵循爱因斯坦关系

由式(10)同样可以得到电导率与扩散系数的关系,即Nernst-Einstein 方程
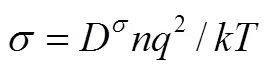
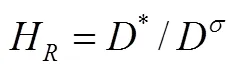
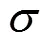
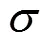
1.2 载流子的宏观传输机理
导电行为的研究可从宏观和微观两个尺度上来叙述。宏观上,一般考察材料的电导率随温度的变化关系及其符合的经验方程;微观上,主要从粒子尺度探究载流子的迁移是如何进行的。
(1)电子的宏观传输机理[7]
一般来说,半导体的电子电导率在一定温度范围内,随温度的变化关系遵循Arrhenius关系
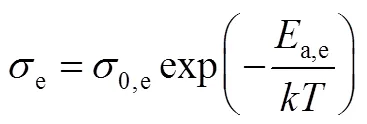
式中,e为电子电导率,通过直流极化法或交流阻抗法得到;0,e是指前因子;a,e是电子传输的活化能;是Boltzmann常数;是温度。
(2)离子的宏观传输机理[4-5,8]
晶体中离子的输运主要依靠点缺陷进行,点缺陷主要为Frenkel缺陷与Schottky缺陷,缺陷使得晶体中存在一定浓度的空位与间隙离子,由于离子的热振动,离子有一定几率跃迁到邻近的间隙位或空位,从而实现离子的迁移。
在不发生相变的温度范围内,离子电导率可以表示为
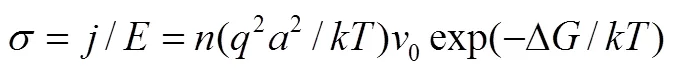

在Frenkel缺陷的固体中,则电导率可进一步表示为

在Schottky缺陷的固体中,则电导率可进一步表示为:
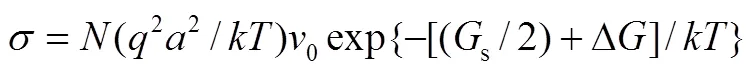
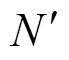
对以上两个公式进行进一步总结可得到Arrhenius 类型的公式
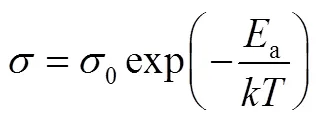
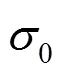
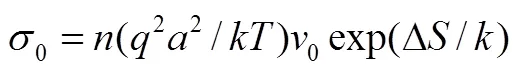
0对于Frenkel缺陷与Schottky缺陷分别对应于不同的形式,可以分别从式(15)、式(16)进一步推得,不再赘述。
此外,不同于上述有序晶体的Arrhenius行为,对于无序的玻璃态和聚合物、也包括某些锂离子与“空位”无序占据的固体电解质,通常可以用基于准热力学模型(如自由体积模型或构型熵模型)的半经验Vogel-Tamman-Fulcher(VTF)方程来更好地拟合
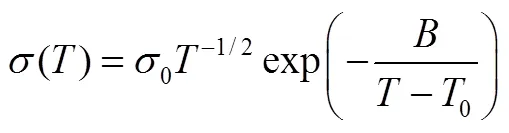

2 电导率测试方法
活性材料的离子输运、电子输运以及电解质材料的离子输运决定了锂电池的倍率性能,因而研究锂电池中各部分材料离子、电子的动力学性能具有重要意义。以离子的输运为例,除了示踪原子扩散、同位素标记-二次离子质谱法、固体核磁共振(SS-NMR)、中子衍射等直接方法,还有直流法(DC)、交流阻抗法(AC impedance)、直流极化法(DC polarization)等通过电导率表观结果借以表征的间接方法。这里主要关注电学测试手段,对锂电池中重要的电解质和电极材料电导率测试的常用方法进行简要回顾。
电导率的测试方法有两个关键点,一是测试装置的设计和组装;二是测试方法的选择和组合。以上需要根据被测材料的物理化学性质和测试内容设计方案。
2.1 测试装置的构建和电极选择
最常规的测试装置将测试材料夹在两片测试电极之间,构成一个三明治结构,如图1所示。而对于薄膜材料,则必须设计合适的微电极,一般分为两种:三明治结构和面内电极结构(叉指电极、平行条状电极)。具体的电极结构设计将在后续具体实验过程中详细说明。
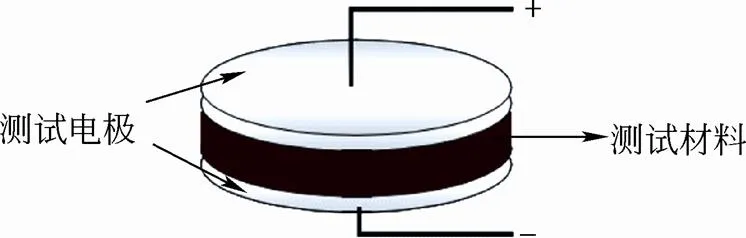
图1 测试电极示意图
构成测试装置的极片有3类,可逆电极(reversible electrode)、全阻塞电极(blocking electrode)和半阻塞电极(semi-blocking electrode)。可逆电极和全阻塞电极对应于传统电化学中交换电流很大的理想不极化电极和交换电流接近于零的理想极化电极,半阻塞电极常用于混合导体中离子电导率和电子电导率的区分。利用这些电极可以组成不同类型的测试装置,以满足不同导电特性材料的不同测试需要。不同类型电极的特点列于表1,在锂电池中,常用金属锂作为电子、离子全导通的可逆电极,不锈钢片(SS)、Au、Ag、Pt、碳片等电极作为离子阻塞电极,LiI、PEO(掺杂LiI)等作为电子阻塞电极。
图2给出3种测试离子电导率和电子电导率的电极构筑方式。BUSCHMANN等[10]分别用金属锂可逆电极和Au离子阻塞电极作为测试电极进行交流阻抗谱测试[图2(a)],得到材料的离子电导率和电子电导率之和;图2(b)用金属锂作为测试电极(170 ℃退火处理,保证测试电极和测试材料之间的良好接触)进行四电极直流法测试,得到总电导率和交流阻抗谱的结果基本一致;图2(c)一侧用Au电极,一侧用金属锂电极,通过Hebb-Wagner直流极化,混合离子和电子的高瞬态电流很快下降,并最终达到稳定的电子电流,从而确定电子和空穴的电导率;之后,由交流阻抗谱得到的总电导率和直流极化法得到的电子电导率,用迁移数的定义[式(9)]计算电子迁移数。

表1 不同电极类型及特点[9]
2.2 离子电导率和电子电导率的测试方法
这里主要介绍直流法(IV测量、伏安特性测试)、交流阻抗法、直流极化法3种方法,结合不同的测试电极,可以有不同的应用。实现以上功能的设备众多,如Zahner IM6、Solartron、Autolab、辰华等电化学工作站。各种电化学工作站可以实现的频率范围、直流电压和直流电流的范围和精度,以及基本功能总结于表2中。

图2 不同电极构筑方式的示意图(a)用两个金属锂电极作为测试电极的交流阻抗谱测试;(b)用四金属锂电极作为测试电极的直流电导率测试;(c)一侧为金属锂电极、一侧为Au离子阻塞电极的Hebb-Wagner型电子电导率测试[10]
Fig.2 Scheme of different electrode arrangements (a) for ac conductivity measurements with two lithium electrodes; (b) for dc conductivity measurements with four lithium electrodes and; (c) for Hebb-Wagner type electronic conductivity measurements with one lithium and one Li ion blocking gold electrode[10]
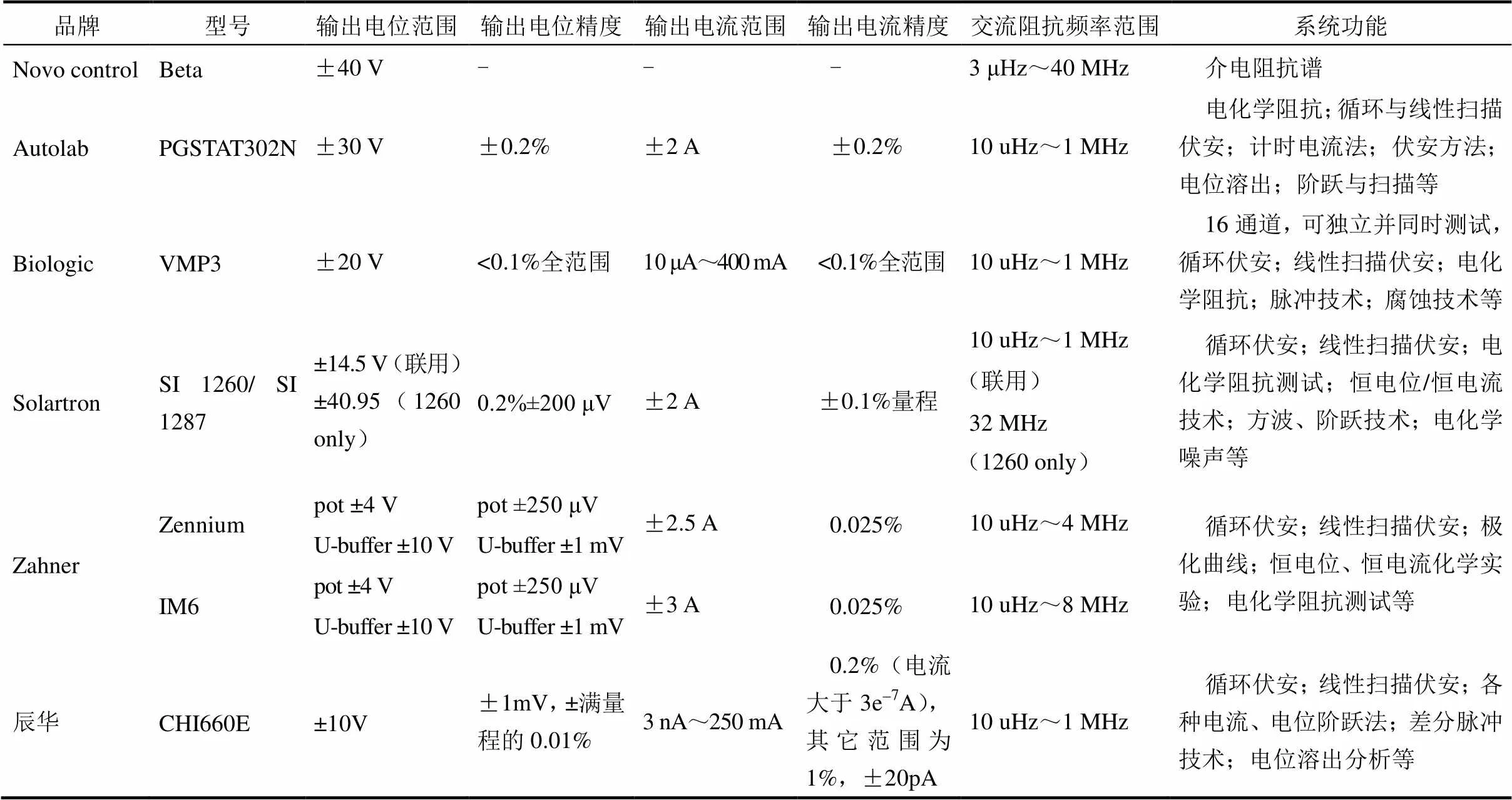
表2 常用电化学工作站的特点及功能[11]
2.2.1 直流法
直流法是一种常规的电化学测试方法,根据欧姆定律=/,通过测量导体的直流电流和电压降计算电阻,进而由几何尺寸计算电导率。当有离子参与导电时,直流法的应用要求测量电极对混合导体有较好的可逆性,但此时由于电荷转移电阻的引入产生了一定误差。因而,直流法最常选择离子阻塞电极,应用于电子电导率的测试。
(1)二探针和四探针的比较
对于总电导率较高的材料,例如石墨等负极材料,此时常规的两电极直流法测试中,导线电阻和接触电阻对于样品电阻已经不可忽略,必须使用直流四探针法精确测定导体电阻。图3为两探针法和四探针法的电极构造和等效电路图,两探针法中的两根探针既作电流探针,又作电压探针,因而测得的电压并非真正半导体的电压,而是包含接触电阻和注入效应的电压。在电流探针之间再加上两根探针,专门测量半导体的电压,则在很大程度上消除了接触电阻的影响。此外,为了进一步消除电压探针本身的接触电阻和注入效应,还采用补偿法来测量电压,使电流不必通过电压探针,从而测试的半导体电阻较为准确。

图3 (a)两探针法和四探针法的电极构建;(b)两探针法和四探针法的等效电路
(2)直流四探针法
直流四探针法可以通过构建四电极体系,再用电化学工作站施加直流源实现;或直接使用四探针电阻率测试仪。四探针电阻率测试仪的电极是离子阻塞电极,因而测试结果为材料的电子导电率。在锂电池的研究和应用中,四探针直流法被用作测试电极材料粉体、薄膜等的电子电导率。
(i)直流四探针法的测试原理
四探针测试法如图4(a)所示,在半径较大的均匀试样上,四根探针位于样品中央,电流从探针1流入,从探针4流出,则可将1和4探针认为是点电流源。距离点电流源点的电位为式(20),从而得到2、3探针的电位差为23[式(21)],得到样品的电阻率为式(22)。
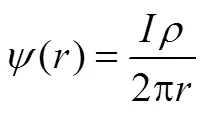
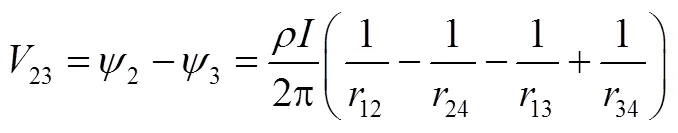
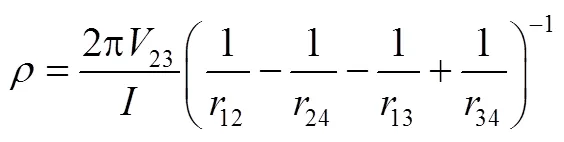
实际测量中,最常用的是直线型四探针[图4(b)],即四根探针的针尖位于同一直线上,并且间距相等,设12=23=34=,则有

通过测试流过1、4探针的电流以及2、3 探针间的电位差23,代入四根探针的间距求出该样品的电阻率。式(23)在半无限大样品的基础上导出,其使用条件必须满足样品厚度及边缘与探针之间的最近距离均大于四倍探针的间距。如果不满足此条件,则需引入适当的修正系数。薄膜样品的样品厚度比探针间距小很多,而横向尺寸相当于无穷大,如图4(c)所示。这时从探针1流入和从探针4流出的电流,其等位面近似为圆柱面,高为。任一等位面的半径设为,类似上面对半无穷大样品的推导,很容易得出当12=23=34=时,薄膜样品的电阻率为
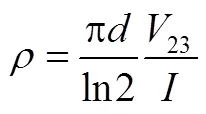
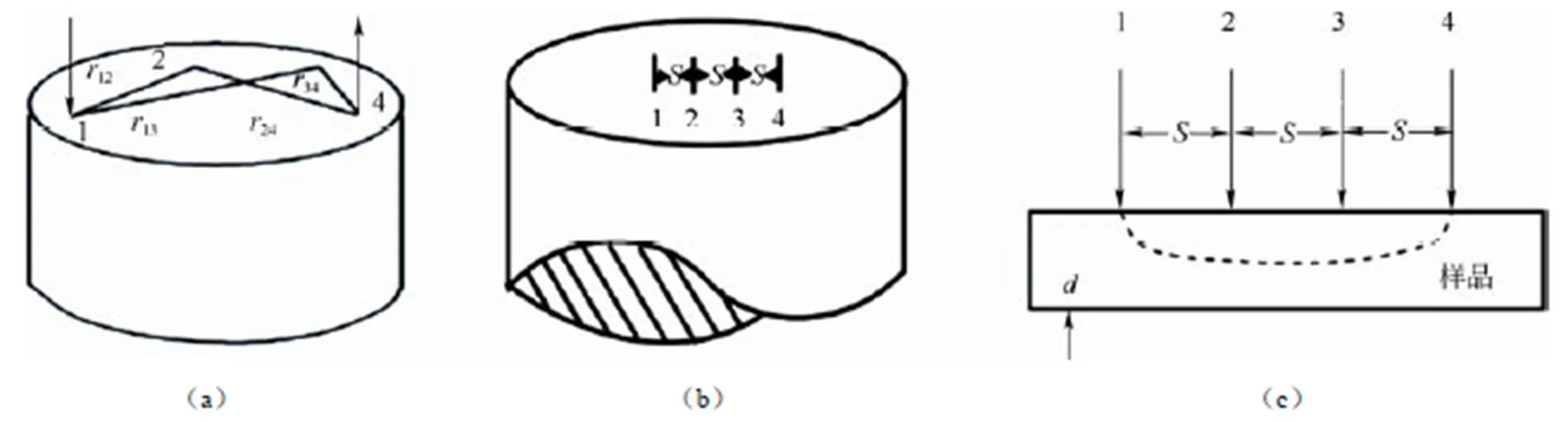
图4 (a)任意位置的四探针测试原理图;(b)直线型四探针测试原理图;(c)薄膜样品四探针测试的原理图
(ii)直流四探针法的测试设备
直流四探针法的基本实验装置通常包括四探针装置、恒流源和电压差计3个部分。图5为MISUBISHI CHEMICAL ANALYTECH公司的Loresta-GX MCP-T700低电阻率测试仪(测试范围为10-4~ 107Ω),可以测得Ω、Ω/□、Ω·cm、S/cm四种相互转换的数据,并且配置四探针修正系数计算软件。采用针距恒定的镀金弹簧探针,且与测试样品接触的压力恒定。适用于电极的电阻测试,通过选择不同探针测试多种类型的样品。

图5 (a)Loresta-GX MCP-T700低电阻测试仪实物图;(b)适用于不同样品类型的探针
Loresta-GX MCP-T700有电阻率修正系数(resistivity correction factor, RCF)计算软件,RCF 通过输入样品形状(正方形或圆形)、样品尺寸和测试位置来确定。确认RCF之后,电阻测试仪得到式(25)的面电阻S(Ω/□)和式(26)的体积电阻率V(Ω·cm)。
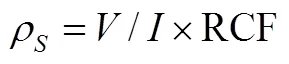
(26)
在文献中,四探针法常用于确定电池极片的电子电导的绝对值,这是由于四探针法消除了探针和样品(压实的片或涂层)之间的接触电阻。但是有两点需要注意:第一,大部分四探针方法选择将电极材料的浆料涂覆薄层或适当厚度于绝缘基底上,而非铝箔等集流体材料。这种在绝缘基底上的涂层是为了避免基底方向的支流,从而精准测试电极材料的电导。如果基底为集流体材料,即便通过调节探针距离等方法避免支路电流,所得到的结果仍只能描述涂层的电阻,因为电流转移的方向和涂层平 行,忽略了基底和涂层的界面电阻,而不是极片的真实情况。其次,电池实际应用中的电极涂层相对较厚(60~150 μm),四探针法仅得到部分涂层的电阻贡献,而忽略了极片的涂层梯度,无法全面表征极片电阻值。因而,研究者为了测试极片的真实情况(集流体+涂层),做出很多测试方法的尝试。WESTPHAL等[12]针对双面涂覆极片设计了两探针测试方法[图6(a)],该方法测得的体相电极电阻包括:探针的体相电阻b,p,探针和涂层的接触电阻c,p/c,涂层的体相电阻b,c,涂层和集流体的接触电阻c,cc/c,集流体的体相电阻b,cc[式(27)]。
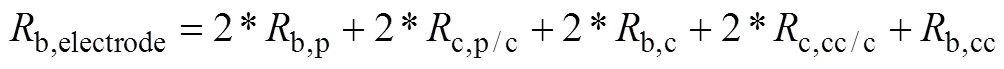
(27)
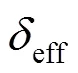
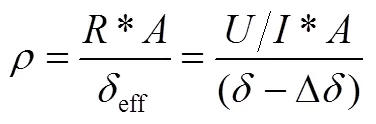
测试参数对测试的电极电阻产生影响,主要是施加的电流和施加的压强。施加的电流对于高电阻材料(LFP极片)影响较小,加载电流较小时就能得到稳定结果,而对于低电阻材料(石墨电极),加载电流相对较高才能得到稳定结果,最终对所有测试电极选择10 mA的加载电流以实现比较稳定的测量结果。加载压力对于测试结果也有重大影响:压力增大使得接触面的接触更为紧密,从而减小接触电阻;此外减小了电极材料颗粒的空间,缩短或产生了新的电子传输路径。350 kPa的压强是一个较好的选择,与真实极片的条件相近,并得到相对稳定的测试结果。
图6 (a)两探针法测试双面涂覆电极的相对电阻;(b)两探针法测试电极电阻的示意图[12]
Fig.6 (a) relevant resistances of a double-side coated electrode at any two-point probe measurement; (b) measurement setup[12]
在极片电子电导率测试中,还需要考虑测试时是否加入电解液的问题。在电解液加入的情况下,其测试更加接近实际应用情况下的电极电阻。在电解液的浸润下,黏结剂溶胀,活性物质、导电添加剂、集流体之间的接触更加紧密。但需要设计测试装置,保证测试过程中的密封性,仍需进一步的 研究。
对于粉末活性材料,则将粉末电阻测试系统MCP-PD51[图7(a)]和Loresta-GX MCP-T700低电阻测试仪连接进行测试。粉末电阻测试并不是对单个粉末颗粒进行测试,而是对于整体聚集的粉末样品。聚集的粉末在圆筒和活塞体系之中,通过与油泵相连的活塞加压。如图7(b)所示,施加的压强小,则样品的密度比较低,从而粉末颗粒之间接触不好,导致低电导率/高电阻率;压强大,则相反。因此,需要特别注意,粉末样品的电阻率/电导率随着所施加的压强持续变化。此外,由于水分改善电导率,测试环境的湿度同样影响测试。基于以上原因,粉末样品电阻率的表述通常并非单一的值,而是通过电阻率对应密度(压强)的图表[图7(c)]。
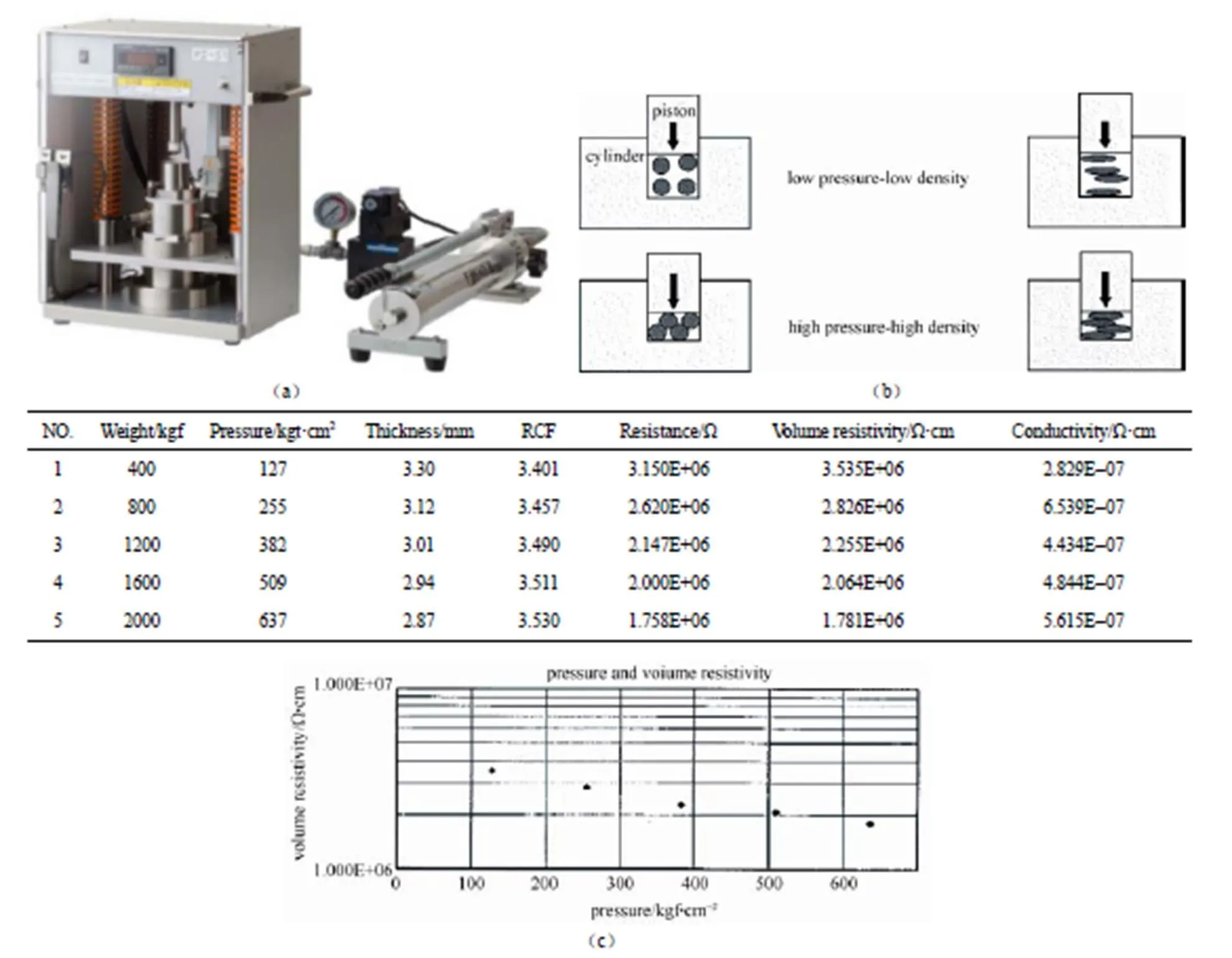
图7 (a)粉末电阻率测试系统MCP-PD51的实物图;(b)粉体密度与所施加压力的关系; (c)锂离子电极材料的测试结果
2.2.2 交流阻抗法
(1)交流阻抗法概述[13-14]
交流阻抗法是在体系处于平衡状态(开路状态)或者某一稳定的直流极化条件下,通过输入不同频域内(或时域内)的小幅度正弦波电压(或电流)交流信号,对所测量体系响应的频谱信号进行分析,进而得出研究体系在不同频率区域内(或时间区域内)的阻抗。其分类通常根据所采用的激励函数的自变量,频域阻抗谱施加以频率为自变量的小幅度正弦激励;而时域阻抗谱则以时间作为自变量记录时间域中的扰动和相应,并且可以通过时间-频率转化技术(拉普拉斯或傅里叶变换)来提取阻抗对应频率的函数。
需要强调的是,交流阻抗法和电化学阻抗谱技术的测试和分析手段基本一致,但并不等同。交流阻抗法运用于线性电学系统,满足阻纳的3个基本条件。第一,因果性条件:输出的响应信号只是由输入的扰动信号引起的。第二,稳定性条件:扰动不会引起系统内部结构发生不可逆的变化,当扰动停止后,系统能够恢复到原来状态,或者近似恢复到原来状态。第三,线性条件:输出的相应信号与输入的扰动信号之间存在线性关系。当用小幅度的正弦波电势信号对系统扰动,电势和电流之间可近似看作呈线性关系。而电化学阻抗谱则是将交流阻抗法引入电化学测试,将电荷转移、传质过程、SEI 的生长演变等电化学过程等效为电子元件组成的电路进行分析。但是由于电化学体系非平衡线性,需要通过电极系统状态的控制和保持控制参量不变 来满足阻纳“因果性、稳定性和线性”的3个基本条件。
(2)交流阻抗法的应用
交流阻抗法可用于测试锂电池中材料的导电性:包括电极材料(粉末、单颗粒、多孔电极、薄膜电极)、电解质材料(液体电解质和隔膜、氧化物电解质、硫化物电解质、聚合物电解质、无机薄膜电解质等)等。
(3)交流阻抗法的测试设备
用于交流阻抗法测试的设备众多,如表2所示。在选择电化学工作站时,要考虑测试对象的特性。对具有电压的体系进行电化学阻抗谱研究时,需选择有源电化学工作站(如Autolab、IM6),而不适用于无源电化学工作站(如Novo control),否则会损伤设备,破坏样品。而对无电压的体系进行交流阻抗谱研究时,则有源、无源电化学工作站都可以考虑。通常认为无源电化学工作站适合高阻抗体系测试,有源电化学工作适用于低阻抗体系测试,具体测试还要根据测试频率范围、电阻范围、偏压范围等需求的情况灵活选择[11]。除了设备的选择,测试时还需考虑测试环境的影响,电磁屏蔽对于高频电感干扰的排除不可缺少,此外还要保证测试时湿度、温度的相对一致。
2.2.3 直流极化法
固体材料中的载流子,不但包括锂离子,还包括电子与空穴。固体电解质需要材料具有高的离子电导率,极低的电子电导率,以增加电池的倍率性能及减少电池的自放电;电极材料需要材料同时具有较高的离子电导率和电子电导率。因此对于电解质和电极材料的研究需要区分离子电导率与电子电导率的大小,对此,直流极化是常用的一种方法。文献中常用的直流极化法包含:Hebb-Wagner直流极化、ITIC直流极化、恒电流直流极化等。
(1)Hebb-Wagner直流极化
Hebb-Wagner直流极化采用不对称电极,得到电子电导率信息。其电极形式为:可逆电极(=0)︱固体电解质︱不可逆电极(=),在电极两侧施加直流电压,开始瞬间,离子在电解质中从=0迁移至=,同时电子与空穴发生迁移。由于一侧电极为阻塞电极,离子电流随时间衰减,并趋近于零。在最终稳态时,电流仅由电子与空穴的迁移产 生[15-16]。Wagner认为在固体电解质中离子和电子都处于电中性的局部平衡态。根据缺陷平衡,假定电子的迁移数与浓度无关,则稳态电流密度与电子的导电性的关系如下文所述[16]。
当迁移离子为阳离子时
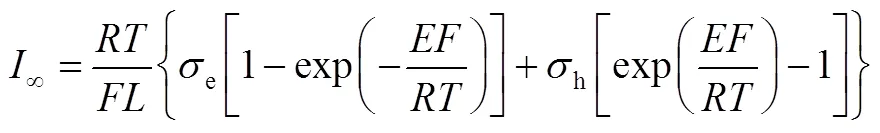
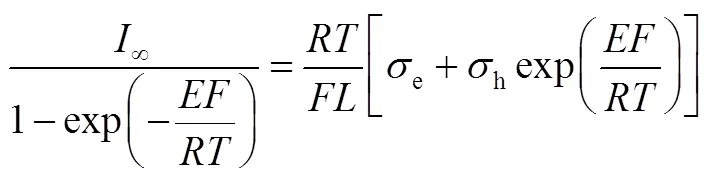
当迁移离子为阴离子时

(2)瞬态离子电流法(ITIC,isothermal transient ionic current)结合离子阻塞电极[17-18]
ITIC直流极化结合离子阻塞电极的测试方法有两种方式,如图8所示。

图8 (a)initial ITIC和(b)second ITIC两种测试方法的示意图及其关系[19]
(i)initial ITIC
在样品两侧施加一个小直流偏压,样品中的离子因为受到电场力的驱动而单向运动,且由于使用离子阻塞电极,运动的离子会在电极的一端逐渐减速,聚集在一起。这个过程体现在测得的电流响 应上的变化就是,随着偏压的施加,先是有一段 指数衰减的电流响应,随后电流响应趋于一个稳定值[20][图9(a)],其中指数衰减的部分对应的便是离子运动的电流响应。假设施加偏压大小为,薄厚为,那么电流密度和偏压施加时间的关系可以描述为
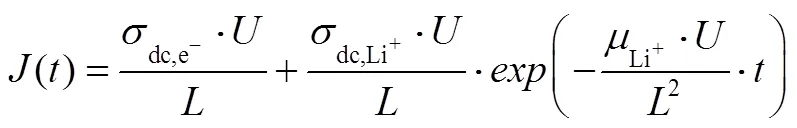
(ii)second ITIC
先在一个初始样品上施加一个偏压一段时间,也即完成initial ITIC过程后,大部分离子都聚集在某一侧电极,体相中不存在离子电流,由于并未等离子在样品中分布均匀,会有较强的空间电荷效应,引起平均电压降eff。这时改变偏压极性,聚集在电极一侧的离子开始向体相运动,离子电流增大;离子电流迁移到另一侧的电极重新聚集,导致体相载流子浓度降低,电流降低[21][图9(b)]。按照这个过程,体相中的离子电流出现峰值,其出现的时间则对应了离子从一侧电极迁移到另一侧电极所需的时间,由此计算出离子的迁移率


图9 (a)Initial ITIC[20];(b)Second ITIC两种测试方法的瞬态离子电流[21]
Fig.9 The isothermal transient ionic current of (a) initial ITIC[20]; (b) second ITIC[21]
(3)恒电流直流极化
除了常用的Hebb-Wagner直流极化和ITIC直流极化和离子阻塞电极结合外,还有文献使用恒电流直流极化。AMIN等[22]在测试磷酸铁锂离子、电子传输的各向异性时,组装电子阻塞电池LiAl/LiI/LiFePO4/LiI/LiAl,施加恒电流,测试电压随时间的演变关系。初始时材料中有离子和电子传输,电压由零增大到eonion/(eon+ion)(ion和eon分别代表锂离子电阻和电子的电阻);随时间变化,电子部分被电极阻碍,从而电压增大并稳定在ion[图10]。

图10 LiAl/LiI/LiFePO4/LiI/LiAl电子阻塞电池恒电流直流极化的结果[22]
Fig.10 Results of galvanostatic DC polarization for the electronically blocking cell LiAl/LiI/LiFePO4/LiI/LiAl[22]
2.3 离子迁移数的测试方法
交流阻抗法获得总的电导率,而其中锂离子电导率是对锂电池倍率性能真正贡献的部分
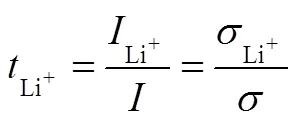

聚合物电解质离子迁移数的测试方法包括核磁共振(NMR)检测法、恒流极化法、恒压极化法等。其中恒压极化法被广泛使用:电解质两侧采用锂的可逆电极,向电解质施加一定的偏压,离子在电场的作用下运动,同时电极发生锂的溶解及沉积。由于电极反应的发生,锂离子可以通过电解质连续的从电极一侧转移到另一侧;而对于阴离子,锂电极为不可逆电极,阴离子会在电极一侧聚集,在电极另一侧耗尽,同时为了维持电解质局部的电荷平衡,相应的锂离子会在一侧聚集,在另一侧耗尽。浓度梯度的建立会驱动离子的扩散,离子的扩散方向与电势驱动的运动方向相反,经过一定的时间,会建立偏压下电解质内部离子输运的稳态。在此过程中,电流的变化如图11所示,施加电压的瞬间,正负离子在电场驱动下共同运动贡献电流,其后,负离子被电极阻塞,载流子的数目逐渐下降,电流逐渐下降,最后只有锂离子运动,电解质体系达到稳态,电流达到一个稳定值[23]。
经过Bruce、Vincent以及Abraham的校正之后,用下式(36)表示[24]


图11 采用锂的可逆电极,在施加一定偏压情况下,电流随时间的变化[23]
Fig.11 Chronoamperogram of 0.68 mol/kg−1LiPF6in EC/DEC (3/7) with an applied voltage of 10 mV. I0indicates the initial current,ssthe steady state current[23]
该方法测试步骤简单、易操作、数据较准确、适用性广。但是当电解质与锂的界面稳定性较差时,测试时间较长。
3 实验流程和数据分析
电极材料和电解质材料的电导率测试在锂电池研究中具有重要意义。电极材料有粉末、单颗粒、多孔电极、薄膜电极等形态;电解质包括电解液和隔膜、无机固体电解质、聚合物膜电解质、无机薄膜电解质等类型。测试装置(电极结构、电极体系)的组装和设计、测试方法的选择和组合,需要根据不同材料的物理形态和物理化学性质以及测试内容具体确定,并根据所需的测试参数选择合适的电化学工作站。下面对交流阻抗法、直流极化法、直流法各举实例,说明实验流程和数据分析中的注意要点。
3.1 交流阻抗法——测试电解质材料的离子电导率
直流法通常不适用于电解质材料的测试,原因如下:在直流电场作用下,如果使用离子阻塞型电极构成测试装置,初始电解质中的离子将向电极迁移形成电流,但离子到达电极后无法穿越电极电解质界面,在电极电解质界面富集,所建立的内电场逐渐抵消外加电场,直至两者抵消,离子的迁移运动停止。因此只有在外加电压的瞬间,才能得到对应总电导率的瞬态电流,难以准确测定并真实反应材料电导率的大小。另一方面,在直流电场下使用可逆电极组成测试装置,其电阻不仅包括电解质本身的电阻,还包括界面输运的电阻以及可逆电极上电化学反应的电阻,用直流电法只能得到总的电阻无法区分各种不同电阻的贡献。因此,无论是离子阻塞电极还是可逆电极,用直流电技术都难以精确测定电解质的电导率,因而通常选择交流阻抗法进行测试。
此外讨论测试电极的选择,图12为无机陶瓷电解质分别以Au为测试电极和以Li为测试电极的Nyquist图和等效电路图。Au因阻塞效应在低频区域产生容抗弧[图12 (a)],而金属锂具备离子和电子导电性,因而一般在低频区域没有明显容抗弧,会出现电荷转移电阻和双电层电容对应的半圆响应,当电解质材料对金属锂不太稳定,在阻抗谱中低频区域还会出现与金属锂界面副反应相关的半圆响应 [图12 (b)]。两种测试装置的交流阻抗法在高频或中频区域获得的半圆响应信号一致,在进行电解质材料离子电导率测试时基本可以获得相似的结果,但由于室温下无机固体电解质体相响应频率比较高,超出了仪器测量的最高频,因此很多材料测量的室温测量结果,只能观察到晶界半圆,无法得到体相半圆。由于金属锂作为测试电极所呈现结果相对复杂,一般情况下在测试电解质电导率时选用离子阻塞电极作为测试电极,在测试电解质稳定性或锂离子迁移数时选用金属锂作为测试电极。
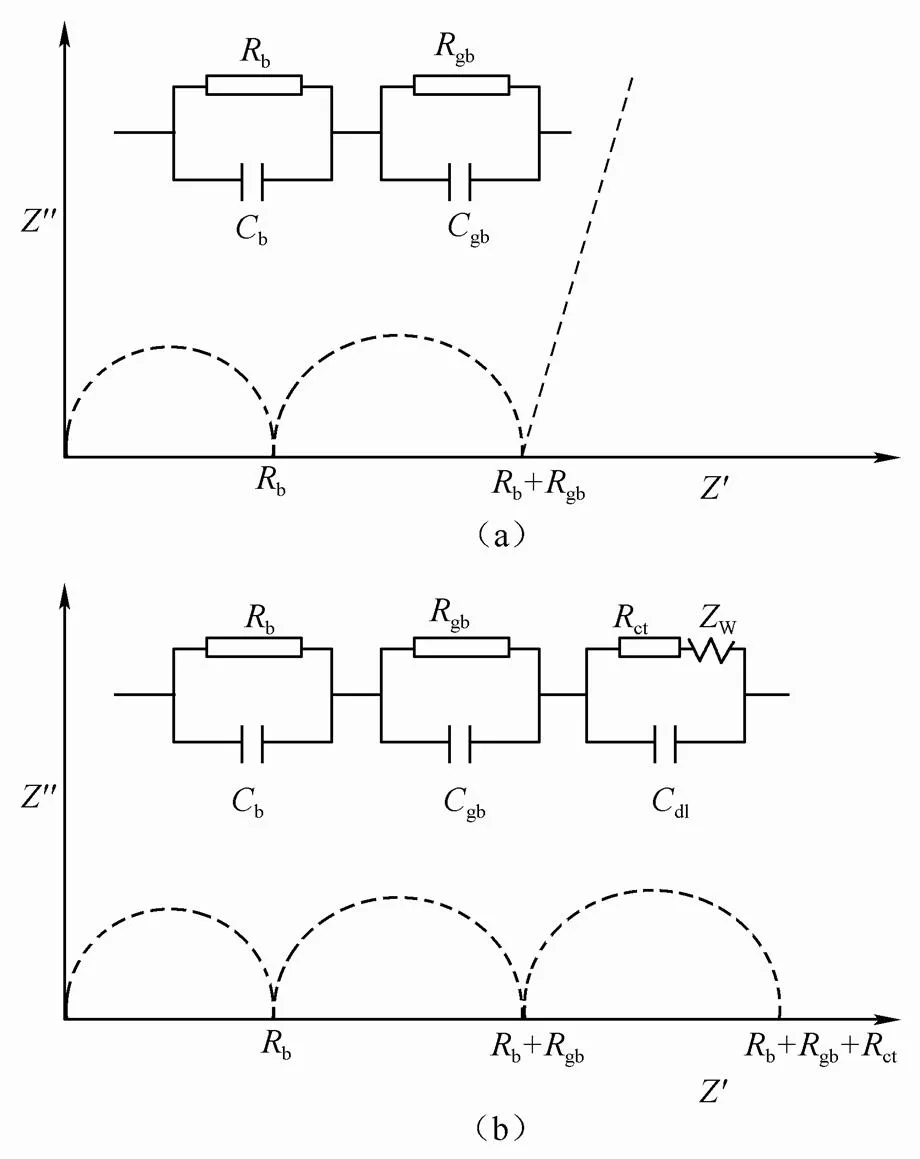
图12 无机陶瓷电解质的等效电路及其理想情况下的Nyquist图(a)以金属Au作为离子阻塞电极;(b)以金属Li作为可逆电极
基于以上分析,电解质的电导率测定采用交流阻抗法方法,并以离子阻塞电极(不锈钢片、Au、Ag、Pt、碳片等)作为测试电极。需要注意的是,此处交流阻抗法得到的实际为电解质总的电导率(离子电导率和电子电导率的加和),但由于电子电导的贡献微乎其微,通常测得的总电导率代表离子电导率。
3.1.1 测试装置的构建
(1)电解液
电解液电导率测试可以直接选择电导电极实现,如图13(a)所示。通常电导电极为面积距离确定的两个平行电极片,对应电极电导常数。通过电化学交流阻抗测得电阻,则电导率=/。
为保证测试的准确性,电导常数在测试前还需通过标准溶液标定。平行电极片为光亮铂电极或铂黑电极,需要结合电解液的大致电导率和不同型号电导电极的测试范围选择。通常光亮电极用于测量较小的电导率,而铂黑电极用于测量较大的电导率。由于铂黑电极表面积较大,从而降低电流密度以减少或消除极化;测量低电导率溶液时,铂黑电极对电解质有强烈的吸附作用,出现不稳定的现象,这时宜用光亮铂电极。
对于水系电解液的测试,直接添加适量电解液于玻璃管内,其添加量需保证液面没过电导电极的极片,如图13(b)所示;而有机电解液则需在充满高纯氩气的手套箱中测试,或根据需要设计密封容器[图13(c)],在接口位置涂覆真空硅脂或凡士林以达到更好的密封效果,最终完成电池组装。组装完成后,将电导电极的两个接线和电化学工作站相接即可进行下一步测试。

图13 电解液电导率测试装置的构建
此外,也有文献采用Swagelok型柱形电池在充满高纯氩气的手套箱内构造测试装置,浸润电解液的PP隔膜夹在不锈钢片之间组成三明治结构,电解液和隔膜的厚度在170~180 μm(多次测量,精度为1 μm)。这种测试装置的构造方式虽然密封性更好,但是厚度测试不易精确,引入一定的误差[25]。
(2)氧化物固态电解质陶瓷片
氧化物电解质冷压后仍有较大孔隙,因而其电导率的测试通常需要压片烧结成致密的圆片,例如Li7La3Zr2O12需要在超过1000 ℃下的高温下烧结以制备致密样品,再进行下一步的测试,如图14所示:(a)首先将烧结得到的圆片的两个圆面磨平和抛光,使圆片的两个平面平整干净,没有缺损;(b)用游标卡尺和数显测厚仪测试圆片的几何尺寸,得到其面积和厚度;(c)用离子溅射仪分别在圆片的两面喷金作为离子阻塞电极,在喷金的过程中,首先要保证圆片两面保持水平,每个面和溅射源的距离相同且喷金时长一致,以实现相同的喷金效果;其次特别注意圆片的侧面,避免被Au溅射,一旦溅射需要用砂纸轻轻打磨掉;(d)喷金完毕得到光亮的表面,Au在两表面均匀致密地分布,其效果用数字万用表简单验证,保证圆面上的任意两点之间电子导通即短路;(e)将得到的“三明治结构”夹在和电化学工作站相连的夹具上,每次测试需要保证夹在相同位置上(中心)。
(3)硫化物固态电解质陶瓷片
不同于氧化物陶瓷电解质的高温烧结以制备致密样品,玻璃态硫化物或玻璃陶瓷硫化物通过一定压强的冷压或较低温度的烧结,就可获得电导率和体相电导率相近的片状样品。图15所示,为75Li2S·25P2S5玻璃态电解质的离子电导率和模具压力的关系,电导率随着模具压力的增加而增大,当压力达到360 MPa时基本与热压得到的体相电导率接近[26]。而在测试装置的构建中,Au电极、不锈钢片、碳纸等方式均有采用。图16为使用模具测试硫化物电解质电导率的过程,图16(a)为模具的示意图,模具直径为10 mm,组装之后加入150 mg左右的硫化物电解质,在300 MPa压强的保持下进行交流阻抗法的测试,以保证电解质和模具的良好接触。测试之后,通过游标卡尺的深度尺进行厚度的测量,大概为1 mm左右。

图14 氧化物电解质测试装置的构建
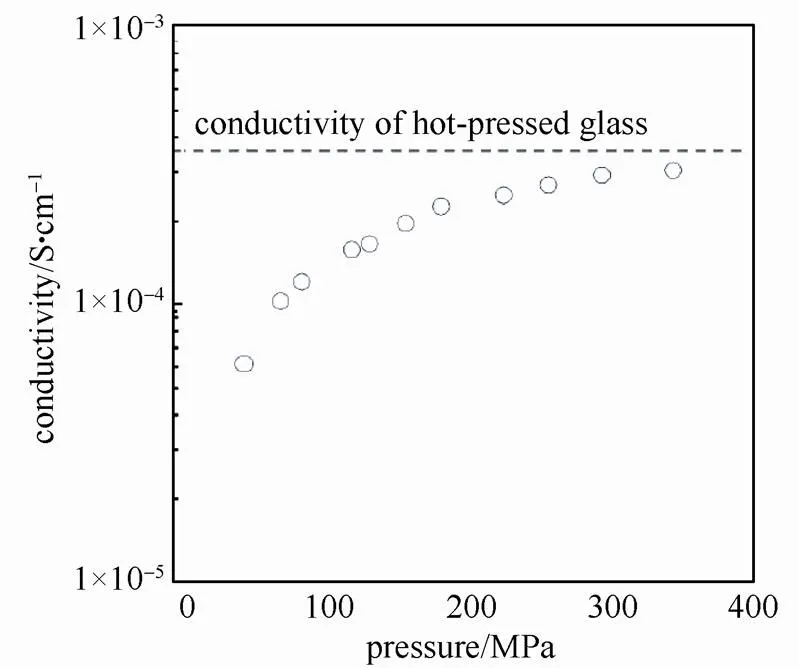
图15 硫化物电解质离子电导率和模具压强的关系[26]

图16 硫化物电解质测试装置的构建
(4)聚合物(基)固态电解质
聚合物电解质通常不能使用溅射等工艺将Au 电极引入测试体系中,因而选用不锈钢片将冲裁的聚合物膜夹在中间,组装扣式电池进行测试(图17)。测试装置几何尺寸的确定是聚合物电导率测试中的难点。聚合物膜冲裁的直径大于不锈钢片,因而面积为不锈钢片的面积;其厚度较薄,并且实际厚度在组装扣式电池时由于压力而发生较大程度的改变,可以选用下面的测试方法:首先组装测试之前测量两不锈钢片的厚度,在测试结束后拆开电池,测量两不锈钢电极与电解质膜的总体厚度,其差值可近似为聚合物电解质膜在测试过程中的实际厚度,通常仅为组装前聚合物膜的1/3~1/4[27]。

图17 聚合物电解质测试装置的构建
(5)无机薄膜固态电解质[11]
前面所述,电解质电导率的测试将测试材料夹在两个测试电极之间,构造三明治结构,而对于薄膜材料(电解质和电极材料),其厚度通常只有几百纳米到几个微米之间,因而单位面电阻较小,则需设计电极结构以保证测量的准确性,具体的设计还需根据电阻(电导率)的大小而定。假设电解质薄膜材料厚度为1 μm,若其单位面电阻小于1 Ω/cm2(离子电导率>10−4S/cm 数量级)则此时常用三明治结构产生的接触电阻、导线电阻等因素无法忽略,测试误差较大,选择因此多采用面内电极结构:叉指电极[28]、平行条状电极[29]等,如图18 (a)、图18(b)所示;若其面电阻大于100 Ω/cm2(离子电导率<10−6S/cm 数量级),可使用三明治结构[30]进行测试,如图18 (c)所示。测试电极主要为溅射方法沉积的金属箔材,如Au、Ag、Pt 、Al、不锈钢等。

图18 无机薄膜电解质的电极结构(a)叉指(梳形)电 极[28];(b)平行条状电极[29];(c)三明治结构[30]
3.1.2 测试环境和测试参数
(1)测试环境
测试时需要考虑测试环境的影响,电磁屏蔽对与高频电感干扰的排除不可缺少[图19(a)]。此外,还要保证测试时湿度、温度的相对一致。
选择适当的温度梯度进行测试,通过ln-1/求解离子传导的激活能。需要注意的是,在每个温度点至少保温30 min,使得样品温度和环境温度保持一致;而对于聚合物电解质,由于其热稳定平衡较慢,在每一个温度点至少恒定2 h再开始测量。Zahner IM6、Solartron、Autolab、辰华等电化学工作站没有温度控制系统,可以通过温湿度试验箱来控制温湿度。图19(b)的高低温(湿热)试验箱,温度范围在-30~150 ℃,湿度范围为(25~98)%RH/(25~85)℃;而NOVO control宽频介电阻抗谱仪自带温度控制系统,温度范围为-160~400 ℃,可根据不同的需求选取不同的温度范围和控制精度。

图19 (a)屏蔽箱;(b)高低温(湿热)试验箱实物图
(2)测试参数
交流阻抗法的测试参数主要如下文所述。①频率的起始和终止范围:频率扫描的方式可以选择从高频到低频、低频到高频以及中间某频率到高频再回至低频、中间某频率到低频再回至高频。通常选择从中间某频率到高频再回至低频,以验证数据的重复性,并且避免起始时太高频率或太低频率造成的体系不稳定而测试中断。不同的测试体系参考文献选择频率的范围,频率范围和温度结合,获取所需信息。②直流电压:一般设在开路电位。③交流振幅:对一般扣式电池和三电极体系,选择5 mV或10 mV;对一般固体材料的测试,选择5 mV或10 mV,也可更大。需要注意:对液体体系而言,交流振幅过小,微扰比较小,得到的响应也比较弱,交流振幅过大,对体系的干扰比较大,体系可能达不到稳态,因而需要谨慎选择合适的振幅范围;对固体体系而言,大的交流振幅对体系可能不会有太大的干扰。
基于以上测试参数,以及预估的电阻范围,选择表2中合适的电化学工作站进行下一步的测试。
3.1.3 交流阻抗法测试
以LAGP陶瓷片为例,采用NOVO Control介电谱仪(图20)进行测量,测量的频率范围为1 Hz~10 MHz;测量的温度范围为-150~60 ℃,温度间隔为30 ℃。具体操作流程见NOVO Control介电谱仪操作说明。

图20 NOVO Control介电谱仪的实物图
(1)将喷金试样安装在样品腔中(图21):①在测量时必须将类似三明治结构的试样电容(或液体试样单元)固定在试样腔的上下电极之间,放置样品时要固定牢,位于上下电极的中间位置,尽量不要偏;为了保证可靠接触,最好在试样表面的接触面上进行金属化处理,如可以采用喷金的办法在试样表面形成金属膜,也可以在试样表面用凡士林粘贴铝箔,或在试样表面刷银粉漆,但要保证试样表面不会被银粉漆溶剂损坏。②旋转试样固定旋钮(the sample mounting screw)将试样腔电极、附加电极、试样三者紧密接触固定。③竖直放入样品腔。

图21 将试样安装在样品腔的过程
(2)条件设置:图22为通常测试之前的条件设置,(a)输入试样的名称及参数;(b)选择变量;(c)设定温度变量的取值点;(d)设定频率的取值点;(e)设定起始条件;(f)设定结束条件。
(3)开始测试:检查前面所做的设置,查看和确认测量设置和试样的细节。硬件电路检查包括检查所有接线是否可靠,试样是否在试样腔里装好,所有需要的设备是否接通电源,所用设备是否校准。检查和确认之后,开始测试。
3.1.4 数据分析
《锂电池研究中的EIS实验测量和分析方法》[11]中简述了阻抗谱的数据拟合流程,需要注意的是阻抗谱和等效电路之间不存在唯一的对应关系,要考虑等效电路在被测体系中是否有明确的物理意义。
(1)利用Nyquist图分析[31]
HUGGINS对电解质和电极材料的Nyquist图谱以及对应符合物理意义的等效电路进行总结,具有借鉴价值。下文简单汇总,具体推导过程不再赘述。注意这里所用均为离子阻塞电极;e代表电子电阻,i代表离子电阻;e代表电子电导,i代表离子电导,totol代表总电导;e代表电子迁移数,i代表离子迁移数。
(i)混合导体(离子电导率和电子电导率比重相当)

图22 条件设置过程

图23 混合导体的(a)Nyquist图谱;(b)等效电路图[31]
Nyquist图谱和等效电路图示于图23,分析低频处2主要为e,而较高频率1则是e和i的并联电阻。因而有

也即

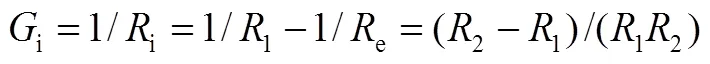


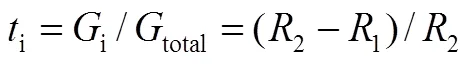

而离子传导为主和电子传导为主则为混合导体的两种极端情况。
(ii)离子传导为主
Nyquist图谱和等效电路图如图24所示,分析认为半圆在低频处与实轴的交点对应于i,并且由于低频处相当于i-int串联,因而呈现垂直的尾巴,对应于离子在电极界面处的阻塞。需要再次强调,得到的电导率是离子电导和电子电导之和,但是由于电子的电导率贡献极小,可以忽略。

图24 离子传导为主的(a)Nyquist图谱;(b)等效电 路图[31]
(iii)电子传导为主
Nyquist图谱和等效电路图如图25所示,分析认为半圆在低频处与实轴的交点对应于e,并且低频处仅相当于电阻e,因而没有电容“尾巴”。
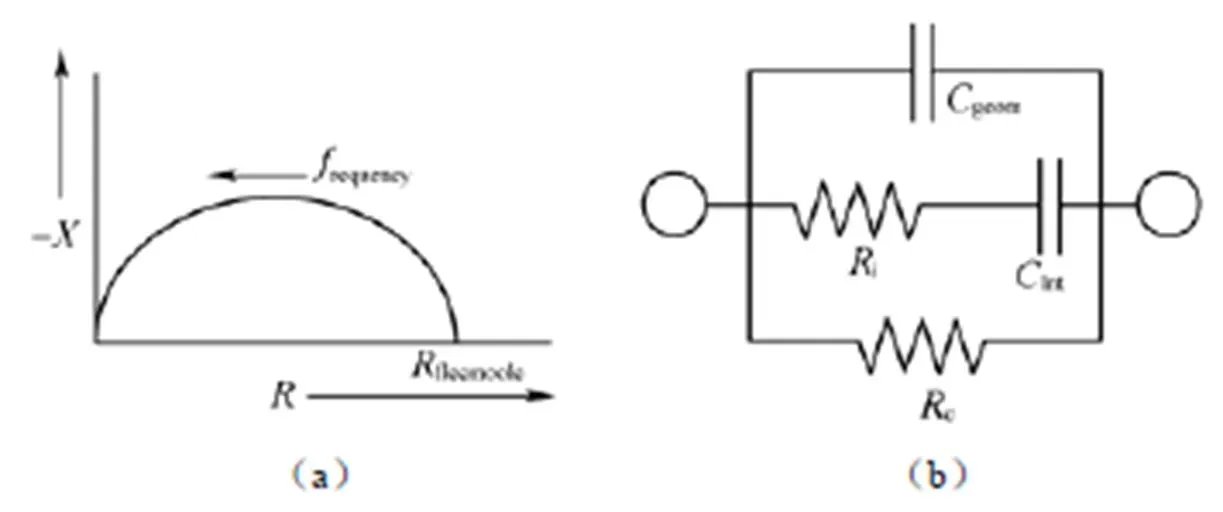
图25 电子传导为主的(a)Nyquist图谱;(b)等效电路图[31]
(iv)在离子导体中附加晶界阻抗
Nyquist图谱和等效电路图示于图26,分析认为

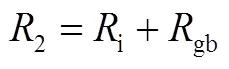
(v)在混合导体中附加晶界阻抗
Nyquist图谱和等效电路图示于图27,分析认为



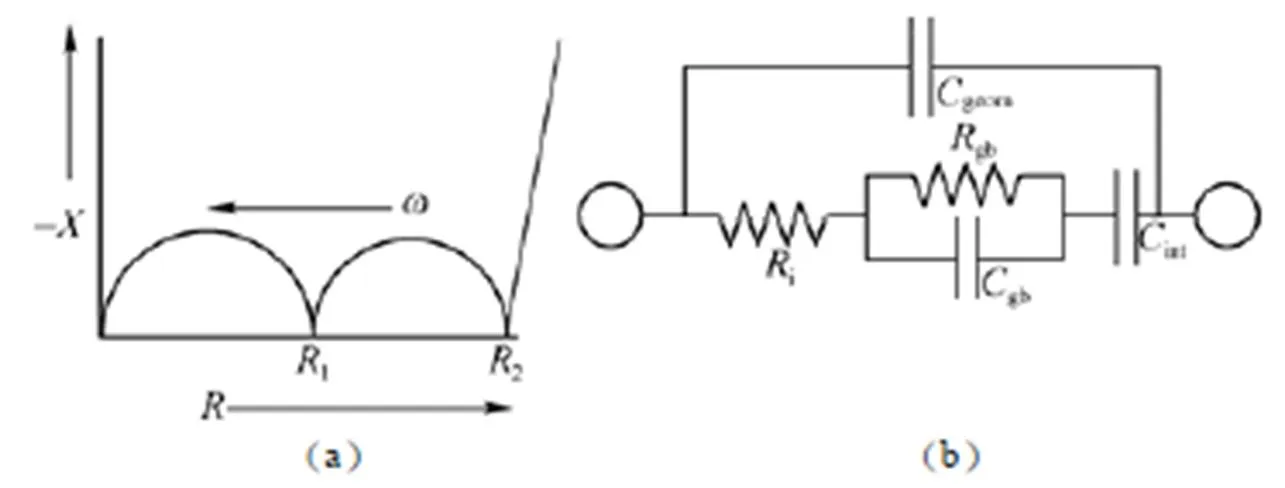
图26 附加了晶界阻抗的离子导体(a)Nyquist图谱;(b)等效电路图[31]
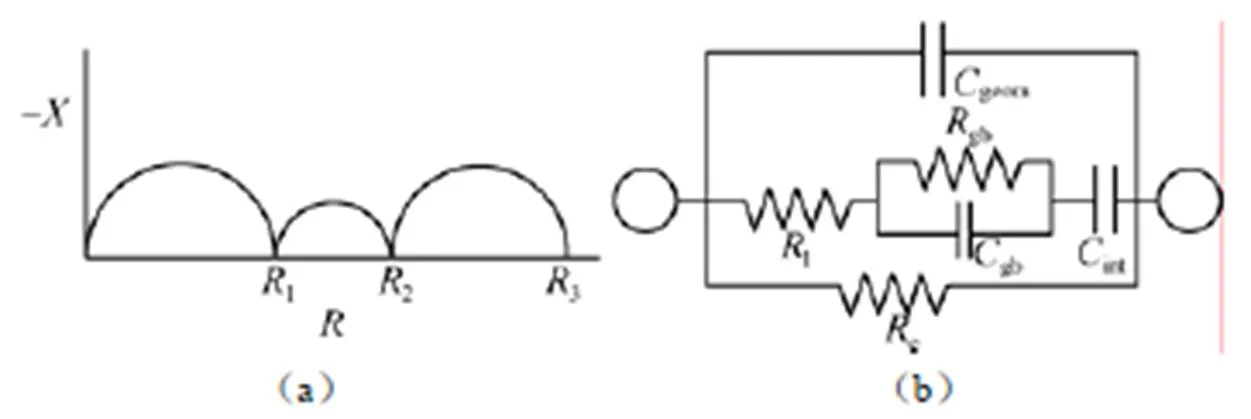
图27 附加了晶界阻抗的混合导体(a)Nyquist图谱;(b)等效电路图[31]
从而有
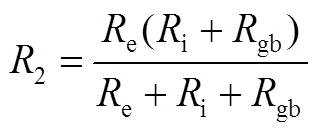

电导和迁移数由此可以推算,这里不再详述推导过程。
(2)Nyquist图和Bode图结合,阻抗谱图和介电模量图结合进行分析[4]
交流阻抗法常用Nyquist图(以阻抗的实部为横轴,负的虚部为纵轴绘制的曲线)和阻抗波特图(两条曲线组成,Bode 模量图描述阻抗模量|Z|对应频率的变化关系;Bode 相位图描述阻抗的相位角随频率的变换关系)。除此之外,还包括介电系数谱(',-"),介电模量谱(',-")等。这些图谱的结合分析,能得到综合的阻抗谱信息。
图29和图30是图28所示等效电路对应的-Nyquist图,-Nyquist图以及"与"的Bode图。
模函数=0=' +'',0=ε0c/,是空白测试装置的电容(c是电极面积,是电极间距)。和分别反应阻抗响应的不同方面,反应出电阻值的大小,而反应出电模系数的大小,而电模系数反比于电容值,因此反应出等效电路中电容值的大小。
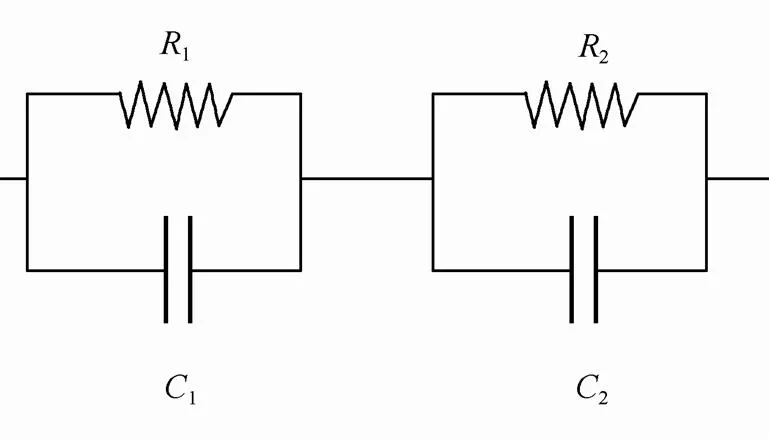
图28 多晶材料电导特性的等效电路图[4]
图29中1=2=1×106Ω,1=1×10-12F,2=1×10-9F。在图29(a),-Nyquist 图中呈现两个阻抗响应的半圆,由max=1可以得到两个电路的特征频率,1=106Hz,ω2=103Hz,两半圆直径分别为1、2,对应图29(c)''的Bode图中的两个峰。图29(b)给出了相应的-Nyquist图,图中仅有一个响应半圆,对应于11的特征响应,半圆的直径为0/1,这是由于''反应的是不同阻抗响应中的大小,而等效电路中1与2数值上有较大的差距,则11响应的值远大与22响应的值,掩盖了22响应的信息,对应在''的Bode图中只能看到11响应的峰。
图30中1=1×108Ω,2=1×106Ω,1=2=1×10-12F。与图29不同,1>>2,而1=2,因此-Nyquist图和''-Bode图中2响应的半圆和峰被掩盖,而-Nyquist 图中可以看到两个响应半圆,直径分别为0/1和0/2,对应的''-Bode 图中可以观察到两个响应峰。

其中R1=R2=1×106 Ω,C1=1×10-12 F,C2=1×10-9 F[4]

其中R1=1×108Ω,R2=1×106Ω,C1= C2=1×10-12 F[4]
基于以上分析,及分别反映等效电路中电阻与电容的信息,如果单独的一种物理量数据,不能得到材料阻抗响应完整的信息,则需要结合与两种数据形式进行分析。
(3)DRT(distribution of relaxation time)在交流阻抗谱数据解析上的应用
阻抗谱中应用较多的为不同频谱区域内的阻抗,但不同的电化学过程可能在频率域上出现重叠,但其动力学时间常数可能有较大差异,因而易于区分。通过傅里叶变换技术,将频率域的阻抗谱数据变换到时间域。近些年来,基于傅里叶变换的弛豫时间分布技术(distribution of relaxation time)DRT 在阻抗谱的数据解析上获得了广泛的应用,如图31所示。
3.2 恒电位直流极化法——和交流阻抗法结合测试聚合物电解质的离子迁移数()
电导率测试方法部分阐述了锂离子迁移数的测试原理,下文简单介绍其测试流程[8]。

(1)组装测试装置:如图32所示,在手套箱中组装测试装置。将干燥的聚合物薄膜放置在两个对称的金属锂电极间,组装锂锂对称扣式电池。
(2)将电池在80 ℃恒温箱中放置 2 h再开始 测试,以促进金属锂与聚合物之间的接触。
(3)交流阻抗法测试,频率范围为10-2~106Hz,偏压为5 mV。
(4)恒电位直流极化测试,极化电压为10~50 mV,极化时间1~10 h。
(5)极化完成后再次进行交流阻抗法测试,频率范围为10-2~106Hz,偏压为5 mV。
(6)数据分析

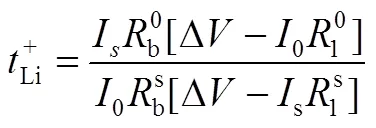

图32 聚合物电解质锂离子迁移数()测试装置的构建
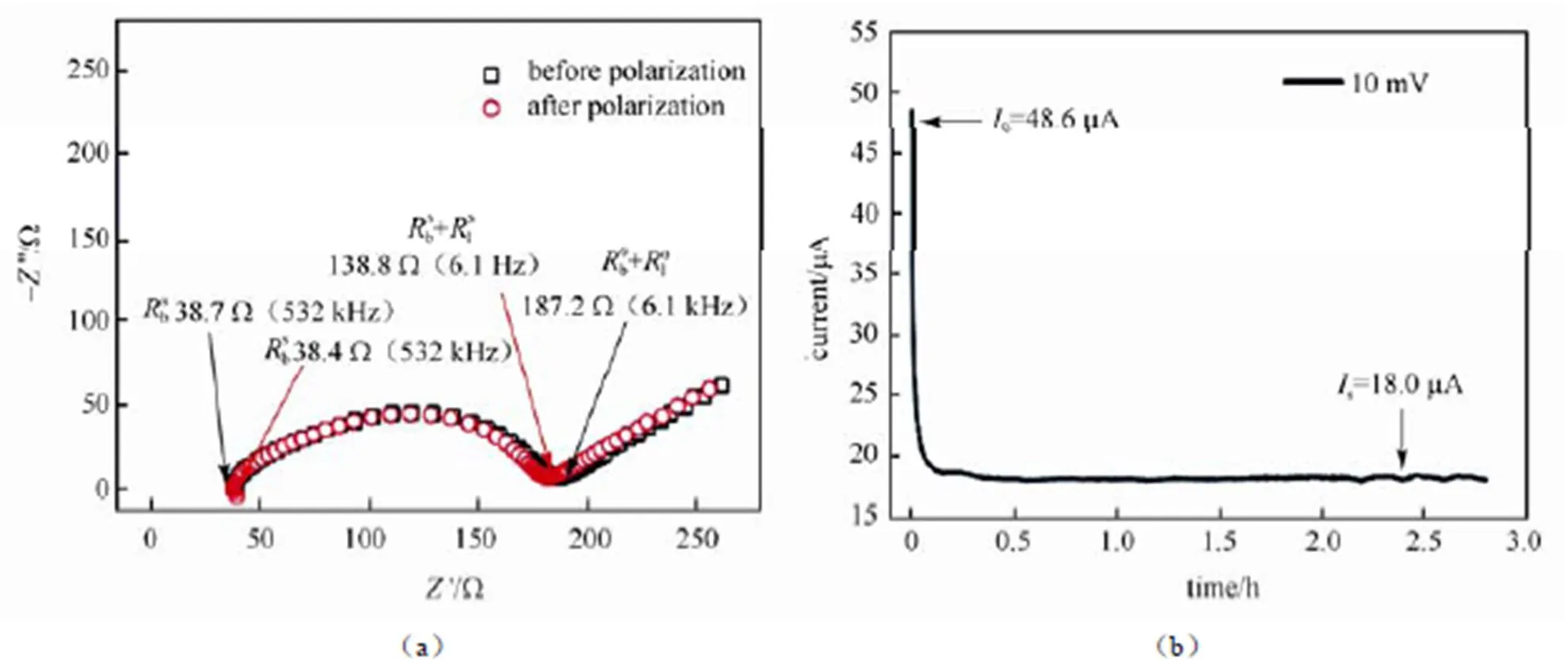
图33 (a)交流阻抗法;(b)直流极化的时间响应曲线[8]
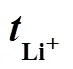
表3 用于计算的各项参数值以及由此计算的80 ℃时的[8]
3.3 直流四探针法——粉末材料电子电导率的测试
用粉末电阻测试系统MCP-PD51和Loresta-GX MCP-T700低电阻测试仪连接,测试粉末材料的电子电导率,具体的操作流程详见操作说明,这里就几个注意事项重点说明。
(1)硬件连接
(2)测试之前一定进行清零。压力清零:设备开启电源20 min后压力清零,按前面板zero约2 s钟执行清零。厚度清零:无样品情况下在施加1 kN 左右的压力时执行厚度清零(电子尺)[图34(a)]。
(3)称取适当质量的粉体材料。一定要确保 20 kN压力下样品厚度为3~5 mm,因而根据质量=密度*体积公式计算在3~5 mm厚度下的样品质量。
(4)将样品轻轻倒入腔体,并尽可能用压头将其沉入模腔底部、避免粉体附着在腔壁上。(如图34(b)将称量纸卷起,腔体稍倾斜)。
(5)打开软件进行参数设置,输入称取的样品质量,设置施加压力次数以及压力间隔。本系统最大施加压力为 20 kN,设置压力值禁止超出量程[图34(c)]。
(6)按步骤及软件提醒界面施加压力,读取厚度并输入[图34(d)]。要时刻关注压力示数,当压力达到设定值时停止,并且保持操作力臂的力以避免压力泄漏;施加压力不可过快,否则导致粉体分散在模腔体内造成测试结果误差;当有可视的压力泄漏拧紧截止阀以便保持当前压力。
(7)数据处理:软件自动计算出电导率、电阻率等值[图35(a)],需要注意的是,得到的是电导率对应密度(压强)的图表,而非绝对的电导率数值,因而其主要用于材料之间的相对比较[图35(b)]。
3.4 方法总结以及误差分析
综合上文所述的方法,对于不同的测试材料和测试内容,在测试装置和测试方法的设计上有所不同,总结于表4。
误差在电导率的测试中难以避免,表5对电 导率测试和分析过程中引入的误差进行分析。总 误差一方面与各个物理参数测量的误差有关,包 括电化学工作站电信号的误差,以及几何参数的 误差;另一方面是在数据分析过程中引入的 误差。

图34 直流四探针法测试粉末材料电子电导率的步骤
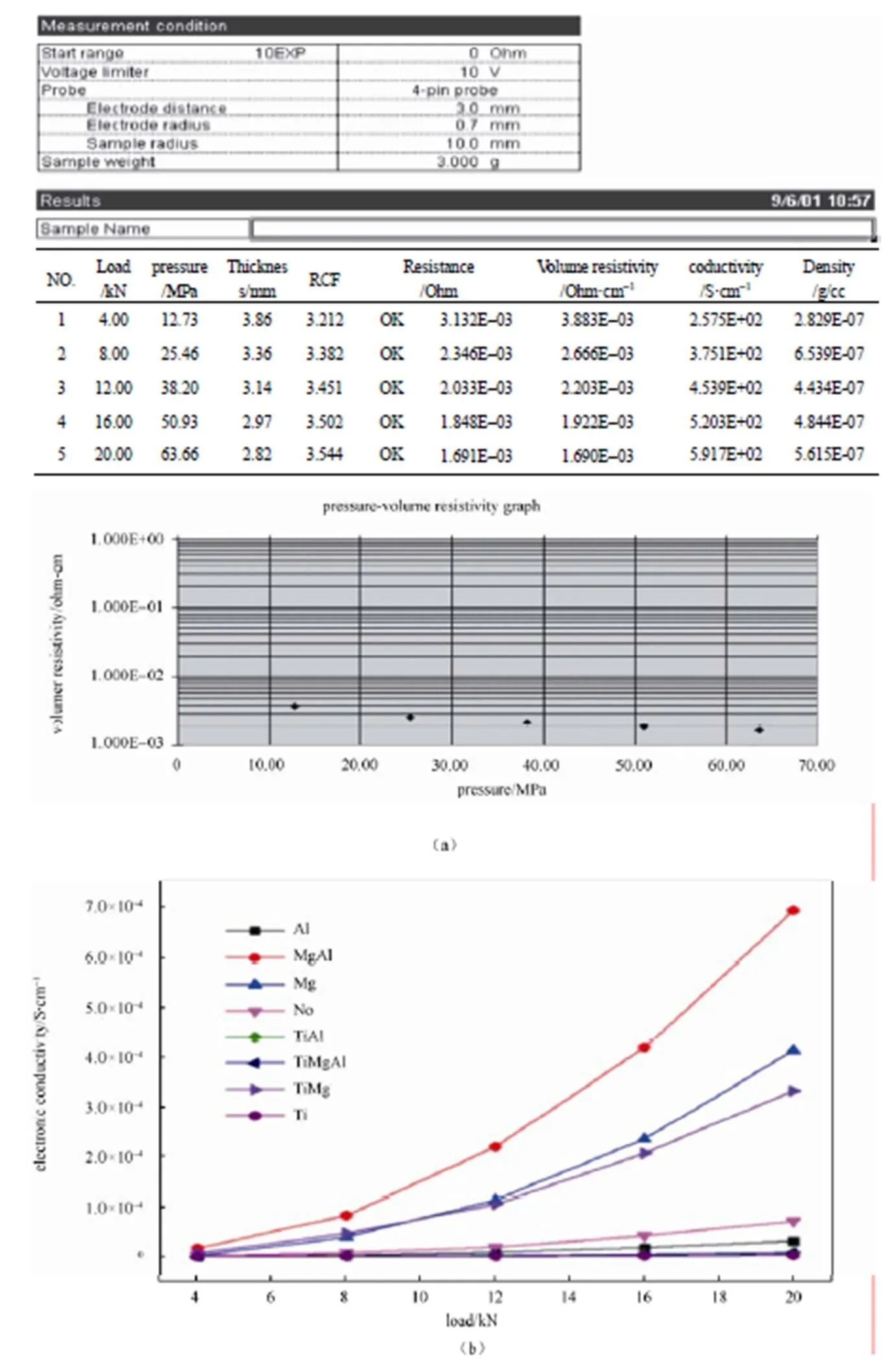
图35(a)测试结果举例;(b)掺杂样品的电子电导率测试结果[33]
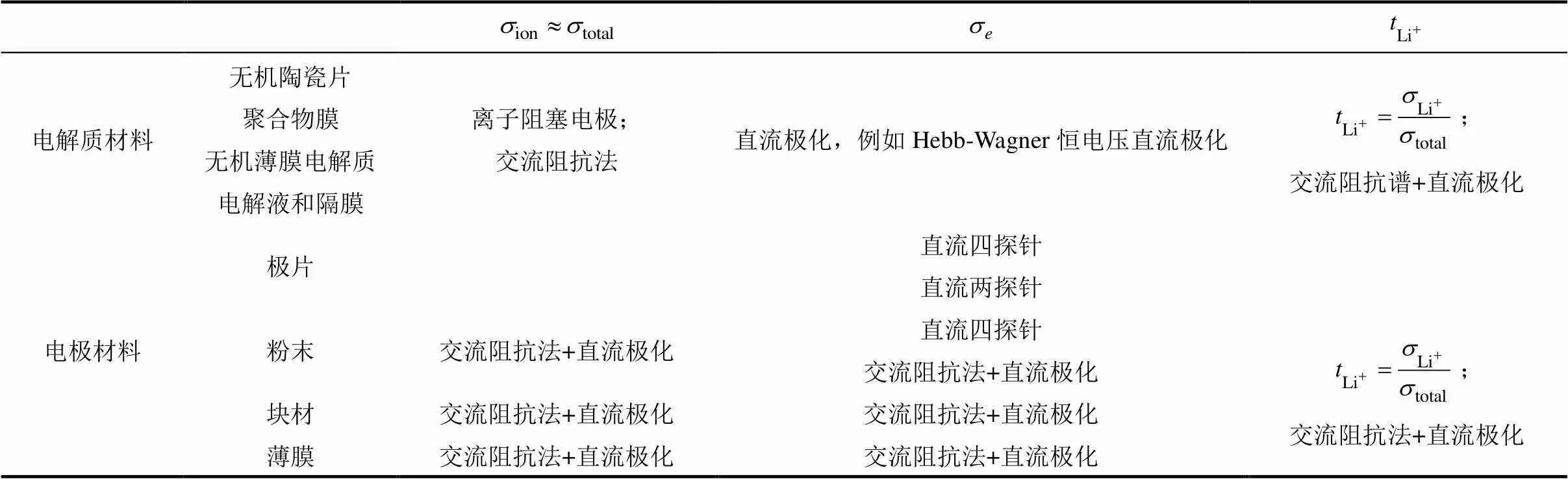
表4 电导率测试方法总结

表5 电导率测试中的误差分析
4 案例分析
锂电池研究中,需要研究电解质材料和电极材料的电导率。在研究过程中,通常需要根据不同电池材料的物理形态及物化性质,选择相应的电极体系(阻塞电极、可逆电极、半阻塞电极)和电极构型,结合各种电导率测试方法,得到准确可信的电导率。下面根据文献中的测试方法和结果,详细 分析。
4.1 电解质的电导率测试
对离子阻塞电极构建的测试装置运用交流阻抗法,适用于以离子电导为主的固体电解质的研究。这里简单介绍氧化物电解质、硫化物电解质、聚合物电解质和无机薄膜电解质的具体案例。
4.1.1 氧化物电解质
由于材料内部的结构及组份不均匀,因而材料内部不同结构区域具有不同的电导特性。相对于其他电导测量方法来说,交流阻抗法方法能够有效区分材料内部不同电导特性的区域。图36(a)为理想条件下氧化物陶瓷固态电解质的交流阻抗复平面图,高频和低频的两个半圆分别对应与不同区域的离子传递过程。这种区分不是将固态电解质膜看作一个简单晶粒,而是简化为仅含不同晶粒和晶界的离子传导体系。
阻抗谱所对应的等效电路可以表示为两个并联的串联起来的电路。等效电路的电阻可以通过半圆与实轴的交点得到,半圆顶点的频率即为电导响应的特征频率max,进而通过以下公式得到半圆对应电导行为的电容和特征弛豫时间。
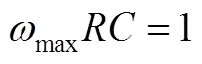
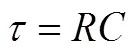
此外,需要进一步指认出高频、低频两个响应半圆分别对应体相电导还是晶界电导。可以根据阻抗谱中不同的响应半圆所对应的电容大小判断。通过砖块模型(brick layer model)来分析陶瓷材料的响应特征[图36(c)],陶瓷体相电容值一般在10-11~10-13F数量级范围内,晶界电容的数值范围一般为10-11~10-8F,具体电化学过程对应的电容范围如表6所示。从而认为高频半圆对应体相电导,低频半圆对应晶界电导[34]。
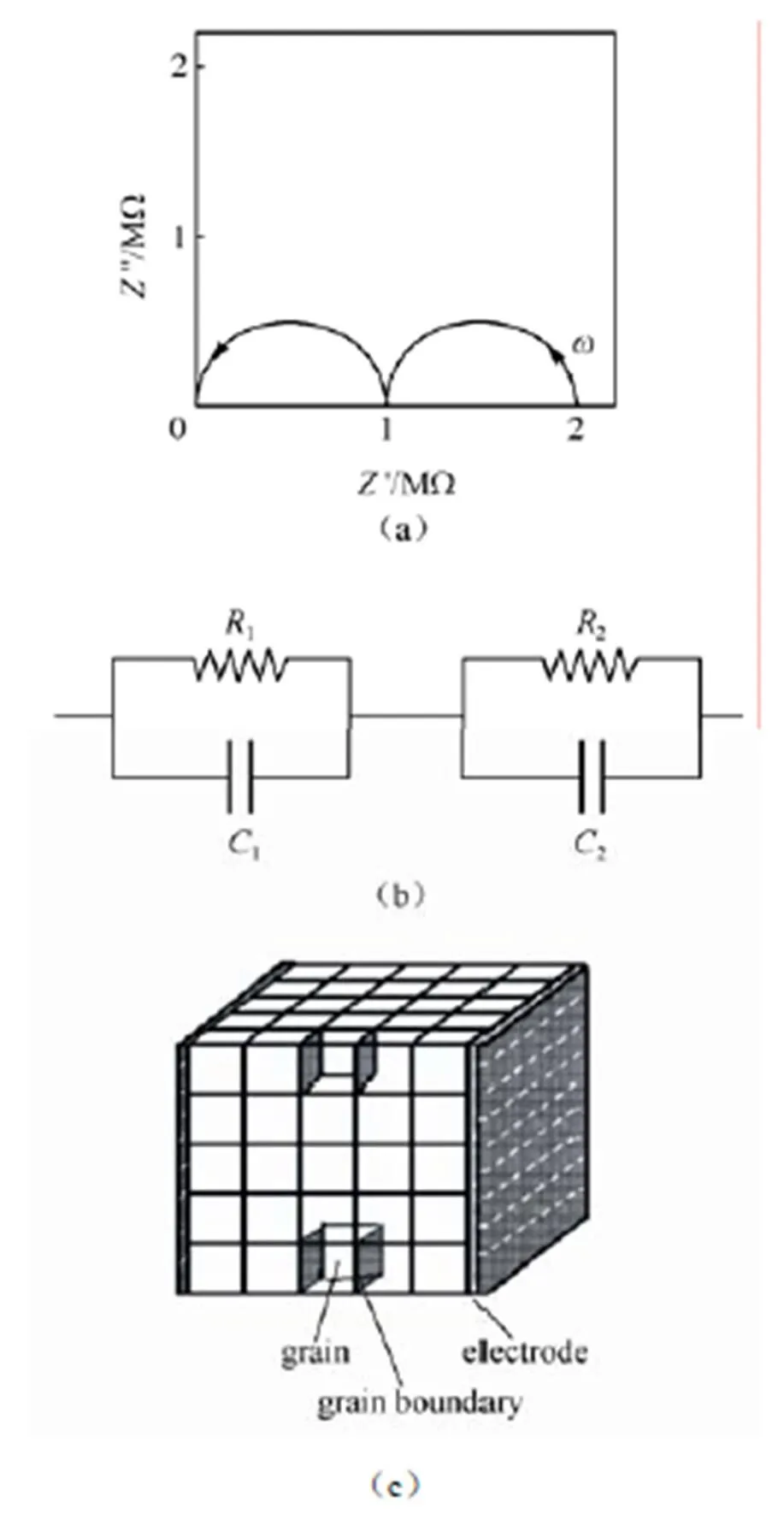
图36 (a)理想条件下陶瓷固态电解质的阻抗谱;(b)多晶材料电导特性的等效电路(1、2分别代表体相电导特征区域和晶界电导特征区域);(c)brick layer model 示意图[4]
4.1.2 硫化物电解质
和氧化电解质相比,硫化物电解质具有更高的离子电导。KAMAYA等[35]通过固相烧结法合成新的晶体结构的一维快锂离子导体Li10GeP2S12,在室 温下可以达到12 mS/cm的电导率,和有机电解液相接近。将Li10GeP2S12在氩气氛围中压片(直径10 mm,厚度3~4 mm),在其表面镀金作电极,之后在真空中500 ℃热处理。将所组装的Au/ Li10GeP2S12/Au电池在氩气氛围下从-110~110 ℃进行交流阻抗测试,测试过程重复2~3次,施加100~500 mV的偏压,频率范围为106~10-1Hz (Solartron,1260)。所得到不同温度下的阻抗谱如图37所示,包含一个半圆和一条斜线,吻合纯离子导体的阻抗谱。由此获得晶界电阻和体相电阻之和,进而根据硫化物片材的表观尺寸计算电导率。由此得到,在室温27 ℃下电导率为12 mS/cm,相对较高。之后,根据Arrhenius方程进行拟合,得到-110~110 ℃温度范围内离子传导的激活能为24 kJ/mol,和快离子导体的典型激活能相一致。为进一步验证,在25 ℃下对(-)Li/Li10GeP2S12/Au(+)电池进行Hebb-Wagner直流极化,从而通过从2.8~3.5 V的线性拟合,计算得到在非对称电池的不可逆Au-Li10GeP2S12界面上的总电子电导率(电子+空穴)为5.70×10-9S/cm,基本认为是离子导体。

图37 Li10GeP2S12从低温到高温的阻抗谱图以及Arrhenius电导率图[35]
4.1.3 聚合物电解质
固态聚合物电解质具有质量轻、柔性、不易燃等优势,从而为有机液态电解质的安全性问题提供了一个解决方案。其中PEO基聚合物电解质是重要的一类,但在室温下的电导率比较低,而在80 ℃以上处于黏流态,无法缓解锂枝晶的生长问题。对此,很多研究工作集中于提升PEO基聚合物电解质的离子电导率和力学性能,包括纳米尺寸填料(1D,2D,3D)的使用和纳米结构的嵌段/接枝共聚等方法,以促进局域非晶区域的形成。CUI等[36]通过原硅酸四乙酯的原位水解合成了PEO-单分散超细SiO2(MUSiO2)复合聚合物电解质,合成过程中MUSiO2球和PEO链段的强化学/力学的相互作用成功抑制了PEO的结晶,有效提升了离子电导率。通过组装SS/SPE/SS电池(不锈钢片SS上通过电子束蒸发镀有250 nm的Pt),测试其从0~90 ℃的离子电导率,如图38所示,这种原位复合的方法较之机械共混得到的复合聚合物电解质积大提升了离子电导率。

图38 不同制备方法得到的PEO-SiO2复合聚合物电解质和无复合的PEO聚合物电解质离子电导的Arrhenius图[36]
4.1.4 无机薄膜电解质
通过PLD、ALD、射频磁控溅射沉积等方法制备的无机薄膜电解质较之于常规无机电解质,在面电阻上有极大程度的降低,可制备成全固态薄膜电池,适用于电子产品中微型电池的需求,此外可用于电解质体相中锂离子扩散的机理研究。
LOBE等[29]通过射频磁控溅射法在不锈钢基体上沉积Ta和Al替换的Li7La3Zr2O12薄膜。通 过XRD、SEM 和ToF-SIMS等表征手段,确认在700 ℃及以上的沉积温度下,可以得到厚度为1.8 μm 的单相立方晶体结构的LLZ薄膜,并且形成0.2 μm 厚的γ-LiAlO2中间层[图39(a)]。这里电导率的测试选用了平行电极结构,在样品表面沉积四个平行条状Au电极。交流阻抗法的测试选用两种方式,如图39(b)所示,一种是垂直于薄膜,一种是平行于薄膜。垂直于薄膜测试得到的阻抗谱如图39(c)所示,对应室温下总的电导率为2.0×10-9S/cm,远低于LLZ体相电导率(约10-4S/cm),结合各种表征,分析认为包含γ-LiAlO2的氧化层电阻率较高,从而导致横截面的电导率较低。平行于薄膜的阻抗谱测试则得到不同的结果[图39(d)],室温下总电导率为1.2×10-4S/cm,对应于0.47 eV的激活能。
4.2 电极材料的电导率测试
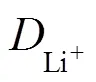
4.2.1 LiFePO4单晶离子传输和电子传输的各向异性
AMIN等[37]通过LiFePO4单晶研究其离子传输和电子传输的各向异性,设计Ti/LiFePO4/Ti离子阻塞电极组装的对称电池和Li/LiI/LiFePO4/LiI/Li电子阻塞电极组装的对称电池,通过交流阻抗法和恒电流直流极化方法的结合,得到[100]、[010]、[001] 3个方向的总电导率、电子电导率、离子电导率、离子扩散系数,从而对于材料中载流子传输的各向异性进行分析讨论。
(1)Ti/LiFePO4/Ti电池,交流阻抗法测试。所得到阻抗谱图如图40(a)所示,和3.1.4节数据分析中电子电导为主的阻抗谱[图25]一致,得到总电导率(≈eon)。

图39 (a)700 ℃下沉积的LLZ薄膜的横截面背散射图像;(b)交流阻抗谱的两种测试方式;(c)横截面阻抗谱测试的Nyquist图;(d)面内阻抗谱测试的Nyquist图[29]

图40 (a)[100] (a-axis) and [001] (c-axis)方向的归一化阻抗谱;(b)[001] (c-axis)方向的极化、去极化电压和时间的关系[37]
(2)Ti/LiFePO4/Ti电池,恒电流直流极化测试。对离子导电的材料在离子阻塞电极下进行直流极化时,初始有离子传导的贡献,后面逐渐稳定为电子电导的部分,因而电压先上升后稳定。这里电压始终保持稳定而没有离子被阻塞的影响[图40(b)],说明该材料以电子电导为主,并得到电子电导率eon。
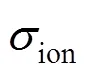
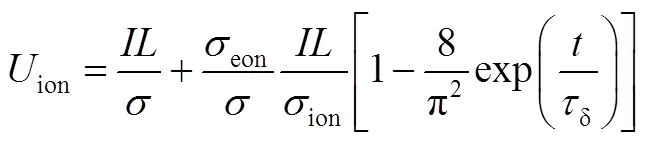

因为金属锂作为电极不能对材料在较高温度下测试,因而在恒电流极化时难以实现稳态,所以后续研究者选用LiAl/LiI/LiFePO4/LiI/LiAl电子阻塞电极组装的对称电池,在大于200 ℃条件下测试,得到了更为准确的结果[22]。
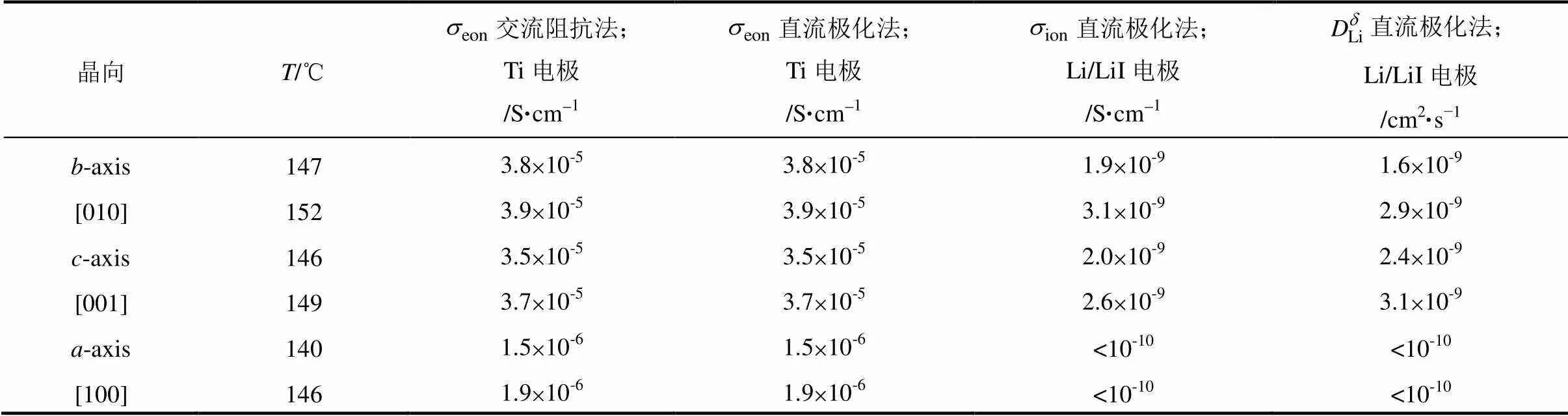
表7 LiFePO4在a、b、c三个方向的总电导率、电子电导率、离子电导率和化学扩散系数[37]
4.2.2 电极材料离子电导率测试的讨论
电极材料的离子电导率测试通常先将电极材料进行处理,WANG等[7]通过放电等离子体烧结方法(SPS)在800 ℃,5 min内将LCO和NMC粉末致密化,涂覆Ag浆作为离子阻塞电极,选用交流阻抗谱和恒电压直流极化测试结合的方法,测试得到离子电导率和电子电导率。需要注意的是,SPS方法有效去除了晶界,从而简化了交流阻抗谱和直 流极化的分析。AMIN等[38]则将NMC粉末加压 340 MPa,并在900 ℃温度下烧结12 h,从而得到相对密度为96%~98%的片材,从而减小了孔隙的影响(接触面积),可以认为测得的电导率代表体相电导率。之后将得到的片材组装Ag|NMC|Ag电子阻塞对称电池和Li|PEO|NMC|PEO|Li离子阻塞对称电池,分别进行交流阻抗谱和恒电流直流极化的测试,得到互相印证的离子电导率和电子电导率。PATEL等[39]则直接冷压(20 MPa)得到正极材料的片材,涂覆Ag浆作为离子阻塞电极,交流阻抗的拟合得到电子和离子对应的电阻,并和Hebb-Wagner直流极化的测试结果一致。
活性粉末材料的电子电导率可以通过直流四探针法测试(得到和压强相关的相对值),离子电导率的测试也希望找寻简单有效、便于生产中测试的方法。尝试思考在如图16(a)模具中加入粉末材料,一边保持压力一边进行ITIC直流极化测试。但考虑到仅施压的条件下,颗粒之间接触较差,粉末与电极的接触较差,影响测试结果的一致性,所得到的离子电导率和真实体相的离子电导率有相当误差,并且随施加压力的大小而改变,因而用于不同种材料的离子电导的相对比较。图41是对钴酸锂材料在一定压力下,进行10 mV恒电压直流极化的测试结果,并根据式(32)进行拟合。

5 结 语
锂电池各组成材料中的载流子应具备优异的动力学性能,以满足锂电池高倍率性能的要求。电导率这一物理量在宏观尺度上描述了固体的电学性能,是一种相对简单直观的表述方法,在锂电池的研究中对材料开发和机理研究具有重要意义。电导率的测试方法众多,其关键点在于测试装置的构建,需根据具体测试材料的物理化学性质设计合理的电极结构和电极体系;二是测试方法的选取,根据测试材料的导电特性和测试内容,选择不同方法的结合。需要注意的是,电导率受测试条件的影响较大,温度、湿度、压强都会在一定程度上对结果产生影响,因而通常用于同一文献中的相对比较,以及不同文献中数量级之间的比较;此外不同测试方法得到的电导率测试结果也存在一定偏差。本文基于文献报道和实验的经验总结了常规电解质和电极材料的测试装置的构建,测试方法的选取,以及数据的分析方法,尚未经广泛讨论和全面论证。因而期待行业内专家的批评指正,促进电导率测试的条件和方法的规范化和标准化,以共同提升电导率测试数据的可靠性。
[1] MAIER J. Physical chemistry of ionic materials: Ions and electrons in solids[M]. New Jersey: John Wiley & Sons, 2004.
[2] AGRAWAL R, GUPTA R. Superionic solid: Composite electrolyte phase—An overview[J]. Journal of Materials Science, 1999, 34(6): 1131-1162.
[3] 郑浩, 高健, 王少飞, 等. 锂电池基础科学问题(VI)——离子在固体中的输运[J]. 储能科学与技术, 2013, 2(6): 620-635.
ZHENG Hao, GAO Jian, WANG Shaofei, et al. Fundamental scientific aspects of lithium batteries (VI)—Ionic transport in solids[J]. Energy Storage Science and Technology, 2013, 2(6): 620-635.
[4] 王少飞. 锂电池固体电解质材料的研究[D]. 北京: 中国科学院物理研究所, 2014.
WANG S F. Investigation on solid state electrolyte materials for lithium battery[D]. Beijing: Institute of Physics, Chinese Academy of Sciences, 2014.
[5] 高健. 若干锂离子固体电解质中的离子输运问题研究[D]. 北京: 中国科学院物理研究所, 2015.
GAO J. Investigation on ion transport in several lithium ion solid electrolytes[D]. Beijing: Institute of Physics, Chinese Academy of Sciences, 2015.
[6] 杨勇. 固态电化学[M]. 北京: 化学工业出版社, 2016.
YANG Y. Solid state electrochemistry[M]. Beijing: Chemistry Industry Press, 2016.
[7] WANG S, YAN M, LI Y, et al. Separating electronic and ionic conductivity in mix-conducting layered lithium transition-metal oxides[J]. Journal of Power Sources, 2018, 393: 75-82.
[8] 张恒. 含双(氟磺酰)亚胺阴离子的纯固态聚合物电解质的制备、表征及性质[D]. 武汉: 华中科技大学, 2015.
ZHANG H. Solid polymer electrolytes based on bis(fluorosulfonyl) imide anion: Synthesis, characterization, and properties[D]. Wuhan: Huazhong University of Science & Technology, 2015.
[9] 应风晔. Ba0.5Sr0.5Co0.8Fe0.2O3-混合导体导电性能研究[D]. 上海: 上海大学, 2007.
YING F Y. Research on conductivity of mixed Conductors- Ba0.5Sr0.5Co0.8Fe0.2O3-[D]. Shanghai: Shanghai University, 2007.
[10] BUSCHMANN H, DOLLE J, BERENDTS S, et al. Structure and dynamics of the fast lithium ion conductor "Li7La3Zr2O12"[J]. Phys. Chem. Chem. Phys., 2011, 13(43): 19378-19392.
[11] 凌仕刚, 许洁茹, 李泓. 锂电池研究中的EIS 实验测量和分析方法[J]. 储能科学与技术, 2018, 7(4): 732-750.
LING S G, XU J R, LI H. Experimental measurement and analysis methods of electrochemical impedance spectroscopy for lithium batteries[J]. Energy Storage Science and Technology, 2018, 7(4): 732-750.
[12] WESTPHAL B G, MAINUSCH N, MEYER C, et al. Influence of high intensive dry mixing and calendering on relative electrode resistivity determined via an advanced two point approach[J]. Journal of Energy Storage, 2017, 11: 76-85.
[13] BARSOUKOV E, MACDONALD J R. Impedance spectroscopy theory, experiment, and applications[M]. 2nd Ed. USA: John Wiley & Sons, 2005.
[14] 曹楚南, 张鉴清. 交流阻抗法导论[M]. 北京: 科学出版社, 2002.
CAO C N, ZHANG J Q. An introduction to electrochemistry impedance spectroscopy[M]. Beijing: Science Press, 2002.
[15] HEBB M H. Electrical conductivity of silver sulfide[J]. The Journal of Chemical Physics, 1952, 20: 185-190.
[16] WAGNER C. Galvanische zellen mit festen elektrolyten gemischter stromleitung[J]. Zeitschrift fuer Elektrochemie und Angewandte Physikalische Chemie, 1956, 60: 4-7.
[17] FRENNING G, STR MME M. Theoretical derivation of the isothermal transient ionic current in an ion conductor: Migration, diffusion, and space-charge effects[J]. Journal of Applied Physics, 2001, 90(11): 5570-5575.
[18] WATANABE M, RIKUKAWA M, SANUI K, et al. Evaluation of ionic mobility and transference number in a polymeric solid electrolyte by isothermal transient ionic current method[J]. Journal of Applied Physics, 1985, 58(2): 736-740.
[19] 郑浩. 全固态锂空气电池和新型薄膜固态电解质研究[D]. 北京: 中国科学院物理研究所, 2015.
ZHENG H. Studies on the solid state Lithium air battery and a new thin film solid state electrolyte[D]. Beijing: Institute of Physics, Chinese Academy of Sciences, 2015.
[20] HAILE S M, WEST D L, CAMPBELL J. The role of microstructure and processing on the proton conducting properties of Gadolinium-doped barium cerate[J]. Journal of Materials Research, 1998, 13(6): 1576-1595.
[21] AGRAWAL R C, KATHAL K, GUPTA R K. Estimation of energies of Ag+ion formation and migration using transient ionic current (TIC) technique[J]. Solid State Ionics, 1994, 74: 137-140.
[22] AMIN R, MAIER J, BALAYA P, et al. Ionic and electronic transport in single crystalline LiFePO4grown by optical floating zone technique[J]. Solid State Ionics, 2008, 179(27/32): 1683-1687.
[23] ZUGMANN S, FLEISCHMANN M, AMERELLER M, et al. Measurement of transference numbers for lithium ion electrolytes via four different methods, a comparative study[J]. Electrochimica Acta, 2011, 56(11): 3926-3933.
[24] ABRAHAM K M, JIANG Z, CARROLL B. Highly conductive PEO-like polymer electrolytes[J]. Chemistry of Materials, 1997, 9: 1978-1988.
[25] NIEDZICKI L, KASPRZYK M, KUZIAK K. Liquid electrolytes based on new lithium conductive imidazole salts[J]. Journal of Power Sources, 2011, 196(3): 1386-1391.
[26] SAKUDA A, HAYASHI A, TATSUMISAGO M. Sulfide solid electrolyte with favorable mechanical property for all-solid-state lithium battery[J]. Scientific Reports, 2013(3): 2261-2265.
[27] 程琥. 锂二次电池聚合物电解质的制备、表征及其相关界面性质研究[D]. 厦门: 厦门大学, 2007.
CHENG H. Synthesis, characterization and their interfacial properties of polymer electrolytes for secondary lithium batteries[D]. Xiamen: Xiamen University, 2007.
[28] KIM S, HIRAYAMA M, TAMINATO S. Epitaxial growth and lithium ion conductivity of lithium-oxide garnet for an all solid-state battery electrolyte[J]. Dalton Transactions, 2013, 42(36): 13112-13117.
[29] LOBE S, DELLEN C, FINSTERBUSCH M. Radio frequency magnetron sputtering of Li7La3Z2O12thin films for solid-state batteries[J]. Journal of Power Sources, 2016, 307: 684-689.
[30] SU Y, FALGENHAUER J, POLITY A. LiPON thin films with high nitrogen content for application in lithium batteries and electrochromic devices prepared by RF magnetron sputtering[J]. Solid State Ionics, 2015, 282: 63-69.
[31] HUGGINS R A. Simple method to determine electronic and ionic conductivity of the components in mixed conductors—A review[J]. Ionics, 2002(8): 300-313.
[32] UHLMANN C, BRAUN P, ILLIG J, et al. Interface and grain boundary resistance of a lithium lanthanum titanate (Li3-La2/3−xTiO3, LLTO) solid electrolyte[J]. Journal of Power Sources, 2016, 307: 578-586.
[33] 张杰男. 电压钴酸锂的失效分析与改性研究[D]. 北京: 中国科学院物理研究所, 2018.
ZHANG J N. Failure analysis and modification research on high voltage LiCoO2[D]. Beijing: Institute of Physics, Chinese Academy of Sciences, 2018.
[34] IRVINE J T, SINCLAIR D C, WEST A R. Electroceramics: characterization by impedance spectroscopy[J]. Advanced Materials, 1990, 3(2): 132-138.
[35] KAMAYA N, HOMMA K, YAMAKAWA Y, et al. A lithium superionic conductor[J]. Nature Materials, 2011, 10(9): 682-686.
[36] LIN D, LIU W, LIU Y, et al. High ionic conductivity of composite solid polymer electrolyte via in situ synthesis of monodispersed SiO2nanospheres in Poly(ethylene oxide)[J]. Nano Letters, 2015, 16(1): 459-465.
[37] AMIN R, BALAYA P, MAIER J. Anisotropy of electronic and ionic transport in LiFePO4single crystals[J]. Electrochemical and Solid-State Letters, 2007, 10(1): A13-A16.
[38] AMIN R, CHIANG Y M. Characterization of electronic and ionic transport in Li1-Ni0.33Mn0.33Co0.33O2(NMC333) and Li1-Ni0.50Mn0.20Co0.30O2(NMC523) as a function of Li content[J]. Journal of the Electrochemical Society, 2016,163(8): A1512-A1517.
[39] PATEL R L, PARK J, LIANG X H. Ionic and electronic conductivities of atomic layer deposition thin film coated lithium ion battery cathode particles[J]. RSC Advances, 2016, 6: 98768-98776.
Conductivity test and analysis methods for research of lithium batteries
XU Jieru, LING Shigang, WANG Shaofei, PAN Du, NIE Kaihui, ZHANG Hua, QIU Jiliang, LU Jiaze, LI Hong
(Institute of Physics, Chinese Academy of Sciences, Beijing 100190, China)
Lithium ionic conductivity, electronic conductivity of active electrode materials and lithium ionic conductivity of electrolyte materials are closely related to the dynamic behavior of lithium batteries. Therefore, conductivity test and analysis contribute the understanding of electrochemical properties of materials, including direct current method (DC), alternating current impedance (AC impedance), and direct current polarization method (DC polarization). Based on the different conductivity characteristics of electrolyte materials and active electrode materials, this paper introduced the methods, principles, equipments, test procedures and precautions of conductivity test. Besides, the analysis of data was illustrated with specific cases of lithium batteries.
conductivity; direct current method; alternating current impedance; direct current polarization method; lithium batteries
10.12028/j.issn.2095-4239.2018.0162
TM 911
A
2095-4239(2018)05-926-31
2018-08-16;
2018-08-23。
国家重点研发计划(2016YFB0100300,2016YFB0100100)以及中国科学院战略性先导科技专项(XDA09010000)。
许洁茹(1993—),女,硕士研究生,主要研究方向为固态电池关键材料及固态电池中界面问题的研究,E-mail:jieruxu@163.com;
李泓,研究员,研究方向为高能量密度锂离子电池,固态电池及失效分析,E-mail:hli@iphy.ac.cn。

