罗氟司特联合二甲双胍对肥胖型多囊卵巢综合征的疗效及糖脂代谢和性激素水平的影响*
玛娜尔·朱马汗 周立红 夏依扎·卡玛力 鲁春雁 阿依古丽·热哈提
(1.阿勒泰地区人民医院妇科,新疆 阿勒泰 836500 ;2.新疆医科大学附属肿瘤医院妇外三科,新疆 乌鲁木齐 830000)
多囊卵巢综合征(polycystic ovary syndrome,PCOS)属妇科常见内分泌疾病,是指女性因生殖内分泌及代谢功能异常而导致卵泡发育障碍[1]。临床上PCOS患者以多囊卵巢、稀发排卵、高雄激素血症为主要特征,以肥胖、不孕、月经稀发、子宫异常出血、闭经、多毛、胸背痤疮等为主要表现[2]。研究[3]发现,PCOS患者均存在不同程度的糖脂代谢和性激素水平异常,严重影响患者生殖功能。另有数据[4]显示,50%~75%的PCOS患者存在肥胖情况,且以腹部肥胖居多。肥胖会在一定程度上加重PCOS患者胰岛素抵抗和高雄激素血症,加大治疗难度。因而如何治疗肥胖型PCOS患者是临床研究的热点[5]。现代医学对于肥胖型PCOS尚无根治之法,临床多以促发排卵、调整月经周期,辅以减轻胰岛素抵抗、降低雄激素水平和体质量为主要治疗原则[6]。
二甲双胍是临床治疗PCOS的常用药物,也可增加胰岛素的敏感性[7]。有研究[8]显示,磷酸二酯酶-4抑制剂罗氟司特可有效改善肥胖型PCOS患者机体的葡萄糖状态,降低体质量。故本研究以我院收治的肥胖型PCOS患者92例为研究对象,探讨肥胖型PCOS应用二甲双胍联合罗氟司特治疗的临床效果及对糖脂代谢和性激素水平的影响,现将结果报告如下。
1 资料与方法
1.1 一般资料 选取我院2015年1月~2017年1月收治的92例肥胖型多囊卵巢综合征(PCOS)患者,所有患者均自愿参加本研究、签署知情同意书。纳入标准(参照2003年鹿特丹会议标准[9]):①无排卵或稀发排卵。②超声检查表现为多囊卵巢:卵巢体积≥10ml或一侧(双侧)卵巢直径2~9cm,卵泡数目≥12个。③高雄激素血症或高雄激素临床表现。④身体质量指数(Body Mass Index,BMI)≥28kg/m2。排除标准:①合并高泌乳素血症、甲状腺功能亢进或减退症、糖尿病等内分泌疾患者。②近三个月内服用激素类药物者。③伴有严重消化系统、造血系统、肝肾功能、呼吸系统、心脑系统等原发疾患者。④对本研究使用药物过敏或为过敏体质者。⑤精神异常或依从性较差者。⑥哺乳或妊娠期妇女。⑦临床资料不完整者。本研究经我院医学伦理委员会同意。
采用随机数字表法均分为两组。观察组46例;年龄20~39岁,平均(26.5±3.3)岁;病程2~8年,平均(3.8±1.2)年;BMI 28.2~32.6kg/m2,平均(29.5±1.5) kg/m2。对照组46例,年龄21~40岁,平均(26.4±3.2)岁;病程2~9年,平均(3.9±1.1)年;BMI 28.3~32.9kg/m2,平均(29.6±1.6) kg/m2。两组基线资料相比差异均无统计学意义(P>0.05),具有临床可比性。
1.2 治疗方法 所有患者均采取相同的一般处理,包括:①饮食指导:根据患者身高、体重、腰围等计算进食总量,严格限制总进食量。②运动指导:指导患者定期进行有规律有氧运动,运动强度以轻、中度为主,可选择游泳、跳绳、慢跑等。对照组:在此基础上,予以盐酸二甲双胍片(中美上海施贵宝制药,国药准字H20023370,规格0.5g/片)治疗;口服,0.5g/次、2次/d,药物随三餐分次服用。观察组:在对照组基础上,加用罗氟司特(瑞士奈科明,批准文号S20120055,规格0.5mg/片)治疗;口服,0.5mg/d。两组均以3个月为疗程。
1.3 观察指标
1.3.1 一般临床指标 于治疗前和治疗3个月后记录两组患者体重、身高等指标,并计算BMI,BMI=体重(kg)/身高2(m)。
1.3.2 糖脂代谢指标检测 ①于治疗前和治疗3个月后清晨对每位患者各采集10ml/次的空腹肘静脉血,离心分离血浆后保存于-20℃冰箱中待检。②测定指标包括低密度脂蛋白胆固醇(LDL-C)、总胆固醇(TC)、甘油三酯(TG)、空腹血浆胰岛素(FINS)、空腹血浆葡萄糖(FPG)。③LDL-C、TC、TG测定仪器采用全自动生化分析仪(拜尔,型号ADVIA 1800),FINS采取葡萄糖氧化酶法测定,FPG采取化学发光法测定,试剂盒均由烟台奥斯邦提供;④以上各指标测定步骤均严格遵照各自配套说明书执行。
1.3.3 性激素指标测定 ①分别在治疗前和治疗3个月后于月经周期3~5d清晨对每位患者各采集10ml/次的肘静脉血,离心分离血清,保存于-80℃冰箱中待检。②测定指标包括睾酮(T)、卵泡刺激素(FSH)、促黄体生成素(LH),测定仪器采用全自动酶标仪(美国Thermo,型号Multiskan FC)。③T、FSH、LH均采取化学发光法测定,试剂盒均购自拜尔公司。④以上各指标测定步骤均严格遵照各自配套说明书执行。


2 结果
2.1 两组患者治疗前后一般临床指标的比较 与治疗前比较,观察组治疗3个月后体质量、BMI均显著下降(P<0.01),且显著低于对照组同期(P<0.01);对照组治疗前后体质量、BMI对比差异无统计学意义(P>0.05),见表1。

Table1Comparisonofthegeneralclinicalindexesbetweentwogroupsbeforeandaftertreatment

组别n身体质量指数(kg/m2)治疗前治疗后P观察组4629.5±1.526.3±1.40.000对照组4629.6±1.629.2±1.50.216P0.7580.000
2.2 两组患者治疗前后糖脂代谢水平的比较 与治疗前对比,两组治疗3个月后血浆LDL-C、TG、TC、FPG、FINS水平均显著下降(P<0.01),且观察组降低更显著(P<0.01),见表2。
2.3 两组患者治疗前后性激素水平的比较 与治疗前相比,两组治疗3个月后血清性激素T、FSH、LH水平均显著下降(P<0.01),且观察组以上指标降低较对照组更显著 (P<0.01),见表3。

表2 两组患者治疗前后糖脂代谢水平的比较±s,mmol/L)Table 2 Comparison of the glucose and lipid metabolism level between the two groups before and after treatment
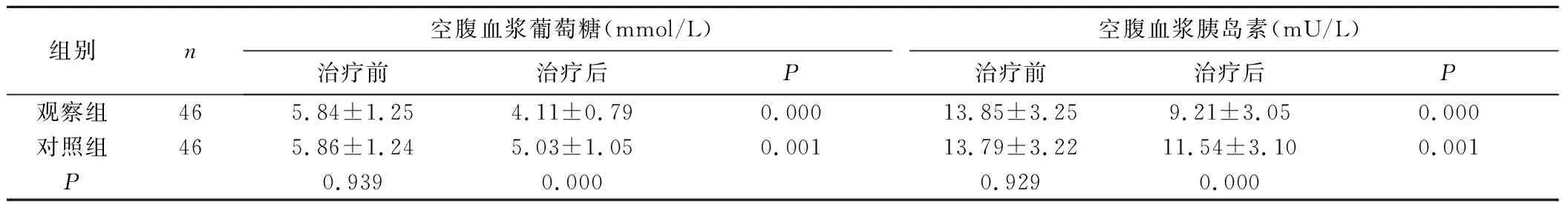
组别n空腹血浆葡萄糖(mmol/L)空腹血浆胰岛素(mU/L)治疗前治疗后P治疗前治疗后P观察组465.84±1.254.11±0.790.00013.85±3.259.21±3.050.000对照组465.86±1.245.03±1.050.00113.79±3.2211.54±3.100.001P0.9390.0000.9290.000

表3 两组患者治疗前后血清性激素水平的比较±s)Table 3 Comparison of the serum sex hormone levels between the two groups before and after treatment
2.4 两组患者临床疗效的比较 治疗3个月后,观察组总有效率为91.3%(42/46),较对照组明显升高[73.9%(34/46),P<0.05],见表4。
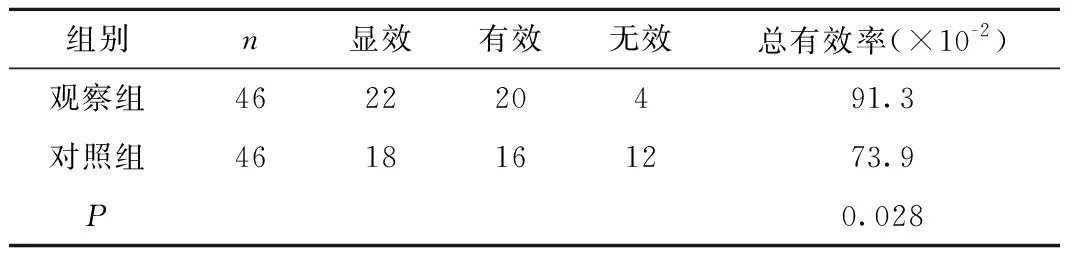
表4 两组患者临床疗效的比较Table 4 Comparison of the clinical effect between the two groups
3 讨论
PCOS病因尚未明确,现主要认为其发生发展与肾上腺功能异常、高胰岛素血症、肥胖、胰岛素生长因子失调等因素有关。PCOS属内分泌紊乱性疾病,主要生理病理改变涉及蛋白质代谢、神经内分泌障碍、卵巢局部调控异常、糖脂类代谢等多个方面[11]。现代医学认为PCOS两大生理病理基础为胰岛素抵抗与高雄激素血症,两者均可对胰岛素受体产生作用,促进卵泡膜细胞分泌雄激素等。因而对于PCOS治疗关键在于减轻胰岛素抵抗,降低雄激素水平[12-13]。另有研究[14]发现PCOS对胰岛素的作用与脂肪分布有关,肥胖可导致糖耐量异常、高雄激素血症、月经失调甚至不孕症。肥胖还可导致患者对促性腺激素反应迟缓,严重影响患者的生殖能力。此外研究[15]显示肥胖型PCOS患者减少2%~5%BMI,即可显著改善患者临床症状。BMI的降低不仅能够改善患者外周组织对胰岛素的敏感性,还能增强细胞内胰岛素作用,减少雄激素的合成。因而对于肥胖型PCOS患者降低其BMI为其治疗当中的重要举措。合理饮食、加强运动虽能在一定程度上减轻BMI,但多数患者依从性较低,疗效有效,因此亟需寻找有效的减重方法改善肥胖型PCOS患者病情发展[16]。
二甲双胍为临床常用胰岛素增敏剂,其治疗PCOS的优势在于能通过增加胰岛素受体,提高胰岛素敏感性,缓解高雄激素血症,以恢复PCOS患者生育功能[17],其具体作用机制为[18-19]:①通过改善胰岛素抵抗,阻断胸腺垂体异常分泌LH,进而起到减少卵巢雄激素水平和降低LH水平的作用;②直接通过抑制刺激腺苷酸环化酶激活剂的mRNA的表达,抑制卵巢泡膜细胞合成雄激素,达到改善高雄激素血症的效果;③通过提高外周组织胰岛素与其受体结合,促进葡萄糖氧化磷酸化,提高胰岛素外周水平敏感性。一项动物实验[20]显示二甲双胍能通过降低PCOS大鼠内质网应激水平和激活肝脏组织AMPK通路改善肝脏脂肪沉积和胰岛素抵抗,发挥抗PCOS作用。大量临床研究[21-22]也已表明二甲双胍能通过改善PCOS患者改善胰岛素抵抗的途径提高治疗效果,且安全性高。罗氟司特属磷酸二酯酶-4抑制剂,其用于治疗肥胖型PCOS患者的作用机制可能是①通过调节PCOS病理生理信号通路,对应答炎症反应和类固醇激素产生调控作用,促进内分泌稳定;②通过影响机体内葡萄糖稳态,以达到降低患者BMI的作用[23]。曹旭等[24]研究显示哮喘-慢阻肺重叠综合征经口服罗氟司特干预后其血清炎性细胞因子水平显著降低,这可能与罗氟司特具有的抗炎作用关系密切。同时报道[25]称肥胖型PCOS患者采用罗氟司特治疗能显著减轻BMI,缓解临床症状。
本研究中与仅予以二甲双胍治疗的对照组同期相比,在此基础上加用罗氟司特治疗的观察组治疗3个月后体质量、BMI均显著降低,这与相关报道[25]结果相似;提示肥胖型PCOS患者采用罗氟司特联合二甲双胍治疗方案更有助于降低患者体质量和BMI,究其原因可能与罗氟司特影响机体内葡萄糖稳态有关。有文献[26]也发现罗氟司特可通过影响2型糖尿病患者机体内的葡萄糖稳态,起到减轻BMI的作用。有研究[27]指出肥胖型PCOS患者性激素T、FSH、LH水平均显著高于正常人群,其机制可能与脂肪细胞因子和胰岛素抑制促性腺激素释放激素有关。本研究显示与对照组同期对比,观察组治疗3个月后血清性激素T、FSH、LH水平均下降更显著;提示肥胖型PCOS患者采用罗氟司特联合二甲双胍治疗更有助于调节机体性激素水平,分析原因可能与罗氟司特、二甲双胍两者能通过各自的药理作用机制协同发挥细胞因子调节作用有关,这可能也是本治疗方案治疗肥胖型PCOS的重要机制之一。目前尚未发现直接证据证实罗氟司特对类固醇激素合成分泌途径的影响,推测可能与罗氟司特具有广泛的抗炎作用密切相关。有文献[28]称PCOS机体慢性炎症状态与性激素含量具有相关性。罗氟司特可能通过直接调控PCOS患者机体炎性因子表达水平,继而间接发挥调节性激素分泌的作用。相关研究[29-30]显示肥胖型PCOS患者存在糖脂代谢紊乱状态,其糖耐量显著降低,糖尿病风险显著上升。本研究中观察组治疗3个月后血浆LDL-C、TG、TC、FPG、FINS水平均显著低于对照组同期;提示罗氟司特联合二甲双胍治疗肥胖型PCOS对内分泌系统具有良好的调控作用,更有利于改善机体糖脂代谢紊乱状态,这或许也是两者联合治疗肥胖型PCOS增效的另一关键机制。同时本研究结果显示与对照组(73.9%)比较,观察组治疗3个月后总有效率达91.3%,明显升高;表明该联合用药方案更能有效缓解肥胖型PCOS患者的症状体征,这与本研究患者机体糖脂代谢、性激素水平的改善结果是一致的;究其原因可能与罗氟司特与二甲双胍联合用药方案降低肥胖型PCOS患者BMI有关,通过BMI的降低可提高外周组织对胰岛素的敏感性,继而减少卵巢合成雄激素,降低机体内雄激素水平,进而发挥增效作用[31]。当前对于肥胖型PCOS患者的体质量控制多采用饮食控制和规律运动,利用罗氟司特减轻肥胖型PCOS患者BMI的研究较为少见,本研究从控制肥胖型PCOS患者BMI和减少胰岛素抵抗两方面设计治疗方案,采用罗氟司特和二甲双胍联合治疗方案,从而提升整体治疗效果。
4 结论
本文资料显示,应用罗氟司特联合二甲双胍治疗肥胖型PCOS患者能有效降低患者BMI,改善糖脂代谢和性激素水平,缓解或消除症状体征,疗效显著。但其作用机制及长期疗效与安全性仍需临床大样本、多中心、长期的研究加以探讨与分析。

