阿莫西林胶囊特征指纹溶出过程图谱研究
陈 荣,邹自旺,李焕欣,刘 珊,刘文彬
(1.东华理工大学 化学生物与材料科学学院,江西 南昌 330013;2.东华理工大学 长江学院,江西 抚州 344000)
抗生素相比其它药品,应用广泛,但存在着大量假冒仿制品(Delepierre et al.,2012),为确保其质量,目前开发出的检测方法众多,主要包括检测抗生素制剂活性成分的技术(Abigall et al.,2013)和药品特征指纹图谱技术(陈荣等,2011)。特征指纹图谱技术相比于制剂活性成分检测,不仅能检测所含活性成分,还可探查其生产工艺及采用的原材料的不同,更有利于高仿产品的区分,从而确保用药安全及生产企业的利益。目前开展的此项技术主要有红外光谱法、拉曼光谱法及表面常温常压解吸质谱技术(Zhang et al.,2010 ),但这些技术相对于我国假药流通盛行的偏远地区而言,对当地检测人员的素质、检测费用及设备配置都提出了挑战。因此,有必要开发一种新的特征指纹图谱技术以实现我国落后地区假劣药品的快速筛查。
相关文献表明,抗生素原料的晶型及晶粒大小、非晶状态、制剂的赋形剂、制备工艺等不仅影响了制剂的稳定性,还影响制剂中有效成分的溶出(陈格等,2013;Feng et al.,2006;Narang et al.,2012)。溶出度长期以来用作药物制剂质量的一项考量方法,各国药典虽然对抗生素制剂明确提出了在一定条件下活性成分的溶出要求,但国内目前在新药审评和药检机构后期制订国家标准时,其拟定试验参数的出发点是为了让即有产品合格,而国外原研企业出于自身利益,只对外公布了较为宽松的货架质量标准,而对最具区分力的内控实验条件给予保密(谢沐风,2014),该因素可能导致不同厂家抗生素制剂虽然在规定时间内达到药典规定的溶出量,但溶出曲线却存在差异,大量文献也证实了这一现象(顾珉等,2012;Zuo et al.,2014)。但目前的文献对该种现象仅给出了产品质量评估及仿制药开发两方面的评价,尚未有用于制剂来源鉴定方面的相关报道。考虑到假劣药品主要分布在欠发达的农村,药品溶出仪可能存在短缺,故在本文中利用不同来源制剂有效成分溶出速度可能存在的差异,采用易于获取的1 000 mL的烧杯取代溶出杯进行有效成分溶出量的检测。
阿莫西林由于其药效好,价格低,在临床上有着更为广泛的应用,生产厂家众多(张骁等,2002),故在本研究中以阿莫西林为研究对象,利用原料及工艺不同导致的溶出及稳定性的不同这一特性,改变溶出条件,建立同一厂家在多个条件下的溶出曲线指纹图谱,通过在不同条件下溶出过程曲线走势及在图中的相对位置确定制剂来源,以适用于偏远地区抗生素质量及来源的快速检测。
本文分别模拟中壮年及老年期人体胃部及肠道酸度为溶出条件,建立不同厂家的溶出过程指纹图谱,该图谱的建立不仅可用于制剂来源的检测,还可考察制剂质量及其在体内不同部位及时期的有效性,该法操作简单,对设备及人员素质要求不高,将有效促进偏远地区抗生素假劣制剂的排查,保障人们的健康,同时有利于正当制药企业的健康发展。
1 仪器与药品
UV757CRT型紫外可见分光光度计(苏州江东精密仪器有限公司);AR124CN型电子天平(上海实干实业有限公司);DF-101S集热式恒温加热水浴锅(金坛市盛威实验仪器厂);PHS-3C型pH计(上海仪电科学仪器股份有限公司)。市售阿莫西林胶囊0.25 g/粒(A厂家、B厂家和C厂家各取三个批次);阿莫西林胶囊0.5 g/粒(D厂家及E厂家各取三个批次);盐酸;去离子水。
2 实验方法
用去离子水和盐酸溶液配成900 mL不同酸度(pH分别为1.2,4.5,6.8)的溶液为溶出介质,水浴锅(37±0.5) ℃恒温加热,转速100 r/min,测定阿莫西林胶囊60 min内的溶出情况。检测波长272 nm,前20 min每5 min检测一次,后40 min每10 min检测一次。
3 结果与讨论
图1至图3分别为A,B和C三个厂家的0.25 g规格的阿莫西林胶囊在溶出介质pH分别为1.2,4.5,6.8条件下的溶出过程特征曲线图谱。
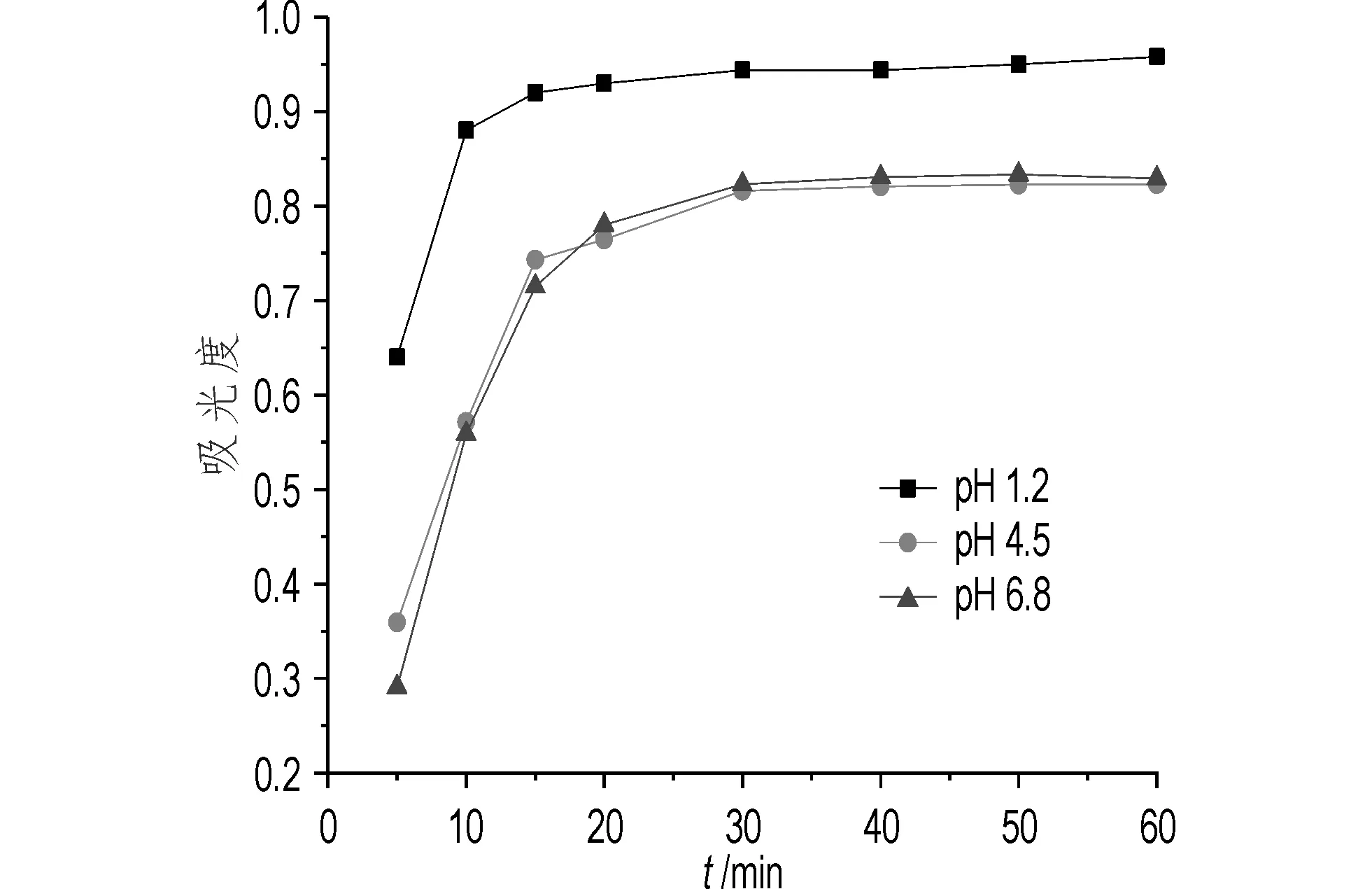
图1 A厂家阿莫西林胶囊的溶出曲线Fig.1 Dissolution profiles of A factory amoxicillin capsules
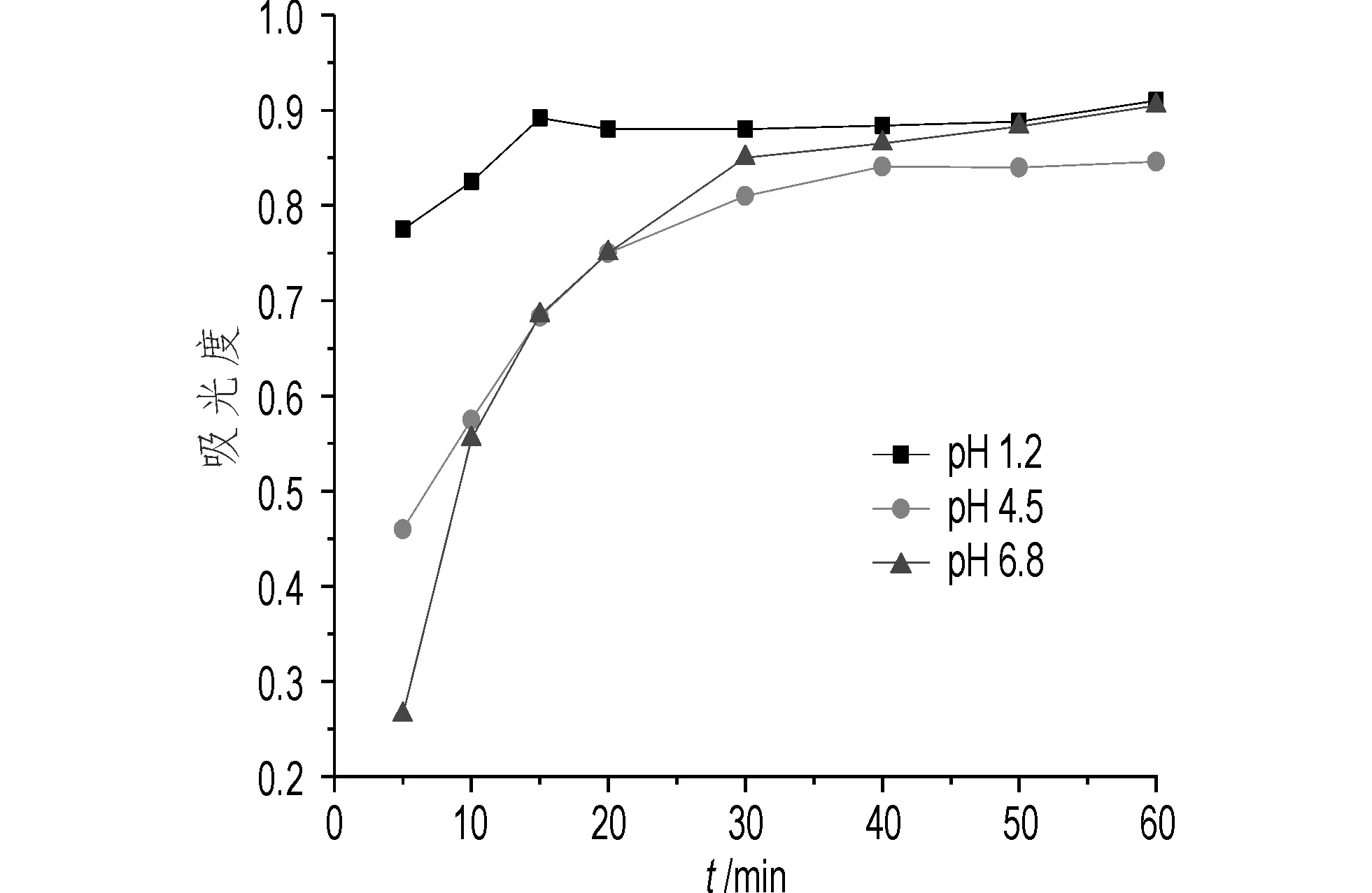
图2 B厂家阿莫西林胶囊的溶出曲线Fig.2 Dissolution profiles of B factory amoxicillin capsules

图3 C厂家阿莫西林胶囊的溶出曲线Fig.3 Dissolution profiles of C factory amoxicillin capsules
由图1可看出,A厂家的药剂在溶出介质pH为1.2时在整个溶出过程中的溶出量明显高于pH 4.5和pH 6.8条件下的溶出量,在20 min时达到最大溶出,随后在溶液中的溶出量基本平稳;而在 pH 4.5和pH 6.8条件下,30 min后才达到最大溶出量,其中,pH 4.5时在溶出近20 min之前,溶出量稍高于pH 6.8条件下的溶出量,但其后溶出量稍低,并有轻微降解;溶出介质pH 6.8时,30 min达到最大溶出后,溶出量表现平稳,直到50 min后有轻微降解。该图通过曲线的相对位置及走势建立了A厂制剂的特征指纹溶出图谱,而且,由图1还可看出,A厂胶囊相比于在弱酸条件下,在强酸条件下快速释放,释放量大,后期药物浓度平稳,适合于在强胃酸条件下释放。由图2可知,B厂家阿莫西林胶囊在溶出介质pH 1.2时其溶出前期即获得快速溶出,在15 min时达到最大溶出量,但随后表现出少量降解;pH 4.5及pH 6.8条件下制剂溶出速度20 min前明显低于pH 1.2条件下的溶出量,在20 min时溶出量差距明显开始减小,pH 4.5条件下溶出量20 min前呈现快速增长,其后慢速增长,至40 min后溶出量保持平稳;pH 6.8条件下20 min前溶出量小于或等于pH 4.5条件下的溶出量,但20 min后则高于pH 4.5条件下的溶出量,并一直呈现上升的趋势,60 min时近似于pH 1.2条件下的溶出量。该三条曲线构成了B厂家的特征指纹溶出图谱,此外,由图2可看出,B厂胶囊在强酸状态表现了降解,会引发更多的降解产物,可能导致致敏物质增加,且后期药物浓度与弱酸条件药物浓度接近,故更适合在弱胃酸及肠道吸收条件下使用。由图3可知,C厂家阿莫西林胶囊在溶出介质pH 1.2条件下20 min时达到最大溶出量,其后出现轻微降解;在pH 4.5时40 min达到最大溶出量,其后溶出量基本保持平稳;在pH 6.8条件下溶出量在经历15 min的快速上升期后,增长速度明显放缓;C厂家胶囊在这三个条件下的溶出曲线总体表现为在15 min前溶出量快速上升,其后变化放缓,溶出量随酸度升高而增大。这三条溶出曲线构成了C厂家的特征指纹溶出图谱,此外,由图3可看出,C厂胶囊在肠道酸度下溶出较小,更适合胃部使用,应用于空腹下使用。将图1,图2及图3的特征指纹图谱相比较,图谱表现出明显的不同,可有效区分三厂家产品。
图4和图5分别为D,F厂家的0.5 g规格的阿莫西林胶囊在pH分别为1.2,4.5和6.8条件下的溶出曲线特征图谱。
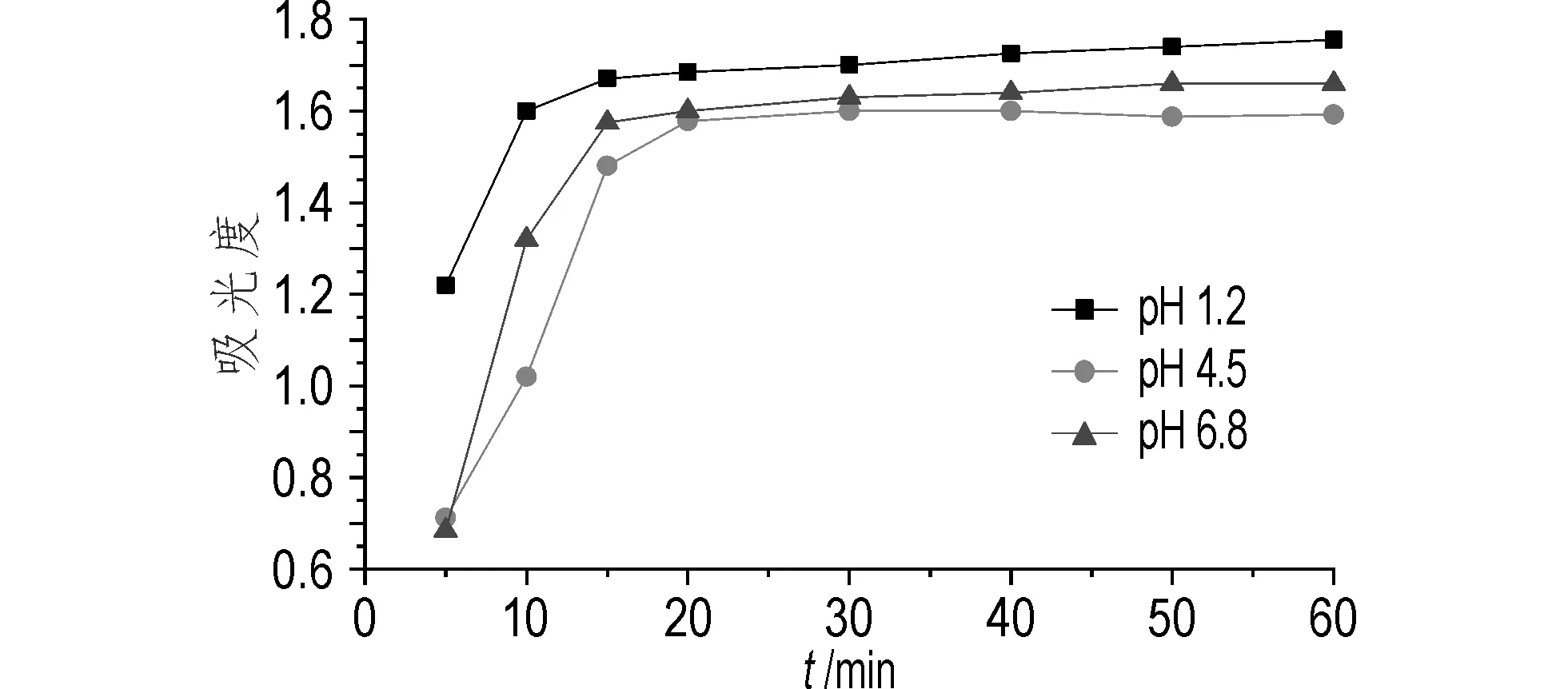
图4 D厂家阿莫西林胶囊的溶出曲线Fig.4 Dissolution profiles of D factory amoxicillin capsules
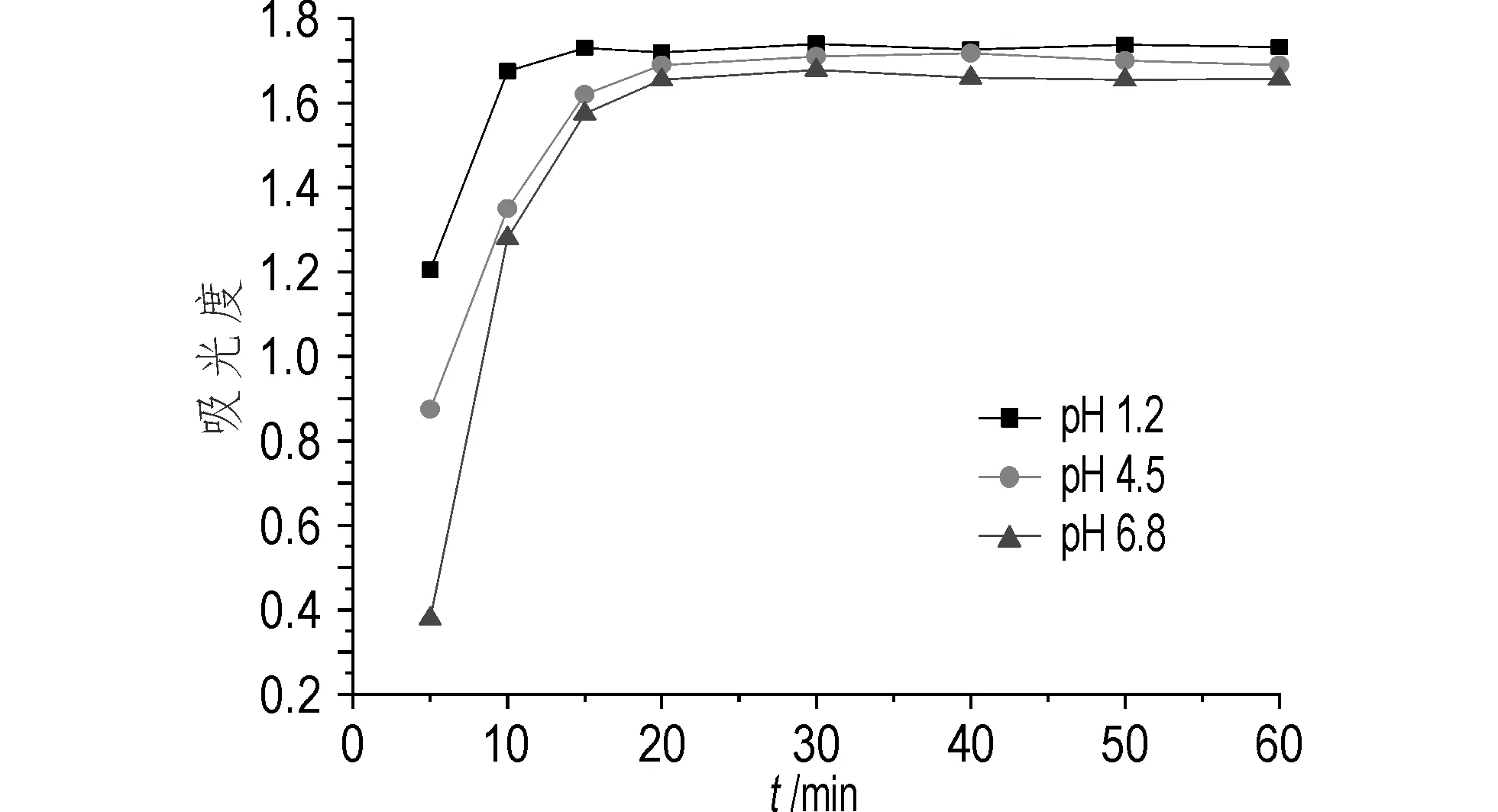
图5 E厂家阿莫西林胶囊的溶出曲线Fig.5 Dissolution profiles of E factory amoxicillin capsules
由图4可知,D厂家阿莫西林胶囊在溶出介质pH 1.2条件下起始溶出量快速增加,在15 min时达到最大溶出,其后溶出量增长缓慢;pH为4.5条件下,胶囊除起始溶出稍高于pH 6.8条件下,其它时间的溶出均低于pH 6.8条件下,且20 min达到最大溶出后,出现缓慢降解;pH为6.8条件下,胶囊溶出量在15 min前快速增加,其后增长缓慢,虽低于pH1.2条件下,但曲线图走向类似。这三条溶出曲线构成了D厂家的特征指纹溶出图谱。由图5可知,E厂家阿莫西林胶囊三条溶出曲线随酸值下降,溶出曲线也依次向下排列,其中,在pH 1.2条件下15 min达到最大溶出量,但随后出现降解;pH 4.5条件下前15 min溶出量快速增长,接着增长缓慢,40 min达到最大溶出度,其后出现轻微降解;在pH 6.8条件下,溶出量前15 min是快速增加,然后缓慢增长至30 min溶出量达到最大,其后出现轻微降解。这三条溶出曲线构成了E厂家的特征指纹溶出图谱。将图4和图5相比较,两谱图仍显示出较明显差异。但0.5 g规格的胶囊相比于0.25 g规格的胶囊,溶出量受pH影响程度更低,三条曲线溶出走势及溶出量相近,容易导致误判。针对这种状况,实验改变溶出温度,选取pH 1.2条件下的D和E厂家胶囊进行了溶出度检测(图6)。
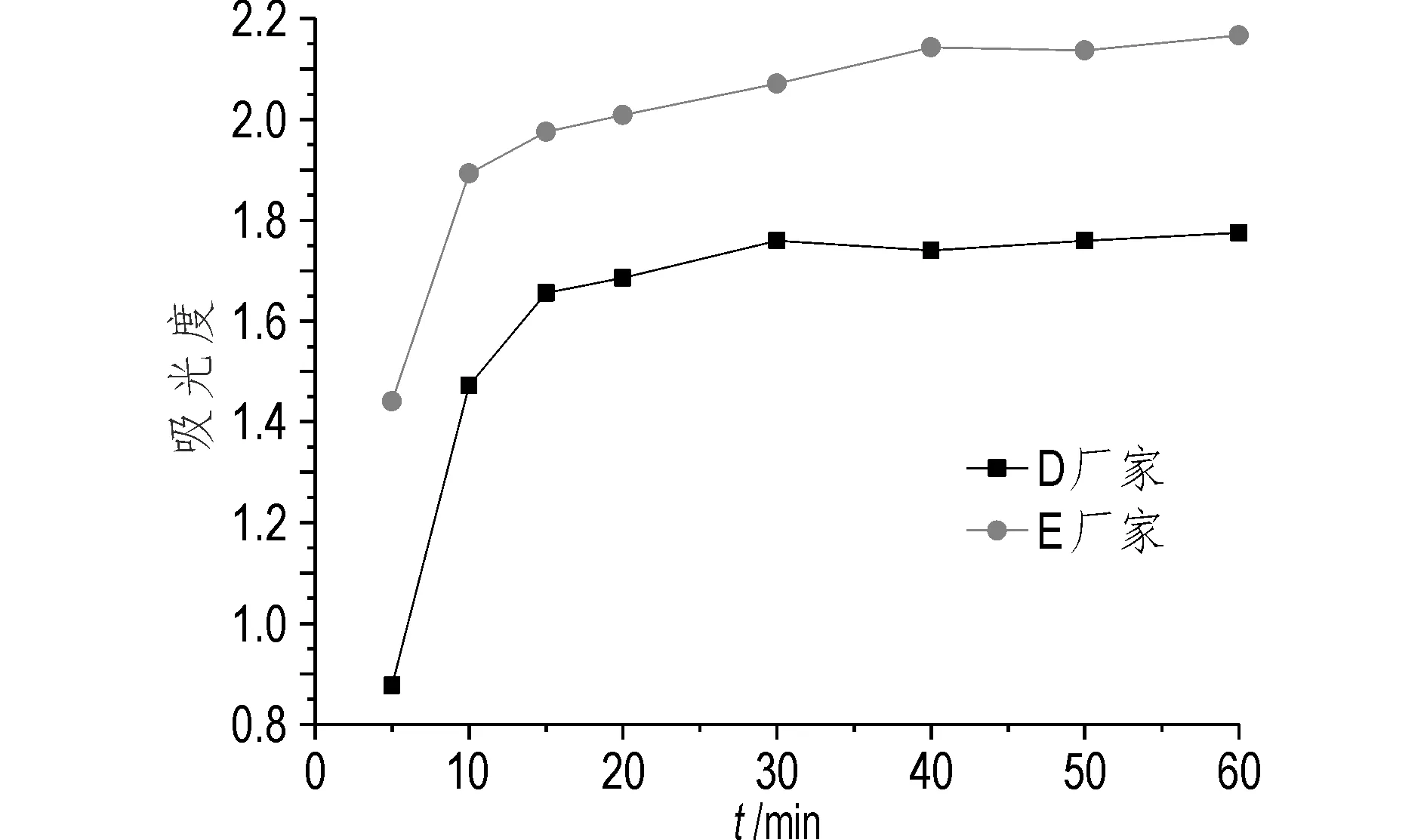
图6 pH 1.2,45 ℃条件下D和E厂家阿莫西林胶囊溶出曲线Fig.6 Dissolution profiles of D and E factories amoxicillin capsules at 45 ℃ in pH 1.2
由图6可知,在pH 1.2溶出介质中,E厂家阿莫西林胶囊在45 ℃条件下相比于D厂家阿莫西林胶囊,其整个溶出曲线大幅上移,区分明显,说明其溶出受温度影响更大。由此可见,对于一些常规检测条件下特征指纹图谱区分不大的制剂,可通过改变温度这一条件进一步将其区分开,这可能是由于原料及制备工艺的不同导致其对温度的敏感度不同,从而造成溶出差异。
4 结语
本文采用的药品均采自市场常见知名厂家制剂,前期研究表明其同批次及不同批次溶出稳定,此类企业产品由图1至图5比较可知,建立溶出介质pH分别为1.2,4.5及6.8条件下的特征溶出过程曲线图,通过这三个条件下三条溶出曲线图的溶出走势及溶出曲线的相对位置所构成的特征指纹图谱可有效地判断药品厂家来源。对部分差异不明显的指纹图谱,可通过改变温度实现进一步区分。但对于文献中提出的极少量生产质量不稳定的厂家产品的区分有待于作进一步研究。此外,以上指纹图谱的建立也揭示了其在人体中应用的有效性,及在人体不同部位的释放性及稳定性,如果能建立齐全的阿莫西林胶囊的特征指纹溶出图谱,不仅可用于药物的来源筛查,还能用于人体用药的选择及质量参考。

