花状SnO2纳米粉体的制备与气敏性能
焦万丽,张 磊
(山东理工大学 材料科学与工程学院,山东 淄博 255049)
0 引 言
氧化锡是一种原材料丰富、价格低廉、无毒的宽禁带n型半导体氧化物,禁带宽度为3.65 eV,在透明导电膜、气敏传感器、光催化和太阳能转换等领域都有广泛的应用。其中最重要的用途之一就是制作气敏传感器件[1-3]。由于其气敏机理属于表面控制型,所以SnO2粉体粒径的大小、表面形貌以及比表面积的大小对气体灵敏度的影响十分重要。采用液相法制备纳米SnO2半导体氧化物颗粒的方法很多, 例如: 化学沉淀法[4]、溶胶- 凝胶法[5]、微乳液法[6]和水热法[7,8]等,其中水热法因其反应简单、操作简便、易于控制,并且成本较低被优先考虑。除零维纳米颗粒外, 其它形态的纳米材料都具有各向异性,比表面积大的特点, 因此改变纳米SnO2形貌的研究受到广大科技工作者的关注。表面活性剂一直是作为辅助控制纳米粉体形貌的一种常用的方法。而不同的表面活性剂在不同的制备工艺下,产生的影响机理也不同。贾铁昆等[9]以十六烷基三甲基溴化铵(CTAB)为软模板,采用水热法制备了蠕虫状介孔金红石型SnO2,介孔尺寸为5.8 nm,增大了材料的比表面积,有效提高了电化学性能。Wang等[10]采用水热法,制备了ZnO-SnO2中空球及纳米片,Zhou等[11]以PEG-400为表面活性剂,采用水热法制备出由纳米棒组装形成的SnO2微球。刘程等[12]采用原位掺杂法制备了Pt-SnO2花状纳米结构,详细研究了反应物中Pt与Sn的摩尔比对花状纳米结构的影响。虽然近年来研究者们通过掺杂金属如Pb[13]、Al[14]或其它金属氧化物粉体如ZnO[15]、La2O3
[16]、CuO[17]和NiO[18]来改善气敏材料的选择性,但掺杂或改性的第二相物质通常采用浸渍法或二次生长法附着或生长于基体材料表面,因此要想获得高的比表面积,基体材料具有大的比表面积和异形结构是十分重要的。
本文以SnCl4·5H2O和NaOH为原料,详细考察了溶液pH值、水热反应温度和时间以及不同表面活性剂等对花状SnO2纳米结构形成过程的影响。并对其制备的旁热式气敏元件的气敏性进行了测试。
1 实 验
1.1 SnO2纳米粉体的制备
准确称量7.0 g结晶SnCl4·5H2O溶在20 mL蒸馏水中,分别取一定量的7 mmol/L的NaOH溶液倒入SnCl4溶液中,pH值分别控制为2、4和11,持续搅拌1 h,将上述悬浊液转移到50 mL高压反应釜里进行水热反应,填充率为70-75 %,水热反应温度分别设定为180 ℃、220 ℃及260 ℃,水热反应时间分别定为9 h、12 h及15 h,反应结束后使其自然冷却至室温,后取出,反复用蒸馏水及无水乙醇清洗,离心分离后干燥待测,确定出水热反应的最佳制备工艺。为了改变SnO2纳米晶形貌,分别加入一定量的十六烷基三甲基溴化铵(CTAB)和聚乙二醇—600(PEG)表面活性剂,按照上述最佳制备工艺制备SnO2纳米晶,考察不同表面活性剂对SnO2纳米晶相结构及形貌的影响。
1.2 气敏元件的制备
将去离子水和无水乙醇按1︰2配制成溶液,按溶液质量与粉体质量按2︰1配制成料浆,均匀涂敷在带有金电极和Pt电极引线的氧化铝陶瓷管上,陶瓷管尺寸为:外径1.5 mm,壁厚0.3 mm,长4 mm。干燥后在烧结炉中分别在450 ℃、550 ℃和650 ℃下热处理1 h,将铂电极和加热丝焊接到底座上制成旁热式气敏元件,具体请参见文献[19]。
1.3 性能测试
采用日本理学D/max-RB型X射线衍射(X-ray diffraction, XRD)仪分析SnO2纳米粉体样品的物相,CuK,管压40 kV,管流100 mA,测角仪半径185 mm,采用-2步进扫描方式,步长2为0.02 °,扫描速度为8 °/min。用FEI Sirion 200型扫描电镜(scanning electron microscope, SEM)观察SnO2纳米晶微观形貌。采用WS-30A气敏元件测试系统测试气敏元件对乙醇气体的气敏性,测试电压Vc=5 V,元件灵敏度S = 洁净空气中的电阻R0 /测试气体中的电阻Rg。测试之前,元件在老化台上老化4天。
2 结果与讨论
2.1 pH的影响
对不同pH下,水热反应温度均为260 ℃,反应时间为12 h的粉体进行XRD分析,结果如图1所示。
由图1(a)和(b)可以看出,当pH值为2和4时,所制备样品的衍射峰完全与SnO2的标准图谱吻合,而且无杂质峰,三个主要衍射峰所对应的晶面为(110)、(101)、(211),其相应的衍射角分别为2θ=26.50 °,33.88 °,51.74 °。表明样品为纯净的四方金红石型结构的SnO2。当pH=2时,其衍射峰宽化现象严重,衍射峰强度较低,受背底峰的影响明显,说明此时合成的SnO2纳米晶晶粒尺寸小,结晶度不高,存在较多的缺陷。当pH=4时,衍射峰峰形尖锐,强度增强,说明此样品结晶度良好,晶粒尺寸长大。这是由于当加入NaOH而使溶液瞬间显现为碱性时发生如下反应[20]:

[Sn(OH)6]2-阴离子是前驱体,随着反应的进行,[Sn(OH)6]2-水解生成SnO2晶核。但很快OH-消耗尽溶液呈现酸性,Cl-取代OH-发生如下反应:


图1 不同pH值SnO2粉体的XRD图谱Fig.1 XRD patterns of SnO2 powders prepared at different pH values: a) pH = 2, b) pH = 4, c) pH = 11
在这个过程中,[SnCl6]2-阴离子是前驱体,是Sn4+和Cl-在酸性环境中络合而成的。实验结果证明,[SnCl6]2-水解生成SnO2晶核,然后随着水热反应的不断进行而长成SnO2晶体,直至[SnCl6]2-阴离子消耗尽为止。但当pH=11时,除了存在四方金红石型SnO2相的特征峰,还存在SnO的特征峰,而且SnO的特征峰强度很高,说明粉体中大部分为SnO相。分析原因可能是因为在强碱溶液中,新形核的SnO2与NaOH在高温高压环境中发生反应,形成Na2SnO3和Na2SnO2,随着温度的升高Na2SnO3和Na2SnO2分别分解成SnO2和SnO沉淀。
通过分析可以确定当pH=4时,水热法合成纯净的四方金红石型结构的SnO2相,且SnO2纳米晶结晶效果最好。
2.2 水热反应温度的影响
对在pH = 4的条件下,水热反应温度分别为180 ℃、220 ℃及260 ℃,水热反应时间均为12 h,制备的粉体进行XRD分析,结果如图2所示。
由图2可以看出,在不同的水热反应温度下均合成了纯净的四方金红石型结构的SnO2。当在180 ℃较低的反应温度为时,衍射峰的半高峰宽较大,衍射峰强度较低,这表明此时所获得的SnO2晶粒较小,结晶度不高。随着水热反应温度的升高,特征峰的半高峰宽变窄,说明SnO2晶粒长大,结晶度良好。
根据Scherrer公式按(110)晶面计算不同温度下的晶粒粒径:

图2 不同水热反应温度SnO2粉体的XRD图谱Fig.2 XRD patterns of SnO2 powders prepared at different hydrothermal temperatures: a) 180 °C, b) 220 °C, c) 260 °C

其中,Dsize为样品中晶相的统计平均宽度即晶粒粒径;B为微晶产生的峰的变化,即峰的半高宽;k为比例系数;λ为X射线的波长;θ为衍射角。所得结果如表1所示。
从图2还可以看出,图2(c)中的(110)晶面所对应的特征峰的强度比(101)晶面所对应的特征峰的强度高,而图2(a)和(b)中的(101) 晶面所对应的特征峰的强度明显比(110) 晶面所对应的特征强,由此可以判断在高温下(110)晶面生长加快而较低温度下(101)晶面优先生长。综上所述,最终确定水热反应的温度为220 ℃。
2.3 水热反应时间的影响
对在pH=4,水热反应温度为220 ℃的条件下,水热反应时间分别为9 h,12 h及15 h制备的粉体进行SEM分析,结果如图3所示。由图3可以看出在不存在表面活性剂的情况下,由于[SnCl6]2-阴离子相互桥连,新生成的SnO2晶核表面能高,容易聚集生长,SnO2颗粒呈现出花状结构的生成过程。文献[12]同样在未加表面活性剂的前提下,得到了由SnO2短纳米棒自组装生长的纳米花结构。当反应时间低于9 h时(图3a所示),SnO2纳米棒生长发育不好,在颗粒表面存在一层无定形的物质,但同样可以看出颗粒聚集在一起呈花状生长趋势;当反应时间为12 h时,SnO2纳米棒晶体生长发育完全,晶粒尺寸均匀,平均直径为40 nm,长度约为100 nm,而且由纳米棒组成的花状结构明显。当反应时间为15 h时,聚集在一起生长的SnO2纳米棒之间间距增大,有从花状结构中分离出来的趋势,图3c中存在一些离散状的SnO2纳米棒,平均直径为100 nm,长度约为250 nm。由于这种SnO2纳米棒聚集生长花状结构有较高的比表面积,对后期粉体作为气敏元件的应用有益,但时间太长晶粒尺寸太大,反而会降低粉体的比表面积,因此,水热反应的时间定为12 h最佳。
2.4 表面活性剂的影响
图4是采用不同的表面活性剂后,按照上述最佳水热制备工艺得到的SnO2粉体的SEM图。

表1 不同温度下所合成SnO2的晶粒尺寸Tab.1 Grain sizes of SnO2 prepared at different hydrothermal temperatures

图3 不同反应时间制备的SnO2粉体SEM图Fig.3 SEM images of SnO2 powders prepared after different hydrothermal reaction time: a) 9 h, b) 12 h, c) 15 h
由图4(a)可以看出,添加十六烷基三甲基溴化铵(CTAB)后,SnO2纳米粉体大部分是分散的纳米棒状结构,还存在小部分花状结构。原因是当CTAB处于水中时,因其两端分别是疏水的十六烷基基团和亲水的氨基基团,[SnCl6]2-阴离子会与CTAB的NH4+络合吸附,而较长的疏水链露在外面,其空间位阻效应阻碍了[SnCl6]2-阴离子的聚集生长,使得类似花状的生长趋势不明显。但当携带有[SnCl6]2-阴离子的CTAB形成胶束时,随着水解的不断进行,CTAB的空位不断由SnO2晶核所取代,最终就得到了分散的SnO2纳米棒。从图4(a)右上角放大的图中可以明显看到,在纳米棒顶端有很多细小的SnO2纳米晶堆积生长,纳米棒侧面较平整。而添加聚乙烯醇(PEG-600)后,SnO2纳米粉体同样是棒状结构,但生长方式由原来的花状转变为层片状排列(图4b所示)或阵列状排列(图4c所示),而且与图3所示SnO2纳米棒相比,添加PEG-600后,纳米棒尺寸明显增大,平均颗粒直径为200 nm,长度约为500 nm。从图4(c)右侧局部放大图可以看出,添加PEG- 600和添加CTAB后纳米棒尖端形貌有所区别,纳米棒顶端有较大的SnO2纳米晶堆积,且呈现笋状生长。

图4 不同表面活性剂制备的SnO2粉体SEM图Fig.4 SEM images of SnO2 prepared with different surfactants:a) CTAB, b) PEG-600, c) PEG-600
2.5 气敏性能
将在最佳水热制备条件下制备的未加表面活性剂的花状SnO2粉体制成旁热式气敏元件,干燥后在烧结炉中分别于450 ℃、550 ℃和650 ℃下热处理1 h,目的是使SnO2气敏膜与氧化铝陶瓷管形成较高的结合力,不易脱落,同时增加SnO2粉体的稳定性,温度太低达不到上述目的,而温度太高,容易使粉体颗粒长大,降低材料的气敏性能,具体热处理温度一般均由实验决定。图5是不同热处理温度煅烧制备的SnO2气敏元件在300 ℃的工作温度下对低浓度乙醇气体的灵敏度曲线。
由图5可以看出,不同热处理温度对SnO2气敏元件气敏性能的影响不大,当热处理温度为550 ℃时,气敏性能最佳。SnO2气敏元件灵敏度随着乙醇气体浓度的增大而逐渐增加。由于SnO2气敏材料具有花状结构,具有较高的气体通道,当气体到达SnO2花状颗粒表面时,气体会沿着SnO2纳米棒进入颗粒内部,使得粉体具有相对高的比表面积,而SnO2气敏元件属于表面控制型,在空气中,氧分子将在SnO2纳米材料表面吸附,并且俘获SnO2纳米材料中的电子形成O-2,O2-,O-,这就导致本来为N 型导电类的SnO2纳米颗粒电子耗尽,呈现高阻态。当接触到还原性气体时,O-和O2-可以与吸附在金属氧化物表面上的还原性气体离子基团迅速反应,同时将氧俘获的电子归还n-SnO2,表层缺电子层得到电子补充,接触势垒降低,元件电阻降低。因此,比表面积越大,与气体接触的几率越高,元件的灵敏度增大,因而花状SnO2气敏元件对较低浓度的乙醇气体(70 μL·L-1)具有较高的灵敏度,在工作温度为300 ℃时,灵敏度能达到6.5,相比文献[21]采用物理蒸发法制备的细条状SnO2纳米粉体,其对200 μL·L-1的乙醇蒸汽的灵敏度也只有5左右。对气体的响应-恢复特性是气敏元件能否实用化的另一个主要参数,图6是SnO2气敏元件对70 μL·L-1乙醇气体的响应-恢复曲线。
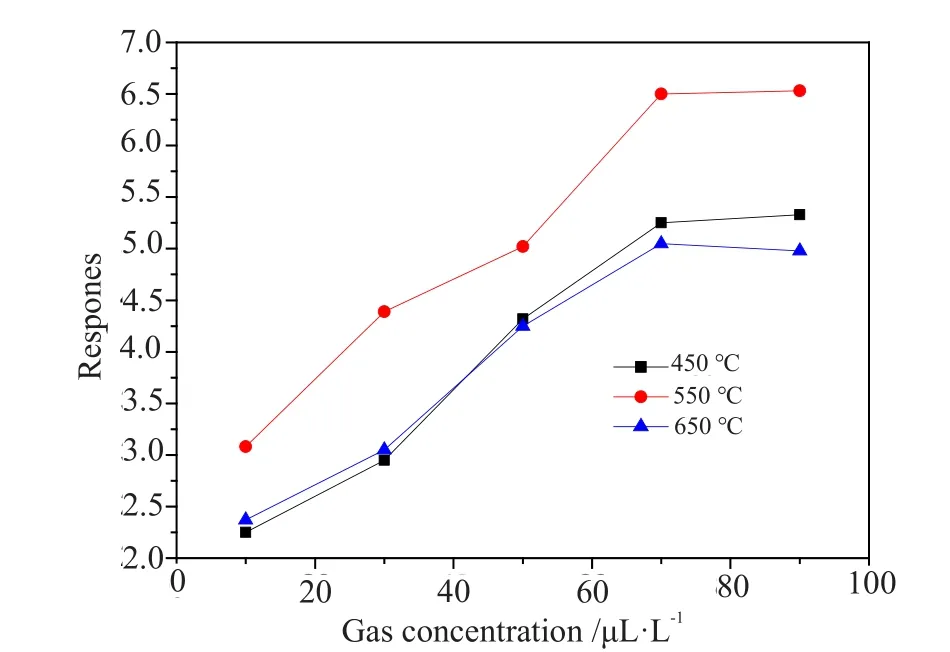
图5 不同热处理温度制备的SnO2气敏元件对乙醇气体的灵敏度Fig.5 Gas responses vs. alcohol gas concentration of SnO2 gas sensors annealed at different temperatures

图6 SnO2气敏元件响应-恢复曲线Fig.6 Response- recovery curve of SnO2 gas sensor
由图6可以看出SnO2气敏元件对70 μL·L-1乙醇气体的响应-恢复时间分别为2 s和20 s,响应恢复特性良好。
3 结 论
以SnCl4·5H2O和NaOH为原料,通过水热法合成了SnO2纳米粉体,其最佳制备工艺为:溶液pH值为4,水热反应温度为220 ℃、时间为12 h,此时制备的金红石型SnO2纳米颗粒呈现花状,由平均直径为40 nm,长度约为100 nm的纳米棒组成。添加表面活性剂CTAB阻碍了SnO2纳米棒的聚集生长,而添加PEG-600则可以将原来的SnO2纳米棒花状聚集生长改变为层片状排列或阵列状排列,纳米棒尺寸增大,纳米棒尖端呈现笋状生长。花状SnO2颗粒制备的气敏元件在300 ℃下对70 μL·L-1的乙醇气体的灵敏度为6.5,响应-恢复时间为2 s和20 s,响应恢复特性良好。

