俄罗斯杨水培苗对硼胁迫的生长和生理响应
吴英青,冯 阳,唐 容,龙丽蓉,欧庸彬
(西南科技大学 生命科学与工程学院,四川绵阳 621010)
硼元素是植物必需的微量元素之一,对植物正常生长和农作物产量有着重要作用[1]。但是,适合植物生长发育的土壤有效硼浓度范围非常狭窄,一般认为是0.5~1.0 mg/kg,因此经常出现缺硼和硼中毒的现象[2]。由于土壤形成母质及干旱、半干旱地区降水稀少、蒸发量大等原因,世界范围内很多地区土壤有效硼含量较高[3]。中国西部和北方地区土壤有效硼含量较高,西藏阿里地区盐碱土有效硼浓度高达23 mg/kg[4]。另一方面,人类活动也可能导致土壤有效硼的积累,中国涉硼企业面积大、分布广,硼的总排放量较大,辽宁宽甸硼矿开采区的土壤全量硼含量高达1 195 mg/kg[5]。
植物硼中毒的一般症状,先是叶尖或叶缘褪绿,接着出现黄褐色的坏死斑,扩展到侧脉,进而向中脉延伸,最终导致叶片坏死或呈枯萎状,并过早脱落[6]。另外,植物根系对高硼胁迫比较敏感,根尖分生组织活性被抑制,细胞分裂速度减缓,根长变短[7]。在高硼条件下,植物受到活性氧伤害,输导组织被破坏,木质素和木栓质在植物体内累积,进而影响组织分生,导致植物生长停滞[8]。
杨树对高硼胁迫具有很强的耐性,是硼超累积植物。当土壤有效硼浓度为40 mg/kg时,杂交杨叶片积累的硼浓度高达1 200 mg/kg,是同一条件下其他物种的20倍[9]。研究表明,某些杂交杨能耐受的土壤有效硼浓度达到93 mg/kg,且其生物量与对照相比没有降低[10]。考虑到杨树生长迅速,生物量大,根系发达,适应性强等特点,可以利用杨树对富硼土壤和硼污染进行生物修复。目前,该方法已被成功应用于造纸厂所排放富硼废弃物的修复[11]。最近的研究显示,来自于杨柳科的8个树种中,黑杨(P.nigra)最适合用于修复湿地生态系统的硼污染[12]。我们课题组的前期研究分析了土培盆栽杨树对长时间(2个月)硼胁迫处理的生理响应特征,发现分布在中国西北部的新疆杨(P.bolleca, 银白杨变种)和俄罗斯杨(P.russkii, 欧洲黑杨杂交种)均对硼胁迫具有较高的耐性[13]。本研究进一步采用水培试验,分析俄罗斯杨对短期(7 d)硼胁迫的生理响应特征,为进一步研究杨树的高硼耐性机理和利用俄罗斯杨修复硼污染提供理论基础。
1 材料和方法
1.1 植物材料培养
本研究采用俄罗斯杨(Populusrusskii)作为实验材料。为了避免不同单株之间的差异,减小实验误差,实验材料取自同一棵生长于西南科技大学温室旁的树龄为3年的俄罗斯杨。实验从2017年7月29日开始进行。剪取直径约为1 cm的枝条,去除叶片,剪成长约10 cm的插穗,约150枝。将插穗下端2 cm浸在自来水中,遮光,生根5 d,每天换水。挑选生根良好的插穗,置于1/2 Hoagland溶液中水培,每周更换营养液。水培4周后,挑选生长情况较一致的植株用于后续实验。水培和后续处理均在西南科技大学温室中完成,采用自然光照,水帘降温。
1.2 实验设计
调查显示,涉硼工业区土壤和水体硼浓度均较高,辽宁宽甸的地下水平均硼浓度为1.7 mmol/L,涉硼企业所排放污水的平均硼浓度为13.0 mmol/L[14]。因此,本试验设置4个硼浓度处理,采用1/2 Hoagland溶液加入硼酸配制而成,即CK(1/2 Hoag-land溶液,硼酸浓度为0.05 mmol/L)、BS1(1/2 Hoagland溶液+1 mmol/L硼酸)、BS5(1/2 Hoag-land溶液+5 mmol/L硼酸)、BS10(1/2 Hoagland溶液+10 mmol/L硼酸)。每种浓度处理18株,分为3个实验重复。处理7 d后,先测定植物叶片净光合速率和叶绿素荧光参数;然后取第5~10叶位的成熟叶片,用锡箔纸包装,液氮速冻,-80 ℃冰箱保存,并在2周内进行相关生理指标测定。
1.3 测定指标及方法
叶片净光合速率(Pn)采用Li-6400便携式光合作用测定系统(Li-Cor, Lincoln, NE, USA)测量,叶绿素荧光参数PSⅡ原初光能转换效率(Fv/Fm)采用M-PEA植物光合效率分析仪(Hansatech Instruments Ltd., UK)测定。测定时,选择植株第4叶位的叶片在天气晴朗的上午9: 00~11: 00进行活体测定。
其他生理指标采用苏州科铭生物技术有限公司生产的试剂盒进行测定。先将样品在液氮中充分研磨,取约0.2 g粉末至2 mL或10 mL离心管(分析天平称重,液氮预冷),分析天平称出总重,并计算出样品净重。然后参照试剂盒说明书测定以下指标:光合色素含量(货号:CPL-2-G)、过氧化氢含量(H2O2-2-Y)、丙二醛含量(MDA-2-Y)、超氧化物歧化酶活性(SOD-2-Y)、过氧化物酶活性(POD-2-Y)、抗坏血酸过氧化物酶活性(APX-2-W)、抗坏血酸含量(ASA-2A-W)、脯氨酸含量(PRO-2-Y)、可溶性糖含量(KT-2-Y)和可溶性蛋白质含量(KMSP-2-W)。
1.4 数据处理与分析
实验数据利用Microsoft Excel 2013软件处理并作图,用SPSS17.0软件进行方差分析及差异显著性检验(Tukey’s test,P< 0.05)。
2 结果与分析
2.1 硼胁迫对俄罗斯杨水培苗生长状态的影响
俄罗斯杨水培苗在硼胁迫处理7 d后的生长状态如图1所示。其中, BS1处理水培苗根系和叶片均未见硼毒害症状,且叶片比对照更为鲜绿; BS5处理水培苗叶片褪绿变黄,但幼嫩茎和根系与对照无明显差异; BS10处理水培苗叶片严重变黄,成熟叶片表现尤为明显,幼叶轻微卷曲,幼嫩茎节间伸长明显受到抑制,根系长度变短,颜色略显黄色,根尖数量变少。可见,俄罗斯杨水培苗在1 mmol/L硼酸处理下生长得到促进,在5 mmol/L硼酸处理下呈现轻微胁迫症状,而在10 mmol/L硼酸处理下表现出严重毒害症状。
2.2 硼胁迫对俄罗斯杨水培苗净光合速率和PSⅡ原初光能转换效率的影响
随着硼酸浓度的增加,俄罗斯杨叶片净光合速率(Pn)呈先升高后下降的变化趋势,并在BS1处理时达到最高;BS1处理叶片Pn是对照(CK)的1.358倍,且与对照差异达显著水平(P<0.05),而BS5和BS10处理的Pn与对照无显著差异(图2,A)。同时,俄罗斯杨叶片PSⅡ原初光能转换效率(Fv/Fm)在BS1和BS5处理下与对照无显著差异,而在BS10处理下比对照显著下降(图2,B)。以上结果表明,适合俄罗斯杨水培苗生长的最佳硼浓度可能在1 mmol/L左右,远高于1/2 Hoagland溶液中的硼浓度(0.05 mmol/L);但当硼浓度为10 mmol/L时,幼苗的光合作用受到明显的抑制。
2.3 硼胁迫对俄罗斯杨水培苗叶片光合色素含量和比例的影响
随着硼浓度的增加,俄罗斯杨水培苗叶片叶绿素a、叶绿素b和类胡萝卜素含量均表现出先升后降的变化趋势,并均在BS1处理达到最大值,且BS1处理均显著高于对照,而BS10处理均与对照无显著差异(图 3,A~C)。同时,水培苗叶片叶绿素a与叶绿素b的比值(Chla/Chlb)随着硼浓度的增加呈逐渐降低的趋势,且BS1处理与对照无显著差异,而BS5和BS10处理均比对照显著下降(图3,D)。以上结果显示,俄罗斯杨捕获的光量子在光反应中的利用效率下降,可能导致活性氧生成量增加。

CK、BS1、BS5和BS10处理培养液中的硼酸浓度分别为0.05、1、5和10 mmol/L。下同图1 硼胁迫下俄罗斯杨水培苗生长状态的变化The boric acid concentrations in the culture solution of CK, BS1, BS5 and BS10 treatments were 0.05, 1, 5, and 10 mmol/L, respectively. The same as belowFig.1 The growth situation of hydroponic Populus russkii seedling under boron stress
2.4 硼胁迫对俄罗斯杨水培苗叶片过氧化氢和丙二醛含量的影响
俄罗斯杨水培苗叶片过氧化氢(H2O2)含量在4种硼浓度处理下均没有显著变化(图4,A);其丙

2.5 硼胁迫对俄罗斯杨水培苗叶片抗氧化酶活性及抗坏血酸含量的影响
俄罗斯杨水培苗叶片SOD和APX活性随着硼胁迫浓度的升高均呈先上升后下降的变化趋势,且各硼胁迫处理均显著高于对照;两种酶活性分别在BS5和BS1处理下达到最大值,分别是相应对照的1.374倍和19.076倍(图5,A、B)。同时,水培苗叶片POD活性在BS1和BS5处理下与对照相近,而在BS10处理下比对照显著上升,达到对照的1.250倍(图5,C)。另外,俄罗斯杨水培苗叶片抗坏血酸含量在各浓度硼胁迫处理下均不同程度上调,其中BS1和BS10处理的增幅达到显著水平,分别是对照的1.983和2.492倍(图5,D)。

数据为平均值±标准差,n = 3;不同小写字母表示处理间在0.05水平存在显著性差异(Tukey’s test)。下同图2 硼胁迫下俄罗斯杨水培苗净光合速率(Pn)和PSⅡ原初光能转换效率(Fv/Fm)的变化Data shown are mean ± SD (n = 3). Different normal letters indicate statistical significance among different treatments at the 0.05 level according to Tukey’s test. The same as belowFig.2 The Pn and Fv/Fm in leaves of hydroponic P. russkii seedling under boron stress
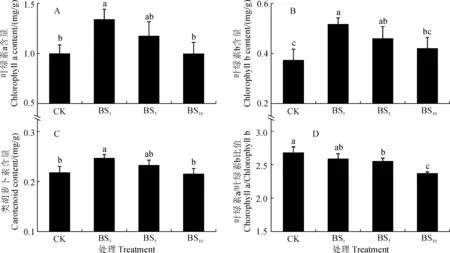
图3 硼胁迫下俄罗斯杨水培苗叶片光合色素含量和比例的变化Fig.3 The contents and ratio of photosynthetic pigments in leaves of hydroponic P. russkii seedling under boron stress
2.6 硼胁迫对俄罗斯杨水培苗渗透调节物质含量的影响
随着硼酸浓度的增加,俄罗斯杨水培苗游离脯氨酸和可溶性糖含量呈上升趋势,但仅在BS10处理下与对照差异显著,此时分别是对照的3.369倍和1.255倍(图6,A、B);同时,各处理水培苗可溶性蛋白含量与对照相比均无显著差异(图6,C)。
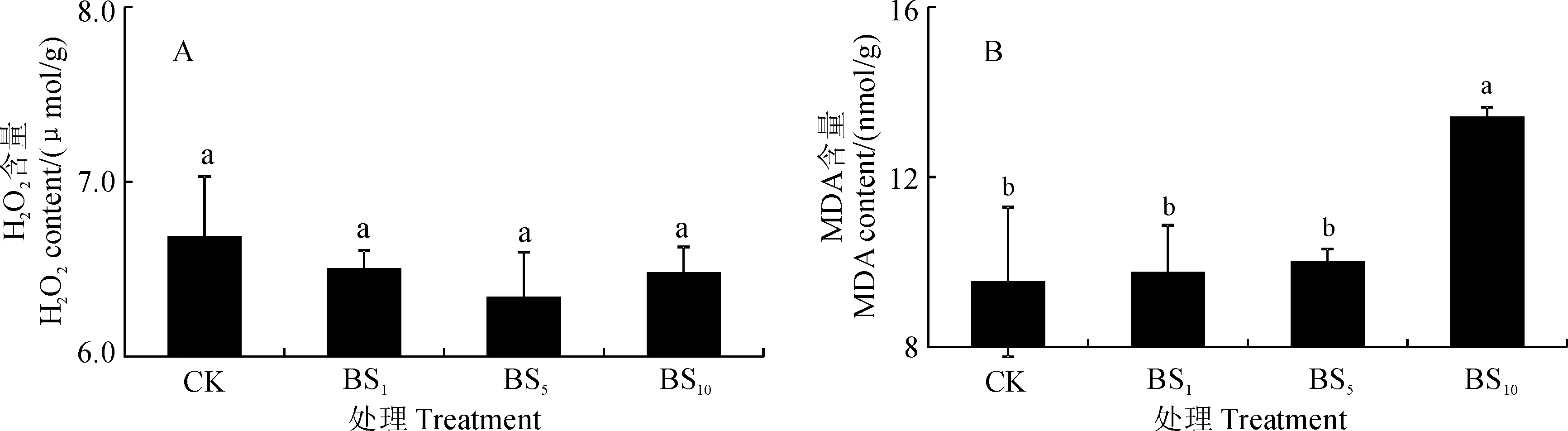
图4 硼胁迫下俄罗斯杨水培苗叶片过氧化氢和丙二醛含量的变化Fig.4 The contents of H2O2 and MDA in leaves hydroponic P. russkii seedling under boron stress
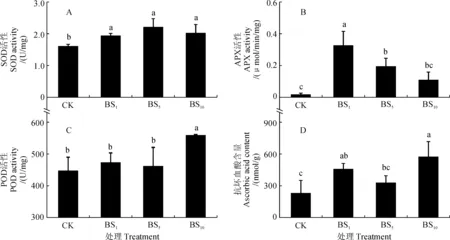
图5 硼胁迫下俄罗斯杨水培苗叶片抗氧化酶活性和抗坏血酸含量的变化Fig.5 The activities of antioxidant enzymes and the content of ascorbic acid in leaves of hydroponic P. russkii seedling under boron stress

图6 硼胁迫下俄罗斯杨水培苗渗透调节物质含量的变化Fig.6 The contents of osmoprotectants in leaves of hydroponic P. russkii seedling under boron stress
3 讨 论
本本研究显示,当硼酸浓度为1 mmol/L时,俄罗斯杨叶片与对照相比更为鲜绿,叶片光合色素含量和Pn增加,而Fv/Fm、H2O2和MDA含量与对照无显著差异。当硼酸浓度为5 mmol/L时,叶片褪绿变黄,Chla/Chlb比值下降,但其他参数,特别是Pn和MDA含量,与对照无显著差异。当硼酸浓度为10 mmol/L时,植株的生长受到严重的抑制,Chla/Chlb和Fv/Fm显著下降,MDA含量显著上升。结果表明,俄罗斯杨的生长情况在添加1 mmol/L硼酸时优于1/2 Hoagland溶液,在添加5 mmol/L硼酸时受到轻微硼胁迫,在添加10 mmol/L硼酸时出现严重硼毒害症状。与其他常见物种如拟南芥[7]、小麦[15]、水稻[16]、苹果[8]、柑橘[17]等的相关研究相比,本研究采用的硼酸浓度较高,而毒害症状主要在10 mmol/L硼酸处理时出现,表明俄罗斯杨具有较强的硼毒耐性。
等活性氧有关。
AsA是植物细胞中重要的非酶抗氧化剂,在保护叶绿体免于氧化损伤中起着重要的作用[23]。本研究中,俄罗斯杨叶片AsA含量在硼处理条件下显著增加,在一定程度上反映了其抗逆性;但是,在10 mmol/L高硼条件,AsA含量的上调还可能与APX活性的下调(相比于1 mmol/L和5 mmol/L)有关,即AsA分解量减小。另外,本研究中游离脯氨酸和可溶性糖含量在10 mmol/L硼处理时显著上调。脯氨酸也具有非酶抗氧化剂的功能,同时参与植物细胞的渗透势调节[21]。植物细胞的渗透调节作用是植物适应胁迫环境、增强抗逆性的基础。
综上所述,俄罗斯杨水培苗在低浓度硼溶液中能正常生长,甚至优于对照;在中等硼浓度胁迫条件下,其叶片SOD和APX活性显著上调,有助于清除活性氧,免于其遭受膜脂过氧化伤害,表现出较强的耐硼性;但在有效硼浓度过高的情况下,叶片褪绿变黄、茎尖和根尖生长受抑制,Fv/Fm下降,Chla/Chlb比值下降,MDA含量上升;同时其POD活性、游离脯氨酸和可溶性糖含量上调,仍有助于减少高硼胁迫造成的损伤。

