罗丹明B修饰金纳米星构建检测Zn2+的荧光传感器
王凯乾, 曾 艳, 陈荣生, 梁 峰
(武汉科技大学化学与化工学院,湖北武汉 430081)
锌是一种重要的微量元素,它在人体内的含量仅次于铁[1]。锌对于细胞的生长,发育和体内平衡、转录、分裂、氧化应激、衰老和凋亡有着重要的影响,对精子生成和胎儿生长以及人体适当的骨矿化,血液凝固和认知功能都具有关键的作用[2]。因此对Zn2+的检测,尤其是活体细胞和组织中Zn2+的测定已成为近年来生物化学家非常关注的领域。
目前Zn2+检测的常用方法有电化学检测法[3 - 5]、荧光法[6 - 12]以及电感耦合等离子体原子发射光谱法(ICP-AES)[13 - 14]。其中,电化学方法大多需要严格的预处理且干扰因素多,ICP-AES操作比较复杂,且需要一定的耗能,成本较高。而荧光化学传感器法是目前公认的一种高效、快速的金属离子的检测方法,但是在传统的荧光化学传感器中,作为连接单元的有机物存在合成程序复杂,水溶性差,荧光漂白易于失活以及选择性差等问题。近年来,研究发现金纳米粒子(Au-NPs)具有表面等离子体共振(LSPR)消光系数大,稳定性高等优点,使得它可以代替有机分子成为制造荧光化学传感器的支架单元。
Daniela等人[15]将强荧光物质罗丹明B(RhB)连接到Au-NPs表面构建了一种开启式的荧光传感器来检测Zn2+并取得了较好的效果。本文采用种子生长法[16]制备的金纳米星(Au-NSs)和罗丹明B来构建荧光传感器,通过优化实验条件,Zn2+的最低检测浓度可达到0.013 mg/L。与已有的方法相比,本文所使用的方法不需要进行复杂的前体制备,不需要严格的预处理,不需要大量的耗能,且操作更为简单快捷,效率更高,测量范围从0.2 μmol/L跨越到5 mmol/L,且相对于其他过渡态金属离子而言,对Zn2+有着较好的选择性,具有更大的应用潜力。
1 实验部分
1.1 主要仪器及试剂
UV-3600紫外近红外分光光度计(日本,岛津公司);LS-55荧光分光光度计(上海珀金埃尔默有限公司);BSA124S电子天平(北京赛多利斯仪器有限公司);KQ2200D数控超声波清洗器(昆山市超声仪器有限公司);MS-H-Pro+数显加热型磁力搅拌器(北京大龙兴创实验仪器有限公司)。
HAuCl4·4H2O(Au≥47.8%,Sigma-Aldrich),二水合柠檬酸三钠(分析纯,国药集团化学试剂有限公司),AgNO3(分析纯,国药集团化学试剂有限公司),抗坏血酸(分析纯,国药集团化学试剂有限公司),罗丹明B(RhB)(分析纯,国药集团化学试剂有限公司)。金属离子Zn2+、Mn2+、Cu2+、Co2+和Ni2+的溶液均由它们的乙酸盐(分析纯,国药集团化学试剂有限公司)配制。实验用水为蒸馏水。
1.2 实验步骤
1.2.120nmAu-NPs的制备向三口烧瓶中加入25 mL HAuCl4水溶液(1 mmol/L),加热至100 ℃后,在500 r/min的搅拌速度下逐滴加入4 mL柠檬酸钠水溶液(38 mmol/L),并持续反应15 min,停止搅拌,待样品降至室温后,置于4 ℃冷藏保存。
1.2.280nmAu-NSs的制备以制备的20 nm Au-NPs为金种,利用种子生长法制备尺寸约为80 nm Au-NSs。向60 mL HAuCl4水溶液(0.25 mmol/L)中依次加入0.6 mL HCl(1 mol/L),0.6 mL金种,0.6 mL AgNO3水溶液(3 mmol/L)和0.3 mL抗坏血酸水溶液(0.1 mol/L),整个过程在700 r/min的搅拌速率下进行[17]。在这方面本课题组进行了大量的研究[18 - 21]。
1.2.3荧光传感器在不同条件下的紫外-可见-近红外光谱先通过紫外分光光度法测定制备的80 nm Au-NSs 和罗丹明B水溶液的最大吸收波长及吸光度,再取多份浓度为5 μmol/L的罗丹明B溶液1 mL,依次向该溶液中加入1、2、3、4 mL的Au-NSs,加蒸馏水定容至5 mL,观察各样品紫外光谱的变化情况。取多份浓度为5 μmol/L的罗丹明B溶液1 mL,同时向所有样品中加入2 mL Au-NSs,然后分别向其中依次加入0.02、0.05、0.1、0.5、2.0 mL浓度为50 mmol/L的Zn2+,最后将所有样品定容至5 mL,测量各样品的紫外-可见-近红外光谱。
1.2.4荧光传感器在不同条件下的荧光强度取多份浓度为5 μmol/L的罗丹明B溶液1 mL,分别向其中加入浓度为0、0.4、0.8、1.2、1.6、2.0、2.4、2.8、3.2、3.6 mL制备的80 nm Au-NSs,然后将各样品定容至5 mL,检测各样品的荧光强度;取多份浓度为5 μmol/L的罗丹明B溶液1 mL,同时向所有样品中加入2 mL制备的80 nm Au-NSs,然后分别向各样品中加入不同浓度不同体积的Zn2+溶液,最后将所有样品定容至5 mL,使各样品中Zn2+浓度分别为0.2、2、20、50 μmol/L及0.2、0.5、1、2、5 mmol/L,测量各样品的荧光强度。
1.2.5荧光传感器检测其他过渡金属离子取多份浓度为5 μmol/L的罗丹明B溶液1 mL,同时向所有样品中加入2 mL制备的80 nm Au-NSs,然后分别向各样品中加入0.1、0.2、0.3、0.4、0.5、1、1.5、2 mL浓度为50 mmol/L的Mn2+、Cu2+、Co2+、Ni2+,测量各样品的荧光强度。
2 检结果与讨论
2.1 罗丹明B修饰金纳米星后加入Zn2+过程中的UV-Vis-NIR光谱变化情况
如图1所示,通过种子生长法制备的Au-NSs最大吸收波长在933 nm左右,吸光度为0.6529,其吸光系数为9.77×109mol/(L·cm)[22],通过朗伯-比尔定律可计算出该Au-NSs摩尔浓度约为70 pmol/L。罗丹明B的水溶液最大吸收峰在554 nm附近,且在520 nm附近有一个较弱的吸收带,主要是罗丹明B的二聚物引起的。将二者进行混合,罗丹明B浓度均为1 μmol/L,随着Au-NSs浓度的增大(图1),罗丹明B的特征峰向长波方向移动,且峰的相对强度逐渐减弱,其原因可能是越来越多的罗丹明B与Au-NSs结合,Au-NSs的束缚使得罗丹明B的电子跃迁变得更难发生,这种束缚的作用力主要来自于罗丹明B中带正电荷的氮原子与Au-NSs表面带负电荷的抗坏血酸之间的静电作用力。在浓度为28 pmol/L的Au-NSs 和1 μmol/L的罗丹明B混合液中加入不同浓度的Zn2+,结果显示罗丹明B的特征峰值又逐渐增强,且增加量与Zn2+浓度呈正比,特征波长出现少量的蓝移逐渐回到554 nm附近,如图2所示。这说明Zn2+的存在会削弱罗丹明B和Au-NSs的相互作用。
2.2 利用荧光传感器检测Zn2+浓度
如图3所示,罗丹明B在580 nm附近存在一个明显的发射波长。在浓度为1 μmol/L的罗丹明B中加入不同浓度的Au-NSs后,罗丹明B的荧光强度会显著减弱。通过线性拟合,发现荧光猝灭的程度F0/F(y)与Au-NSs的浓度(x)呈良好的线性关系,线性拟合方程为:y=0.07x+0.9378,相关系数(R2)为0.9926。其中F0表示罗丹明B溶液的荧光强度,F表示罗丹明B加入Au-NSs后的荧光强度。在此体系中Au-NSs 充当猝灭剂,线性关系的成立说明这种猝灭现象的机制为静态猝灭。
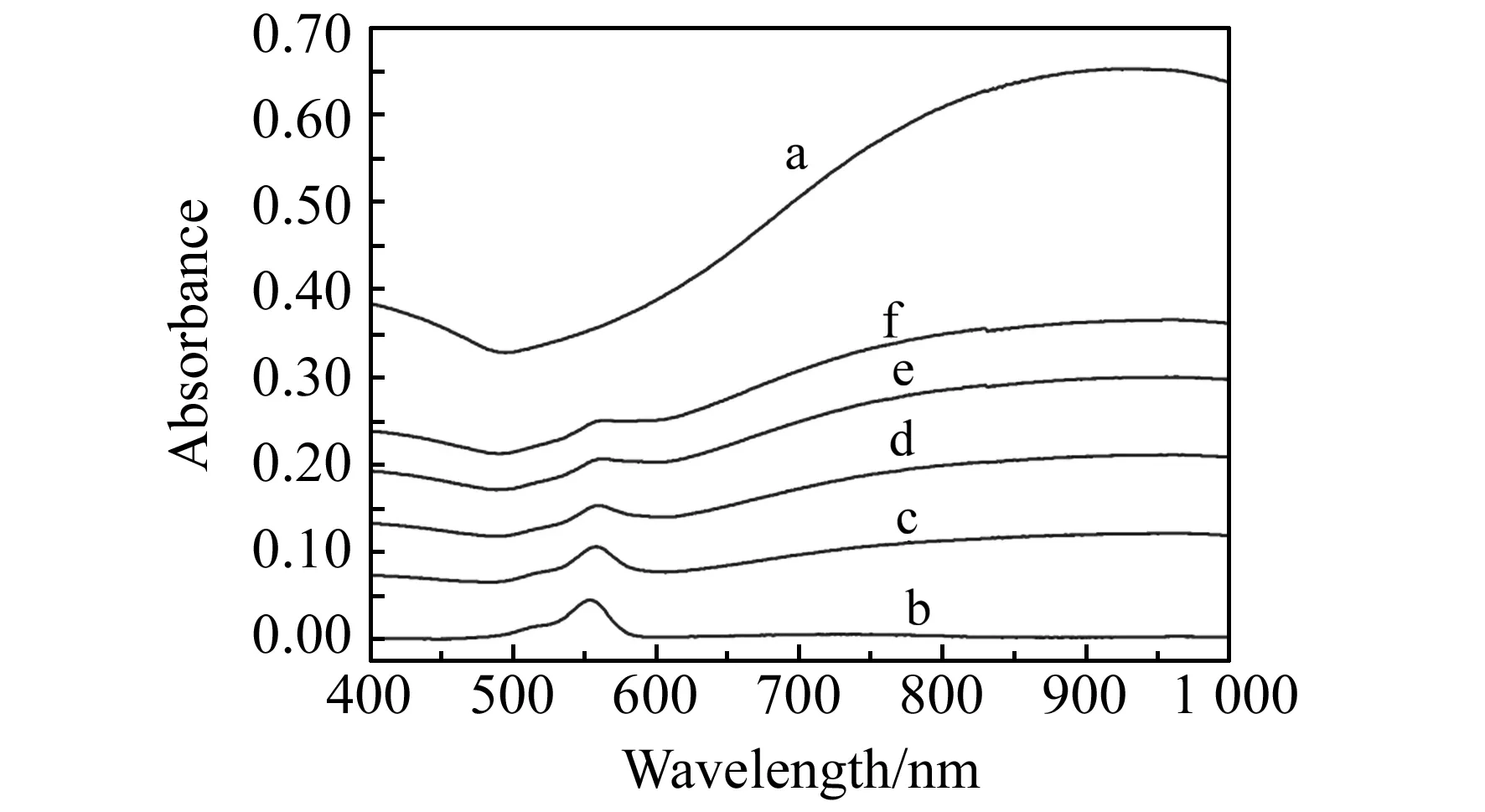
图1 Au-NSs(a)、罗丹明B(b)以及二者混合(c,d,e,f)的UV-Vis-NIR图Fig.1 UV-Vis-NIR absorbance spectra of Au-NSs(a),Rhodamine B(b) and mixture of them(c - f)The concentrations of the added Au-NSs are c:14 pmol/L;d:28 pmol/L;e:42 pmol/L;f:56 pmol/L.
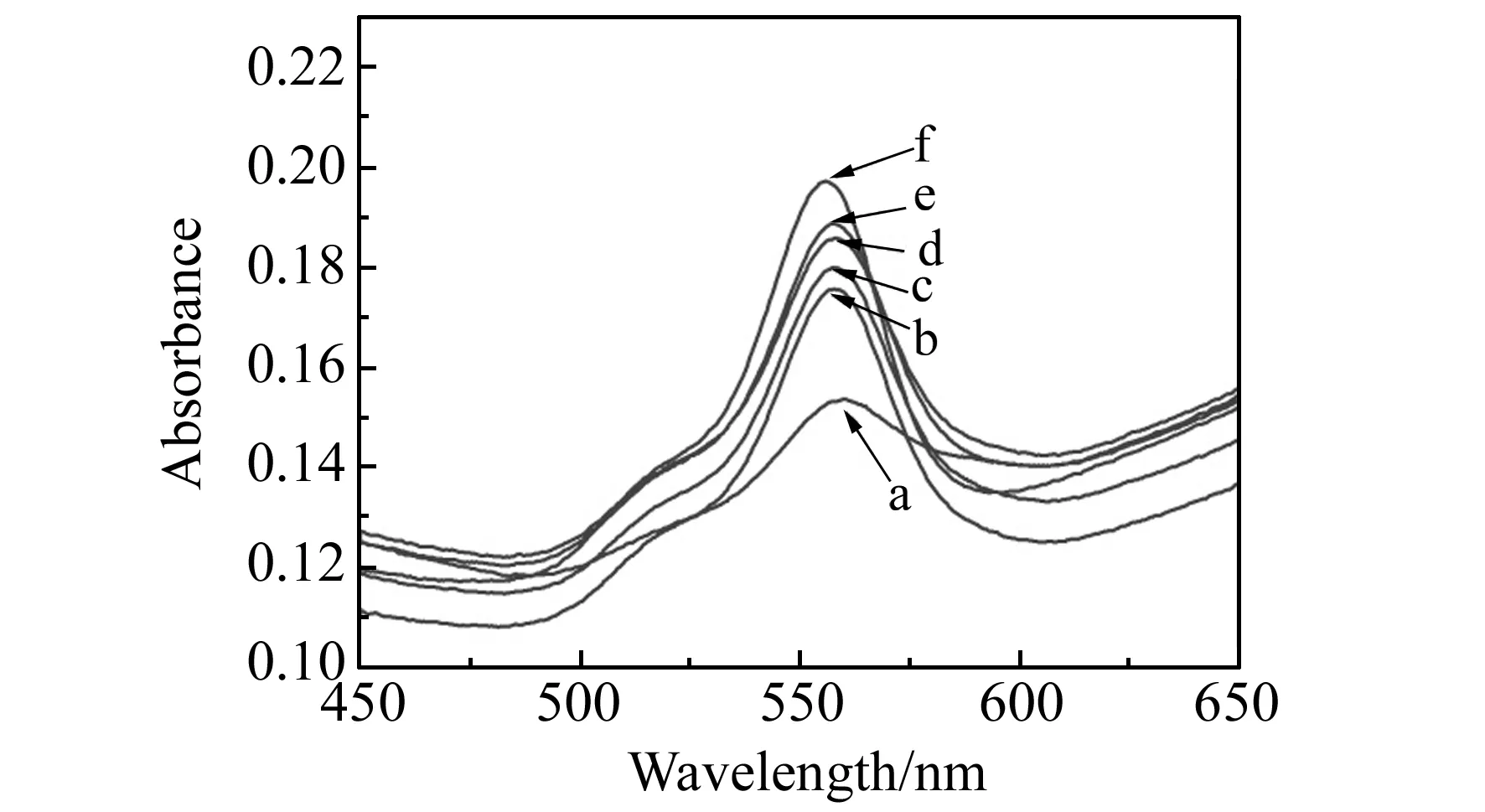
图2 罗丹明B修饰Au-NSs后加入不同浓度Zn2+的UV-Vis-NIR图Fig.2 UV-Vis-NIR absorbance spectra of Rhodamine B modified Au-NSs after adding different concentrations of Zn2+ a:0 mmol/L;b:0.2 mmol/L;c:0.5 mmol/L;d:1 mmol/L;e:5 mmol/L;f:20 mmol/L.
随后将罗丹明B和Au-NSs二者混合,固定罗丹明B浓度为1 μmol/L和Au-NSs浓度为28 pmol/L不变,分别向其中加入不同浓度的Zn2+,发现罗丹明B的荧光强度明显地恢复(图4),而且其荧光恢复率:(Fon-Foff)/F0(y)与Zn2+的浓度(x)呈良好线性关系,线性拟合方程为y=0.0811x+0.01158,R2=0.9950。其中F0表示罗丹明B水溶液的荧光强度,Foff表示罗丹明B修饰Au-NSs后的荧光强度,Fon表示在罗丹明B修饰Au-NSs后加入Zn2+的荧光强度。在本次实验条件下,Zn2+的最低检测浓度可达到0.013 mg/L,线性范围为0.2 μmol/L~5 mmol/L。
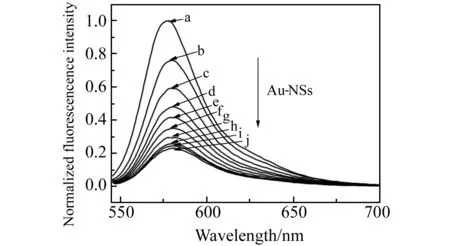
图3 在罗丹明B中加入不同浓度的Au-NSs的荧光光谱图Fig.3 Fluorescence pattern of Rhodamine B after adding different concentrations of Au-NSsa:0 pmol/L,b:5.6 pmol/L,c:11.2 pmol/L,d:16.8 pmol/L,e:22.4 pmol/L,f:28 pmol/L,g:33.6 pmol/L,h:39.2 pmol/L,i:44.8 pmol/L,j:50.4 pmol/L.(From top to bottom).

图4 罗丹明B修饰Au-NSs后加入不同浓度Zn2+的荧光光谱图Fig.4 Fluorescence pattern of Rhodamine B modified Au-NSs after adding different concentrations of Zn2+The top is 1μmol/L RhB(a) and the bottom is 1 μmol/L RhB+28 pmol/L Au-NSs(b),between them are 1 μmol/L RhB+28 pmol/L AuNSs+Zinc ions of different concentrations.c:0.2 μmol/L,d:2 μmol/L,e:20 μmol/L,f:50 μmol/L,g:0.2 mmol/L,h:0.5 mmol/L,i:1 mmol/L,j:2 mmol/L,k:5 mmol/L.
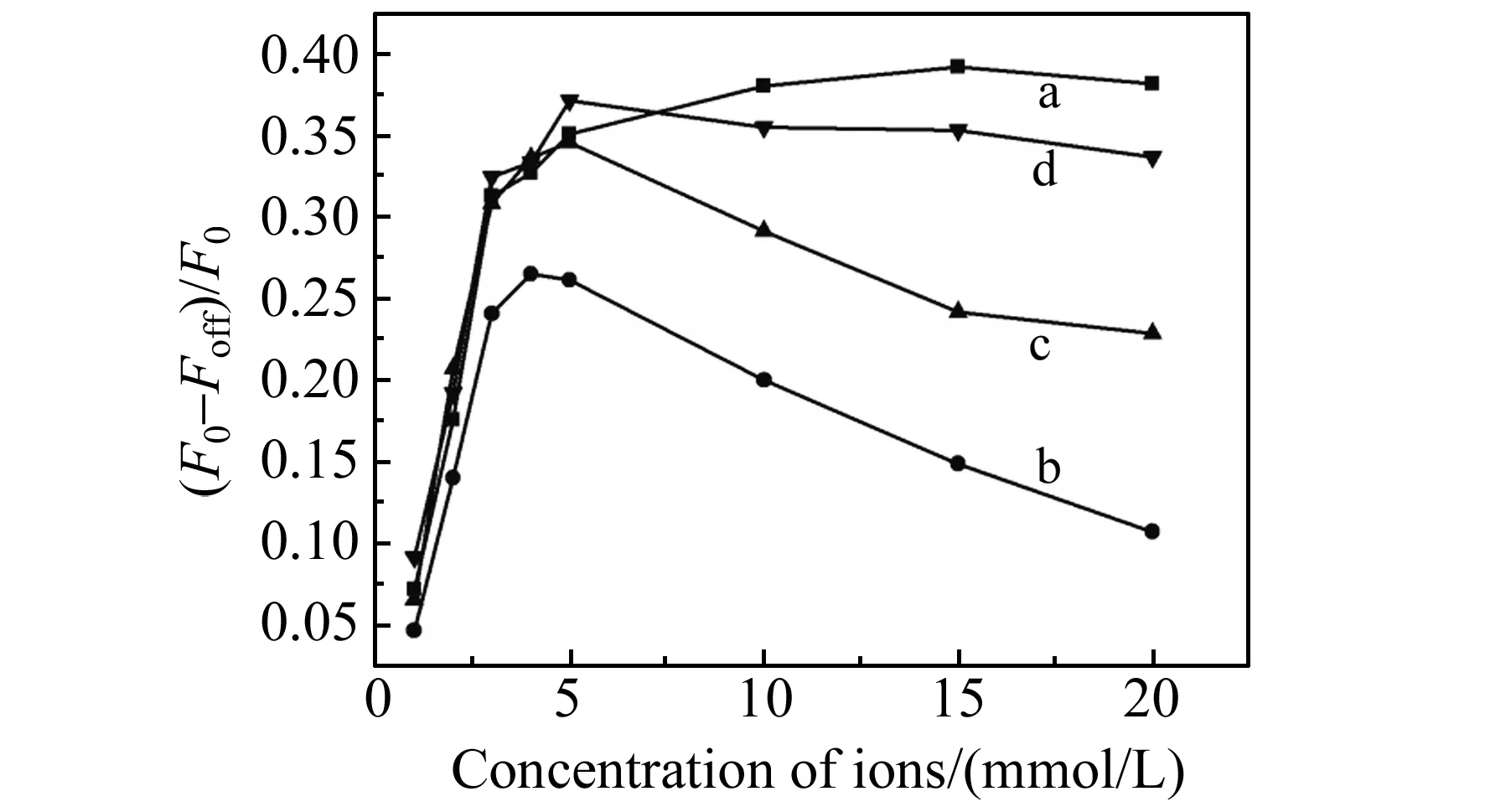
图5 荧光恢复率与各种离子浓度的关系Fig.5 Relationship between fluorescence recovery rate and concentration of various ionsa:Mn2+;b:Cu2+;c:Co2+;d:Ni2+.
2.3 荧光传感器的选择性
为了观察罗丹明B修饰的Au-NSs体系对其他离子是否也具有选择性,在罗丹明B修饰的Au-NSs中加入了不同浓度的Mn2+、Cu2+、Co2+和Ni2+,观察体系是否存在荧光恢复及其恢复程度的变化规律。从图5可以看出,当加入了一定量的其它金属离子后罗丹明B的荧光强度均存在一定的恢复,但其荧光恢复率与加入的离子浓度均无良好的线性关系,且恢复效率不理想。这说明罗丹明B修饰的Au-NSs对于Zn2+浓度的检测具有一定的特异性,这可能与Zn2+最外层更紧密的电子排布有关,具体原因还有待进一步研究。
3 结论
Au-NSs会促使罗丹明B发生明显的荧光猝灭,但是在Zn2+的存在下,其荧光强度逐渐恢复,且荧光恢复率与Zn2+浓度呈良好的线性关系。因此我们构建了一种高效、方便快捷、操作简单的用于检测Zn2+的荧光传感器,具有一定的应用潜力。

