辣椒叶片表观表面自由能的计算方法
徐广春,顾中言,徐德进,许小龙,徐鹿
辣椒叶片表观表面自由能的计算方法
徐广春,顾中言,徐德进,许小龙,徐鹿
(江苏省农业科学院植物保护研究所,南京 210014)
【目的】农用化学品叶面喷雾的效率与植物叶面理化性能的复杂性密切相关。为了更好地理解农用化学品喷雾液与植物叶面内在结构的界面互作效应,本研究以辣椒叶片为例从热力学角度出发寻求其内在的关联性,以期为植株上农药的高效使用提供依据。【方法】以水(W)、丙三醇(G)和二碘甲烷(DM)为检测液,借助接触角测量仪测定其在3种辣椒叶片上的稳定接触角后,分别采用Wu调和平均数法(HM)、Owens-Wendt-Rabel-Kaelble法(OWRK)、Van-Oss-Chaudhury-Good法(OCG)以及ZDY法计算叶片的表面自由能及其分量并进行比较,同时对辣椒叶面的溶解度系数进行分析。【结果】水在苏紫1号和GR甜椒叶片上表现出较好的润湿性(<90°),而在苏椒13叶片上的润湿性一般(>90°)。在估测辣椒叶片表面表观自由能的4种方法中,OCG法采用3种检测液进行分析,较其他方法获得的辣椒叶面特征物理量较多,3种辣椒叶片表观表面自由能的非极性分量所占百分率(>85%)均高于极性分量(<15%)。采用2种检测液的方法为HM法和OWRK法,当2种检测液均为极性(W-G)时,辣椒叶片表观表面自由能的非极性分量和极性分量所占百分率变化较大,甚至相反;当2种检测液为极性和非极性组合(W-DM或G-DM)时,以OCG法计算获得辣椒叶面表观表面自由能的数值为基准,OWRK法计算获得的数值比HM法获得的数值偏差要小。采用1种检测液的方法为ZDY法,计算获得辣椒叶面表观表面自由能的数值远高于其他3种方法,比OCG法获得辣椒叶面表观表面自由能的数值偏差均>100%。以OCG法为基准,偏差在10%以内,苏紫1号辣椒叶面表观表面自由能为37.72—43.11 mJ·m-2,溶解度系数为18.89—22.77 mJ1/2·m-3/2;GR甜椒叶面表观表面自由能为37.53—40.95 mJ·m-2,溶解度系数为18.81—20.09 mJ1/2·m-3/2;苏椒13号辣椒叶面表观表面自由能为33.21—36.92 mJ·m-2,溶解度系数为17.17—18.58 mJ1/2·m-3/2。【结论】以水、丙三醇和二碘甲烷为检测液,ZDY法不适用计算辣椒叶片表观表面自由能;HM法、OWRK法、OCG法可用来计算辣椒叶片表观表面自由能,其中HM法和OWRK法应注重选择检测液组合的极性问题。同时,3种辣椒叶面表面自由能的非极性分量的比率均高于极性分量的比率。
辣椒叶面;接触角;表面自由能;表面自由能分量;溶解度系数
0 引言
【研究意义】叶面喷雾过程中,不同种类的植物叶片在不同生育期表现出的润湿性不同[1]。叶片润湿性的好坏直接影响着喷洒雾滴的附着和扩散能力,进而影响喷洒药液药效的发挥[2-3]。在农药制剂设计到喷洒到植株上的过程中,不可忽视的是靶标植物叶面的物理化学性质[4-5]。界面现象研究的科学家通过接触角的测量,推导和量化出叶面的内在属性,如表面自由能。植物叶片表面自由能及其分量一方面可用于表征其叶面的物理化学属性,另一方面可用于指导农药药液的叶面喷雾及特定靶标植物上农药剂型的设计。【前人研究进展】农药雾滴在靶标植物叶面上的润湿是一个热力学过程,因此从能量的角度出发,测定靶标植物叶面表面自由能及其分量可以更好地描述其润湿性能[6-7]。固体表面自由能的估算方法较多,最简便的方法就是接触角法[8]。Young于1805年首次确立了界面张力与表面自由能的关系,即Young方程(平衡接触角与固/气γ、固/液γ和液/气γ界面自由能之间的关系,即γ-γ=γcos)。表面自由能的估测在随后的时间内获得较大的发展,测量的方法主要有Wu调和平均数法(HM)、Owens-Wendt-Rabel-Kaelble法(OWRK)、Van-Oss-Chaudhury-Good法(OCG)、朱定一等提出的ZDY法以及Zisman法等[9-12],其中Zisman法获得的是临界表面张力值,事实上临界表面张力并不等同于固体的表面自由能,而是与理论非常接近的实验值。临界表面张力是从力的角度表征表面现象,而表面自由能是从能量的角度表征表面现象,两者单位不同,但在数值上是相等的。虽然该方法较为简便,但在cos=1时(即=0°),γ是否为0尚无法判断,易引起误差。目前,这些方法更多的用在聚合物表面自由能的估算,而用在植物材料表面能尤其是植物叶片表面自由能的估算相对较少。上述方法中表面自由能的测定多采用1—3种不同的测试液体进行估算,检测液的选择尤其注重其极性。水、丙三醇和二碘甲烷等是常用的检测液,在OCG法中具有较好的重现性且获得表征量较多[13],Shalel- Levanon等[14]通过数学的方法证实了这一点,表明OCG法可以用于测定叶片的表面自由能。利用纯液体的接触角来研究靶标植物表面自由能及其分量,可以从定量和定性两个角度来研究靶标叶面结构特性,是研究靶标叶面与雾滴行为关系的基础,考虑到叶片表面化学成分和表面粗糙度对接触角均产生影响,因此叶片表面自由能应为表观表面自由能。在利用OWRK法计算不同时期、不同部位小麦叶片表观表面自由能及其分量的过程中发现,近轴面叶片的表观自由能均低于远轴面,其中色散分量数值下降明显,同时近轴面和远轴面极性分量或色散分量比例相似[15]。关明杰等[16]利用OCG法分析了化学处理对竹笋壳润湿性的影响。Fernández等[13]通过比较发现OCG法更适合用于澳洲红铁()叶片理化性能的表征,同时对其溶解度系数进行了研究。溶解度系数常用来预测叶表面极性、非极性以及分子间氢键的相互作用,可进一步理解叶表面的化学组成和粗糙度。目前已测得植物表面的溶解度系数多介于15—50 mJ1/2·m-3/2[17]。【本研究切入点】药液兑水叶面喷雾的方法是病虫害防治过程中常用的方法,由于缺乏喷洒靶标植株对象表面属性的数据,使得喷雾过程中忽视了药液表面张力与雾滴行为的内在联系,一定程度上影响了农药利用率。前期估测辣椒叶片的临界表面张力介于27.92—45.27 mN·m-1[18],在此基础上,以OCG法为基准,比较HM法、OWRK法以及ZDY法计算获得不同品种辣椒叶片的表观表面自由能。【拟解决的关键问题】在比较不同方法计算获得辣椒叶片表观表面自由能数值差异的基础上,筛选出适合的表观表面自由能计算方法,同时明确品种差异对表观表面自由能的影响程度,以期为农药叶面喷雾中靶标植株叶片参数库的建立提供依据。
1 材料与方法
试验于2017年在江苏省农业科学院植物保护研究所农药应用技术项目组实验室完成。
1.1 试验材料
采集设施大棚中种植的不同辣椒品种坐果期植株上部新鲜、干净且无病虫害污染的叶片进行测试,辣椒品种分别为苏紫1号、GR甜椒和苏椒13。所用试剂为二次蒸馏水、甘油(丙三醇,99%,上海阿拉丁生化科技股份有限公司)、二碘甲烷(98%,上海阿拉丁生化科技股份有限公司)。
1.2 供试仪器及软件
接触角测量仪JC2000C1B购自上海中晨数字技术设备有限公司;表面张力仪DCAT11EC购自德国dataphysics公司;0—50 μL微量注射器购自上海高鸽工贸有限公司。
1.3 试验方法
1.3.1 叶面接触角的测定 将待测的辣椒叶片保持自然状态平整地固定在接触角测量仪的载物台上,用微量注射器将体积为2 μL的液滴点滴在辣椒叶面上,用接触角测量仪上的CCD摄像头每5 s摄下叶面上的液滴,输入电脑,用拟合分析法计算出液滴在辣椒叶面上的稳定接触角(约40 s),每处理用坐果期辣椒植株上部新鲜叶片重复10次。
1.3.2 液体表面张力的测定 用量筒量取50 ml液体到表面张力仪的测试皿后,用吊片法测定相应液体的表面张力,重复3次,测定时的温度为(20± 2)℃。
1.3.3 辣椒叶片表面自由能的计算方法 Wu调和平均法(HM):Wu[9]基于Fowkes公式存在问题的基础上,在考虑色散力作用的同时也考虑分子间的极性力的影响;另一方面采用倒数平均法计算不同分子间的界面张力。

式中γ、γ和γ分别表示固/液界面自由能、固体表面自由能和液体表面自由能(或界面张力)。公式(2)—(8)、(10)和(12)同;和分别表示固体和液体的色散力分量;和分别表示固体和液体的极性分量,公式(2)—(5)同。
结合Young方程,可得到:

只要测定2种或2种以上已知表面张力的液体在固体表面的接触角,联立方程可获得固体表面能分量和,再利用如下公式计算求得表面能。
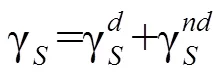
Owens-Wendt-Rabel-Kaelble法(OWRK):根据贝特乐假说,对界面产生作用的不仅仅是色散力,包括氢键在内的极性作用力也能够影响界面作用[10],因此固体表面自由能可以表示为:
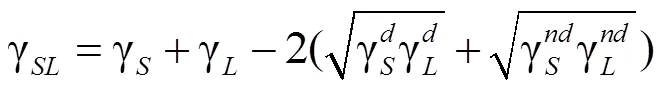
结合Young方程,可得到

只要测定2种已知表面张力的液体在固体表面的接触角,联立方程可获得固体表面能分量和,再利用上述公式(3)计算求得表面能。
Van Oss-Chaudhury-Good法(OCG):Van oss等[11]认为固体表面自由能可以表示为Lifshitz-van der Waals分量γ(代表表面自由能中非极性相互作用)和酸碱作用分量γ(代表表面自由能中极性相互作用)之和,其中γ又包含了Lewis酸分量γ+和Lewis碱分量γ-。因此,对于固体或液体的表面能可由方程(6)和(7)计算获得:

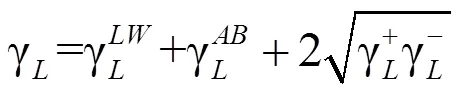
根据上述方程(6)和(7),可以得到新的界面张力与固体和液体之间的关系,如公式(8)所示。
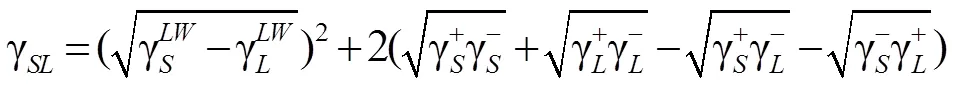
结合Young方程,可得到

ZDY法:朱定一等[12]通过分析有限液固界面体系的表面能平衡关系,推导出了无限液固界面系统中液固界面能和固体表面能的关系:
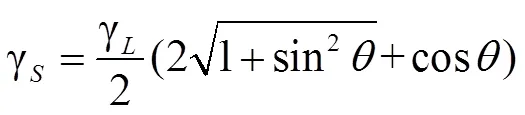
1.3.4 溶解度系数溶解度系数与内聚能ec的密度密切相关,而内聚能与表面自由能息息相关[19]。
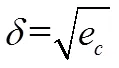
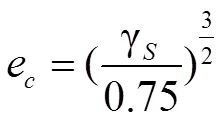
2 结果
2.1 检测液表面自由能及其分量
试验中所用的检测液的表面自由能及其分量如表1所示。采用的3种检测液(W、G和DM)的极性分别为极性、极性和非极性,其表面张力分别为72.80、63.70和50.80 mN·m-1。常温常压下表面张力的数值与表面自由能数值相一致,因此表面能分别为72.80、63.70和50.80 mJ·m-2。测定辣椒叶片表观表面自由能时,HM法和OWRK法需要至少2种检测液以及检测液的非极性分量γ和极性分量γ;OCG法需要3种检测液以及检测液的Lifshitz-van der Waals分量γ(代表表面自由能中的非极性相互作用,其中包含London力、Keesom力和Debye力)和酸碱作用分量γ(代表表面自由能中的极性相互作用,包含电子受体分量γ+和电子给体分量γ-);ZDY法只需要1种检测液。
2.2 检测液在不同品种辣椒叶片上的稳定接触角
不同检测液在不同品种辣椒叶片正反面的稳定接触角见表2。从表中可以看出,极性检测液(W、G)在3种辣椒叶片正反面的接触角均高于非极性检测液(DM)在辣椒叶片上的稳定接触角。苏紫1号辣椒和GR甜椒均能被3种检测液所润湿(<90°);虽然水在苏椒13叶片上较难润湿(>90°),但可被丙三醇和二碘甲烷润湿(<90°)。水和二碘甲烷在苏椒13叶片上的稳定接触角均高于苏紫1号和GR甜椒叶片上的稳定接触角(<0.05)。

表1 检测液的表面自由能及其分量(20℃)
表中数值为平均值±标准差(=3),丙三醇的γ、γ和γ数值除外(=7)Data in the table are mean±SD(=3), except γ, γand γdata of glycerol (=7);*表示数值引用文献[11]和[20]中的平均值* indicates mean values citation from references [11] and [20]
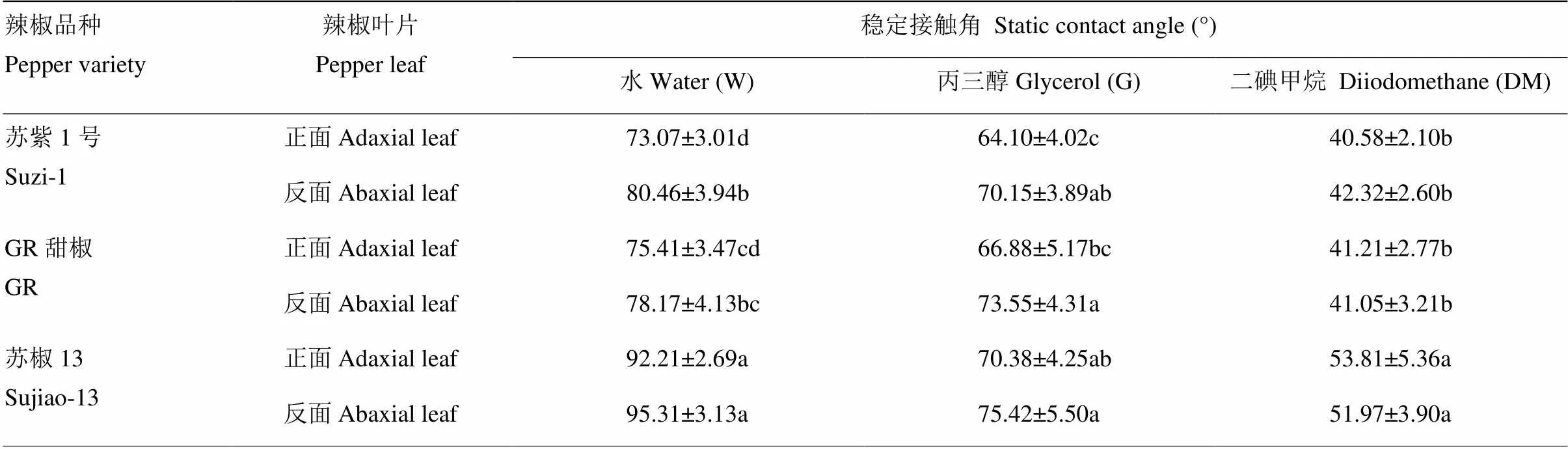
表2 检测液在不同品种辣椒叶片上的稳定接触角
表中数值为平均值±标准差(=10)。同列不同小写字母表示差异显著(<0.05)
Data in the table are mean±SD(=10). different letters in the same column indicated significantly different (DMRT,<0.05)
2.3 表观表面自由能计算
2.3.1 苏紫1号辣椒叶片表观表面自由能 根据OCG、HM、OWRK和ZDY 4种方法计算苏紫1号辣椒叶面的表观表面自由能值见表3和表4。通过3种具有不同极性分量和非极性分量检测液(W-G-DM)获得的辣椒叶面特征物理量要多于2种检测液的组合(W-G、W-DM、G-DM)或1种检测液(W、G、DM)。苏紫1号辣椒叶片正面表观表面自由能的值介于32.98—111.36 mJ·m-2,溶解度系数介于17.08—42.54 mJ1/2·m-3/2;辣椒叶片背面表观表面自由能的值介于29.55—108.30 mJ·m-2,溶解度系数介于15.73—41.66 mJ1/2·m-3/2。ZDY计算的叶面表观表面自由能与OCG法相比,偏差均高于100%,其中极性检测液(W、G)计算获得的表观表面自由能值均高于非极性检测液(DM)计算获得值;OWRK法中选用极性检测液组合(W-G)计算获得表面自由能偏差要高于极性和非极性组合(W-DM、G-DM)计算获得的值;HM法中的组合(G-DM)计算获得的表观表面自由能的偏差相对组合(W-G、W-DM)要低。根据公式(1)—(12)可计算出γ、γ、γ、γ、γ+和γ-。苏紫1号辣椒正反面表观表面自由能的非极性分量γ或γ均高于极性分量γ或γ,其中HM法中的极性组合(W-G)计算获得的辣椒正面表观表面自由能的非极性分量均低于极性分量。
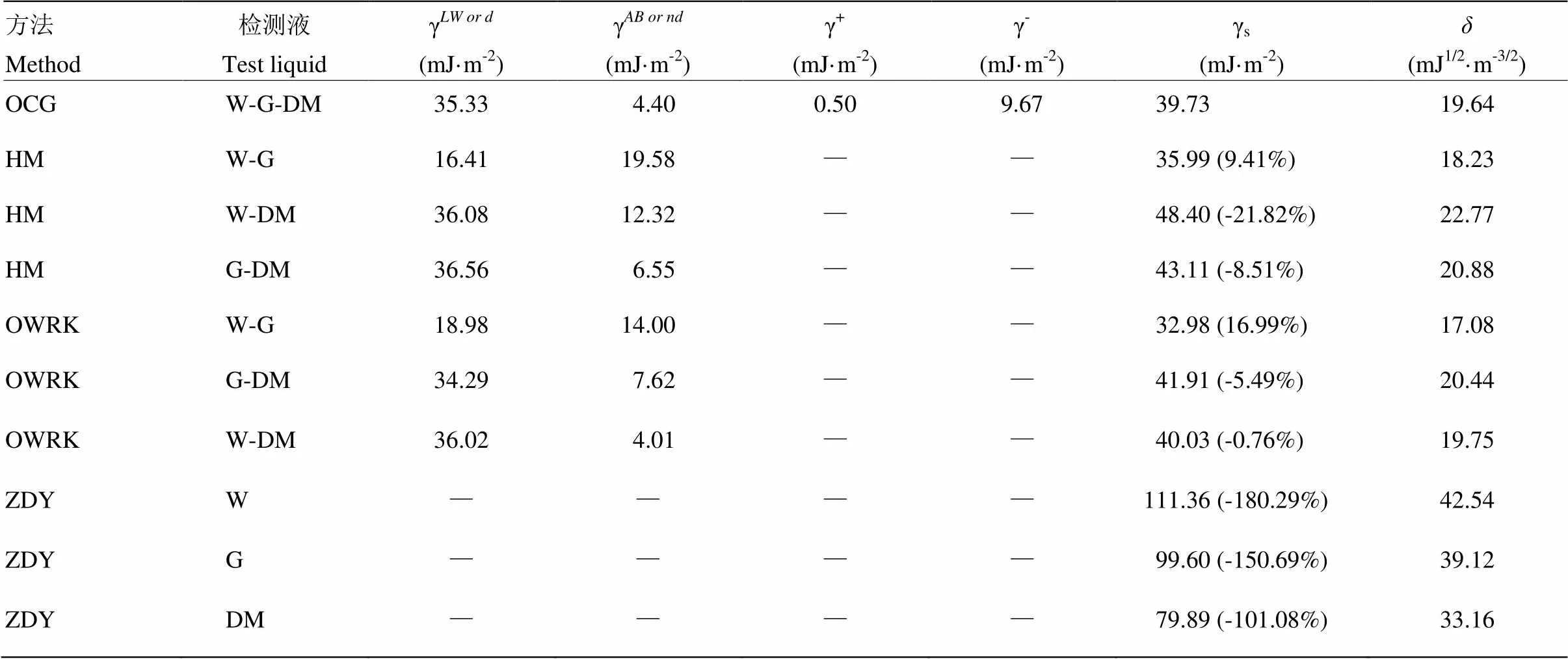
表3 苏紫1号辣椒叶片正面表观表面自由能
括号中数值为与OCG方法获得数值的偏差,表4—8同
The data in brackets are the deviations from the OCG method. The same as table 4-8
2.3.2 GR甜椒叶片表面自由能 根据OCG、HM、OWRK和ZDY 4种方法计算GR甜椒叶面的表面自由能值见表5和表6。通过3种具有不同极性分量和非极性分量检测液(W-G-DM)获得的甜椒叶面特征物理量要多于2种检测液的组合(W-G、W-DM、G-DM)或1种检测液(W、G、DM)。GR甜椒叶片正面表观表面自由能的值介于30.99—110.49 mJ·m-2,溶解度系数介于16.30—42.29 mJ1/2·m-3/2;甜椒叶片背面表观表面自由能的值介于26.72—109.35 mJ·m-2,溶解度系数介于14.58—41.96 mJ1/2·m-3/2。ZDY计算的叶面表观表面自由能与OCG法相比,偏差均>100%,其中极性检测液(W、G)计算获得的表观表面自由能值均高于非极性检测液(DM)计算获得值;OWRK法中选用极性检测液组合(W-G)计算获得表观表面自由能偏差要高于极性和非极性组合(W-DM、G-DM)计算获得的值;HM法中的组合(G-DM)计算获得的表观表面自由能的偏差相对组合(W-DM)要低。根据公式(1)—(12)可计算出γ、γ、γ、γ、γ+和γ-。GR甜椒正反面表观表面自由能的非极性分量γ或γd均高于极性分量γ或γ,其中HM法中的极性组合(W-G)计算获得的甜椒正反面表观表面自由能的非极性分量均低于极性分量,OWRK法中选用极性检测液组合(W-G)计算获得的甜椒反面表观表面自由能的非极性分量均低于极性分量。
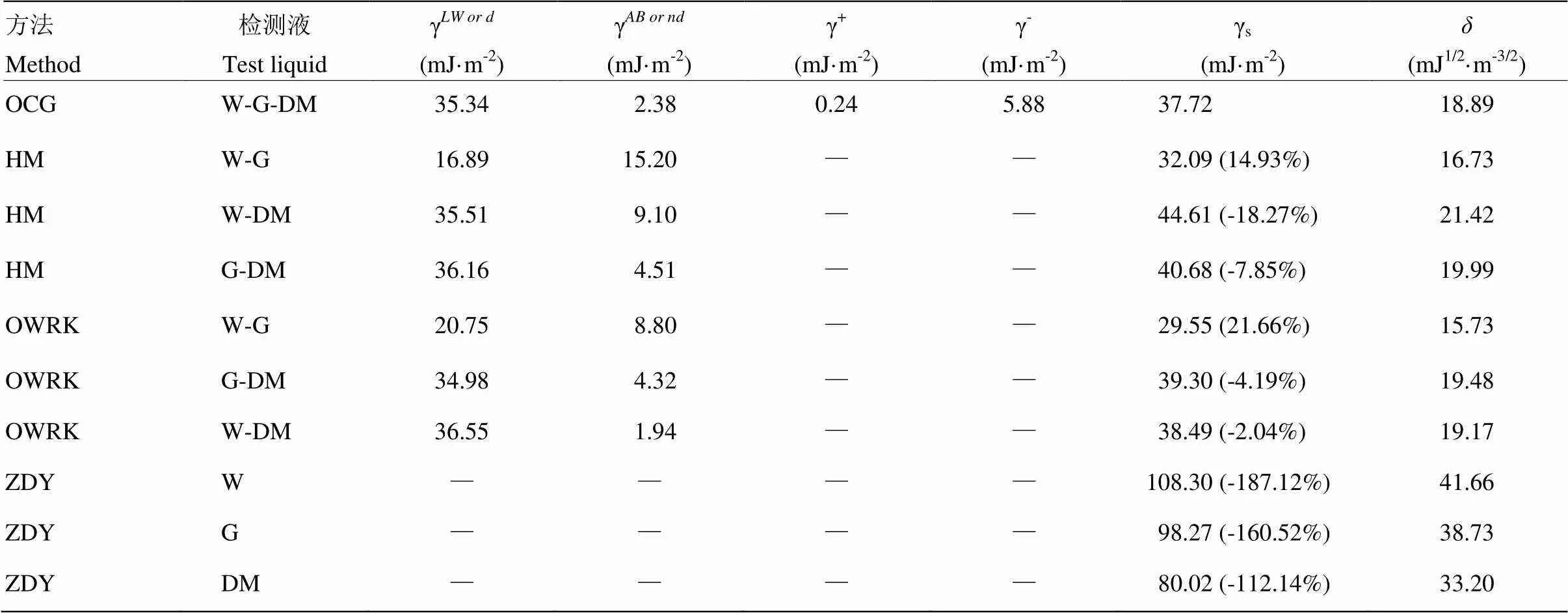
表4 苏紫1号辣椒叶片反面表观表面自由能
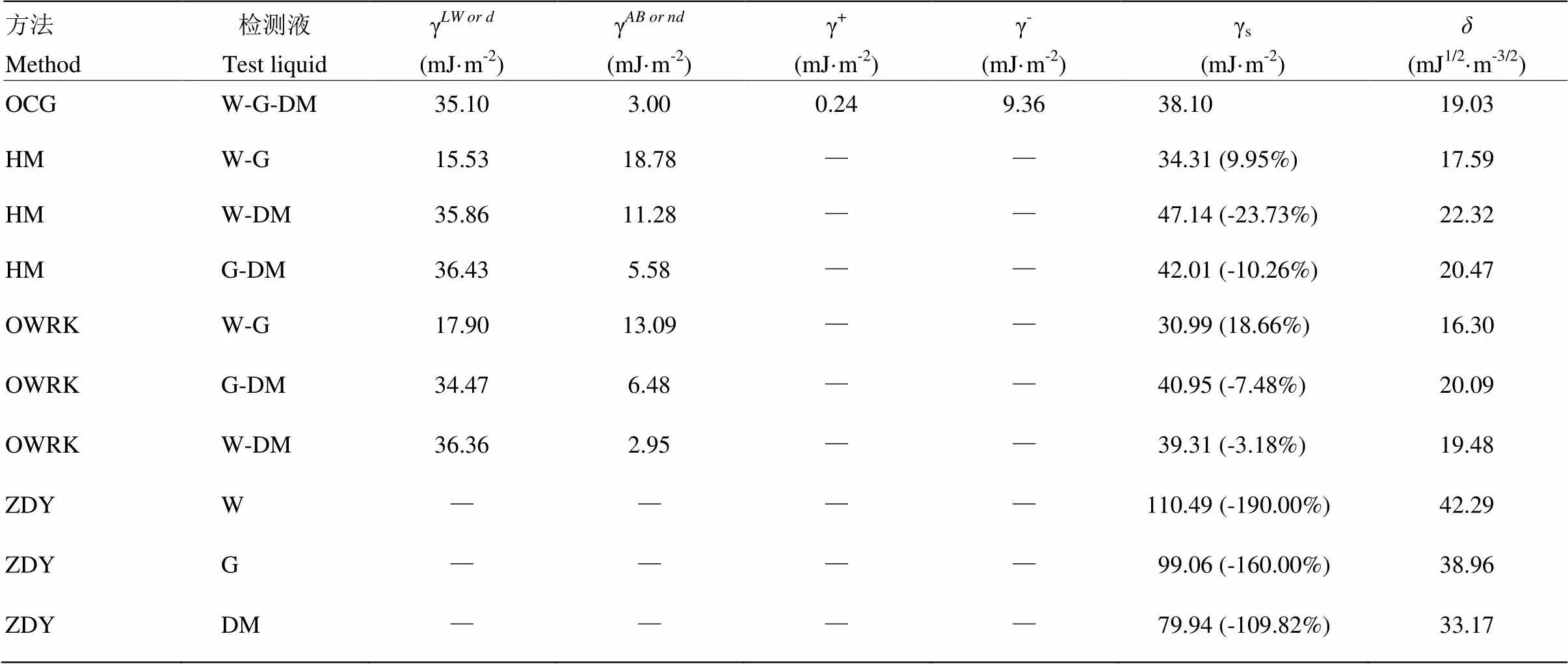
表5 GR甜椒叶片正面表观表面自由能
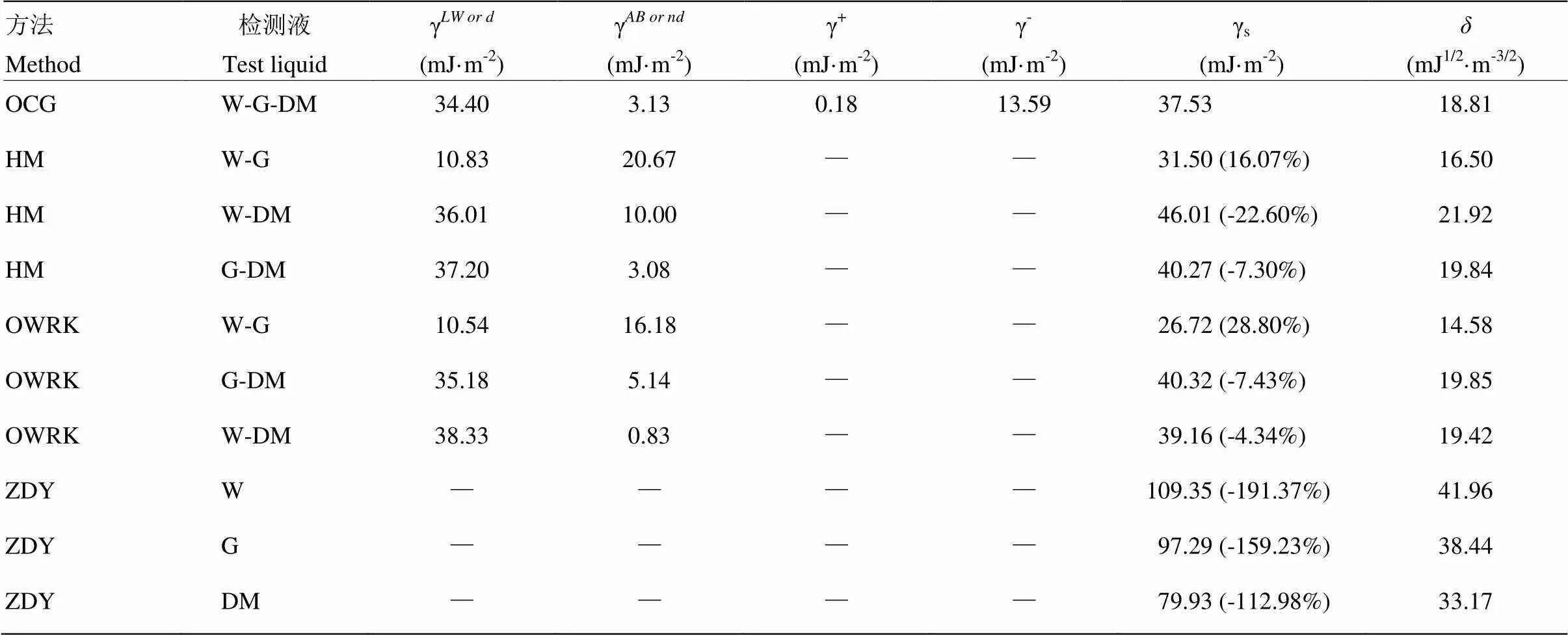
表6 GR甜椒叶片反面表观表面自由能
2.3.3 苏椒13辣椒叶片表面自由能 根据OCG、HM、OWRK和ZDY 4种方法计算苏椒13辣椒叶面的表观表面自由能值见表7和表8。通过3种具有不同极性分量和非极性分量检测液(W-G-DM)获得的辣椒叶面特征物理量要多于2种检测液的组合(W-G、W-DM、G-DM)或1种检测液(W、G、DM)。苏椒13叶片正面表观表面自由能的值介于32.19—101.54 mJ·m-2,溶解度系数介于16.77—39.69 mJ1/2·m-3/2;苏椒13叶片反面表观表面自由能的值介于33.22—99.40 mJ·m-2,溶解度系数介于17.17—39.06 mJ1/2·m-3/2。ZDY计算的叶面表面自由能与OCG法相比,偏差均>100%,甚至>200%,其中极性检测液(W、G)计算获得的表观表面自由能值均高于非极性检测液(DM)计算获得值;OWRK法中选用极性检测液组合(W-G)计算获得表观表面自由能偏差要高于极性和非极性组合(W-DM、G-DM)计算获得的值;HM法中的组合(W-DM、G-DM)计算获得的表面自由能的偏差相对组合(W-G)要低。根据公式(1)—(12)可计算出γ、γ、γ、γ、γ+和γ-。苏椒13辣椒正反面表面自由能的非极性分量γ或γ均高于极性分量γ或γ。
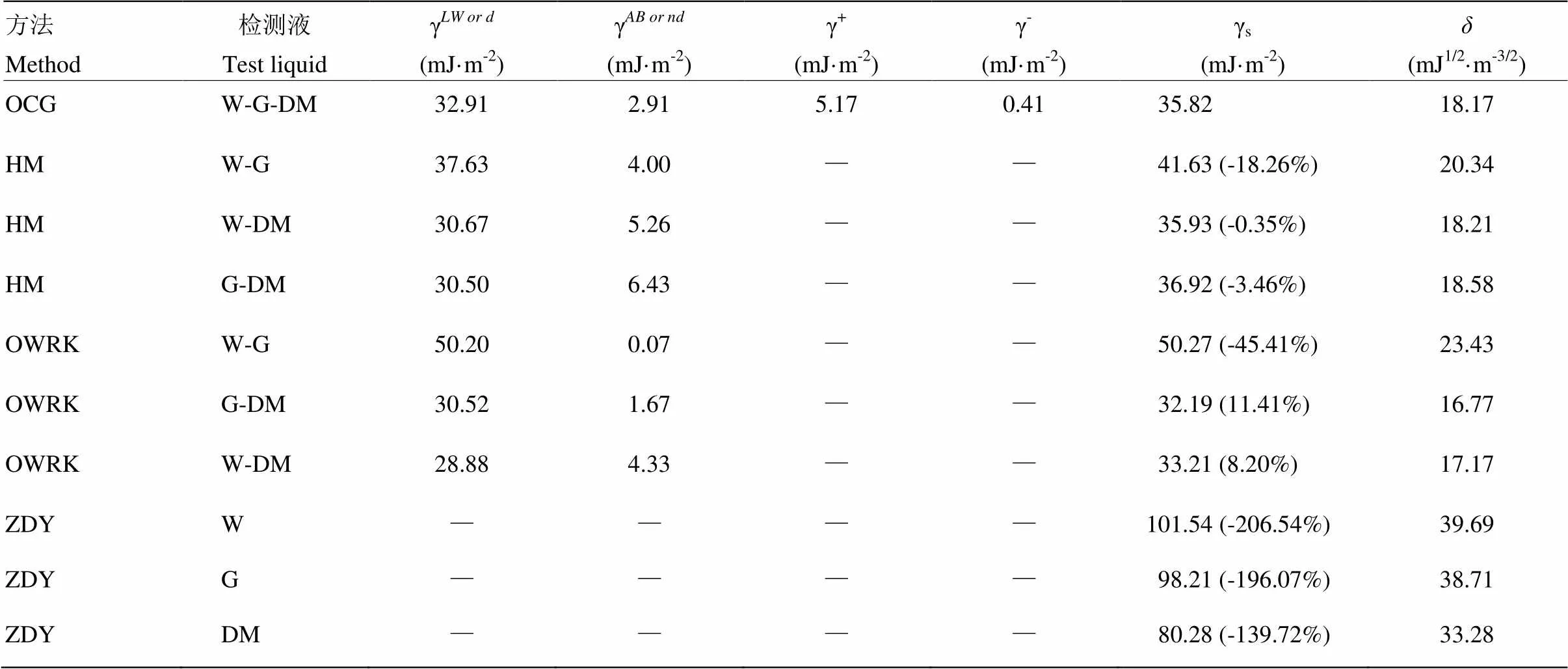
表7 苏椒13辣椒叶片正面表观表面自由能
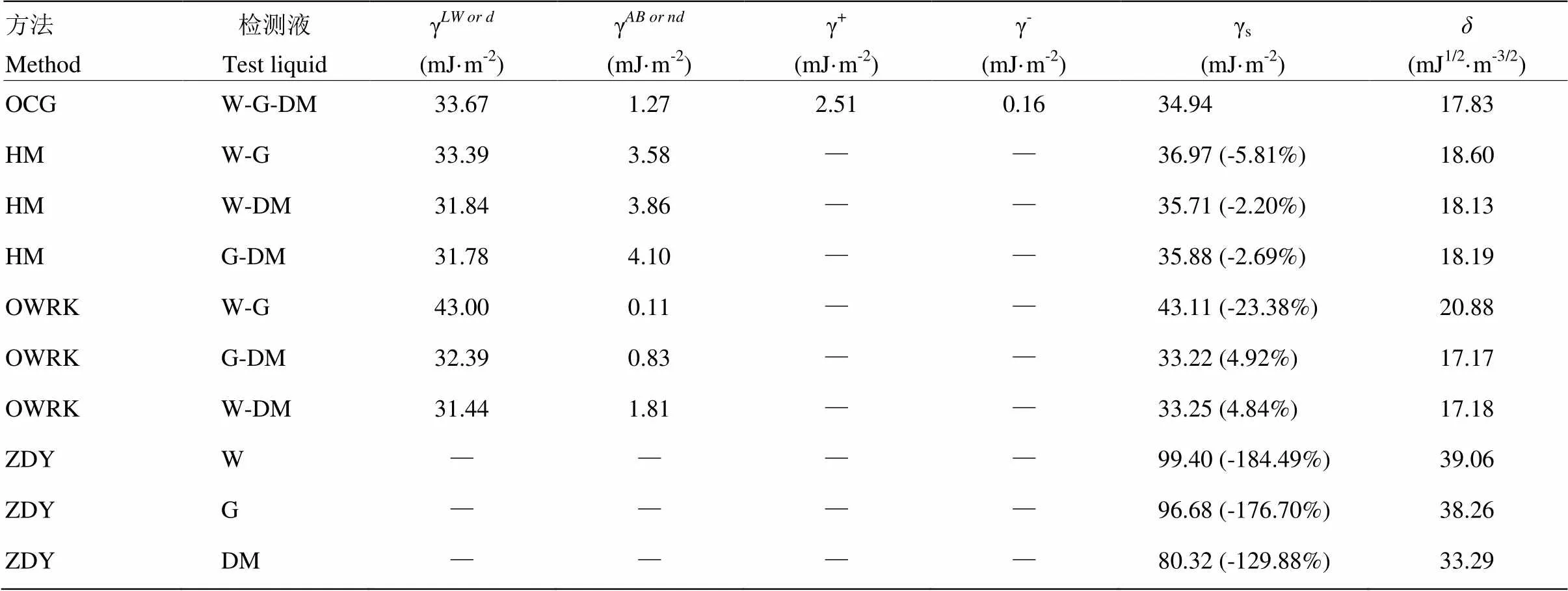
表8 苏椒13辣椒叶片反面表观表面自由能
2.4 表面自由能分量比例分析
3种辣椒叶片正反面的表观表面自由能分量所占比例见表9。OCG法的结果表明3种辣椒正反面表观表面自由能的Lifshitz-van der Waals分量γ所占比例均>85%,且均高于酸碱作用分量γ所占的比例。HM法中选用极性与非极性组合(W-DM、G-DM)获得3种辣椒叶片表观表面自由能的色散分量所占比例均高于极性分量所占比例;选用极性组合(W-G)获得的苏紫1号和GR甜椒叶片表观表面自由能的色散分量所占比例均低于极性分量所占比例,其中苏紫1号正面表观表面自由能的色散分量所占比例略高于极性分量所占比例;苏椒13号叶片表观表面自由能的色散分量所占比例均高于极性分量所占比例。OWRK法中选用极性与非极性组合(W-DM、G-DM)获得3种辣椒叶片表观表面自由能的色散分量所占比例(>80%)均高于极性分量所占比例(<20%);选用极性组合(W-G)获得的苏紫1号辣椒叶片表观表面自由能的色散分量所占比例均高于极性分量所占比例,GR甜椒正面表观表面自由能的色散分量所占比例略高于极性分量所占比例,其反面表观表面自由能的色散分量所占比例低于极性分量所占比例,苏椒13号辣椒叶片表观表面自由能的色散分量所占比例(>99%)远高于极性分量所占比例(<1%)。
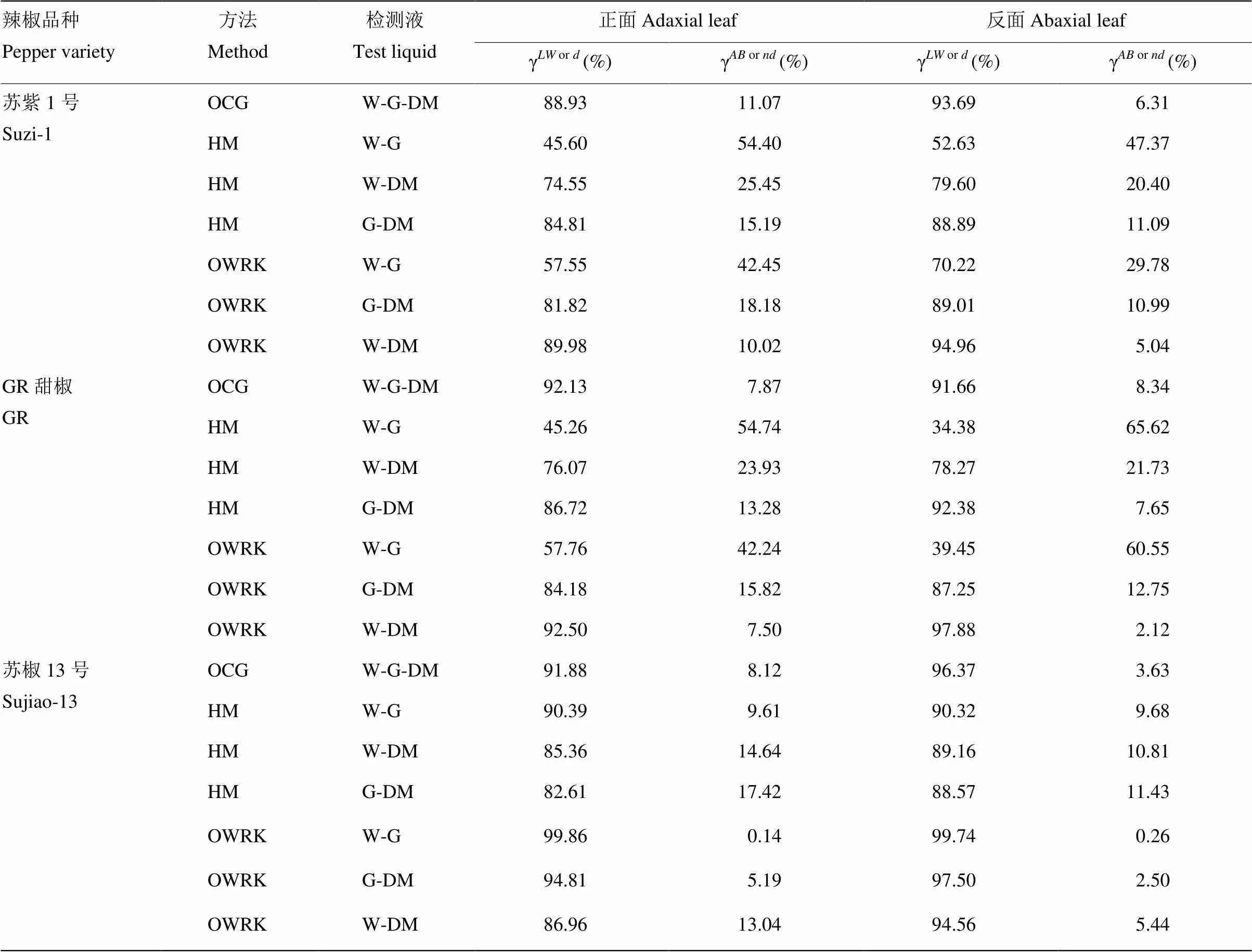
表9 辣椒叶片表面自由能分量百分率
3 讨论
农田植株上病虫害的防治多以喷雾方式为主,其叶片内在属性直接影响着药液液滴的润湿性、黏附性以及渗透性等[21-23]。固体表面自由能和溶解度系数常被用来预测水与固体表面或药液与固体表面间的互作效应以及可能的药液吸收或传导方式[24]。基于接触角的固体表面自由能的计算方法很多[25],由于植物表面的多样性以及表面形貌结构特性,使用OCG法可以描述未知理化性能植物叶面极性分量与非极性分量的组成,同时可获知更多表面的表征数据,其在检测液组合的选择上多采用水、丙三醇和二碘甲烷(W-G- DM)组合,并被证实具有较好的重现性,该方法适用于非极性或极性表面,而HM法和OWRK法只适用于非极性表面[26]。绝大多数植物叶片表面能均由非极性分量和极性分量组成,当极性分量占比达到一定程度后,HM法和OWRK法的适用性有待进一步验证。本研究以3种辣椒叶片为对象,通过比较不同检测液组合来估测辣椒叶面表观表面自由能,从结果来看,ZDY法分别以单一的水、丙三醇或二碘甲烷作为检测液计算获得3种辣椒叶片正反面的表观表面自由能数值与OCG法获得数值偏差均>100%,因此ZDY法不适用于估测辣椒叶面的表观表面自由能,更多的适合聚合物或固体石蜡表面自由能的估算[12];HM法和OWRK法中选用极性和极性检测液组合(W-G)时,色散分量和极性分量所占比例与OCG法获得的结果相差较大或截然相反,同时获得的辣椒叶片表观表面自由能偏差较大,因此选用HM法和OWRK法计算表观表面自由能时,检测液选择至少要含有一种非极性的检测液;HM法和OWRK法中选用极性和非极性检测液组合(W-DM、G-DM)时,色散分量和极性分量所占比例与OCG法获得的结果相差不大,计算获得的辣椒叶片表观表面自由能偏差多在10%以内(其中HM法W-DM组合在苏紫1号和GR甜椒叶片正反面,G-DM组合在GR甜椒叶片正面;OWRK法G-DM组合在苏椒13号叶片正面除外)。
叶面表面化学成分及含量与叶面非极性分量和极性分量的组成密切相关[27],研究表明辣椒表皮蜡质多由C20-C35长链烷烃、伯醇、醛、酮、C16-C32的脂肪酸及三萜烯类化合物等组成[28]。对于3个辣椒品种而言,无论是辣椒叶片正面还是反面,非极性分量所占比例均高于极性分量,同时每种辣椒叶面非极性分量和极性分量所占比例大致相同,这就表明3种辣椒叶片表面具有相似极性,只是叶面蜡质各组分物质含量上存在着差异。3个辣椒品种叶面表观表面自由能存在差异,其中苏椒13号辣椒叶面表观表面自由能最低,为33.21—36.92 mJ·m-2。一般认为液体表面张力低于靶标叶面表面自由能时,液体能在固体上表现出较好的润湿性[29-30],而在常用杀虫剂推荐剂量药液的表面张力测定过程中发现多数药液的表面张力与喷雾的药液量密切相关[31],多介于30—50 mN·m-1[32],由此可见,辣椒叶面的表面自由能处于常规药液表面张力的范围中,故在进行病虫害防治喷雾过程中,根据实际情况选择合适的桶混助剂来降低药液的表面张力,调节药液在辣椒叶面上的润湿效果,从而提高农药的利用率。
4 结论
选用水、丙三醇和二碘甲烷3种检测液按HM法、OWRK法、OCG法和ZDY法4种方法计算辣椒叶片表观表面自由能,发现ZDY法不适用辣椒叶片表观表面自由能的计算;OCG法、HM法和OWRK法可用于辣椒叶片表观表面自由能的计算,其中HM法和OWRK法在检测液的选择上尽可能选用极性与非极性的组合(如W-DM、G-DM),避免选用极性组合(如W-G)。
3种辣椒叶片正反面表观表面自由能的非极性分量γ或γ均高于极性分量γ或γ。
[1] Puente D W, Baur P. Wettability of soybean (L.) leaves by foliar sprays with respect to developmental changes., 2011, 67(7): 798-806.
[2] Taylor P. The wetting of leaf surface., 2011, 16(4): 326-334.
[3] 袁会珠, 杨代斌, 闫晓静, 张琳娜. 农药有效利用率与喷雾技术优化. 植物保护, 2011, 37(5): 14-20.
Yuan H Z, Yang D B, Yan X J, Zhang L N. Pesticide efficiency and the way to optimize the spray application., 2011, 37(5): 14-20. (in Chinese)
[4] MÜller C, Riederer M. Plant surface properties in chemical ecology., 2005, 31(11): 2621-2651.
[5] Schreiber L. Transport barriers made of cutin, suberin and associated waxes., 2010, 15(10): 546-553.
[6] Gaskin R E, Steele K D, Forster W A. Characterising plant surfaces for spray adhesion and retention., 2005, 58: 179-183.
[7] Nairn J J, Forster W A. Methods for evaluating leaf surface free energy and polarity having accounted for surface roughness., 2017, 73(9): 1854-1865.
[8] 范仁俊, 张晓曦, 周璐, 曹冲, 杜凤沛. 利用OWRK法预测桃叶表面润湿性能的研究. 农药学学报, 2011, 13(1): 79-83.
Fan R J, Zhang X X, Zhou L, Cao C, Du F P. Research on the wettability of peach leaf surfaces by OWRK method., 2011, 13(1): 79-83. (in Chinese)
[9] Wu S. Calculation of interfacial tension in polymer systems., 1971, 34(1): 19-30.
[10] Owens D K, Wendt R C. Estimation of the surface free energy of polymers., 1969, 13(8): 1741-1747.
[11] Van Oss C J, Chaudhury M K, Good R J. Interfacial Lifshitz-van der Waals and polar interactions in macroscopic systems., 1988, 88(6): 927-941.
[12] 朱定一, 戴品强, 罗晓斌, 张远超. 润湿性表征体系及液固界面张力计算的新方法(Ⅰ). 科学技术与工程, 2007, 7(13): 3057-3062.
Zhu D Y, Dai P Q, Luo X B, Zhang Y C. Novel characterization of wetting properties and the calculation of liquid-solid interface tension (Ⅰ)., 2007, 7(13): 3057-3062. (in Chinese)
[13] Fernández V, Khayet M. Evaluation of the surface free energy of plant surfaces: toward standardizing the procedure., 2015, 6: 510.
[14] Shalel-Levanon S, Marmur A. Validity and accuracy in evaluating surface tension of solids by additive approaches., 2003, 262(2): 489-499.
[15] 张晨辉, 赵欣, 雷津美, 马悦, 杜凤沛. 非离子表面活性剂Triton X-100溶液在不同生长期小麦叶片表面的润湿行为. 物理化学学报, 2017, 33(9): 1846-1854.
Zhang C H, Zhao X, Lei J M, Ma Y, Du F P. Wettability of Triton X-100 on wheat () leaf surfaces with respect to developmental changes., 2017, 33(9): 1846-1854. (in Chinese)
[16] 关明杰, 薛明慧. 化学处理对竹笋壳润湿性的影响. 农业工程学报, 2016, 32(11): 309-314.
Guan M J, Xue M H. Wettability of bamboo shoot shell under chemical treatment., 2016, 32(11): 309-314. (in Chinese)
[17] Revilla P, Fernández V, Alvarez-Iglesias L, Medina E T, Cavero J. Leaf physico-chemical and physiological properties of maize (L.) populations from different origins., 2016, 107: 319-325.
[18] 顾中言. 植物的亲水疏水特性与农药药液行为的分析. 江苏农业学报, 2009, 25(2): 276-281.
Gu Z Y. Analysis of the relationship between hydrophilic or hydrophobic property of plant and action of pesticides solution on plants leaves., 2009, 25(2): 276-281. (in Chinese)
[19] Khayet M, Fernández V. Estimation of the solubility parameters of model plant surfaces and agrochemicals: a valuable tool for understanding plant surface interactions., 2012, 9: 45.
[20] Jañczuk B, Bialopiotrowicz T, Zdziennicka A. Some remarks on the components of the liquid surface free energy., 1999, 211(1): 96-103.
[21] Kolyva F, Stratakis E, Rhizopoulou S, Chimona C, Fotakis C. Leaf surface characteristics and wetting inL., 2012, 207(8): 551-556.
[22] Zheng Q S, Lu C J. Size effects of surface roughness to superhydrophobicity., 2014, 10: 462-475.
[23] Zhu L, Ge J R, Qi Y Y, Chen Q, Hua R M, Luo F, Chen P R. Droplet impingement behavior analysis on the leaf surface ofunder different pesticide formulations., 2018, 144: 16-25.
[24] Sikorska D, Papierowska E, SzatyłowiczJ, Sikorski P, Suprun K, Hopkins R J. Variation in leaf surface hydrophobicity of wetland plants: the role of plant traits in water retention., 2017, 37(5): 997-1002.
[25] Domińczuk J, KrawczukA. Comparison of surface free energy calculation methods., 2015, 791: 259-265.
[26] 陈晓磊. 固体聚合物表面接触角的测量及表面能研究[D]. 长沙: 中南大学, 2012.
Chen X L. Surface free energy and contact angle measurement of solid polymer[D]. Changsha: Central South University, 2012. (in Chinese)
[27] Fernández V, Sancho-Knapik D, Guzman P, Peguero- Pina J J, Gil L, Karabourniotis G, Khayet M, Fasseas C, Heredia-Guerrero J A, Heredia A, Gil-Pelegrin E. Wettability, polarity, and water absorption of holm oak leaves: effect of leaf side and age., 2014, 166(1): 168-180.
[28] Bauer S, Schulte E, Thier H P. Composition of the surface waxes from bell pepper and eggplant., 2005, 220(1): 5-10.
[29] 徐广春, 顾中言, 徐德进, 许小龙. 稻叶表面特性及雾滴在倾角稻叶上的沉积行为. 中国农业科学, 2014, 47(21): 4280-4290.
Xu G C, Gu Z Y, Xu D J, Xu X L. Characteristics of rice leaf surface and droplets deposition behavior on rice leaf surface with different inclination angles., 2014, 47(21): 4280-4290. (in Chinese)
[30] Gaskin R E, Pathan A K. Characterising plant surfaces and adjuvant interactions to improve pesticide spray retention and coverage on avocados., 2006, 6: 63-70.
[31] 顾中言, 徐德进, 徐广春. 田间药液用量影响农药单位剂量防治效果的原因分析. 中国农业科学, 2018, 51(13): 2513-2523.
Gu Z Y, Xu D J, Xu G C. The cause of influence of spray volume on control effect of pesticide unit dose in rice fields., 2018, 51(13): 2513-2523. (in Chinese)
[32] 徐广春, 顾中言, 徐德进, 许小龙, 董玉轩. 常用农药在水稻叶片上的润湿能力分析. 中国农业科学, 2012, 45(9): 1731-1740.
Xu G C, Gu Z Y, Xu D J, Xu X L, Dong Y X. Wettablity analysis of pesticides on rice leaf., 2012, 45(9): 1731-1740. (in Chinese)
(责任编辑 岳梅)
Calculation Methods for the surface free energy of pepper leaf surface
XU GuangChun, GU ZhongYan, XU DeJin, XU XiaoLong, XU Lu
(Institute of Plant Protection, Jiangsu Academy of Agricultural Sciences, Nanjing 210014)
【Objective】The efficiency of foliar-applied agrochemicals is closely related to the complexity of physicochemical properties of plant leaf surfaces. For better understanding the interfacial interaction between agrochemical spray liquids and plant leaf surfaces, the internal relation would be seek from the thermodynamic point based on pepper leaf surfaces. This will provide a basis for efficient use of pesticides on plants.【Method】Three test liquids were water (W), glycerol (G) and diiodomethane (DM). Their static contact angles of a single droplet on the pepper leaf surfaces of different varieties were determined by contact angle meter. Then the total surface free energy (SFE) and its components were evaluated by Harmonic mean (HM) method, Owens-Wendt-Rabel- Kaelble (OWRK) method, Van-Oss-Chaudhury-Good (OCG) method and ZDY method. Accordingly, solubility parameter () of pepper leaf surfaces was calculated.【Result】The leaves of Suzi-1 and GR pepper were wettable (<90°) for W and Sujiao-13 pepper leaves were unwettable (>90°) for W. Among the 4 methods, more physical characteristic information was obtained by the OCG method with 3 test liquids (W-G-DM) and calculated percentages of non-polar components of the SFE of pepper leaf surfaces (>85%) were higher than the polar components (<15%). The HM and OWRK methods based on 2 test liquids. When the 2 test liquids were polar (i.e. W-G), the percentages of non-polar or polar component of the SFE of the pepper leaf surface varied greatly, or even the opposite to the percentage obtained in the OCG method. When the 2 test liquids were polar and non-polar combination (i.e. W-DM or G-DM), the deviation of the SFE values calculated by OWRK method was lower than that by HM method based on the OCG method. The SFE values calculated by ZDY method with 1 test liquid were much higher than that of the other three methods. Compared with OCG method, the deviation of the SFE of pepper leaf surfaces was >100%. Based on the deviation from the OCG method within 10% of the SFE, SFE of Suzi-1 leaf surface was 37.72-43.11 mJ·m-2and solubility parameter was 18.89-22.77 mJ1/2·m-3/2. SFE of GR leaf surface was 37.53-40.95 mJ·m-2and solubility parameter was 18.81-20.09 mJ1/2·m-3/2. SFE of Sujiao-13 leaf surface was 33.21-36.92 mJ·m-2and solubility parameter was 17.17-18.58 mJ1/2·m-3/2.【Conclusion】Using water (W), glycerol (G) and diiodomethane (DM) as the test liquid, ZDY method is not suitable for calculating the SFE of pepper leaf surfaces and the rest methods (HM, OWRK, OCG) can be used to calculate the SFE. Among them, the HM or OWRK method should be paid more attention to the polarity of selecting test liquid combination. Meanwhile, the percentage of non-polar component of the SFE of 3 kinds of pepper is higher than that of the polar component.
pepper leaf surface; static contact angle; surface free energy; surface free energy components; solubility parameter
2018-03-14;
2018-05-02
国家重点研发计划(2017YFD0200305)
徐广春,Tel:025-84390403;E-mail:xgc551@163.com。
顾中言,Tel/Fax:025-84390403;E-mail:guzy@jaas.ac.cn
10.3864/j.issn.0578-1752.2018.16.005
