茶多酚改性对蛋清蛋白凝胶特性的影响及机理
周绪霞,陈 婷,吕 飞,顾赛麒,刘建华,丁玉庭*
蛋清蛋白具有凝胶性、持水性、起泡性和乳化性等多种功能特性,在食品工业中有着广泛应用,常用于火腿、腊肠、鱼糜制品等的增稠剂及面类制品的增强剂。如何进一步改善鸡蛋清蛋白的功能特性也一直是国内外研究的热点。蛋白质改性主要通过改变蛋白质氨基酸残基和多肽链结构,引起蛋白质大分子的空间结构变化,导致其理化性质改变,从而获得更好的功能特性[1]。目前常用的方法包括物理法、化学法和生物酶法等[2]。但是物理改性存在耗时长、效果不明显等缺点,生物酶法则对反应条件要求苛刻,且成本较高,而化学改性方法则可能存在一定安全隐患。因此探索一种经济安全高效的改性方法对改善蛋清蛋白的凝胶等功能特性具有重要意义。
多酚是一类广泛存在于植物体内的、具有许多活性基团的多元酚类化合物,其能以氢键、疏水作用力、共价键等与蛋白质结合而对蛋白质产生改性作用[3]。Asano等[4]认为,多酚的大量酚羟基与蛋白质主链的肽基NH—CO,侧链上的—OH、—NH2以及—COOH以氢键的形式多点结合。目前关于多酚与蛋白质的相互作用的研究已有报道[5-7]。Staszewski等[8]研究表明,绿茶多酚能通过加速β-乳球蛋白或酪蛋白凝胶网络的形成而对β-乳球蛋白凝胶的黏弹性有显著影响,且对蛋白质生物活性无影响。Jia Na等[9]研究表明,高浓度的儿茶素会通过阻碍凝胶网络的形成、掩盖蛋白质的活性功能基团而影响猪肉肌原纤维蛋白的功能特性。Wu Weiguo等[10]研究表明,低添加量的绿茶提取物能提高蛋清蛋白的发泡能力和泡沫稳定性。Hatanaka等[11]发现,红茶、绿茶、乌龙茶的茶叶提取物改性作用可显著提高蛋清蛋白凝胶的黏弹性,并有助于其形成更紧密的网络结构。但目前关于茶多酚与蛋清蛋白相互作用对蛋清蛋白凝胶特性影响及其内在机理变化的研究鲜见报道。
为此,本实验以茶多酚为研究对象,研究不同添加量的茶多酚对蛋清蛋白凝胶强度、持水力以及微观结构等特性的影响,探讨茶多酚改性对蛋清蛋白表面疏水性和巯基含量的影响,并通过差示扫描量热(differential scanning calorimetry,DSC)法和傅里叶变换红外光谱(Fourier transformed infrared spectroscopy,FTIR)法对改性蛋清蛋白热稳定性和二级结构进行分析,揭示茶多酚与蛋清蛋白的作用机理,为日后生产更高凝胶特性的蛋清蛋白并拓宽其应用范围提供的理论基础。
1 材料与方法
1.1 材料与试剂
散装蕴康土鸡蛋 杭州世纪联华和平店;茶多酚(食品级) 上海梦荷生物科技有限公司;Tris、甘氨酸、尿素(均为分析纯) 北京鼎国昌盛生物技术有限责任公司;磷酸二氢钠、十二水合磷酸氢二钠、无水乙醇(均为分析纯) 国药集团化学试剂有限公司。
1.2 仪器与设备
DF-101S集热式恒温加热水浴磁力搅拌器 河南省予华仪器有限公司;TA.XT.Plus型质构仪 英国Stable Micro System公司;E-201-C pH复合电极 上海仪电科学仪器股份有限公司;ARL Advant X荧光光谱仪、Nicolet 6700 FTIR仪 美国Thermo公司;SP-75紫外-可见分光光度计 上海光谱仪器有限公司;Q100 DSC仪美国TA公司;FD-1-50真空冷冻干燥机 北京博医康实验仪器有限公司;S-4700(II)扫描电镜 日本日立公司。
1.3 方法
1.3.1 样品处理
选取新鲜无破壳的鸡蛋分离出蛋清液,用磁力搅拌器搅拌均匀后除去上层泡沫,蛋清蛋白质含量采用Bradford法测定,然后分别添加质量分数0%、0.2%、0.4%、0.6%、0.8%的茶多酚并搅拌均匀。将混合好的溶液置于恒温水浴磁力搅拌器中,在(25±1)℃条件下反应90 min[12],反应完毕后,将改性后的蛋清蛋白溶液置于4 ℃冰箱中冷藏备用。
1.3.2 蛋清蛋白凝胶制备
分别取40 mL改性后的各组蛋清蛋白-茶多酚溶液灌入直径为21 mm的人造肠衣中,两端扎紧,然后置于90 ℃水浴锅中恒温水浴30 min,取出后迅速放入冰水浴中冷却至常温,放入4 ℃冰箱中冷藏过夜[13],测定各指标。
1.3.3 凝胶强度的测定
采用TA-XT Plus质构仪测定样品的凝胶强度。将蛋清蛋白凝胶切成直径21 mm、长25 mm的圆柱体,采用直径为0.5英寸的圆柱状平头探头,测定条件为:测前速率2 mm/s,测试速率2 mm/s,测后速率5 mm/s,触发力5.0 g,下压距离为15 mm。凝胶强度用硬度即探头下压过程中的最大感应力(单位g)表示,每组样品平行测定8 次取平均值。
1.3.4 凝胶持水力的测定
称取一定质量(m1)的蛋白凝胶,用一层滤纸包裹,置于50 mL离心管中,4 ℃、4 000 r/min离心10 min,离心完毕后取出样品并称质量(m2),按公式(1)计算失水率:

1.3.5 表面疏水性的测定
参考迟玉杰等[14]的方法测定。将改性样品溶液用磷酸盐缓冲液(pH 7.4,0.01 mol/L)分别配制成1、2、3、4 mg/mL和5 mg/mL的蛋白溶液(蛋白质含量采用Bradford法测定)。取各蛋白样品溶液4 mL,分别加入20 μL 8-苯氨基-1-萘磺酸溶液(8 mmol/L),混合均匀后在室温条件下静置15 min,设置激发波长370 nm,发射波长470 nm,利用荧光光谱仪测定样品的荧光强度,以未加8-苯氨基-1-萘磺酸的蛋白溶液的荧光强度为空白。以相对荧光强度对蛋白质浓度作图,采用最小二乘法进行曲线拟合,直线斜率即为蛋白质的表面疏水性。以原蛋白的表面疏水性为100%计,计算改性蛋清蛋白的表面疏水性的相对百分比。
1.3.6 巯基含量的测定
参考Plancken等[15]的方法并略作修改。将样品溶液稀释2 倍,然后取1 mL样品溶液加入4 mL包含0.01 mol/L的乙二胺四乙酸的Tris-甘氨酸(pH 8.0,0.1 mol/L)缓冲液,混合均匀后,在40 ℃条件下保温30 min,加入125 μL 5,5’-二硫代双(2-硝基苯甲酸)(5,5’-dithiobis-(2-nitrobenzoic acid),DTNB)试剂(20 mg DTNB溶于pH 8.0 5 mL 0.1 mol/L Tris-甘氨酸缓冲液),25 ℃条件下保温10 min,测定412 nm波长处的吸光度。
总巯基含量的测定:所用的Tris-甘氨酸缓冲液中另含有0.25 g/mL十二烷基硫酸钠,其他条件与表面巯基的测定相同。按公式(2)计算总巯基含量:
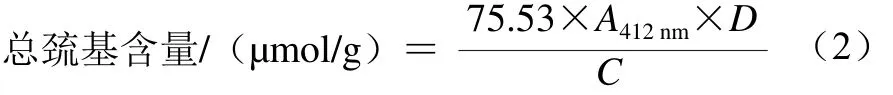
式中:C为样品质量浓度/(mg/mL);D为样品稀释倍数,5.125。
以原蛋清中巯基数为100%计,计算改性蛋清中巯基相对含量。
1.3.7 DSC分析
参考Iesel等[16]的方法。准确称取1.3.1节中反应好的样品放入铝坩埚中,密封,并用相同的空坩埚作参比,以5 ℃/min的升温速率从25 ℃加热到105 ℃。整个过程均在干燥N2条件下进行,吹扫气速率20 mL/min,保护气速率60 mL/min。
1.3.8 FTIR分析
参考Cheng Zhengjun等[17]的方法。将反应后的样品进行冷冻干燥,然后准确称取1~3 mg样品,加入100~300 mg磨细的干燥溴化钾,研磨成均匀干燥的粉末,压成薄片,利用FTIR仪收集样品的红外图谱,设置波长范围4 000~400 cm-1,分辨率4 cm-1,扫描次数32 次,温度25 ℃,以空气为背景,每个样品扫描前扣除背景。通过OMNIC V8.0软件对1 600~1 700 cm-1位置进行傅里叶去卷积,将去卷积图谱进行二阶导,比较带的位置和数目,以保证不被过度去卷积,二级结构含量的定量分析通过Gausse函数对图谱进行多次拟合,然后根据各子峰与不同二级结构的对应关系及其积分面积,计算出各种二级结构的相对含量[18]。
1.3.9 凝胶扫描电镜分析
参考Salvador等[19]的方法。将凝胶样品中心部位切成小块,用2.5%的戊二醛溶液浸泡固定,4 ℃条件下放置24 h。固定好的样品在室温条件下用磷酸盐缓冲液(pH 7.4,0.01 mol/L)漂洗3 次,每次10 min,然后依次用体积分数60%、70%、80%、90%及100%的乙醇溶液分别浸泡20 min,逐级脱水,之后再用叔丁醇浸泡3 次,每次10 min,然后将处理好的样品进行冷冻干燥。干燥后的样品用导电双面胶固定到样品台上,经溅射仪喷金后,置于扫描电镜下观察。
1.4 数据处理
采用SPSS 17.0统计软件进行相关性分析和方差分析,Duncan法进行多重比较(P<0.05,差异显著),采用Origin 8.0对数据进行绘图。
2 结果与分析
2.1 凝胶强度的变化
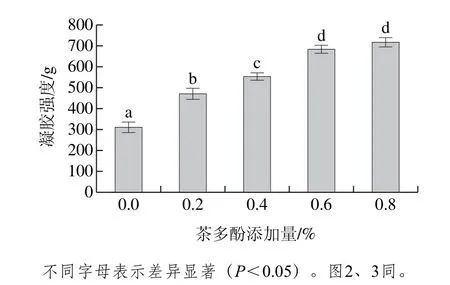
图1 茶多酚添加量对改性蛋清蛋白凝胶强度的影响Fig. 1 Effect of tea polyphenols addition on gel strength of modified egg white protein
由图1可以看出,茶多酚改性可明显增加蛋清蛋白的凝胶强度,且茶多酚添加量越多,增加越明显。当茶多酚添加量为0.8%时,改性蛋清蛋白的凝胶强度达到720.7 g,比未改性蛋清蛋白凝胶提高了130.2%(313.1 g)。茶多酚富含大量活性羟基,能与蛋白质主链的肽基NH—CO,侧链上的—OH、—NH以及—COOH以氢键的形式多点结合,同时吸附大量水分子,增加蛋白质的水合能力,同时减少水溶性蛋白对凝胶形成的影响,提高凝胶结构的致密性[20],最终使得改性后的蛋清蛋白凝胶网络更加稳定。因此蛋清蛋白凝胶强度的增加可能归因于茶多酚与蛋清蛋白之间发生了交联作用,促进了蛋清蛋白凝胶网络的形成。有研究认为,多酚具有多羟基结构使其具有较强的亲水能力,而蛋白质兼具亲水亲油性,多酚的亲水基团能够与蛋白质的亲油基团发生氢键作用形成紧密的结构[21]。当茶多酚添加量增加到0.8%时,凝胶强度上升趋势减缓,推测此时茶多酚与蛋清蛋白的结合已趋于饱和[22]。
2.2 蛋清蛋白凝胶持水性的变化

图2 茶多酚添加量对改性蛋清蛋白凝胶失水率的影响Fig. 2 Effect of tea polyphenol addition on expressible moisture content of modified egg white protein gel
由图2可以看出,蛋清蛋白经茶多酚改性后失水率显著降低。与未改性的凝胶相比,随着茶多酚添加量的增加,蛋白凝胶失水率持续下降,当茶多酚添加量为0.8%时,凝胶持失水率达到最低,从29.41%降至19.29%。这与凝胶强度的变化趋势相一致,表明茶多酚改性使蛋清蛋白形成更紧密的网络结构,具有更好的保水性。
2.3 蛋清蛋白表面疏水性的变化
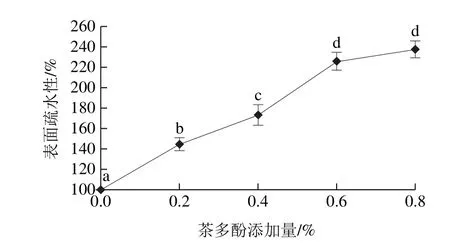
图3 茶多酚添加量对改性蛋清蛋白表面疏水性的影响Fig. 3 Effect of tea polyphenols addition on surface hydrophobicity of modified egg white protein
如图3所示,改性后蛋清蛋白质的表面疏水性发生显著变化,随着茶多酚添加量的增加,蛋白质的表面疏水性持续增加。蛋白质高级结构展开后疏水性脂肪族与芳香族氨基酸侧链基团的暴露会导致蛋白质疏水性的变化,因此,表面疏水性可反映蛋白质解折叠的程度[23]。当茶多酚与蛋清蛋白发生作用时,蛋白质的分子链不断伸展,分子内部的疏水基团不断暴露,从而导致蛋白质表面疏水性的不断增加。有研究认为蛋白质的表面疏水性在凝胶形成的初期,对立体网状结构的形成起着非常重要的作用[24]。
2.4 蛋清蛋白中巯基含量的变化
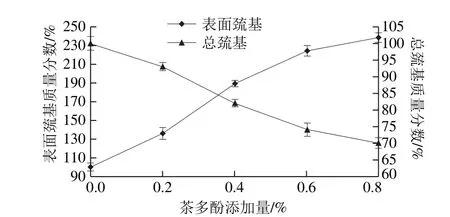
图4 茶多酚添加量对改性蛋清蛋白巯基含量的影响Fig. 4 Effect of tea polyphenols addition on sulfhydryl content of modified egg white protein
Matsudomi等[25]研究表明蛋白的总巯基数和表面巯基数对蛋白质的凝胶性能起着明显的作用。而巯基和二硫键是蛋白质分子中稳定蛋白质构象的重要化学键,会影响蛋白质凝胶性、持水性等功能特性[26]。如图4所示,随着茶多酚添加量的增加,蛋清蛋白中总巯基含量不断下降,而表面巯基的含量不断增加。这可能是由于蛋清蛋白与茶多酚在相互作用的过程中,蛋白质的构象发生了变化,一方面,蛋清蛋白质改性后分子结构展开,使得包埋于分子内部的巯基不断暴露出来,造成了表面巯基含量的增加,暴露于表面的巯基数增多,分子间和分子内的相互作用增强,蛋清蛋白的凝胶性能提高;另一方面,由于蛋白质分子内部或分子间的巯基氧化反应或巯基/二硫键交换反应形成更多二硫键[27],最终导致了总巯基含量的下降。
2.5 DSC分析

图5 茶多酚添加量对改性蛋清蛋白热特性的影响Fig. 5 Effect of tea polyphenols addition on thermal properties of modified egg white protein
由图5可以看出,每组蛋清蛋白样品都出现了2 个吸收峰T1和T2,第1个峰为卵转铁蛋白变性峰,第2个峰为卵清蛋白变性峰[10]。随着茶多酚添加量的增加,2 个吸收峰均向右迁移。原蛋清蛋白的2 个吸收峰分别是67.5 ℃和84.2 ℃,当添加0.8%的茶多酚时,改性后的蛋清蛋白的2 个吸收峰分别迁移至69.9 ℃和88.9 ℃,表明茶多酚改性有效提高了蛋清蛋白的热稳定性。推测由于茶多酚中的活性羟基与蛋清蛋白质主链以及侧链上的基团多点结合,使蛋白质结构更加紧密,不易被破坏,从而增加了蛋白质的热稳定性。Wang Xiaoya等[28]在研究表没食子儿茶素表没食子酸酯与α-乳白蛋白交联作用中得到了类似的结论,并认为蛋白质热稳定性的增加是由于多酚与蛋白质之间发生了共价交联作用。
2.6 FTIR分析

图6 不同添加量茶多酚改性蛋清蛋白的FTIR图谱Fig. 6 FTIR spectra of egg white proteins modified with different amounts of tea polyphenols
如图6所示,蛋白质的酰胺I带(1 600~1 700 cm-1)主要是由C=O的伸缩振动引起的,与蛋白质的二级结构有关。蛋白质分子内多肽链可形成螺旋、折叠、转角以及无规则卷曲等特定的二级结构,其中α-螺旋和β-折叠属于紧密有序结构,β-转角属于比较松散的部分有序结构,而无规则卷曲为松散的无序结构。基于Jackson等[29]提出的理论,1 600~1 639 cm-1为β-折叠,1 640~1 650 cm-1为无规则卷曲,1 651~1 660 cm-1为α-螺旋,1 661~1 700 cm-1为β-转角,据此计算出的蛋清蛋白各二级结构相对含量如表1所示。随着茶多酚添加量的增加,α-螺旋相对含量不断下降,而β-折叠相对含量显著上升,这表明茶多酚改性在一定程度上破坏了蛋清蛋白原有的刚性结构,柔性结构增加,使分子由有序变为无序,表明多酚会导致蛋白质结构展开,这个结果与Jia Jingjing[30]和Hasni[31]等的结果相类似。茶多酚与蛋清蛋白分子发生反应时,用于稳定α-螺旋的蛋白质氢键断裂,蛋白质活性基团逐渐暴露参与凝胶形成,进而使得蛋清蛋白凝胶强度得到改善。董昳廷[32]研究发现α-螺旋结构含量的变化与β-折叠结构分别凝胶持水性和凝胶强度呈正相关关系。因此推测蛋清蛋白改性后凝胶强度与失水率的变化与蛋白质各二级结构相对含量变化有关,而两者之间的具体联系,有待日后进一步验证。

表1 不同茶多酚添加量对蛋清蛋白二级结构的影响Table 1 Effects of dtea polyphenols addition on secondary structures of egg white protein
2.7 凝胶微观结构
凝胶网络结构的形成是蛋白质变性的结果,导致了分子间发生共价和非共价相互作用,同时还包括二硫键和疏水性相互作用[13]。由图7可知,未添加茶多酚的原蛋清凝胶表面粗糙不均匀,而经茶多酚改性后蛋清蛋白可以形成表面更加有序的凝胶网络结构,并且随着茶多酚添加量的增加,凝胶表面更加平滑,均匀。这可能是由于茶多酚含有的活性羟基与蛋清蛋白主链或侧链上的基团发生了交联作用,进而形成更加有序均匀的网络结构,凝胶网络结构越均匀致密,其凝胶性越好,这与凝胶强度的结果相一致。


图7 不同添加量茶多酚改性蛋清蛋白凝胶的扫描电镜图Fig. 7 SEM images of egg white protein gels modified with different amounts of tea polyphenols
3 结 论
利用茶多酚对蛋清蛋白进行改性,研究表明,当茶多酚添加量达到0.8%时,改性蛋清蛋白的凝胶强度提高了130.2%,失水率从29.41%降至19.29%;改性蛋清蛋白的热稳定性增加,即蛋白质的2 个热吸收峰分别从67.5 ℃和84.2 ℃提升至69.9 ℃和88.9 ℃。这一方面与茶多酚改性增强了蛋清蛋白的表面疏水性和表面巯基含量有关,另一方面则与蛋清蛋白质二级结构的改变有关,即随着茶多酚添加量的增加,α-螺旋相对含量不断下降,而β-折叠相对含量显著上升,蛋白质的结构由有序变为无序。当茶多酚的添加量达到0.8%时,其凝胶强度与失水率不再发生显著性变化,推测蛋清蛋白质与茶多酚的结合点达到饱和。

