葛芪降糖颗粒对2型糖尿病周围神经病变患者血清8-iso-PGF2α的临床观察*
肖若然,娄锡恩,王 帅
(北京中医药大学第三附属医院内分泌科,北京 100029)
糖尿病周围神经病变的发病率和致残率,文献报道患病率在40%~90%不等,有的甚至在糖尿病前期就己经出现感觉神经的损伤[1]。目前研究表明DPN发生后,10年内病死率可达25%~50%,发病机制尚不完全明确,单纯西药治疗效果欠佳[2]。
课题组在临床中发现以补肾活血解毒法组方的葛芪降糖颗粒,在治疗DPN有很好的疗效[3]。因此通过观察葛芪降糖颗粒联合甲钴胺对2型糖尿病周围神经病变(肾虚毒滞型)患者的临床观察,探讨中医药延缓、治疗糖尿病周围神经病变发生、发展的作用机制,为临床早干预、早防治糖尿病周围神经病变,探索新的治疗方案,具有十分重要的意义。
1 临床资料与方法
1.1 一般资料 本研究共纳入2型糖尿病并发周围神经病变患者60例,所有病例均来源于北京中医药大学第三附属医院内分泌科门诊或住院的2型糖尿病并发周围神经病变,且中医辨证为肾虚毒滞型的患者。60例患者根据随机数字表按照编号将患者随机分为治疗组和对照组。两组患者的年龄、性别、病程等基线资料均为统计学差异,具有可比性,详见下表1。两组均无患者脱失。
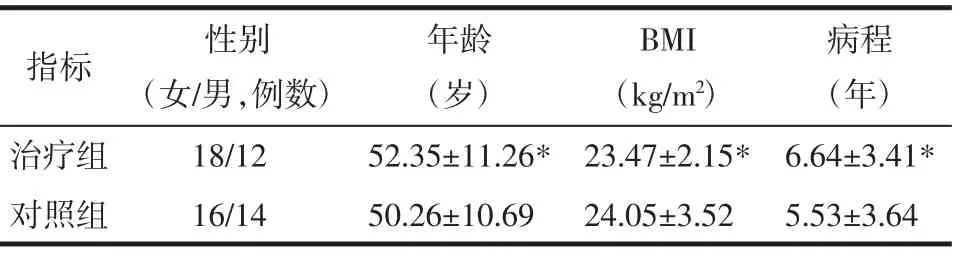
表1 两组患者基线资料结果对比
1.2 诊断标准
1.2.1 西医诊断标准 采用《中国2型糖尿病防治指南2013年版》提出的2型糖尿性周围神经病变病诊断标准。
主要诊断依据包括:1)有糖尿病病史或诊断糖尿病的证据。2)出现感觉、运动神经病变的临床表现。3)神经电生理检查的异常改变。神经电生理检查周围运动神经传导速度(MNCV)<45 m/s,周围感觉神经传导速度(SNCV)<40 m/s。
1.2.2 中医证候诊断标准 参照2002年《中药新药治疗糖尿病的临床研究指导原则》与《消渴病(糖尿病)辨证诊断参考标准》,采用积分辨证法。
肾虚毒滞型:主症:腰膝酸软,性欲减退,畏寒肢冷,五心烦热(肾虚主症);胁痛,腰痛,背痛,刺痛,痛有定处,拒按,脉络瘀血,肢体麻木,癥积,口舌生疮(毒滞主症)。次症:精神萎靡,夜尿频多,动则气虚,口燥咽干,形体消瘦,失眠健忘,齿松发脱,遗精,早泄,经少,经闭(肾虚次症);肌肤甲错,痈肿疮疖,口唇紫暗,面部瘀斑,健忘心悸,心烦失眠,大便秘结(毒滞次症)。肾虚主症和毒滞主症至少各1个,主症记2分,次症记1分,总分≥5分即可辨证为肾虚毒滞型。
1.2.3 研究对象的纳入标准
1)已确诊为2型糖尿病患者。2)均有不同程度的双下肢麻木、疼痛、感觉障碍、腱反射减弱或消失,符合DPN诊断标准。3)血糖保持稳定2月以上,糖化血红蛋白(HbA1c)<7.5%。年龄在30~70岁。4)原用治疗糖尿病周围神经病变的药物停用2周以上。
1.2.4 研究对象的排除标准 1)其他类型糖尿病。2)糖尿病重危急症,如酮症酸中毒,糖尿病高渗状态。3)具有严重的心、肝、肺、肾等功能衰竭及肿瘤或精神病患者。4)妊娠期、哺乳期妇女。5)过敏体质或有对多种药物过敏者。6)参加其他临床试验者。7)工作环境经常变动等易造成失访的情况。
1.2.5 分组方法 分组采用中心随机的方法,将符合条件的患者随机分组,分别对各组进行临床观察。1.2.6 遵循临床观察伦理学原则,提高患者依从性 入组患者签订知情同意书,研究方案和知情同意书均经过北京中医药大学第三附属医院伦理委员会批准,让患者从分知情,完全了解试验过程。药物给予免煎颗粒,便于携带和服用,直接发送给受试者,定制随访卡,及时对受试者进行访视,提高依从性。
1.2.7 治疗方法 中西医结合治疗组的第一阶段:基础治疗2周,包括:糖尿病防治教育,运动,饮食控制,包括低蛋白饮食,控制血糖应用胰岛素。第二阶段:实验观察8周,在基础治疗上加用甲钴胺联合葛芪降糖免煎颗粒(方药组成:生黄芪30 g,葛根20 g,当归 15 g,川芎 12 g,泽泻 12 g,山楂 15 g,鬼箭羽 15 g,漏芦15 g,水煎服2/日早晚餐前 0.5 h)。中西药均由北京中医药大学第三附属医院中心药房提供。
西药组的第一阶段:基础治疗2周同中西医结合组,第二阶段:实验观察8周,在基础治疗上加用甲钴胺。
1.2.8 临床观察 中医证候评分:参照2002年《中药新药治疗糖尿病的临床研究指导原则》制定症状评分表,在治疗前、服药后各1次。
密西根糖尿病性周围神经病评分(MDNS):根据密西根糖尿病性周围神经病评分表评分,在治疗前、服药后各1次。
神经功能测试:采用丹麦产KEYPOINT肌电图机测量正中神经、腓总神经的运动传导速度和感觉传导速度。
指标检测:在治疗前、服药后各采血一次,测定以下生化指标:空腹(FGB)及餐后2 h血糖、糖化血红蛋白(HbA1c)、血清 8-异前列腺素 F2α(8-iso-PGF2α)。
1.2.9 统计分析 实验数据均用均数±标准差表示,计数数据组间比较用单因素方差分析,统计软件采用SPSS 21.0,P<0.01为差异有统计学意义。
3 治疗结果
3.1 治疗结果及疗效比较 见表2。
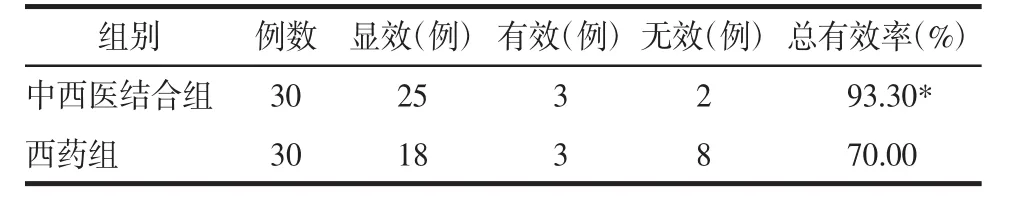
表2 两组治疗结果及疗效比较
3.2 两组中医证侯学评分 见表3。
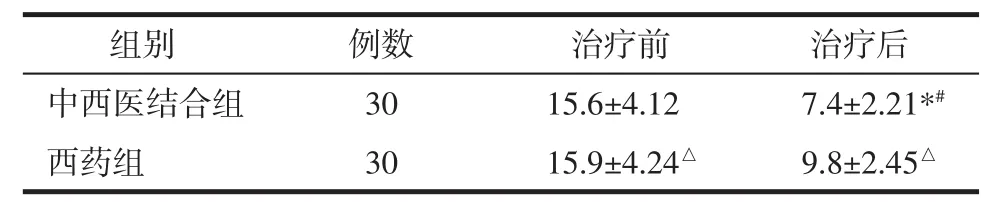
表3 两组中医证侯评分比较(x±s)
3.3 MDNS评分 见表4。
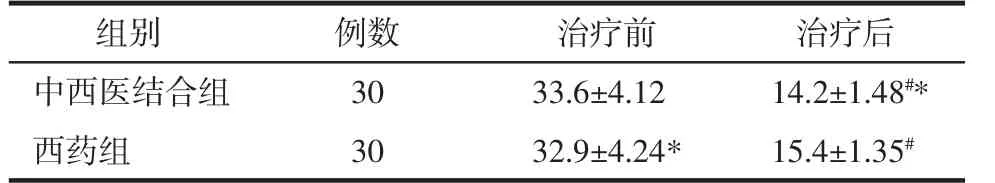
表4 两组MDNS评分比较(x±s)
3.4 FGB、2 h PGB、HbA1c、血清 8-iso-PGF2α 检测 见表5。
3.5 肌电图神经传导速度(NCV)监测 两组治疗前后比较,神经传导速度均有改善,而治疗组改善更为显著(P<0.01),见表 6。
4 讨论
最新研究认为DPN的发生与代谢紊乱、循环障碍、神经营养因子缺乏、氧化应激和免疫等多种因素相关[4]。其中,氧化应激是周围神经病变的核心机制。
DPN的发生与进展是细胞氧化应激导致多个代谢途径受损的最终结果,其中线粒体与细胞内氧化应激和生化途径受损起关键作用[5]。
8-iso-PGF2α是近年来新发现的异前列腺素类代谢产物,由于8-iso-PGF2α在体内生成且结构稳定,不受食物脂质含量的影响,特异性强,能灵敏反映体内氧化应激水平并与疾病严重程度相关,被认为是评价机体氧化应激的理想指标[6-8]。8-iso-PGF2是自由基催化生物膜上的花生四烯酸发生脂质过氧化(非酶促反应)后的特异性产物,具有多种生物学功能[9]:1)具有选择性收缩血管的作用。2)促进血小板的黏附、聚集和变形,加速凝血。3)刺激血管内皮细胞的分化、DNA合成和内皮素-1的表达。4)引起成纤维细胞和心肌细胞的增殖和分化。5)具有较强的极性,氧化损伤后细胞膜上酯化的8-iso-PGF2α增多,可使细胞的完整性受到破坏、流动性发生改变,从而导致细胞的结构、功能受损,甚至导致细胞凋亡。6)在炎症反应早期,可通过直接作用或第二信使系统促使单核细胞黏附于微血管内皮细胞,导致内皮受损。阮园等发现[10],DPN组病人血清8-iso-PGF2α水平显著高于健康对照组,提示糖尿病病人体内有明显的氧化应激,而DPN组病人血清8-iso-PGF2α水平显著高于糖尿病组,提示氧化应激水平随病情加重升高,故提示可以通过测定体内8-iso-PGF2α的水平来监测糖尿病病人病情进展,并作为糖尿病神经病变的监测指标。Comporti等[9]研究也发现,DPN鼠尿8-iso-PGF2α水平较对照组鼠明显增加,推断尿中8-iso-PGF2α浓度可以作为DPN氧化损伤的直接标志物。综上,8-iso-PGF2α是一种反映体内氧化应激水平可靠的检测指标。
中医药在治疗糖尿病慢性并发症方面有其独特的优势。传统中医理论认为,本病属中医“痹证”、“痿证”等范畴,多因久病消渴所致。消渴为病,阴虚为本,燥热为标,阴虚日久,无以化气,致气阴两虚,气虚推动无力,血行不畅缓慢滞涩而成瘀血。同时,瘀血又可阻碍气机,使津液失于输布,致脉络瘀滞,经气不通,则出现肢体麻木、疼痛难忍。总之,本病多为本虚标实之证,以正虚为主。
本课题组在传统中医理论的基础上,根据王永炎院士“毒损脑络”的理论,结合多年的临床观察,提出“肾虚毒滞”为DPN的一个证型,认为“肾虚血瘀,毒损脉络”为糖尿病周围神经病变的基本病机[4],并对此制定了“补肾活血解毒”的干预方法,补肾与活血并重,重视解毒。代表方葛芪降糖颗粒在临床上已经取得较好的疗效,但其作用靶点、作用途径至今尚不明确。本研究表明:葛芪降糖颗粒联合甲钴胺改善DPN患者症状与体征,并且明显抑制血清8-iso-PGF2α活性,这也可能是其改善DNP症状的主要作用靶点,同时为临床治疗糖尿病周围神经病变,提供新的规范化治疗方案。
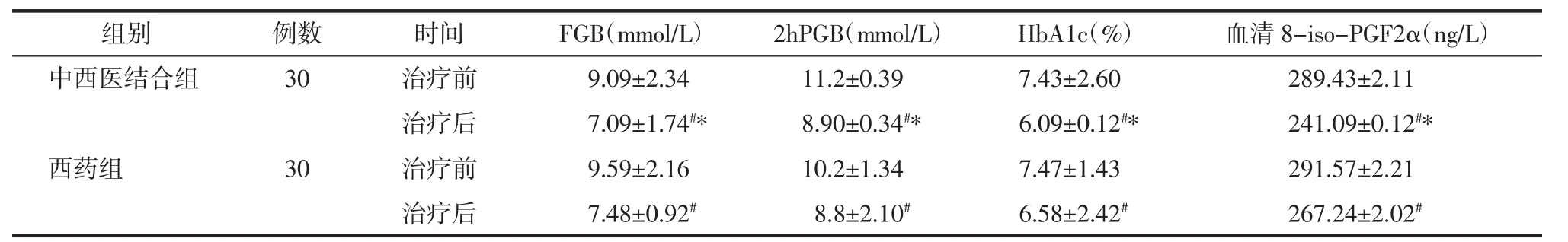
表5 两组治疗前后检测值比较(x±s)
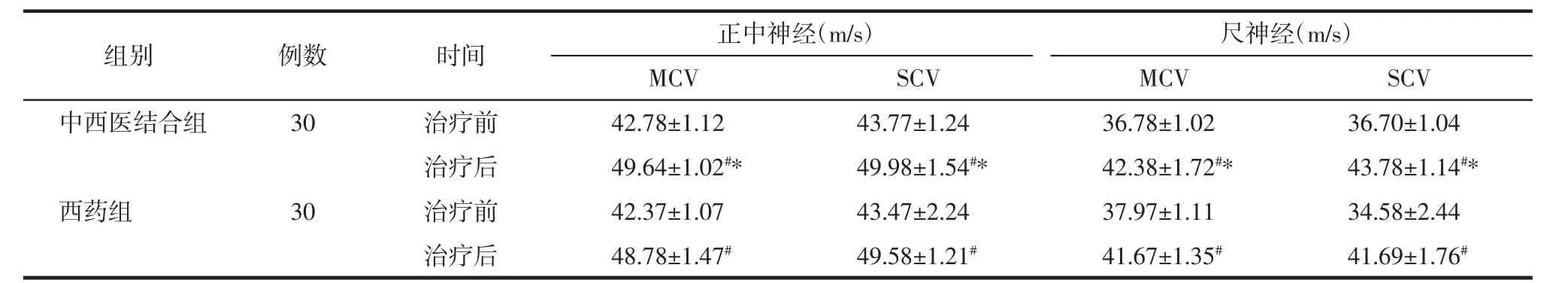
表6 两组肌电图NCV检测(x±s)

