NPSC体系下Ti/HZSM-5在线催化裂解生物油的实验研究
樊永胜, 赵卫东, 蔡忆昔, 李小华, 陈玉炜, 金丽珠
(1.盐城工学院 汽车工程学院, 江苏 盐城 224051; 2.江苏大学 汽车与交通工程学院, 江苏 镇江 212013)
生物质能作为唯一可直接转换成含碳液体燃料的可再生能源,在化石燃料日益枯竭和环境日趋恶化的今天对其开发利用变得越来越重要。生物质热解液化因可高效转化生物质能,并获得具有较高附加值的化工原料和可替代燃料而受到广泛关注[1]。但生物油作为一种初级燃料,在理化性质方面存在明显缺陷,包括高含氧量、强腐蚀性、高运动黏度、低热值和低稳定性等[2]。因此,对生物油进行提质改性是实现其替代石油燃料的关键,在热解液化过程中引入催化手段是当前生物油提质研究的热点[3-4]。但是针对化学组分极为复杂的生物油,单纯依靠催化剂虽能在一定程度上提升生物油的品位,但很难实现质的跨越,且催化剂稳定性较差,易结焦失活[5-6]。Fan等[7]在前期进行的HZSM-5在线催化提质油菜秸秆热解气制备生物油的研究,得到了相似结论。为进一步提高HZSM-5的催化选择性和稳定性,课题组对HZSM-5进行了P、Zn、Ti元素的负载改性研究,发现P、Zn/HZSM-5的芳构化性能较好,生物油中PAHs含量较高;而Ti/HZSM-5具有较强的催化裂解性能,生物油中单环芳香烃(Monocyclic aromatic hydrocarbons, MAHs)和脂肪烃(Aliphatic hydrocarbons, AHCs)含量相对较高,且Ti/HZSM-5对无定型和石墨型两类焦炭的抵抗性能均有明显提升[8]。尽管如此,Ti/HZSM-5催化所得精制生物油中PAHs占比仍达到38.33%,结焦率较HZSM-5降幅为32.59%。因此,传统的催化手段已经难以实质性提高生物油催化裂解过程的提质效率。
“等离子体”一词最早由朗缪尔(Langmuir)于1927年提出[9],是指对气体放电产生的电子、离子、自由基、激发态粒子等高活性物种构成的区域,整体呈现电中性,也被称为物质第四态,宇宙中99%的物质都呈等离子体态[10]。根据热力学平衡状态的不同,可将等离子体分为平衡态等离子体与非平衡态等离子体。平衡态等离子体体系内的电子温度和离子温度几乎相等,在宏观上处于热力学平衡状态,因其体系温度高达上万度,故将平衡态等离子体称为高温等离子体。非平衡态等离子体的电子温度远高于离子温度,可达104K以上,而离子和中性粒子的温度仅有300~500 K,整个体系的宏观温度低,故又将非平衡态等离子体称为低温等离子体[10]。低温等离子体技术主要是利用化学活性极强的高能粒子及活性物种参与化学反应,解决许多传统条件下难以解决的问题[11]。针对HZSM-5在生物油催化裂解过程中的结焦失活现象,笔者在前期研究中率先将低温等离子体技术引入到结焦HZSM-5的再生研究中,在约250℃条件下实现了HZSM-5的快速再生,有效避免了长时间焙烧(500~600℃)再生所带来的结构塌陷问题,催化剂活性恢复至较高水平[12]。相关研究发现,经过低温等离子体处理过的催化剂,活性会显著提升;同时,在低温等离子体反应系统中加入适量的催化剂,高能活性物质与催化剂之间会产生明显的协同效应,可以降低等离子体击穿电压,减少能量损耗,提高反应活性[13-14]。就高能活性物质的能量而言,一般远高于常见化学键的键能。因此,常规化学反应所需温度条件在低温等离子体系统下均会明显降低,因为高能活性物质所提供的能量在较低温度条件下即可达到反应所需最小活化能。
因此,课题组首次尝试将低温等离子技术与生物油的催化裂解过程相结合,通过等离子体放电直接向反应物的化学键输入能量,激发反应物分子,而催化剂的活性中心将对反应方向起到诱导和组织作用,以期分别发挥低温等离子体高效活化的优势和催化剂高选择性的特点。
在本研究中,将基于介质阻挡放电(Dielectric barrier discharge, DBD)原理,在Ti/HZSM-5催化裂解的基础上,建立NPSC体系,考察低温等离子体与Ti/HZSM-5的协同提质性能,包括对生物油的催化转化性能以及对催化剂稳定性的影响,为实现高效提质生物油奠定理论基础和实验依据。
1 实验部分
1.1 生物质原料
以油菜秸秆为原料,将在自然条件下风干的油菜秸秆粉碎成粒径为0.25~0.42 mm的细小颗粒试样,并在恒温干燥箱中于105℃干燥24 h后保存备用。油菜秸秆的工业组成、元素组成及高位热值(High heating value, HHV)测定结果如表1所示。
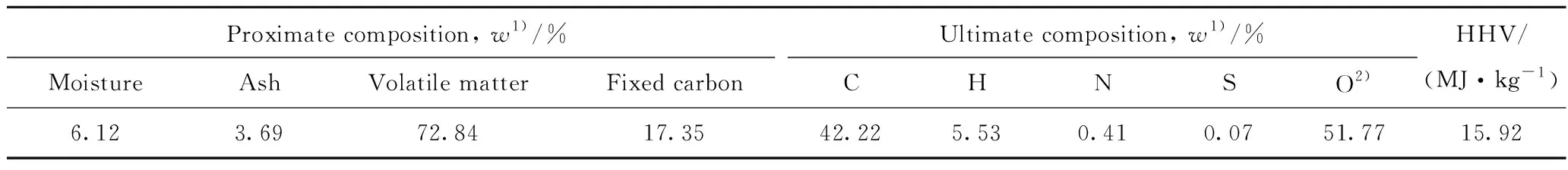
表1 油菜秸秆的工业组成、元素组成及高位热值Table 1 Proximate composition, ultimate composition and HHV of rape straw
1) Dry base in the air; 2) By difference
1.2 改性HZSM-5制备及表征
1.2.1 催化剂制备
将硅/铝比(n(Si)/n(Al))为50的HZSM-5原粉在550℃煅烧2 h后,将其分别浸渍到一定量的TiCl3溶液中,使用集热式磁石搅拌器于80℃恒温搅拌4 h,然后经充分过滤和洗涤后,移入干燥箱中于105℃干燥4 h以除去水分,最后将干燥后的催化剂置于马福炉中以550℃高温焙烧4 h,得到Ti/HZSM-5,金属负载量控制在3%左右。
1.2.2 催化剂表征
采用JSM-7001F型场发射扫描电子显微镜(Scanning electron microscope, SEM)配合X射线微区能谱分析仪(Energy dispersive spectrometer, EDS)检测改性HZSM-5微区表面负载元素分布,分辨率为1.2 nm(30 kV)。
采用D8 Advance型多晶X射线衍射(X-ray diffraction, XRD)仪对分子筛进行物相测定,以CuKα(λ=0.15406 nm)为辐射源,管电压为40 kV、管电流为30 mA,扫描速率为5°/min,扫描范围为2θ为5°~80°。
采用Builder SSA4300型比表面积分析仪对分子筛的比表面积和孔容进行测定。称取约0.15 g试样至样品管内,在MD-200型预处理器上升温至280℃,真空处理2 h,冷却至室温后移至分析仪上进行液氮吸附和脱附实验。由Brunner-Emmet-Teller (BET)模型求得比表面积,并由Barrett-Joyner-Halenda (BJH)模型计算孔容大小。
采用FT-IR Frontier型红外光谱仪配合真空吸附脱附系统测定分子筛的Brönsted酸(B酸)和Lewis酸(L酸)分布。将一定量的样品压成半透明自支撑圆片,并将样品片放入石英吸收池中,与真空系统相连。程序升温至350℃,同时抽真空(10-2Pa)处理样品1 h,降至室温,摄谱得样品骨架谱图;然后,在室温下吸附饱和吡啶蒸气0.5 h,摄谱得样品吸附吡啶谱图;最后,程序升温至200℃,脱附0.5 h,降至室温,摄谱得样品脱附吡啶红外谱图。同时,根据经验公式半定量计算B和L酸的酸量:
c(pyridine on B sites)=1.88IA(B)R2/W
(1)
c(pyridine on L sites)=1.42IA(L)R2/W
(2)
式(1)和(2)中,c为每1 g样品酸量,mmol/g;IA(B/L)为B酸或L酸吸收峰积分面积,cm-1;R为样品圆片的半径,cm;W为样品圆片的质量,mg。
1.3 实验系统和方法
1.3.1 NPSC反应器及系统设计
在低温等离子体领域中,DBD以工作稳定性强、功率密度大等优点被广泛应用[15-16]。如果将催化剂布置在等离子体放电区,放电区与催化层重叠,低温等离子体放电方式由气相放电转变为在催化剂上的表面放电和气相放电两种方式,低温等离子体与催化剂之间通过表面放电而产生相互作用,有助于提高低温等离子体与催化剂的协同作用效果。因此,在本研究中基于DBD原理,提出并设计了在真空条件下工作的NPSC反应器,其结构如图1所示。反应器采用同轴双介质结构,中心电极为不锈钢双头螺栓中空管,外径为8 mm,内孔用于测量反应区温度。外电极为150目的铜网,紧贴于外阻挡介质表面。反应器的放电间隙为14.5 mm。阻挡介质采用厚度3 mm,轴向长度80 mm的透明石英玻璃管。介质管两端为端盖,采用聚四氟乙烯加工,密封处设有氟胶垫片,依靠中心电极两端的螺母预紧力实现密封。
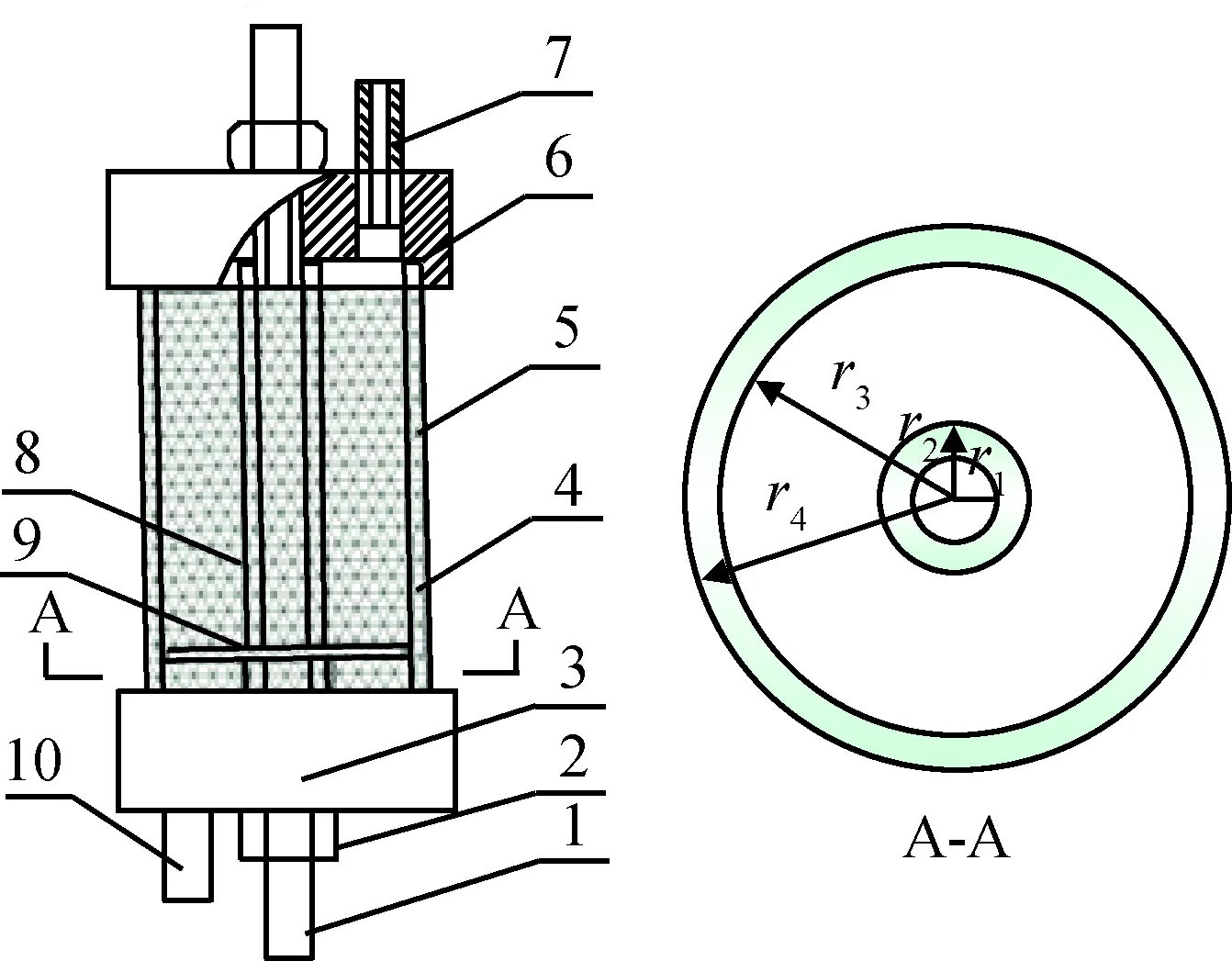
图1 NTSC反应器结构示意图Fig.1 Schematic diagram of the NTSC reactor 1—High-voltage electrode; 2—Tight nut; 3—End cap; 4—Low-voltage electrode; 5—Outside barrier medium; 6—Fluorine rubber gasket; 7—Gas outlet; 8—Inner barrier medium; 9—Catalyst support platform; 10—Gas inlet
以NPSC反应器为核心的NPSC系统如图2所示。通过控制阀及水循环式真空泵实现对反应器内部真空度的控制。系统的放电功率采用电压-电荷Lissajous图形法测量,测量回路是由C1、C2组成的容性分压电路、取样电容Cm和数字示波器构成[17]。催化反应区温度由置于反应器中心盲管内的热电偶及电子测温仪测量并显示。

图2 NPSC系统组成示意图Fig.2 Schematic diagram of the NPSC system
系统对通入的气体进行放电产生的活性物质是影响催化效果的主要因素之一,而放电功率决定了反应器单位时间内放电产生活性物质的数量[18];在电学上,反应器等效于气隙等效电容和介质等效电容的串联,而负载特性是反应器和NTP电源匹配的重要参数。反应器的单位长度介质等效电容Cd、单位长度气隙等效电容Cg和放电功率P的计算公式分别如式(3)、式(4)和式(5)所示:
(3)
式(3)中ε0、εd为真空介电常数和介质相对介电常数,r1、r2为内阻挡介质的内、外表面半径,r3、r4为外阻挡介质的内、外表面半径。
(4)
式(4)中εg为气隙相对介电常数。
(5)
式(3)中f为电源工作频率,Us和U分别为起始放电电压和工作电压。
在前期研究中,课题组考察了放电区温度、体系压力、催化床层高度和粒径等参数对NPSC反应器工作性能的影响规律,发现放电区温度的提升、体系压力的降低以及催化床层高度的增加均有利于NTP辅助催化裂解反应器放电功率的提升,约4 mm 粒径的催化剂颗粒有利于减小催化剂床层的间隙率,可以增加反应器的放电功率[19]。因此,结合前期生物油在线催化提质的研究成果[7],在本研究中,选取催化温度为400℃,体系压力为5 kPa,催化床层高度为30 mm,催化剂粒径为4 mm,电源工作频率f为9 kHz,工作电压U为16 kV,对生物油进行在线催化提质实验。
1.3.2 生物油裂解系统及方法
所采用的基于NPSC的生物油在线催化提质实验系统如图3所示。除NPSC系统外,该实验系统还包括生物质热解反应器、连接管路、过滤装置、冷凝收集系统、真空泵、集气袋、氮气瓶以及温控装置等。热解反应器与NPSC反应器仍呈两段式布置,热解反应器位于下段,NPSC反应器位于上段。两反应器连接处采用石棉垫片以保证气密性,并起到隔热的作用。生物质热解温度与催化反应温度均采用反馈控制,分别以两反应器中心盲管内的测温为反馈信号,实时控制加热电流的通断,对两反应器进行加热,但由于存在热滞后效应,温度在反应器径向分布上存在一定的梯度,中心盲管内的测温与控温存在约±3℃的误差。实验时,体系内部在真空泵的作用下处于负压状态,通过调压阀6调节体系压力,并利用压力表实时监测体系内部压力。

图3基于NPSC的生物油在线催化提质实验系统Fig.3 Experimental system of bio-oil in-situ catalytic upgrading based on NPSC 1—Power supply; 2—Heating sleeves; 3—NPSC reactor; 4—Cooling tower; 5—Pressure stabilizing tube; 6—Pressure regulating valve; 7—Vacuum pump; 8—Nitrogen cylinder; 9—Bio-oil collector; 10—Temperature controller; 11—Pyrolysis reactor; 12—Oscilloscope
前期研究表明,当热解终温为495.5℃,升温速率为19.4℃/min,体系压力为5.0 kPa时,油菜秸秆真空热解生成较多的可冷凝有机蒸气[20]。因此,在本研究中亦采用相同的生物质热解工艺条件。当NPSC反应器达到设定的反应温度,加载电源进行高压高频放电;同时,开始进行生物质热解,一定量的生物质原料裂解形成热解气,热解气经NPSC反应器放电活化,并经分子筛催化后被迅速抽出,经充分冷却(冷却温度为-20℃)后冷凝得到液相产物。实验完毕,停止放电,并关闭真空泵和调压阀,打开氮气瓶截止阀通入一段时间的氮气,确保产物、催化剂等不与空气接触反应而导致产物收率和品质以及催化剂性质的改变。待实验系统温度冷却至室温后,停止通入氮气,移除收集试管进行称量。液相产物会出现明显的分层现象,上层为油相产物,下层为水相产物。利用二氯甲烷(CH2Cl2)试剂萃取分离油相产物及水相产物中的大部分有机物;同时利用CH2Cl2对冷却收集装置包括收集试管及部分管路进行清洗,清洗液加入到CH2Cl2萃取相中,并将萃取相于40℃水浴下蒸发去除CH2Cl2,即得三效提质生物油(定义经HZSM-5催化所得生物油为单效提质生物油,Single Effect upgrading bio-oil, SEUB;经Ti/HZSM-5催化所得生物油为双效提质生物油,Double effect upgrading bio-oil, DEUB;NPSC体系下Ti/HZSM-5催化所得生物油为三效提质生物油,Triple effect upgrading bio-oil, TEUB)。以生物质原料质量为基准,计算液相产物产率以及生物油产率。同时,称量热解反应器中热解残炭的质量,计算固相产率;并根据质量平衡原理,计算气相产物产率。
1.4 三效催化提质性能分析
1.4.1 生物油分析
采用EA3000型元素分析仪测定精制生物油的元素组成;采用比重管法测定生物油的密度(参照GB/T 2540—1981);采用PHS-3型数字pH计测定生物油的酸性(参照GB/T 11165—2005);采用毛细管黏度计法测定生物油的运动黏度(参照GB/T 265—1988);采用ZDHW-5G型氧弹式量热仪测定生物油的高位热值(参照GB/T 213—2003)。
采用Agilent 7890A/5975型气质联用(Gas chromatograph/Mass spectroscopy, GC/MS)分析仪测定生物油有机物组成。GC条件:色谱柱为HP-5毛细管柱,载气为He,流量为1 mL/min,进样口温度为250℃,分流比10∶1,进样量1 μL;MS条件:离子源温度为230℃,MS传输线温度为250℃,电离方式为EI,电子轰击能量为70 eV,扫描质量范围为30~500 m/z,扫描时间为1 s;升温程序:40℃保持2 min,以15℃/min的升温速率升至100℃,然后以8℃/min升温速率升至280℃并保持3 min,设置溶剂延迟时间为3 min。
1.4.2 催化剂结焦分析
采用TGA/DSC 1型同步热分析仪对在NPSC体系下使用一段时间的Ti/HZSM-5进行热重分析(Thermo-gravimetric analysis, TGA),以考察高压放电作用对催化剂结焦率的影响。试样质量为10mg,以空气为载气,流量为50 mL/min,以10℃/min的升温速率将试样从40℃加热到800℃,对实验过程进行热重(Thermo-gravimetric, TG)和热重微分(Differential thermo-gravimetric, DTG)测量。
2 结果与分析
2.1 改性分子筛表征分析
利用SEM EDS检测Ti/HZSM-5表面微区,其SEM扫描照片及表面元素能谱如图4所示。由图4(a)可见,Ti改性后分子筛表面点缀有白色絮状物,分散较为均匀;由图4(b)可见,在Ti改性的HZSM-5上分别检测到了Ti元素的特征X射线(Ti:Kα=4.513 keV,Kβ=4.931 keV,Lα=0.534 keV),表明金属元素的负载改性效果较为理想。
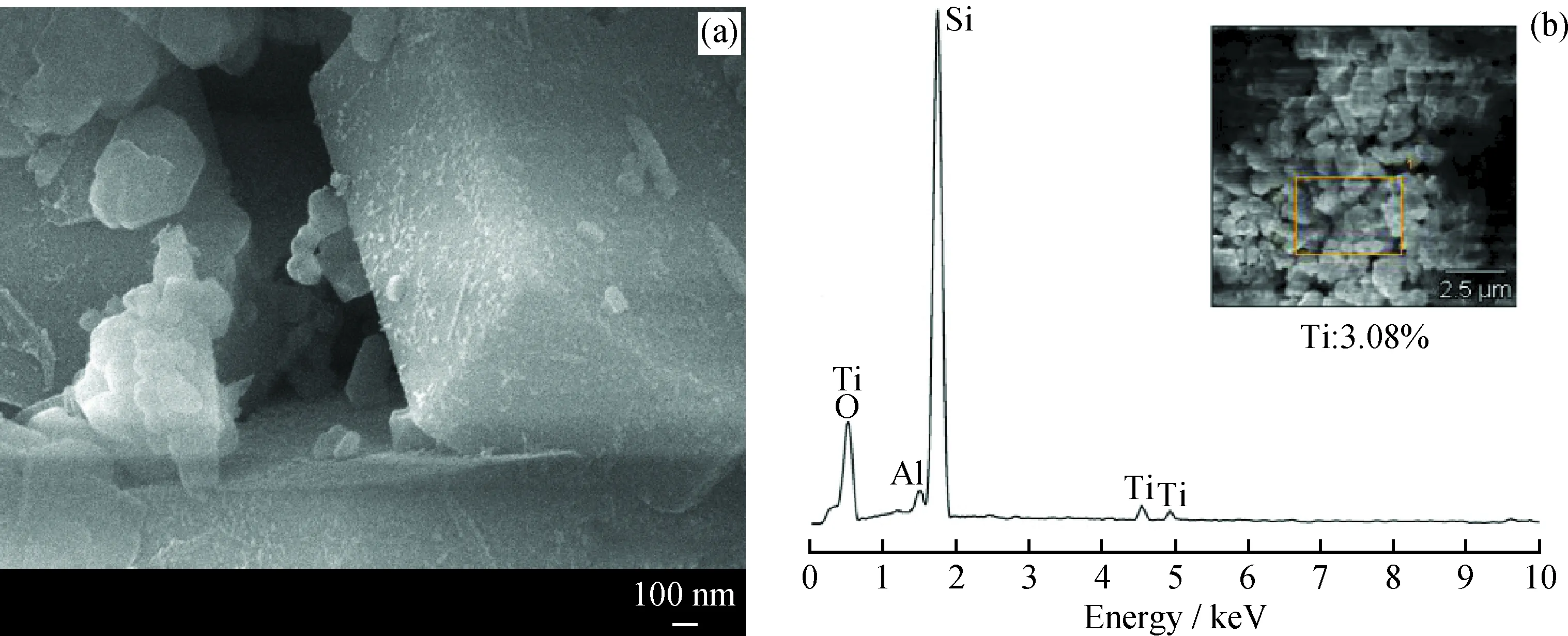
图4 Ti/HZSM-5的SEM扫描照片及EDS能谱图Fig.4 SEM photo and EDS pattern of the Ti/HZSM-5(a) SEM photo; (b) EDS pattern
HZSM-5及Ti/HZSM-5的XRD衍射图谱如图5 所示。由图5可见,Ti/HZSM-5的XRD图谱上除了HZSM-5典型MFI特征峰(2θ=7.96°、8.83°、23.18°、23.99°、24.45°(JCPDS card: PDF 44-0003))之外并未出现其他结晶体的特征衍射峰,表明Ti改性成分负载较为均匀,未出现“团聚”现象,与SEM的扫描分析结果较为一致。同时,由于Ti改性成分的部分遮挡,Ti/HZSM-5特征峰的衍射峰强度均有所降低。

图5 HZSM-5及Ti/HZSM-5的XRD图谱Fig.5 XRD patterns of the HZSM-5 and Ti/HZSM-5
HZSM-5及Ti/HZSM-5表面物理特性参数如表2所示。由表2可知,经过Ti元素改性后,改性成分分散附着于分子筛表面及孔道中,对表面和孔道起到了一定的修饰作用,使Ti改性HZSM-5的表面积和孔容均有所降低。

表2 HZSM-5及Ti/HZSM-5表面物理特性Table 2 Physical properties of the HZSM-5 and Ti/HZSM-5
HZSM-5及Ti/HZSM-5的吡啶红外谱图如图6所示,波数在1450 cm-1附近的吸收峰表示Lewis酸中心,1545 cm-1附近的吸收峰表示Brönsted酸中心,1490 cm-1附近的吸收峰代表B+L酸[21]。对Brönsted酸和Lewis酸的半定量分析结果如表3所示。由表3可见,Ti改性使HZSM-5上Brönsted酸量增加,Lewis酸量减少,B+L酸量亦有所减少。

图6 HZSM-5及Ti/HZSM-5的吡啶红外谱图Fig.6 Py-IR desorption spectra of the HZSM-5 and Ti/HZSM-5

SampleAcid amount/(μmol·g-1)BLL/BHZSM-5141.833.60.24Ti/HZSM-5154.124.00.16
2.2 生物油提质分析
2.2.1 产物产率
生物油在不同条件下发生裂解反应后各相产物的产率(质量分数)如表4所示。由表4可知,不同条件裂解后固体残余量变化较小,表明每次原料的裂解反应具有较高的一致性;随着Ti元素和低温等离子体技术的引入,气相产物产率进一步增大,液相及生物油产率继续降低;当采用NPSC体系时,生物油产率降幅较大,表明NPSC体系配合Ti元素,使整个催化过程的裂解性能显著提升,液相产物中生物油的占比显著降低,即水分含量显著升高;同时,气相产物产率明显升高,达到55.41%。表明随着NPSC体系的采用,Ti/HZSM-5催化过程的裂解脱氧性能显著提升,更多的有机物参与催化裂解反应,生成更多的H2O和CO或CO2。当然,气相产物产率的升高并不完全由增加的CO或CO2所贡献,亦包括来自小分子烃类(可能包括CH4、C2H4、C2H6、C3H6、C3H8等)和H2等气体分子的贡献,但其贡献量应当较小[5,22]。
2.2.2 生物油理化特性
生物油催化前后的理化特性如表5所示,HZSM-5和Ti/HZSM-5催化所得SEUB和DEUB的理化性质[8]以及汽油的理化性质同样列于表5中作为对比参照。由表5可知,三效催化后,随着氧元素的进一步脱除,生物油各项理化性质得到进一步提升或改善,TEUB中含氧量降至9.82%,使各项燃料性质显著提升,密度、pH值、运动黏度和高位热值分别达到0.88 g/cm3、5.50、4.60 mm2/s和37.02 MJ/kg,但与汽油的各项理化性质相比仍存在明显差距。由于生物质本身属于缺氢原料(有效氢/碳比(Hydrogen to carbon effective ratio, (nH/nC)eff<0.3)[23],经过热解和催化后,脱除了大量的氧元素,但生物油中的氢元素含量(质量分数)仍在较低水平(大约8%~9%),精制生物油的(nH/nC)eff仍在1左右,由于催化过程中缺乏可有效转移利用的氢元素,因此(nH/nC)eff很难得到进一步提升。而汽油的氢元素含量几乎是精制生物油的2倍,(nH/nC)eff高达2.25,这一差别使汽油的密度、运动黏度远低于生物油,热值更是高达45~48 MJ/kg。因此,从燃料的理化特性角度分析,想要实质性的提高生物油的理化性质,需提高生物油的(nH/nC)eff。

表4 催化对产物产率的影响Table 4 Effects of catalysis on the product yields
2.2.3 生物油化学组成
采用GC-MS对三效催化后所得精制生物油中的有机化合物组成进行定性和定量分析。三效催化提质后,精制生物油中烃类物质含量及其碳原子数分布情况如表6所示。同时,生物油原油、SEUB中油相产物(Oil phase)及Ti/HZSM-5催化所得DEUB的组成[8]作为对比参照。烃类化合物主要分为单环芳香烃、多环芳香烃和脂肪烃。HZSM-5本身所具有的酸性分布及特殊孔道结构使其具有良好的芳构化能力,生物油经HZSM-5单效催化后,SEUB中芳香烃含量升高,但催化选择性有限[7]。因此,在生物油在线提质过程中进一步引入了P、Zn、Ti改性HZSM-5的双效催化,其中Ti改性后使HZSM-5的催化裂解性能加强,因而Ti/HZSM-5的双效催化反应使DEUB中MAHs和AHCs含量明显升高[8]。

表5 生物油催化前后的理化特性Table 5 The physiochemical properties of the bio-oil before and after catalysis
1) By difference; 2) Not determined

表6 生物油催化前后烃类含量及其碳原子分布Table 6 The hydrocarbon contents and carbon atom distribution in the bio-oil before and after catalysis
由表6可见,与Ti/HZSM-5的双效催化相比,NPSC体系引入后的三效催化使生物油中烃类化合物总含量明显增加。由于存在高能放电作用,生物油中的有机物被活化裂解,部分PAHs直接被破环裂解生成一部分MAHs和小分子碳正离子碎片,然后在催化剂的诱导下,小分子碳正离子会继续发生芳构化反应生成MAHs。相关研究表明,对改性HZSM-5进行放电处理时,会进一步提高催化剂表面的Brönsted和Lewis酸量,这既有利于提高催化剂本身的裂解能力,又有利于增强芳构化过程中的氢转移反应。增加Ti元素进行联合改性,有利于增强分子筛Brönsted酸量,提高裂解性能,因为钛金属阳离子价态较高、半径较小,静电场较强,易极化结晶或吸附的水分子电离产生H+,形成Brönsted酸中心[24]。生物油在高能放电和Ti/HZSM-5 的双重活化裂解作用下,大部分被裂解活化生成较小的碳正离子碎片或带电活性粒子,部分裂解中间产物又在HZSM-5本身诱导下,发生重组芳构化反应。因此,所得TEUB尽管产率较低,但其碳氢化合物总质量分数达到89.49%,其中MAHs为主要成分(59.04%),PAHs质量分数下降至8.98%,AHCs质量分数升高至21.47%。在高压放电作用下,生物油在线活化产生了很多高能活性物种,包括电子、离子、激发态粒子、光子等,可以促进改进元素的价态变化过程,有利于加强碳正离子反应,使生物油中AHCs和PAHs含量升高。同时,Li等[25]发现,ZSM-5分子筛上的改性元素在催化裂解过程中会发生价态变化,Ti4+会还原为Ti3+,该还原过程中电子的迁移有利于促进碳正离子反应的进行。总体而言,在整个催化提质过程中,三效的协同作用较好,即总的裂解反应与芳构化反应达到一个相对理想的平衡状态。裂解作用主要来自三个方面的贡献,包括高压放电作用,分子筛本身的裂解能力以及Ti改性物种的作用,而三种作用因素之间又存在复杂的交互作用,在总的提质效果上表现出相对良好的烃类选择性。
与HZSM-5催化所得油相产物相比,DEUB中C10~C13的烃类占主要部分,虽然PAHs和AHCs均有所增加,但碳数分布相对均一,较大的PAHs和较小的AHCs均减少,生物油中烃类组成得到一定程度的改善;而与DEUB相比,三效催化提质过程的裂解性能较Ti/HZSM-5双效催化提质时显著增强,对生物质热解气的裂解脱氧效果较好,烃类物质总含量达到较高值,烃类化合物的碳数分布显著降低,超过80%的烃类物质碳数位于C6~C9范围内,而一般汽油中烃类物质的碳原子数为6~11。因此,从碳原子数角度,TEUB的烃类组成已达到汽油中烃类组成的要求,但从化学组成来讲,两者则完全不同,汽油主要由脂肪烃和环烷烃等组成,而TEUB主要由MAHs组成,其有效氢/碳比较低,远不及汽油的有效氢/碳比,因而在理化特性方面,两者仍存在较大的差异。
生物油催化前后含氧有机物含量及其氧原子分布情况如表7所示。生物油中含氧有机化合物主要包括酸类、醛类、酮类、酚类、醇类、呋喃类等,其中,酸、醛、酮类化合物因含有羰基(C=O)而具有较强的反应活性,是生物油不稳定性的根源[26]。而酚、醇和呋喃类中含有的氧元素不利于生物油整体燃料特性的提高,所以应最大限度地降低各类含氧有机物的含量。

表7 生物油催化前后含氧有机物含量及其氧原子分布Table 7 The oxygenate contents and oxygen atom distribution in the bio-oil before and after catalysis
由表7可知,与HZSM-5催化所得油相产物相比,Ti/HZSM-5催化所得DEUB中,含氧有机物总含量明显降低,但含氧有机物种类有所增多(如醛类和呋喃类),一方面可能来自于水相部分,另一方面也表明催化裂解反应不完全,部分含氧有机物发生部分裂解或重组生成副产物;含氧有机物中酚类化合物中以酚羟基形式存在的氧元素较难去除,一方面得益于苯环结构的高稳定性对其提供的保护,另一方面缺乏高裂解性能催化剂更加完全的接触诱导。而采用三效催化提质后,在高压放电的协同作用下,Ti/HZSM-5的裂解能力有明显提高,各类含氧有机物含量均下降,含氧化合物总质量分数降至10.51%,特别是酚类化合物大幅减少,羰基团亦明显减少;较难分解的含氧杂环类有机物在高电压作用下被破环裂解,在催化剂和放电的双重裂解作用下,氧元素被大部分脱除,整个提质反应过程的裂解重整效果达到较优状态,残留的含氧化合物包括少量未完全参与反应的酮类、酚类和五氧杂环(呋喃类)有机物。
NPSC技术的引入,增强了反应过程的活化裂解性能,所得TEUB中未检测到3O及其以上氧原子数的有机物;DEUB中1O化合物含量较生物原油和油相产物均明显升高,因为Ti/HZSM-5的裂解脱氧效能较为有限,将2O及其以上含氧化合物进行了部分裂解,生成了部分1O化合物,并且无法再进行进一步的裂解脱氧,使1O化合物含量有所升高,并且,其中酚类化合物仍占主要部分;同时,在Ti/HZSM-5催化过程中,发生了少量副反应,形成少量醛类和呋喃类等含氧有机物,使3O和4O化合物稍有增加。当在Ti/HZSM-5催化提质过程中采用低温等离子体技术进行协同催化时,三效催化反应的裂解脱氧效能达到较高水平,未检测到3O和4O化合物,2O化合物含量明显降低,而1O化合物出现大幅减少。
2.3 催化剂结焦分析
在三效催化中使用后的Ti/HZSM-5热重曲线如图7所示,其催化使用时间与单效和二效催化时相同,以形成对照。由图7可见,随着Ti元素的引入和NPSC技术的采用,催化剂总失重量逐渐降低;HZSM-5及Ti/HZSM-5均存在2个失重峰,在最大失重峰的高温侧存在1个较明显的肩峰,但随着NPSC技术的采用,最大失重峰明显向高温侧偏移,肩峰消失,表明在NPSC体系下,Ti/HZSM-5 上的结焦情况(包括焦炭类型、组成结构等)产生了明显变化。相关研究表明,在HZSM-5催化裂解生物油的过程中,既可能形成结构较疏松的无定型含氧焦炭,又可能形成致密片状结构的石墨型焦炭,无定型含氧焦炭易去除,而石墨型焦炭反之[27]。因此,单效及二效催化中HZSM-5和Ti/HZSM-5 的主失重峰可能由无定型含氧焦炭的氧化分解引起,而肩峰则主要是由少量致密型焦炭的分解造成的。相比较而言,NPSC体系下,在Ti/HZSM-5上结焦的焦炭类型的区分度相对模糊,主失重峰峰值温度向高温方向偏移,主失重峰与肩峰合并,表明不同类型的焦炭具有“同构化”倾向,无定型含氧焦炭可能逐渐转变为较致密性焦炭;同时,失重峰值的绝对值明显降低,热分解反应的剧烈程度有所缓和。
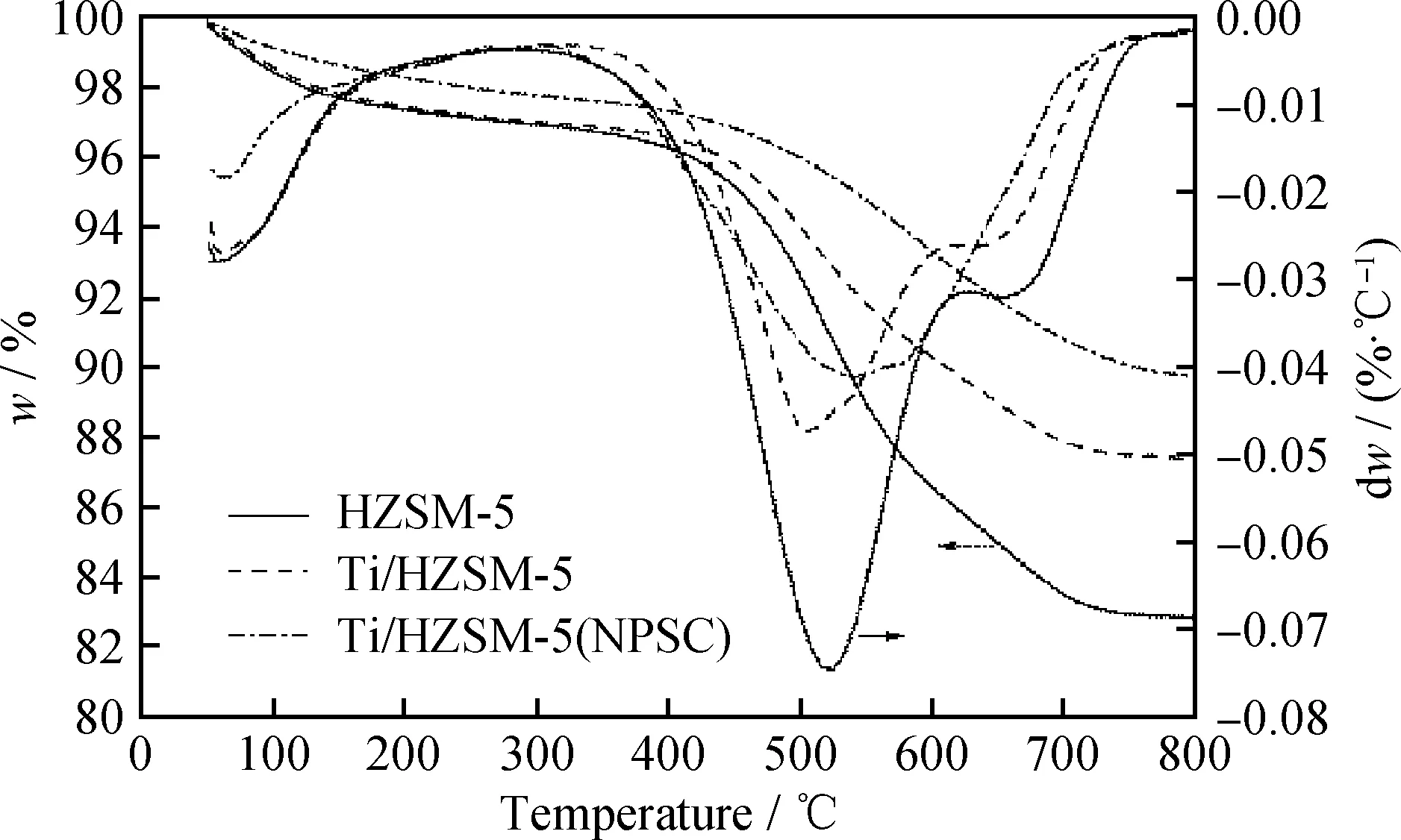
图7 HZSM-5及Ti/HZSM-5的TG-DTG曲线Fig.7 TG- DTG curves of the HZSM-5 and Ti/HZSM-5
为深入分析催化剂结焦的差异性,采用Guassian法对DTG曲线的主失重区间进行拟合积分计算,对单效及二效催化中HZSM-5和Ti/HZSM-5 的主失重区间进行分峰拟合(LTP和HTP分别对应低温失重峰(Low temperature peak)和高温失重峰(High temperature peak)),以区分两类焦炭,对三效催化中Ti/HZSM-5的主失重区间进行单峰拟合,计算结果如表8所示。由表8可见,引入低温等离子体技术与Ti/HZSM-5进行协同催化后,催化裂解性能被进一步加强,生物油产率降低,更多的有机物参与催化反应,有机物裂解脱氢倾向加剧,降低了催化过程中反应物的有效氢/碳比,一定程度上促进了焦炭的生成,使焦炭质量分数(9.75%)较二效催化时有所升高;同时,较强的裂解性能亦使Ⅰ类含氧型焦炭更加趋向脱除氧元素以形成较致密的焦炭,因而,对应的焦炭去除难度逐渐升高,DTG曲线的主失重峰向高温方向偏移,与肩峰相融合,Ⅰ类和Ⅱ类焦炭出现“同构化”趋势。与双效催化时相比,当引入高能放电后,结焦率仍呈明显升高趋势。表明单纯依靠增强催化裂解性能,并不能有效提高催化剂稳定性、降低结焦率,仍应从原料角度考虑,尝试提高原料的有效氢/碳比,提高催化过程中可有效转移利用的氢元素,以实现催化剂更加稳定高效的工作。
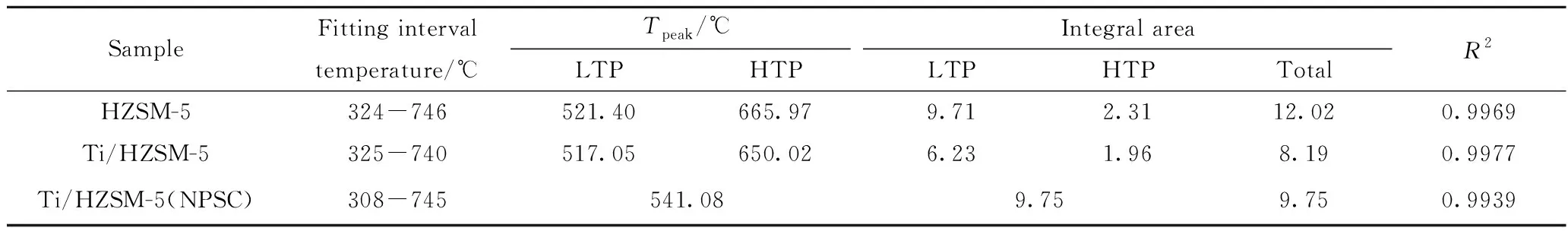
表8 HZSM-5及Ti/HZSM-5的主失重区间的分峰拟合Table 8 Coke contents on the HZSM-5 and Ti/HZSM-5
LTP—Low temperature peak; HTP—High temperature peak
3 结 论
设计并建立了NPSC体系,在该体系中利用Ti/HZSM-5进行了在线催化裂解生物油的实验研究,分析并探讨了三效催化对生物油产率、理化性能以及化学组成的影响规律和作用机理,表征了NPSC体系下Ti/HZSM-5的催化稳定性,所得结论如下:
(1)三效催化使气相产物产率升高,液相及生物油产率降低,但生物油的理化特性得到提升,TEUB的燃料品质相对较高,其密度、pH值、运动黏度和高位热值分别达到0.88 g/cm3、5.50、4.60 mm2/s和37.02 MJ/kg。但原料较低的(nH/nC)eff限制了生物油燃料品位的有效提升。
(2)三效催化使生物油中烃类含量和组成均明显提高和改善,TEUB中烃类总质量分数达到89.49%,并以MAHs和AHCs为主。在三效催化反应中具有多重交互作用,包括高能放电与分子筛、高能放电与Ti改性物种以及分子筛与Ti改性物种之间的相互作用,使裂解性能显著提升,并就整个催化过程而言,裂解反应与芳构化反应达到相对较好的平衡状态。
(3)NPSC体系的引入,并不能有效增强Ti/HZSM-5 的稳定性。生物油的催化裂解过程主要受到催化手段和原料性质两方面的影响,应尝试提高原料的有效氢/碳比,提高催化过程中可有效转移利用的氢,以有效增强NPSC体系中催化剂的抗结焦性能,实现催化剂更加稳定高效的裂解生物油。

