药物涂层球囊与药物涂层支架治疗老年支架内再狭窄的有效性和安全性
随着我国介入心脏病学的发展,经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)已经成为冠心病治疗的主要手段,近10年来行PCI人数的年均增长率高达20%~30%[1]。随着介入器材和介入技术迅猛发展,PCI治疗的方式不断丰富,包括传统单纯球囊扩张、切割球囊成形术、药物球囊扩张、金属裸支架等。随着治疗例数的增加,PCI的治疗中也遇到了新的挑战,如单纯经皮冠状动脉腔内成形术(PTCA)再狭窄率高达30%~60%,裸金属支架(BMS)置入术后再狭窄率可达30%,药物洗脱支架(DES)置入术后再狭窄率达5%~10%[2]。如何有效治疗支架内再狭窄(in-stent restenosis, ISR)成为新的挑战。目前药物涂层球囊与药物涂层支架在治疗ISR中均有研究报道。但是随着我国人口的老年化,老年ISR患病率也随之增加,同时老年病人由于基础疾病多、血管条件差等因素,为ISR的治疗带来了巨大的挑战。为此本中心开展了关于药物涂层球囊与药物涂层支架治疗老年ISR病人的有效性和安全性研究,现报道如下。
1 资料和方法
1.1 研究对象 2015年1月至2016年12月就诊于新疆医科大学第一附属医院心脏中心冠心病二科的病人。纳入标准:(1)年龄>60岁;(2)DES置入术后再狭窄,Mehran 分型Ⅰ~Ⅳ;(3)参考血管直径为2.5~4.0 mm,病变长度≤30 mm;(4)直径狭窄程度≥70% 或≥50% 并有心肌缺血证据。排除标准:(1)1周内急性心肌梗死;(2)分叉病变边支≥2.5 mm;(3)靶血管弥漫性血栓;(4)严重慢性心功能衰竭或NYHA Ⅳ级;(5)严重心脏瓣膜病变;(6)介入术前6个月内发生脑卒中。
1.2 病例分组 研究采用随机对照临床试验(randomized controlled trial,RCT)方法,应用SAS 6.12的PROC PLAN过程完成程序编写和随机化操作,病例按进入临床的先后顺序随机分为球囊治疗组和支架治疗组,按1∶1比例分配入组。
1.3 手术方式 球囊治疗组:采用紫杉醇释放冠脉球囊(SeQuent Please),于病人右侧桡动脉局部浸润麻醉后,用Seldinger穿刺技术,选择多功能造影导管分别行左右冠脉造影,多体位投影评估,明确狭窄血管;采用指引导管送至冠脉口,送Runthrough NS导丝通过原支架内狭窄处至远端,送Ryujin球囊至原支架内狭窄处,由远及近先后预扩张,闭塞开通后,选用SeQuent Please药物球囊,送至原支架内狭窄处扩张,持续45 s,再次造影狭窄消失;术毕撤出导管、导丝,腕部加压包扎。支架治疗组:采用雅培洗脱支架(XIENCE),于病人右侧桡动脉局部浸润麻醉后,用Seldinger穿刺技术,选择多功能造影导管分别行左右冠脉造影,多体位投影评估,明确狭窄血管;送TREK球囊至狭窄处进行预扩张,选用支架送至原支架内狭窄处多体位投影释放,送后扩张球囊(NC TREK)于原支架内后扩张,再次造影;术毕撤出导管、导丝,腕部加压包扎。登记所有病人,术后随访8个月(图1)。
1.4 评价指标 (1)主要结局指标:主要心脏不良事件发生率、靶病变血运重建率、血栓形成率。(2)次要结局指标:参考血管直径、最小管腔直径,采用数字化平板血管造影机对造影结果进行定量冠状动脉造影分析。
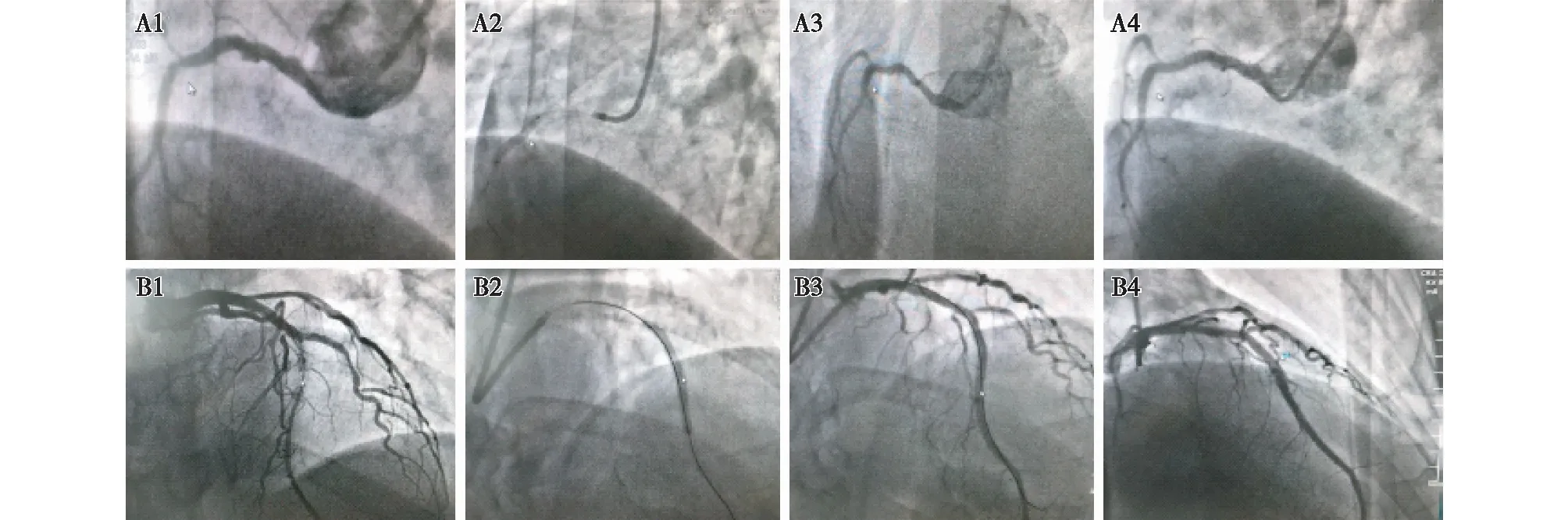
注:A1:右冠状动脉中段支架内80%局限性狭窄;A2:药物球囊植入术中;A3:药物球囊植入后;A4:8个月后随访造影结果;B1:左前降支支架内狭窄(次全闭塞);B2:药物支架植入术中;B3:药物支架植入后;B4:8个月后随访造影结果。图1 典型病例造影结果图
1.5 统计学方法 采用SPSS 16.0软件对研究数据进行统计分析,2组计量资料比较采用t检验;计数资料比较采用卡方检验;P<0.05表示差异有统计学意义。
2 结果
2.1 2组一般资料比较 球囊治疗组和支架治疗组均分别纳入30例病人,年龄60~72岁,随访过程中球囊治疗组丢失1例,支架治疗组丢失2例,最终球囊治疗组纳入29例病人,支架治疗组纳入28病人进入统计分析,2组病人一般资料比较,差异无统计学意义,具有可比性。见表1。
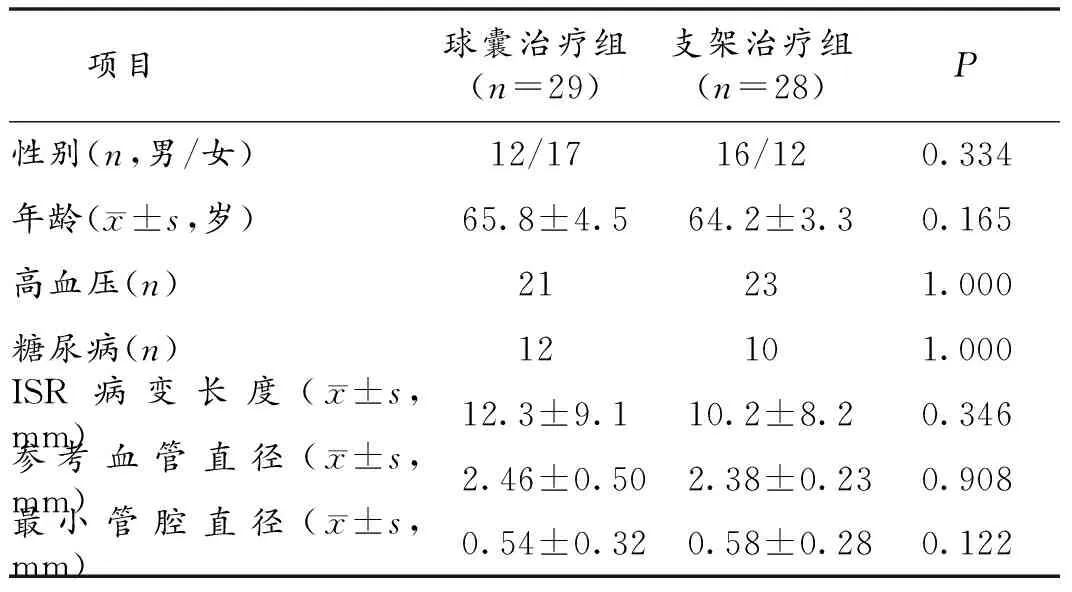
表1 2组病人一般资料比较
2.2 2组主要结局指标比较 球囊治疗组与支架治疗组主要心脏不良事件的发生率分别为6.8%和10.1%,差异无统计学意义(P>0.05)。球囊治疗组与支架治疗组靶病变血运重建率分别为6.8%和21.4%,差异有统计学意义(P<0.05)。血栓形成率球囊治疗组为0,支架治疗组为3.5%,差异无统计学意义(P>0.05)。见表2。
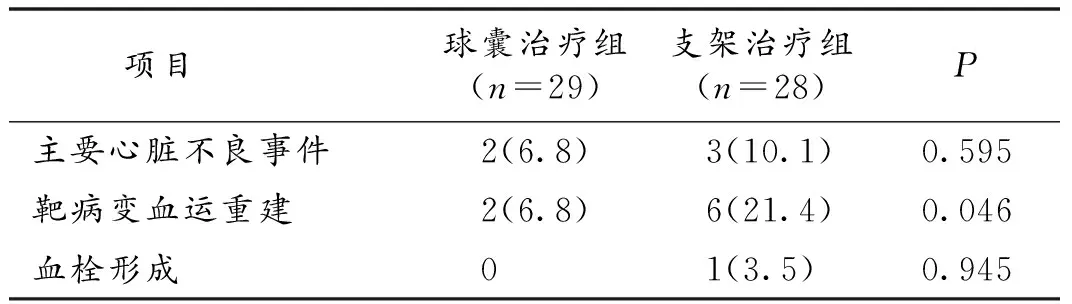
表2 2组病人主要结局指标比较(n,%)
2.3 2组次要结局指标比较 2组间参考血管直径、最小管腔直径差异均无统计学意义(P>0.05)。见表3。
表3 2组病人次要结局指标比较
3 讨论
目前,治疗ISR的主要手段包括单纯球囊扩张术、切割球囊扩张术、冠状动脉斑块旋磨术、再次支架植入术及血管内放射治疗等。2014年ESC/EACTS指南推荐使用药物球囊治疗ISR,证据等级为Ⅰ类A级。同时综合2009年RESERCH的研究和2014年PEPCAD China ISR的结果可以发现药物球囊在ISR治疗中的优势。2009年RESERCH研究纳入了132例ISR病人,随机分为支架治疗组和球囊治疗组,主要结局指标为晚期管腔丢失,6个月后随访发现支架组管腔丢失为(0.38±0.61) mm,球囊组为(0.17±0.42) mm(P=0.03);在继续随访12个月后,主要心脏不良事件在支架组和球囊组分别为22%和9%(P=0.08)[3]。最终研究得出结论,药物球囊在ISR的治疗上优于药物支架。2014年中国的ISR研究,观察的主要结局指标为9个月后晚期管腔丢失,以及12个月后临床不良事件发生率,最终得出了球囊不劣于支架的结果[4]。球囊的具体优势可能体现在球囊扩张狭窄段时释放药物,可保证高浓度药物进入血管壁并维持不到1周时间,这样既可以有效抑制早期平滑肌细胞的增殖,又不影响晚期损伤血管的再内皮化; 缺少了药物载体,减少了支架置入后血管局部的炎症反应;可保证高纯度的药物进人血管壁,且具有广泛的药物接触面积[5]。本研究证实,药物球囊和药物支架均可有效治疗老年ISR,并且均有良好的安全性,治疗过程中2组病人均未发生与治疗相关的不良反应。在药物球囊与药物支架对比中发现,2种治疗方式在主要心脏不良事件和血栓形成率上无差异,但药物球囊组病人靶病变血运重建率低于药物支架组。在后续的分析中发现,发生主要心脏不良事件的病人,均合并有糖尿病。
ISR的机制主要是由于血栓的形成、炎症反应、血管平滑肌细胞迁移和内膜过度增生。血栓主要是由于PCI后冠状动脉内膜及中膜损伤,其内的胶原组织、组织因子暴露于血管腔中,支架本身引起血小板系统和凝血酶系统的活化,促进血液凝固;同时冠状动脉机械性损伤后,会诱发炎性细胞浸润及血小板聚集,它们将释放多种细胞因子和生长因子激活血管中层平滑肌细胞,如果这些平滑肌细胞在修复过程中基因异常表达,迁移增生和分泌细胞外基质过度,均会导致内膜的过度增生[6]。ISR 的危险因素包括吸烟、增龄、糖尿病、血脂异常和高血压等[5]。而老年病人更易合并有多种慢性疾病,因此对于老年ISR病人治疗方案的选择对于病人预后极为重要。本研究发现发生主要心脏不良事件的病人均合并有糖尿病,基于本次小样本的研究,是否糖尿病病人无论采用哪种治疗方案其心血管事件的发生风险都较其他人群升高有待一进步的研究。随着我国人口的老年化,未来有待进一步开展针对老年病人大规模的临床研究,探索药物球囊在老年ISR中的治疗作用。

