全国卷Ⅱ化学反应原理综合题命题特点分析及预测
安徽 尉言勋 徐 楠
化学反应原理综合题,是高考全国卷Ⅱ中三个必考大题之一,往往以实际生产、生活联系紧密的物质为背景材料进行命题,考点源于教材,又略高于教材。命题以基础知识为主线,注重学生能力的考查。纵观近三年的高考试题,考查的基本内容变化不大,常以选择、填空、识图、原因分析等形式呈现。本文对近三年的命题特点进行了对比分析,对典型试题进行了详细解析,总结了命题的特征并对2018年高考进行了预测。
一、近三年化学反应原理综合题真题对比分析

年份呈现特点试题情景、考查角度及知识要点2015年3个小题,9个空,2个图以利用合成气(主要成分为CO、CO2和H2)合成甲醇为背景,考查焓变计算、化学平衡常数、化学反应速率和化学平衡影响因素、转化率、根据图象分析问题等2016年3个小题,9个空,2个图以丙烯腈的制备为背景,考查热力学趋势、反应条件的选择、产率与反应温度的曲线关系、根据图象问题分析原因、影响化学平衡的因素、简单计算等2017年3个小题,7个空,3个图以丁烯为载体,考查焓变的计算、平衡转化率与反应温度、压强关系,产率与进料气、反应温度的关系曲线分析,产率快速降低的原因分析
1.考题的共同特征
(1)以真实的工业生产为载体,知识覆盖面广、综合性较强,各小题之间有一定的独立性。考点一般比较固定,比如每年均考查:①热化学方程式及盖斯定律的应用;②化学方程式的书写,特别是陌生离子方程式的书写,氧化还原反应方程式等。
(2)题目往往给予2~3个图形,有时会有表格。侧重考查学生读取图表信息的能力,利用读取的信息解决实际问题。难点是化学反应条件的控制,化学平衡图象的分析与判断。比如:平衡转化率或产率为纵坐标、温度或反应物浓度比值为横坐标的图形分析。
(3)注重化学计算能力的考查,比如:2015年涉及利用键能和盖斯定律计算焓变,2016年涉及进料气氨、空气、丙烯的理论体积比,2017年涉及盖斯定律的简单计算。
2.考点的框架

3.高频考点——焓变的计算及盖斯定律
(1)用焓的变化(ΔH)来描述化学反应的反应热。焓变的计算方法:

(2)盖斯定律:对于同一个反应不管化学反应是一步完成或分几步完成,其反应热是相同的。如图:

二、真题解析
【例】(2017·全国卷Ⅱ)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷(C4H10)脱氢制1 - 丁烯(C4H8)的热化学方程式如下:



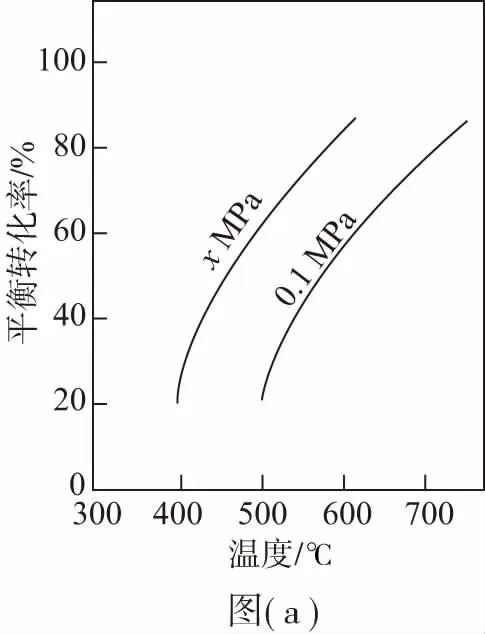
反应①的ΔH1为__________ kJ·mol-1。图(a)是反应①平衡转化率与反应温度及压强的关系图,x__________(填“大于”或“小于”)0.1;欲使丁烯的平衡产率提高,应采取的措施是__________(填标号)。
A.升高温度 B.降低温度
C.增大压强 D.降低压强


(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是__________。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590℃之前随温度升高而增大的原因可能是__________、________;590℃之后,丁烯产率快速降低的主要原因可能是__________。
【答案】(1)+123 小于 AD
(3)升高温度有利于反应向吸热方向进行 温度升高反应速率加快 丁烯高温裂解生成短链烃类
【解析】(1)根据盖斯定律,②-③=①,则ΔH1=ΔH2-ΔH3=-119 kJ·mol-1+242 kJ·mol-1=+123 kJ·mol-1。反应①是一个气体分子数增加的反应,由图(a)可以看出,温度相同时,由平衡转化率(0.1 MPa)<平衡转化率(xMPa),丁烷的转化率增大,即平衡正向移动,所以x的压强较小,x<0.1。由于反应①为吸热反应,温度升高时,平衡正向移动,丁烯的平衡产率增大,则A正确、B错误。反应①正向进行时体积增大,加压时平衡逆向移动,丁烯的平衡产率减小,则C错误,D正确。
(2)由题目给予信息“氢气可以活化催化剂”,所以转化率先升高是因为氢气的量增加,从而使丁烯的产率增加;当进料气中n(氢气)/n(丁烷)增大到一定程度后,由于产物中H2的浓度增大,逆反应速率增大,使反应①平衡逆向移动,从而使丁烯转化率下降。
(3)该反应为吸热反应,590℃之前,温度升高时反应速率加快,平衡正向移动,平衡体系中生成的丁烯增多,产率逐渐增加;当温度超过590℃时,由题目信息可得由于丁烷高温会裂解生成短链烃类,所以副产物曲线迅速上升,导致丁烯产率降低。
【难点突破】(1)分析图象时“三看”:①一看纵坐标与横坐标的意义;②二看线的走向和变化趋势;③三看起点、拐点以及终点。然后根据图象中呈现的关系、题目信息和所学知识相结合,按照要求解答问题。
(2)使用控制变量法要遵循两个原则:①单一变量原则,②对照性原则。命题中经常考查多因素对某一变量产生影响的问题。通过控制变量法可以绘制的曲线图有很多种,要注意结合影响因素回答问题。
【题目分析及预测】
1.命题特点
(1)本题以丁烷催化脱氢制备丁烯的工业过程为载体考查化学反应原理基础知识,同时考查学生对化学知识的认知、复述以及综合利用的能力。通过反应参数图,引导考生从反应速率角度分析平衡态和非平衡态反应的差异,考查学生利用热力学和动力学的知识分析工业生产中有关反应产率的实际问题。
(2)该题目考查了化学核心素养中的变化观念与平衡思想,引导学生认识到化学变化伴随一定的能量转化;通过本题引导学生从多角度分析化学反应,充分利用化学原理去解决实际问题。通过焓变、平衡转化率与反应温度及压强等的关系图,考查提高平衡产率应采取的措施等基本问题间接实现对化学学科素养的考查。
(3)试题命制中提供拓展知识信息,考查学生自学能力、提取有效信息的能力。要求学生在提取有效信息的基础上解答试题。比如题目中给予了重要信息:“氢气的作用是活化催化剂”以及“副产物主要是高温裂解生成的短碳链烃类化合物”,这两句话对题目的解答起到至关重要的作用。学生可以在原有知识的基础上提取、加工、利用该信息,回答问题。题目的设计注重考查学生知识的应用性、思维的灵活性,培养学生形成思维能力。
(4)在试题的呈现方式上,稳中求变、强调应用、突出能力。要求学生对图表和数据进行自主学习、吸收整合、灵活应用。该题中涉及了数学与图形的综合,注重“数”和“形”的有机结合,以关系曲线的形式考查化学理论知识,让考生由此获得化学信息,再回归到基本反应原理理论上,通过综合分析、归纳演绎,推理出可能原因。
(5)对于表述要求较高的地方,题目采用了在大题中设置选择题的方式给学生以提示,增强考查的指向性,方便学生理解考查意图,降低答题障碍,提高考试的区分效果。
2.2018年高考预测
(1)延续近年的命题特点,题目仍然会给予新的信息,要求考生充分利用题目信息,衔接、重组、转换。新信息的叙述有时看上去很随意,但往往隐含着解题的关键信息。
(2)在提取新信息的基础上,回归到基本反应原理和物质结构理论中,通过延伸基础知识、基本理论,在培养学生自学和探究精神方面进行尝试。
(3)从教材基础知识出发,结合反应物的性质和环境特点,对提高反应物的总利用率、控制副反应发生、提高产品产率、如何使反应更加绿色环保等方面进行命题,特别注意“反应产率”是近两年考试的热点。