舒尼替尼和索拉非尼一线治疗转移性肾细胞癌的疗效评估和比较
姚家喜, 胡骁轶, 朱延军, 王 杭, 郭剑明
复旦大学附属中山医院泌尿外科,上海 200032
2016年美国大约62 700例患者诊断为肾癌且其中14 240例死亡[1]。目前,治疗后肾癌患者5年生存率达74%,但是转移性肾细胞癌(metastatic renal cell carcinoma, mRCC)仅8%[2]。肾癌主要转移至肺、骨、肝和脑等部位[3]。近10年,靶向治疗mRCC取得了迅猛发展,靶标分子标志物日新月异。其中,以酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)为代表的抗血管生成药物舒尼替尼、索拉非尼、帕唑帕尼先后上市,并用于国内临床实践,在mRCC治疗中扮演重要角色,显著改善了患者预后[4]。本研究通过回顾分析149例经舒尼替尼、112例经索拉非尼治疗的mRCC患者的临床资料,进一步评估这2种药物的疗效,现报告如下。
1 资料与方法
1.1 一般资料 回顾性分析复旦大学附属中山医院泌尿外科2009年6月至2017年6月经靶向治疗的mRCC患者261例。其中,男性190例,女性71例;年龄14~87岁,中位年龄58岁;肾透明细胞癌226例,非透明细胞癌35例;112例采用索拉非尼治疗,149例采用舒尼替尼治疗。两组基线资料差异无统计学意义(表1)。本研究经医院伦理委员会审核批准。所有患者均知情同意。
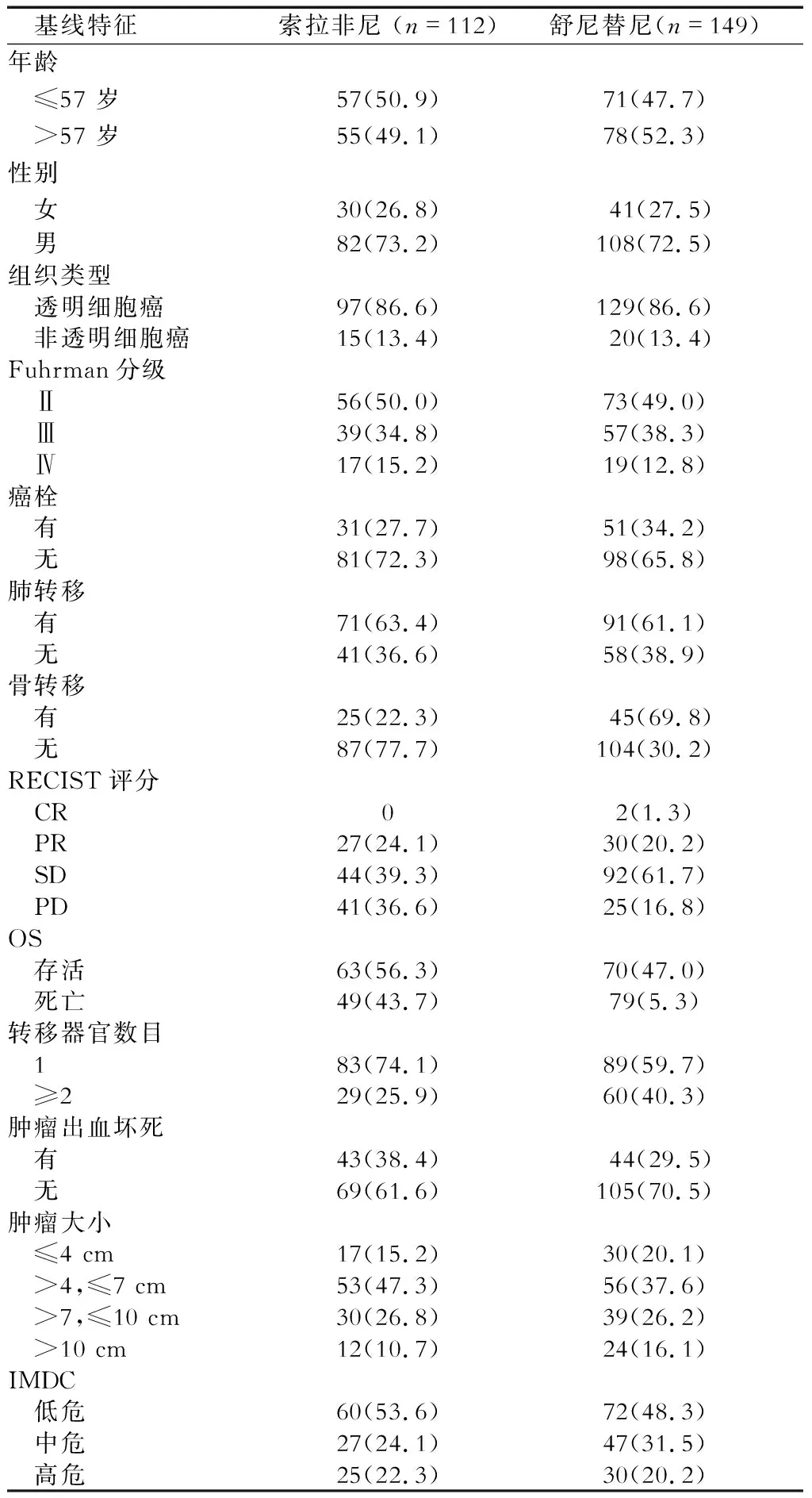
表1 mRCC患者一般临床资料 n(%)
RECIST: 实体瘤疗效评价标准; OS: 总生存时间;IMDC:国际转移性肾细胞癌联合数据库分级系统;CR:完全缓解;PR:部分缓解;SD:疾病稳定;PD:疾病进展
1.2 治疗方法 舒尼替尼50 mg,每日1次,口服,治疗4周停2周,6周为1个周期;索拉非尼400 mg,每日2次,口服,每月为1个周期。每个周期随访1次,每次随访血常规、肝肾功能、凝血功能、甲状腺功能等检查,评估治疗安全性;每2个周期行影像学检查(胸腹部CT或MRI等),评价疗效。
1.3 评价指标 根据国际转移性肾细胞癌联合数据库分级系统(International Metastatic Renal Cell Carcinoma Database Consortium, IMDC),将患者分为低危、中危和高危。IMDC包含如下指标:(1)远期生活质量评估(Karnofsky performance scale,KPS)评分低于80;(2)从诊断到接受TKI治疗时间短于1年;(3)血红蛋白低于正常下限;(4)血钙高于正常上限;(5)中性粒细胞计数高于正常上限;(6)血小板计数大于正常上限。其中,低危符合0个指标;中危符合1~3个指标;高危超过3个指标。
肿瘤对于TKI药物治疗的反应依据实体瘤疗效评价标准(response evaluation criteria in solid tumors, RECIST)进行判断[5-6],包括完全缓解(complete remission, CR)、部分缓解(partial remission, PR)、疾病稳定(stable disease, SD)和疾病进展(progression of disease, PD)。观察并随访患者无进展生存时间(progression free survival, PFS)及总生存时间(overall survival, OS)。观察腹泻、血小板降低、甲状腺功能减退、高血压、肝功能受损等TKI相关不良反应。
2 结 果
2.1 TKI治疗mRCC总体疗效 随访3~96个月,索拉非尼、舒尼替尼治疗的中位OS分别为31.5、36个月,中位PFS分别为15.5、20个月,差异均无统计学意义(P=0.506,P=0.105;图1)。索拉非尼组中21例(18.8%)患者索拉非尼服用剂量由400 mg增为600 mg;6例(5.4%)患者索拉非尼服用剂量由400 mg先增为600 mg,又增为800 mg,持续至疾病进展。
2.2 患者危险分层疾病控制情况比较 索拉非尼组低危60例(53.6%),中危27例(24.1%),高危25例(22.3%);舒尼替尼组低危72例(48.3%),中危47例(31.5%),高危30例(20.2%)。结果(图2)显示:低、中危患者OS明显长于高危患者,3组间差异有统计学意义(P=0.007);3组间PFS差异无统计学意义。
索拉非尼组PR 27例(24.1%),SD 44例(39.3%),PD 41例(36.6%);疾病控制率(PR+SD)为63.4%。舒尼替尼组CR 2例(1.3%),PR 30例(20.2%),SD 92例(61.7%),PD 25例(16.8%);疾病控制率(CR+PR+SD)为83.2%。两组疾病控制率差异有统计学意义(P<0.001)。

图1 两种药物治疗患者的总生存时间和疾病无进展生存时间比较
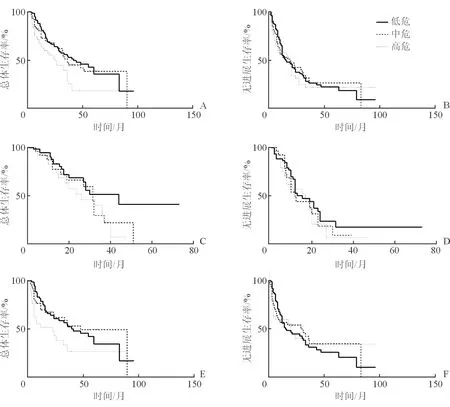
图2 不同IMDC危险分层患者总生存时间(OS)与无进展生存时间(PFS)比较
A: 总体低危、中危、高危患者OS比较(P=0.007);B:总体低危、中危、高危患者PFS比较(P=0.581);C:索拉非尼组低危、中危、高危患者OS比较(P=0.032);D:索拉非尼组低危、中危、高危患者PFS比较(P=0.258);E:舒尼替尼组低危、中危、高危患者OS比较(P=0.048);F:舒尼替尼组低危、中危、高危患者PFS比较(P=0.831)
2.3 mRCC肺转移亚组生存情况比较 索拉非尼组肺外转移41例(36.6%),肺转移71例(63.4%);舒尼替尼组肺外转移58例(38.9%),肺转移91例(61.1%)。结果(图3)显示:总体肺外转移患者OS、PFS长于肺转移患者(P=0.003、P=0.019);舒尼替尼组肺外转移患者OS、PFS长于肺转移患者(P=0.006、P=0.005);索拉非尼组肺转移和肺外转移OS、PFS差异无统计学意义。舒尼替尼组肺外转移患者PFS优于索拉非尼组(P=0.006);两组肺外转移患者OS差异无统计学意义。

图3 mRCC肺转移和肺外转移患者总生存时间(OS)与无进展生存时间(OS)比较
A:总体肺转移、肺外转移患者OS比较(P=0.003);B:总体肺转移、肺外转移患者PFS比较(P=0.019);C:舒尼替尼组肺转移、肺外转移患者OS比较(P=0.006);D:舒尼替尼组肺转移、肺外转移患者PFS比较(P=0.005);E:索拉非尼组肺转移、肺外转移患者OS比较(P=0.207);F:索拉非尼组肺转移、肺外转移患者PFS比较(P=0.994);G:两药物组肺外转移患者OS比较(P=0.105);H:两药物组肺外转移患者PFS比较(P=0.006)
2.4 TKI治疗mRCC的不良反应 索拉非尼组包括高血压(31例)、手足皮肤反应和腹泻(72例),肝损害(24例)。舒尼替尼组包括腹泻(59例)、白细胞降低(97例)、血小板降低(108例)、鼻出血(12例)、口腔炎(62例)、甲状腺功能减退(73例)和高血压(80例),以血小板下降居多。不良反应均可控,患者均可耐受;通过对症支持治疗及调整药物剂量,不良反应缓解。
3 讨 论
mRCC患者的5年生存率较低,且对放疗、化疗不敏感,是临床上的治疗难题[7]。随着对肾癌发病机制研究的不断深入,以TKI为代表的靶向治疗成为目前治疗晚期肾癌的重要手段之一。舒尼替尼和索拉非尼是多靶点TKI,通过抑制血管内皮生长因子受体、血小板源性生长因子受体和干细胞生长因子受体等发挥抗肿瘤血管生成和抑制肿瘤生长的效果。
余霄腾等[8]研究显示,索拉非尼治疗晚期肾癌的疾病控制率为86.6%,患者中位OS为23个月,中位PFS为13个月。Rini等[9]的二线治疗研究显示,经索拉非尼和安慰剂治疗的mRCC患者中位PFS分别为5.5、2.8个月,中位OS分别为17.8、15.2个月,客观反应率分别为2%、0。Escudier等[10]的二线治疗研究显示,经索拉非尼和阿西替尼治疗的mRCC患者的中位PFS分别为4.7、6.7个月,中位OS分别为19.2、20.1个月,客观反应率分别为9%、19%。本研究显示,经索拉非尼一线治疗的mRCC患者的中位PFS为15.5个月,中位OS为31.5个月,优于上述研究。出现以上差异可能与亚州人与欧美人对药物反应不同有关。此外,索拉非尼作为一线药物治疗mRCC后,若患者出现疾病进展,可给予索拉非尼增量治疗,这实际上是一种二线治疗,因此本研究中经索拉非尼治疗的患者OS明显优于国外相关研究。
石泓哲等[11]的研究显示,舒尼替尼治疗晚期肾癌的疾病控制率为87.8%,患者中位OS为23个月、中位PFS为15个月。Motzer等[12]一项大型一线Ⅲ期临床研究显示,舒尼替尼和干扰素治疗mRCC的中位PFS分别为11、5个月,中位OS分别为26.4、21.8个月,客观反应率分别为31%、6%。Motzer等[13-14]一线治疗研究显示,帕唑帕尼非劣效于舒尼替尼,患者的中位PFS分别为8.4、9.5个月,中位OS分别为28.3、29.1个月,客观反应率分别为31%、25%。本研究中,经舒尼替尼治疗的患者中位PFS为20个月,中位OS为 36个月,疾病控制率83.2%,与本课题组前期[15]结果类似,优于上述研究。
本研究中,虽然舒尼替尼组患者OS、PFS较长,但与索拉非尼组差异无统计学意义,可能与随访时间有关,随着随访时间延长,可能出现有统计学意义的差异。而且,索拉非尼组OS是一线治疗加二线治疗(甚至三线治疗)的结果,其一线结果OS可能较短。此外,舒尼替尼疾病控制率明显优于索拉非尼,进一步佐证了舒尼替尼的一线治疗地位。本研究IMDC危险分层分析中,索拉非尼组和舒尼替尼组不同危险分层患者的OS差异有统计学意义(P<0.05),但PFS差异无统计学意义。这可能与样本量不足有一定关系,也说明IMDC标准对亚洲人群的适用性较差。
本研究证实,肺外转移患者OS、PFS明显优于有肺转移者,可能与肺外转移患者的转移器官少于2个、肿瘤负荷较小,而肺转移患者常合并多个肺外器官转移有关。其中,舒尼替尼组肺外转移患者PFS优于索拉非尼组,因此有无肺转移可作为舒尼替尼治疗患者的预后指标,但肺外转移患者中是否可优先选择舒尼替尼,仍有待后续更大样本量研究证实。
舒尼替尼、索拉非尼相关不良事件多为 Ⅰ~Ⅱ级,Ⅲ~Ⅳ 级不良事件少见,患者生活质量较使用干扰素者提高。但由于舒尼替尼、索拉非尼均抑制多个靶点,可能导致多种不良反应的发生,尤其是肝脏毒性、血液学毒性等。本课题组前期研究[15]发现,TKI不良反应存在地域差异,欧美人群以骨髓抑制、高血压等为主,亚洲人群以手足皮肤反应、腹泻、疲劳、血小板减少等为主。本研究中,TKI不良反应多为Ⅰ~Ⅱ级,Ⅲ级以上不良反应少,其中血液学不良反应以贫血、白细胞下降、血小板下降居多,但通过调整药物剂量以及对症处理可以控制,患者恢复。
综上所述,本研究进一步证实,舒尼替尼和索拉非尼一线治疗晚期mRCC可取得较高的疾病控制率,两种药物均能延长患者的OS、PFS,其中以舒尼替尼的效果更好。此外,舒尼替尼和索拉非尼治疗mRCC的不良反应相对较少,患者生活质量受影响较小。在mRCC患者服药期间需严格随访及管理,发生TKI耐药后及时调整方案。然而,本研究为回顾性研究,患者纳入存在一定偏倚,今后须进一步增加样本量、延长随访时间,为临床决策提供更准确的依据。

