ATP荧光检测技术对纤维支气管镜清洗消毒效果评价的研究
杨绍丽,吴文莉,王静,徐晶
(昆明市中医医院,云南 昆明 650000)
随着纤维支气管镜技术的不断发展,其被广泛应用于感染性、非感染性呼吸道疾病的诊断、治疗,如不明原因的胸腔积液、脓胸、气胸、胸腔内异物等[1]。对于感染性呼吸道疾病,常见的病原体有细菌、病毒、真菌,其中院内感染最常见的病原体为克雷伯菌、大肠埃希菌、铜绿假单胞菌,且多为耐药菌,一旦发生交叉感染,临床抗感染治疗难度极大[2-3]。院外感染常见的病原体为支原体、病毒、军团菌,由于我国肺结核的高流行趋势,结核杆菌也是一种常见病原体[5-6]。支气管镜作为一种介入诊疗工具,使用过程中可能对呼吸道造成一定损伤,因其材质特殊、结构复杂精细,使用后若清洗消毒不彻底,或对特殊患者使用过的内镜未进行特殊处理,可能会导致医院交叉感染的发生[4]。三磷酸腺苷(adenosine triphosphate,ATP)荧光检测作为一种既可以反映被测物体微生物负载量,又可以反映有机物残留量的技术,因其方便、快捷的优点,已被广泛运用于食品卫生、环保、医疗卫生等领域。本研究采用ATP荧光检测和滤膜法细菌培养计数两种方法对纤维支气管镜进行检测,对比两种检测结果差异,以探讨ATP荧光检测技术对纤维支气管镜清洗消毒效果现场评价的可行性,现报道如下。
1 资料与方法
1.1临床材料
1.1.1采样方法选取本院肺病脾胃病科、重症医学科、内镜中心三个部门共9支纤维支气管镜,随机抽取“使用期间清洗消毒后”、“保存备用”、“使用后未清洗”三种不同保存状态的纤支镜,冲洗其内腔面获得洗脱样本,再分别利用ATP荧光检测技术和滤膜法细菌培养的方法对洗脱样本进行检测。纤支镜清洗消毒流程按照《软式内镜清洗消毒技术规范》WS507-2016进行,采样依据《医院消毒卫生标准》GB15982-2012中要求进行。
1.1.2采样部位从活检口注入采样溶液冲洗内镜内腔面并全量收集,得到样本。
1.2采样步骤
1.2.1ATP荧光检测法采用3M Clean-Trace ATP荧光检测仪,监测工具包括:水质采样棒、连接器、样品收集杯、50ml无菌注射器和无菌水,采样方法参照GB15982-2012。检测过程:①取出冷藏(2~8℃)的采样棒包装袋(使用前需让其在室温下平衡10 min),持续按住ATP检测仪器上的红色按钮开机后,使仪器主菜单显示“测量样品”,待用;②将内镜末端插入样品收集杯中,将连接器宽头连接到导光部;③用注射器吸取40 ml无菌水(无菌水量约为采样管管腔容积的两倍),将注射器与连接器进行连接,按下吸引阀门,把无菌水缓慢注入管路(持续时间约为5~10 s),然后收集到样品收集杯中(注意内镜末端不要接触样品收集杯中的液体样本);④拔下注射器,吸入60 ml空气后再与连接器进行连接,按下吸引阀门,将空气全部注入管路,以便充分收集采样液;⑤从包装袋中取出采样棒,抽出采样环,将其头部浸入样液中,并轻轻敲击采样环柄以排出气泡,此过程中始终确保采样环的上领口与液面齐平;⑥将采样好的采样环慢慢插回采样管,用力向下推压顶端的红色手柄使采样环彻底插入,激活荧光反应;⑦激活后,以45°的幅度迅速振荡采样棒至少5 s,以混合底部的反应液;⑧打开3M荧光检测仪的样品室,将采样棒插入其中,将盖子按下至正好卡住,按下“选择”键,数秒后屏幕会将结果以“相对光单位(Relative Light Unit,RLU)”显示出来,读数并记录。
1.2.2实验室微生物培养法采样工具包括:由昆明市疾病预防控制中心配制含相应中和剂的液体和采样瓶、50 ml无菌注射器、酒精灯和标记笔。检测过程:①点燃酒精灯制造无菌环境,取清洗消毒后的纤维支气管镜,用无菌注射器抽取50 ml含相应中和剂的洗脱液,从活检口注入冲洗内镜管路,然后将其收集于采样瓶中(注意内镜末端不要接触采样瓶),充分混匀,将样本瓶做好标记后4 h内送实验室;②取样本液1.0 ml接种平皿,将冷至40~45℃的熔化营养琼脂培养基每皿倾注15~20 ml,(36±1)℃恒温箱培养48 h,测定细菌总数(CFU/件);③剩余样本液在无菌条件下用滤膜(0.45µm)过滤浓缩后,将滤膜接种于凝固的营养琼脂平板上,置(36±1)℃温箱培养48 h,测定细菌总数。由市疾控中心出具相应的检测结果报告。
1.3评价标准
1.3.1ATP荧光检测法按3M公司器械产品说明书推荐阈值,软式内镜腔面≤200 RLU为合格。
1.3.2实验室微生物培养法依据GB15982-2012,消毒内镜细菌菌落数≤20 CFU/件为合格。
1.4统计学方法结果采用SPSS 20.0进行统计分析,率的比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
本研究利用ATP荧光检测与滤膜法细菌总数测定两种方法检测,共获得样本各522例。其中,清洗消毒后纤支镜内面样本各488例,保存备用纤支镜内面样本各25例,使用后经床侧预处理但未清洗消毒纤支镜内面样本各9例。滤膜法细菌总数测定:清洗消毒后488例样本,不合格6例,保存备用样本25例,不合格0例,总合格率98.83%;使用后经床侧预处理但未清洗消毒样本9例,不合格6例,不合格率66.67%。ATP荧光检测法:清洗消毒后488例样本,不合格8例,保存备用样本25例,不合格0例,总合格率98.44%,使用后经床侧预处理但未清洗消毒样本9例,不合格9例,不合格率100.00%。两种方法检测结果差异不具有统计学意义,见表1。
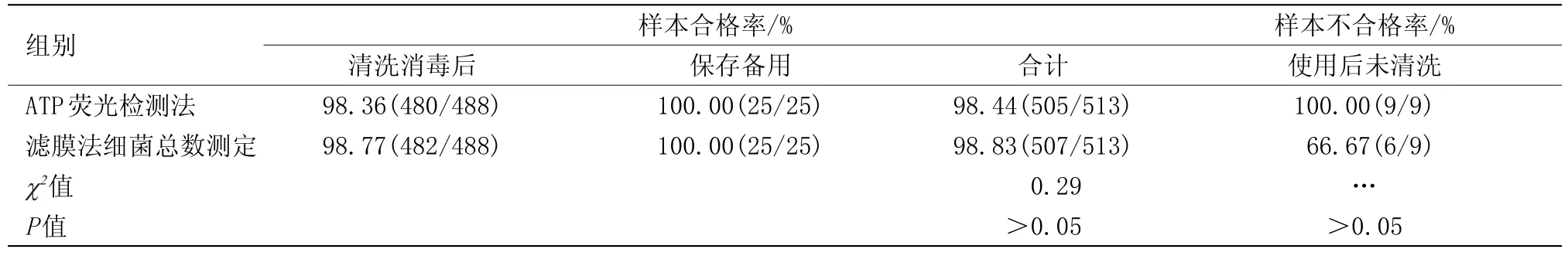
表1 两种检测方法不同时机检测结果Table 1 Results of two detection methods at different times
纤支镜清洗消毒后ATP荧光检测不合格的样本8个,检测数值最高为550.00 RLU、最低为225.00 RLU,中值为296.00 RLU;滤膜法细菌总数测定不合格样本6个,均为25.00 CFU/件。使用后未清洗纤支镜内面冲洗样本ATP荧光检测不合格样本9个,结果数值最高为6822.00 RLU,最低为430.00 RLU,中值为2 930.00 RLU;滤膜法细菌总数测定不合格样本6个,最高菌落数6 300.00 CFU/件,最低菌落数为530.00 CFU/件,菌落数中值为5 000.00 CFU/件。滤膜法细菌总数测定结果有466个样本的菌落数为0 CFU/件,ATP荧光检测结果至少为1.00 RLU,但不超过200.00 RLU;其中有36个样本两种检测方法的结果均不为零,但在允许范围内。从两种检测结果数值的四分位间距看,ATP荧光检测结果波动较大,微生物数量超标的样本ATP荧光检测的结果显著增高,见表2。
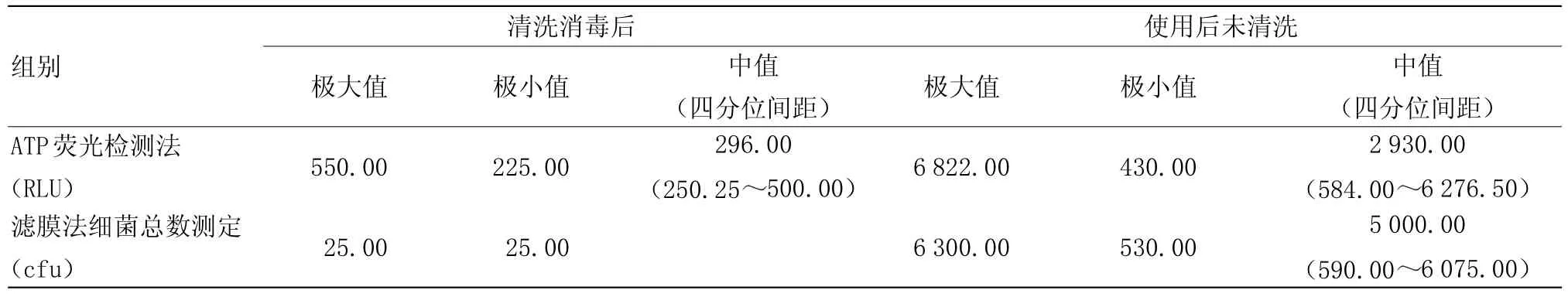
表2 两种检测方法不同状态不合格样本检测结果Table 2 Test results of unqualified samples in different states of two detection methods
3 讨论
有研究对清洗消毒处理不合格的内镜进行细菌培养后,检出的病原体有铜绿假单胞菌、鲍氏不动杆菌、肺炎克雷伯菌、真菌、结核杆菌等[5]。而现行《医院消毒卫生标准》GB-15982~2012对纤维支气管镜的监测仅为3个月1次,细菌总数检测所需时间为48 h,耗时长,不及时,滞后性等原因,无法指导现场清洗消毒工作的改进,因此,找到一种快捷、高效、准确的监测方法尤为重要。2016年国家卫计委颁布并执行的《软式内镜清洗消毒技术规范》WS 507-2016推荐可采用ATP生物荧光测定等方法对内镜的清洗质量进行评价。本研究结果显示:纤维支气管镜清洗消毒后的腔面,滤膜法细菌培养计数和ATP检测合格率分别为98.83%和98.44%,与有学者报道经规范、集中清洗消毒的纤维支气管镜合格率为98.75%~99.08%[6]的结果相近。经卡方检验,两种检测方法的样本合格率差异不具有统计学意义,ATP荧光检测可作为一种有效的快速检测方法,对于纤维支气管镜清洗消毒效果的现场评价具有一定的应用价值,与其他学者研究结果一致[7]。同时,我们还从两种检测不合格样本四分位间距进行了统计,发现不合格样本使用ATP检测结果波动较大,有学者认为,可能是受到其他有机物或体细胞ATP的影响[8],也可能是因为不同微生物的ATP含量不同所致[9],但都从另一个侧面说明ATP检测灵敏度较高。当然,ATP的检测方法也有不足之处,例如:当检测结果不合格时不能甄别病原菌种类,不能鉴定该细菌的耐药性;使用ATP检测时,室内温度、样本中的微生物量过低或过高均会影响检测结果,需要根据检测目的选择不同灵敏度的检测仪器[10]。此外,目前关于该检测技术的采样方法、阈值判断标准等尚无权威的标准或指南,需要进一步进行探索。

