DRGEP与敏感性分析方法构建甲苯简化动力学模型
冯洪庆, 张 静, 张春红, 刘道建, 安 铭
(1.中国石油大学(华东)储运与建筑工程学院,山东青岛 266580; 2.天津大学内燃机燃烧学国家重点实验室,天津 300072)
汽油是多种组分组成的混合物,并且因产地和生产工艺的不同其成分也不尽相同,燃烧过程中无法直接对汽油详细组分构建化学动力学模型。将正庚烷和异辛烷两种组分组成的替代燃料,按照一定的配比用于模拟燃料辛烷值特性,被广泛采用[1-4]。在火花点火发动机研究中常使用将正庚烷和异辛烷掺混形成的混合物,即基础参比燃料(PRF)代替汽油,来模拟辛烷值对燃烧过程的影响,然而,通常汽油组成中包含有20%~50%的芳香烃,其中的甲苯是芳香烃的代表组分。因此,PRF用作替代燃料不能准确模拟实际汽油抗爆性的变化规律。为了更好地模拟汽油燃烧,其替代燃料需要包含更多的组分,正庚烷、异辛烷、甲苯三组分燃料能够更好地再现汽油理化特性[5-6]。但是,甲苯属于芳香烃,其结构与烷烃不同,现有TRF简化机制在详细、半详细机制基础上进行调整的过程中可能忽略掉一些甲苯特有的反应路径。甲苯作为典型芳香烃类的代表物质,其氧化机制的研究也随之不断发展[5,7]。Pitz、Dagaut等[8-14]给出了当前典型的甲苯反应动力学模型。笔者采用直接关系图法对甲苯化学反应动力学机制进行简化,并进行反应速率分析和敏感性分析,将该机制在射流搅拌反应器模型和HCCI发动机模型中对滞燃期进行对比。
1 甲苯简化机制
选取通过广泛验证的Metcalfe甲苯详细机制作为初始机制,此详细机制包含有329种组分、176个反应,通过基于误差传递的直接关系图法(DRGEP)进行简化,得到初步框架,将组分减少至92,反应数减少至607。直接关系图法(DRG)是由Law等[15]提出的机制简化方法,用于简化大型复杂反应机制,使用组分A对B生成率的正规化贡献rAB分析组分A与B之间的耦合关系。Desjardins等[16]对rAB进行改进,将组分间的耦合关系重新定义为
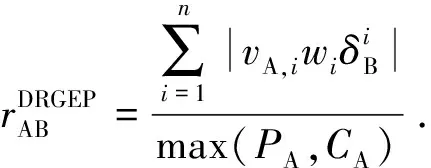
(1)
(2)
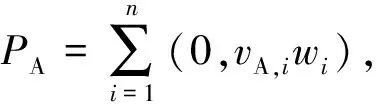
(3)
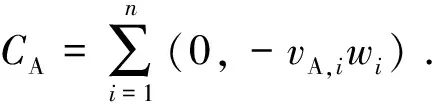
(4)
当rAB大于给定阈值ε时,则称A与B强耦合。
简化工况压力为0.1~1 MPa,温度为400~1 000 K,当量比为0.25~2.0,分别以C6H5CH3、H2O、CO2为初始组分,阈值为0.05。初步简化的机制已经去除了大量反应过程中相对次要的组分,之后,再以温度敏感性分析和反应速率、反应路径分析找出较为主要的路径,进一步优化。
1.1 反应速率分析
图1给出了温度为500 K、压力为0.2 MPa、当量比为0.5时部分物质的反应速率分析结果,图中的反应编号是甲苯简化机制中的序号。从图1中可以直观看到各反应对某指定组分生成、消耗的影响程度。对于甲苯,在上止点前约21 ℃A(℃A表示曲轴转角单位)开始缓慢反应,消耗最快的反应是被羟基氧化生成苯甲基,其次是与O原子生成OC6H4CH3。苯甲基主要由甲苯氧化生成(R1、R2),通过生成苯甲醛(C6H5CHO)及C6H5CH2OO(R17、R18)消耗掉。
R1:C6H5CH3+OH=C6H5CH2+H2O,
R2:C6H5CH3+O2=C6H5CH2+HO2,
R17:C6H5CH2+HO2=C6H5CH+H+OH,
R18:C6H5CH2+O2=C6H5CH2OO.
重要中间产物苯(C6H6)主要通过反应R8中OC6H4CH3分解生成,通过氧化为苯基(R36)和苯氧根离子(R35)消耗。
R8:OC6H4CH3=C6H6+CO+H,
R36:C6H6+OH=C6H5+H2O,
R35:C6H6+O=C6H5O+H.
苯甲基(C6H5CH2)除了直接氧化为苯甲醛(C6H5CHO)外,还有另外一条重要间接反应途径,即生成C14H14(R13):
R13:C6H5CH2+C6H5CH2=C14H14.
在一系列低温氧化之后,环戊二烯基(C5H5)在上止点前20.4 ℃A左右通过苯氧根离子(C6H5O)的分解而生成,接着被OH氧化为C4H6小分子,或C5H4O、C5H4OH为开环反应做准备。
经过反应速率以及反应路径分析,明确了甲苯氧化过程所产生的中间物质主要的生成、消耗途径。
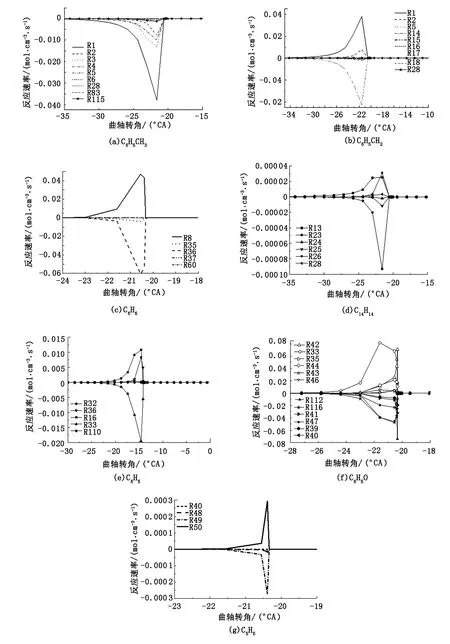
图1 几种物质的反应速率分析Fig.1 Reaction rate analysis of some species
1.2 温度敏感性分析
敏感性分析也是机制简化过程中一种常用的分析方法[17],主要是分析系统对微小扰动的响应。对于燃烧系统来说,是指在给定工况下分析各化学反应的速率常数发生微小变动时引发的反应速率、温度、压力等系统特征量的变化程度,其响应值称为敏感度。敏感系数反映出各反应的重要程度,通过对敏感系数比较,保留相对重要的反应,从而实现反应动力学机制的简化。由于低温均质压燃过程对温度比较敏感,故继续采用温度敏感性分析对甲苯氧化过程进行研究。图2给出了各种运行工况下的温度敏感性分析结果,敏感值可由化学动力学分析软件Chemkin Pro计算导出。计算中采用的HCCI发动机结构参数为:缸径110 cm,冲程120 cm,连杆长度192 cm,压缩比17,转速1 400 r/min。
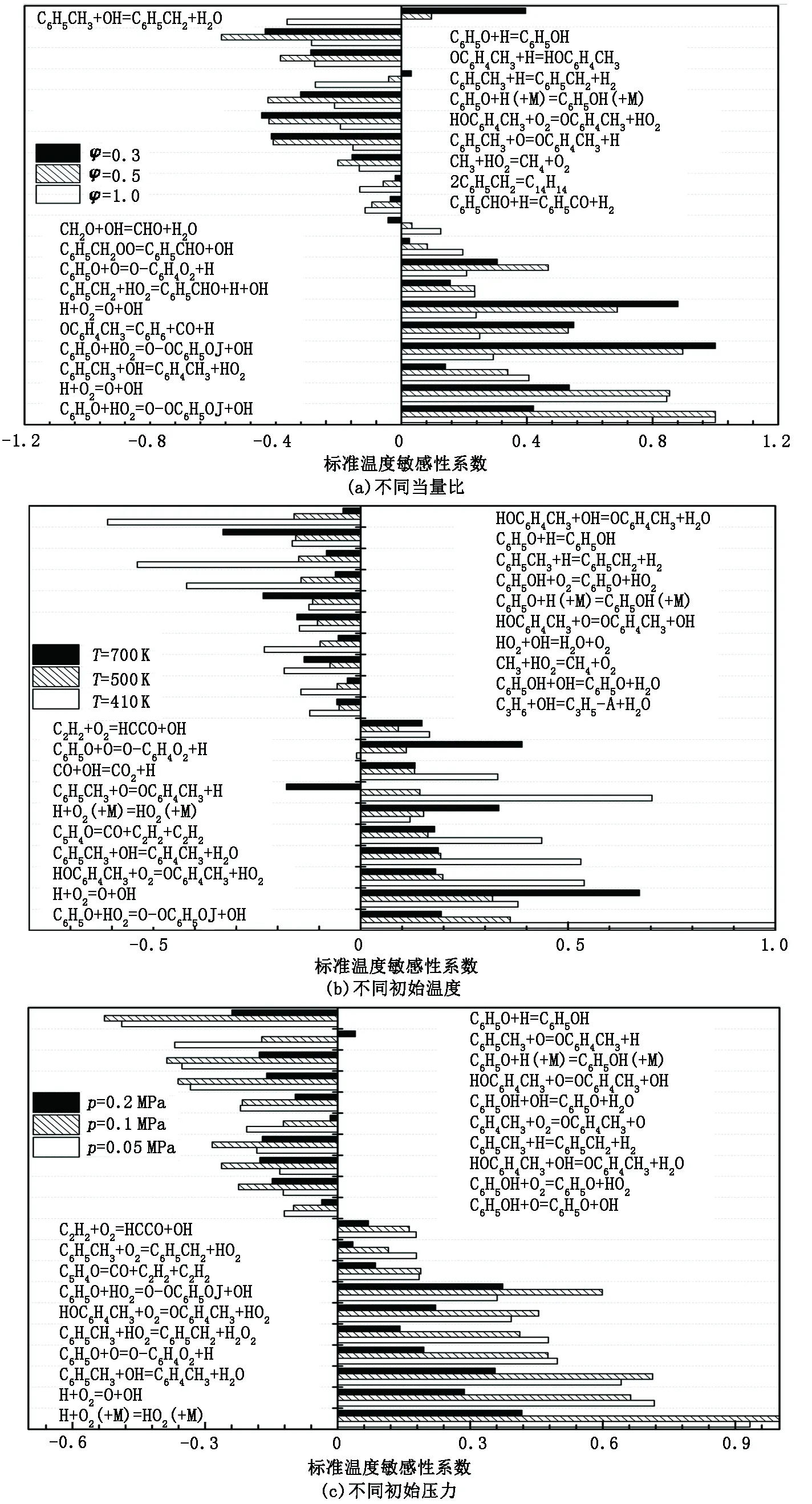
图2 甲苯氧化温度敏感性分析Fig.2 Temperature sensitivity analysis of toluene oxidation
由图2可看出,各反应的温度敏感系数的正值表明该反应的速率常数增加时,系统温度随之升高;负数则说明增加该反应速率常数会导致系统温度减小。敏感系数的绝对值代表反应对系统温度影响作用的强弱,绝对值越大,影响越明显。从图2(a)发现,甲苯被OH基氧化脱氢的反应为C6H5CH3+OH=C6H5CH2+H2O,在浓混合气情况下抑制系统反应的进行;而在稀燃时会促进系统氧化反应,增加系统温度;甲醛氧化为HCO基的反应,CH2O+OH=HCO+H2O,规律则相反,在当量比为0.3时会降低系统温度,而高当量比下促进反应的进行。不同初始温度下,各反应对系统反应过程的影响也不尽相同,甲苯与氧原子产生OC6H4CH3的过程,在低温下会促进系统温度的升高,加快反应进程;而高温下,则会导致系统温度降低。
经过上述温度敏感性分析,发现有32个反应对系统温度有较为明显的影响,这些反应如表1所示,将被保留在最终的简化机制中。

表1 温度敏感性分析结果(32个敏感反应)Table 1 Result of temperature sensitivity analysis (32 sensitive reactions)
1.3 滞燃期敏感性分析
为了更好地拟合试验数据,初步构建的简化机制还需要进一步对反应系数进行优化调整,这部分工作主要通过敏感性分析完成。由于高温反应模型的发展比较成熟,只对甲苯低温氧化裂解反应进行敏感计算。参考Ra等[18]的方法,本文中敏感性分析不局限于某一特定工况,而是在多个目标工况下将指前因子变化前后的模拟值对比分析,进行整体优化。针对激波管滞燃期进行敏感性分析,定容燃烧滞燃期定义为混合物温度达到比起始温度高400 K所需时间。
ai=kiabase.
(5)
式中,abase为某反应的初始值;ai为第i个反应调整后阿伦尼乌斯速率方程中指前因子;k为敏感因子,取3.0。
敏感系数计算为
(6)
对要研究的反应逐个进行分析,每次计算只改变一个反应的指前因子,根据调整前后的数值代入反应机制中得出滞燃期数据;然后对多个温度工况下的结果统计绘图,与试验结果进行对比,更加直观地表现出各个反应对着火时刻的影响作用。
图3为压力5 MPa,温度区间1 000~1 800 K,当量比1.0时的滞燃期敏感性分析结果。敏感系数为正,表明指前因子变大会使得滞燃期延长;反之,为负会使滞燃期减小。图3仅列出了几个对滞燃期影响较大的反应分析结果。
由图3可直观看到,苯甲基与氧原子生成苯基的反应在1 200~1 800 K敏感系数较大,即对滞燃期较敏感,相对低温时敏感系数较小。苯基氧化为苯氧根离子的反应随着温度升高对滞燃期的影响随之增大,到1 500 K左右,影响逐渐减小。苯氧根离子裂解为C5H5和CO的反应随温度升高敏感系数逐渐降低,对着火的抑制作用逐渐减弱。在计算的整个温度区间内,C5H4O裂解为CO和两个C2H2的反应滞燃期敏感系数均为负值,即增加此反应的反应速率会促进着火提前,滞燃期减小。此外还发现,随着温度升高,这种影响力逐渐增强。计算中发现,与O-OC6H4O2相关的反应对着火有重要影响,C6H4CH3与O2形成O-OC6H4CH2的过程随温度升高延迟着火作用增强,而通过C6H5氧化生成的反应则随温度的升高对系统燃烧有促进作用,点火随之提前。综合各种工况下的试验数据,确定需要进行调整的反应,最终做出如表2的修正,以便更好地拟合试验结果。
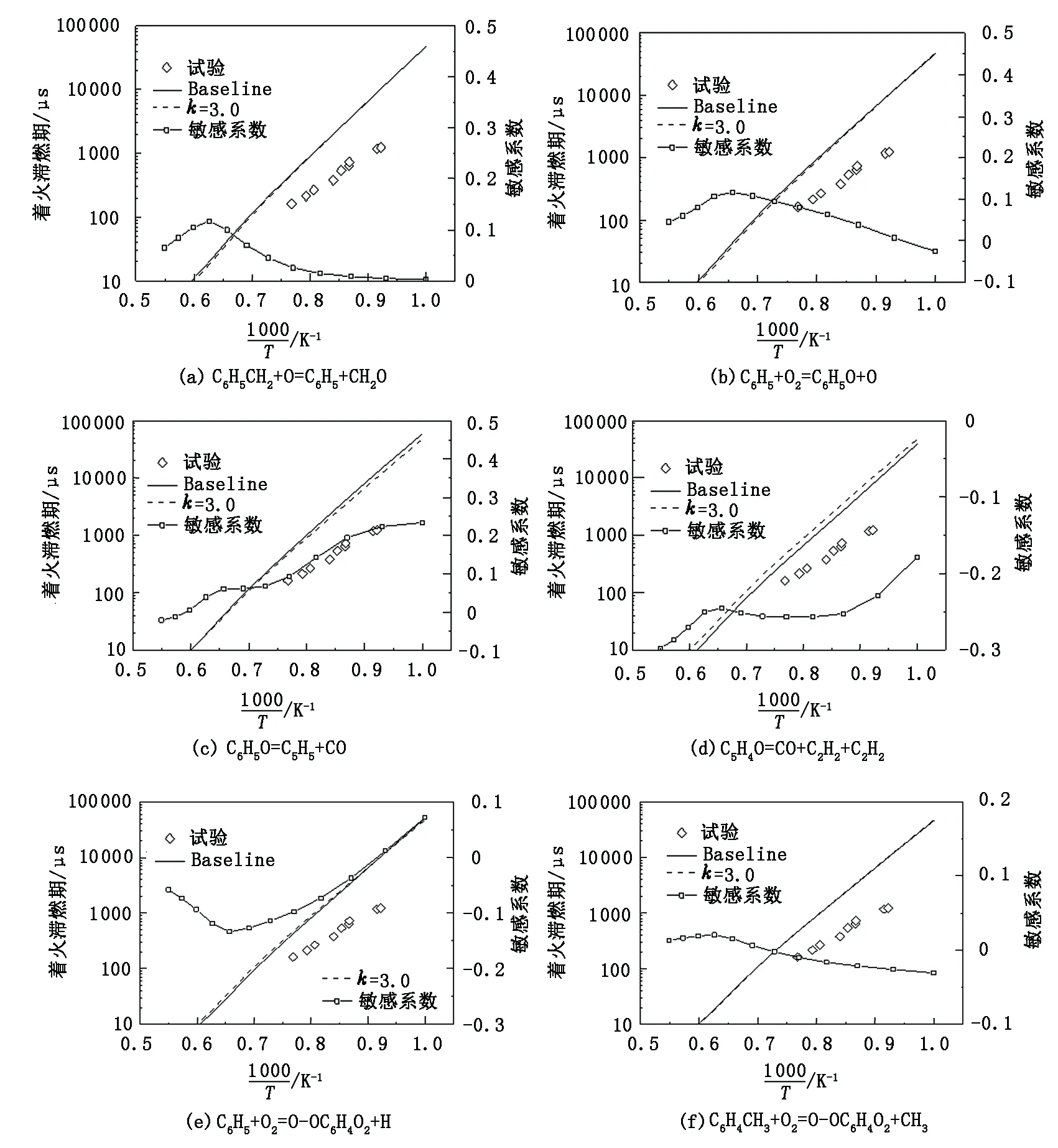
图3 甲苯在激波管中滞燃期的敏感性分析Fig.3 Ignition delay sensitivity of toluene in shock tube
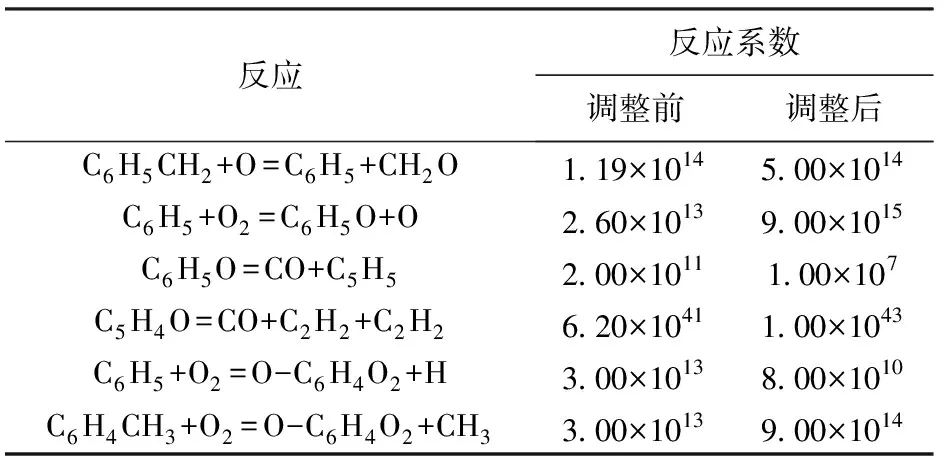
反应反应系数调整前调整后 C6H5CH2+O=C6H5+CH2O1.19×10145.00×1014 C6H5+O2=C6H5O+O2.60×10139.00×1015 C6H5O=CO+C5H52.00×10111.00×107 C5H4O=CO+C2H2+C2H26.20×10411.00×1043 C6H5+O2=O-C6H4O2+H3.00×10138.00×1010 C6H4CH3+O2=O-C6H4O2+CH33.00×10139.00×1014
经过DRGEP初步简化,温度、滞燃期敏感性分析,速率及路径分析的进一步优化,甲苯氧化机制最终简化为48种组分和176个基础化学反应,最后确定的甲苯氧化简化路径如图4所示。
从图4中直观看到,苯(C6H6)、苯基(C6H5)和苯氧根离子(C6H5O)是甲苯氧化过程中几种重要的中间产物。甲苯低温反应主要途径为:甲苯(C6H5CH3)→苯甲基(C6H5CH2)→苯甲醛(C6H5CHO)→苯甲酰(C6H5CO)→苯基(C6H5)→苯氧根离子(C6H5O)→苯酚(C6H5OH),之后是拆环反应。甲苯初步反应中除了脱氢形成苄基,还通过氧化形成OC6H4CH3,进一步分解为苯,苯进而被氧化为苯基和苯氧根离子。苄基是比较稳定的中间产物,是甲苯分子中的甲基碳脱掉一个氢原子形成的一价基团,一般是由C6H5CH3与O2、O、H、HO2基发生脱氢反应而生成。Shen等[19]通过敏感性分析认为甲苯和苯甲基与氧分子的反应非常重要,并测量了这些反应的速率常数,对C6H5CH2+O2反应进行了修正。Silva等[20]指出,在中低温工况下,苄基与HO2自由基的反应是十分重要的氧化路径。苯甲基的主要消耗途径为被HO2、O基氧化为苯甲醛,C6H5CH2+HO2=C6H5CHO+H+OH, C6H5CH2+O=C6H5CHO+H, 生成二甲基联苯(C14H14)及苯基,C6H5CH2+C6H5CH2=C14H14, C6H5CH2+O=C6H5+CH2O。苯氧根离子与H基重组生成苯酚,苯酚同时被氧化为苯氧基,苯氧根离子分解成为环戊二烯基(C5H5)和CO。环戊二烯基主要通过以下过程完成拆环生成小分子:C5H5+O=C5H4O+H, C5H5+OH=C5H4OH+H, C5H4OH=C5H4O+H, C5H4O=C2H2+C2H2+CO, C5H5+OH=C4H6+CO。
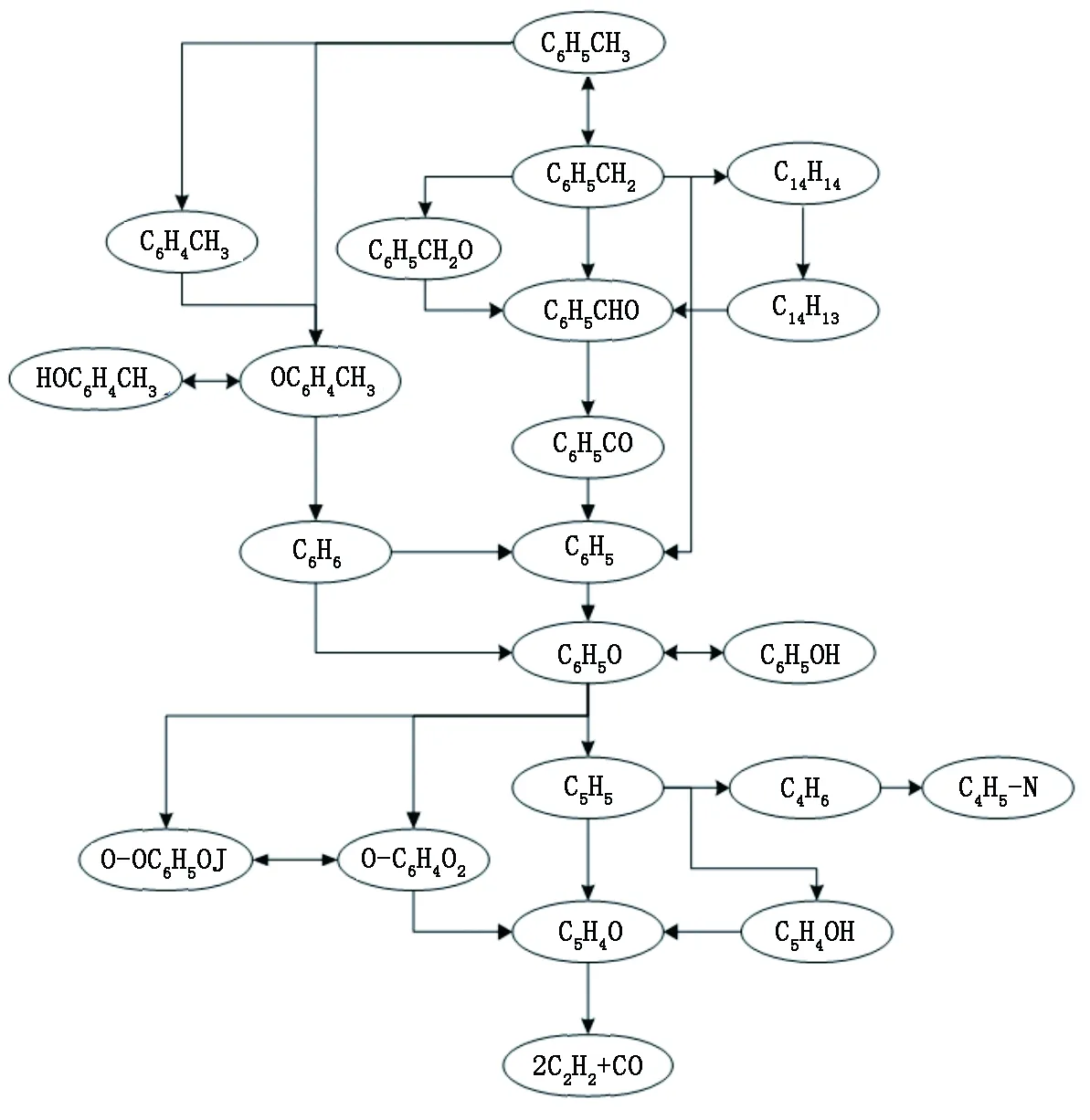
图4 甲苯化学反应动力学路径Fig.4 Reaction path of toluene oxidation
2 甲苯简化机制验证
2.1 滞燃期验证
滞燃期是检验一个机制准确性的重要标准。Shen等[19]在激波管中研究了温度为1 021~1 400 K,压力为1~6.1 MPa,当量比为0.25、0.5、1.0工况下,甲苯/空气混合物的自燃着火过程,测量了相应的着火延迟期。在当量比为1,压力为0.681 MPa的工况下甲苯在激波管中滞燃期详细机制与简化机制的预测值与试验值对比见图5。从图5中可以看出,本文简化机制很好地反映了燃料反应特性与温度之间的关系。
图6~8给出了不同运行工况下甲苯简化机制滞燃期计算结果与试验数据对比情况。为更加全面评估本文提出的简化模型,图中还以Andrae等[21]和Mehl等[22]构建的甲苯参比燃料半详细机制中的甲苯子机制进行侧面对比。
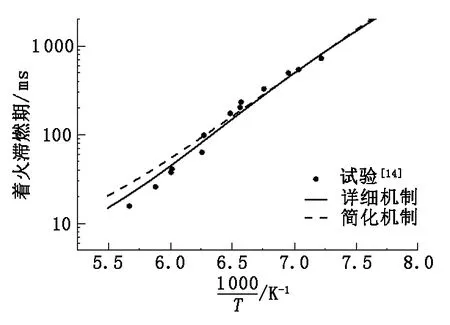
图5 甲苯在激波管中滞燃期详细机制与简化机制的预测值与试验值对比Fig.5 Comparison of detailed and reduced mechanism modeling and experimental results of toluene ignition delay in shock tube
无论哪种模型,在较高压力时(5 MPa)简化机制的预测值明显优于在相对低压时的预测情况,低压稀燃工况下的计算值比试验数据偏高。理论当量比下,本文中构建的简化模型在各种压力范围内的预测结果与试验值吻合很好。对比之下,本文中构建的简化模型结果比较合理,这也说明此简化过程和模型均是可靠的。
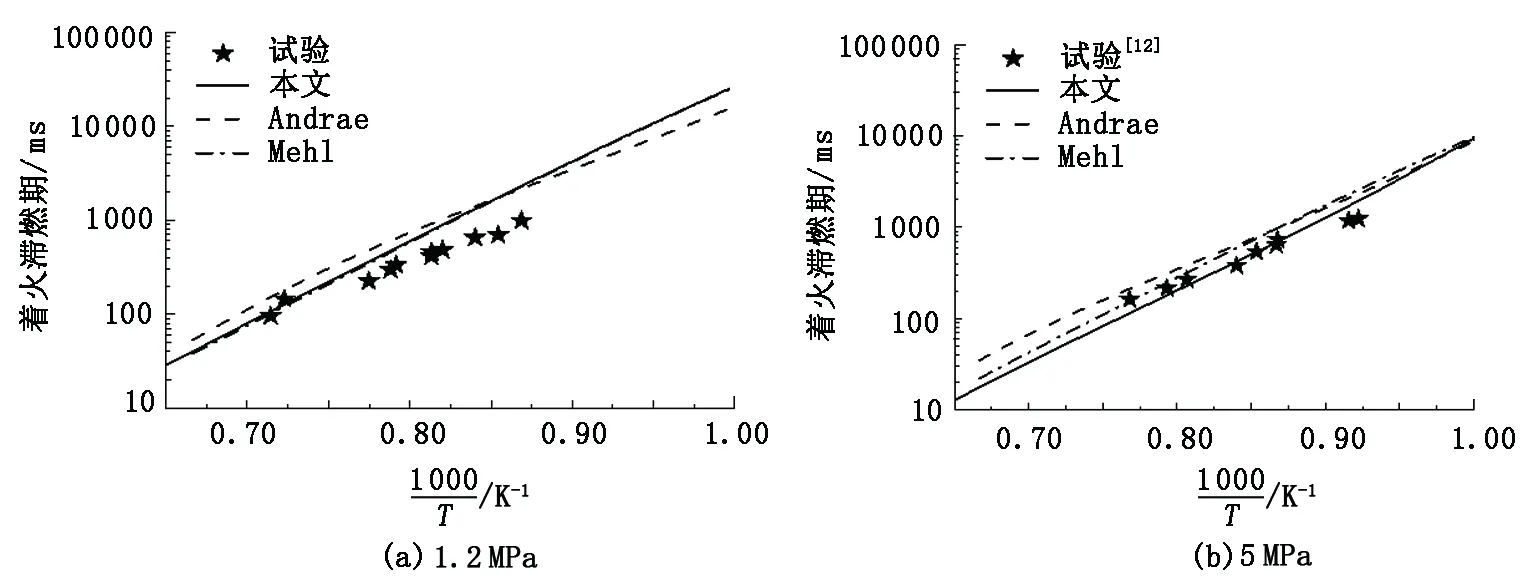
图6 甲苯在激波管中滞燃期计算值与试验值对比(Φ=0.25)Fig.6 Comparison of modeling and experimental results of toluene ignition delay in shock tube(Φ=0.25)
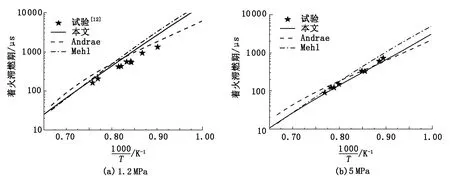
图7 甲苯在激波管中滞燃期计算值与试验值对比(Φ=0.5)Fig.7 Comparison of modeling and experimental results of toluene ignition delay in shock tube(Φ=0.5)
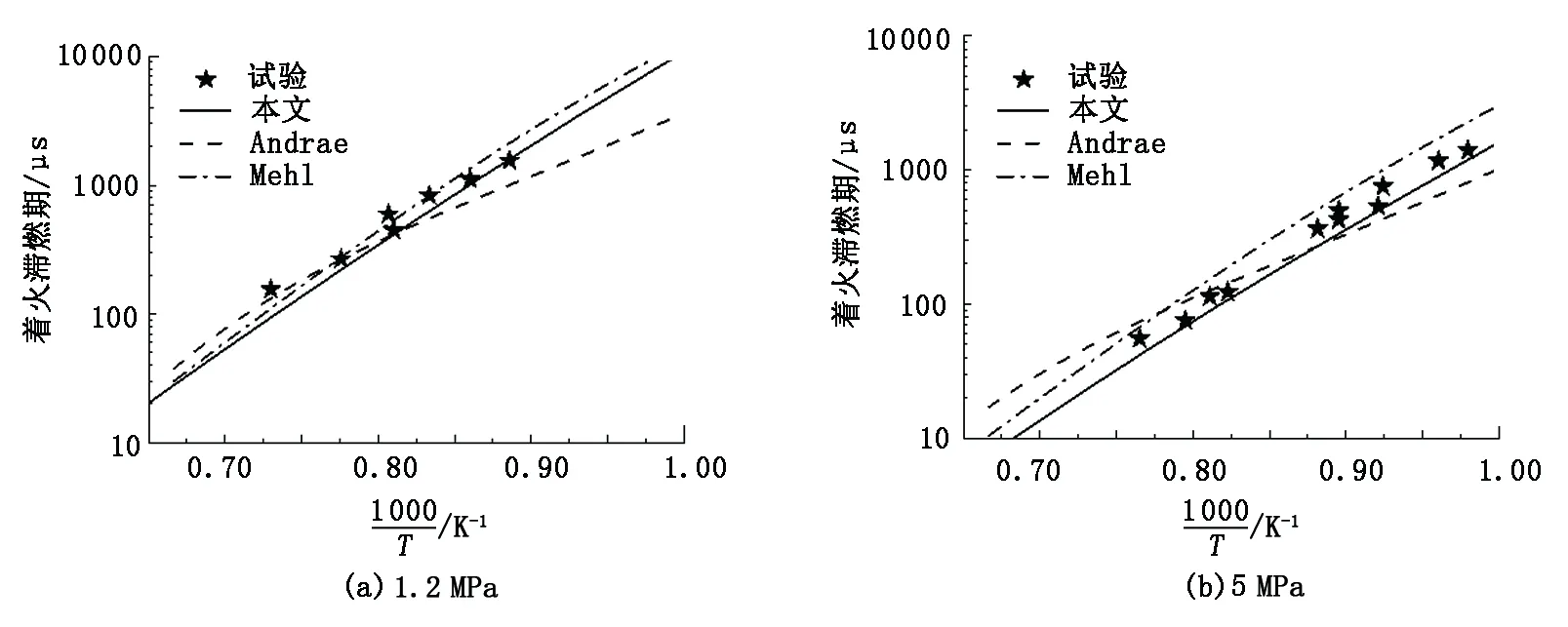
图8 甲苯在激波管中滞燃期计算值与试验值对比(Φ=1.0)Fig.8 Comparison of modeling and experimental results of toluene ignition delay in shock tube(Φ=1.0)
Davidson等[23]也在激波管中测量了甲苯/空气在类似发动机工况下的着火延迟时间,初始反射波温度为855~1 269 K,压力为1.4~5.9 MPa,当量比Φ为0.5和1.0。图9给出了当量比分别为0.5和1.0,压力5 MPa下简化机制计算值与Davidson测量值的对比情况。由图9可见,整个温度区间内简化机制的预测值与试验值变化一致。总体来说,本文简化机制在较宽的温度和压力条件下对滞燃期的预测结果与试验结果的拟合均比较好,说明当前机制能够很好地预测甲苯的着火特性。
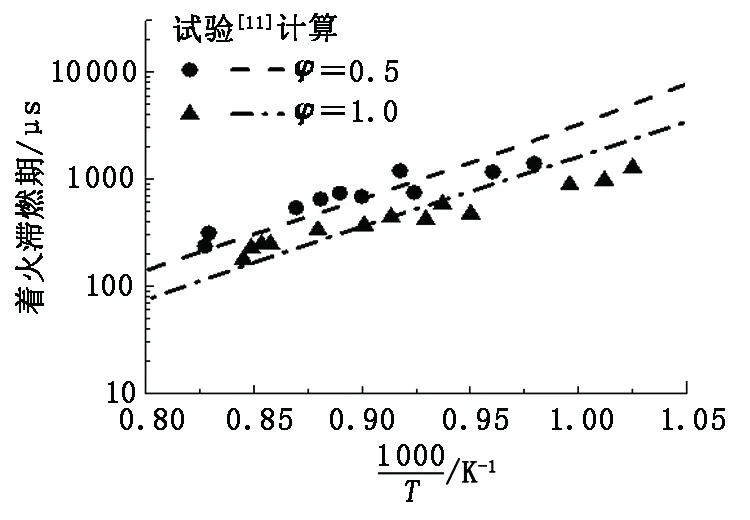
图9 甲苯/空气滞燃期计算值与试验值对比Fig.9 Simulating and experimental results of toluene/air ignition delay
2.2 射流搅拌反应器验证
Dagaut等[9]应用射流搅拌反应器测量了甲苯氧化反应过程中主要组分的浓度变化情况。试验工况为:压力0.1 MPa,温度1 000~1 375 K, 当量比0.5~1.5,甲苯含量0.15%,采用N2稀释。图10给出了主要组分的计算值与Dagaut试验数据对比情况,其中(a)的当量比为1.0,滞留时间为0.1 s;(b)当量比为1.5,滞留时间为0.12 s。从图9中看出,C6H5CH3和O2的计算结果与试验数据能够较好吻合,中间组分CO和CH2O变化趋势与数值也较为一致,C14H14含量随温度升高先增后减,简化模型能捕捉这一变化规律,只是整体变化过程提前,这可能与简化模型中的反应路径大量减少相关。除此之外,DRGEP简化方法采用的反应速率是通过定容均质反应器模块模拟得到的,而这与实际的射流搅拌反应之间存在差异。通常认为在两种情况下可认为模型预测结果较为准确:一是模型曲线与试验曲线拟合非常好;二是模型预测组分的最大摩尔系数在试验测量值的两倍以内。因此该简化机制可认为能够模拟搅拌反应器内组分浓度变化规律。
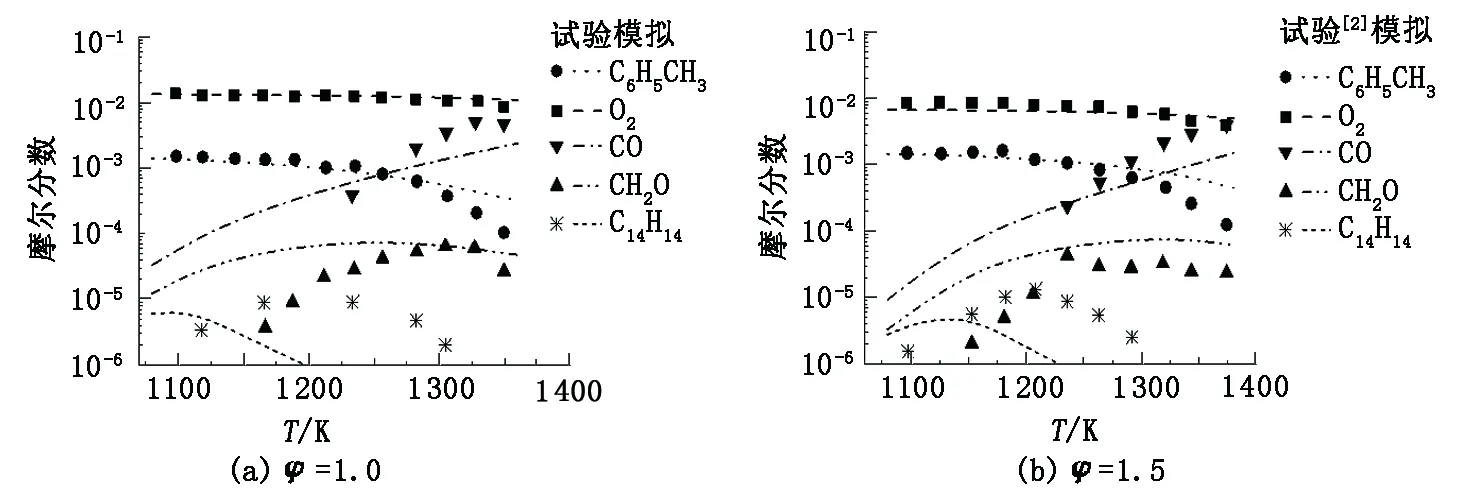
图10 主要组分摩尔分数的计算值与试验数据对比Fig.10 Comparison of intermediates mole fraction for calculated results and experimental data
Moreac等[24]同样应用射流搅拌反应器测量了较高压力、He气稀释下甲苯氧化过程中的主要组分演变过程。试验工况:压力为1 MPa,温度为550~1 180 K,甲苯含量为0.15%,当量比为1.0,滞留时间为1.0 s。图11为使用简化模型的计算值与试验值对比。由图11可知,该简化模型对CO和CO2的预测稍微延迟,但整体来看简化模型可以捕捉组分的演变规律。
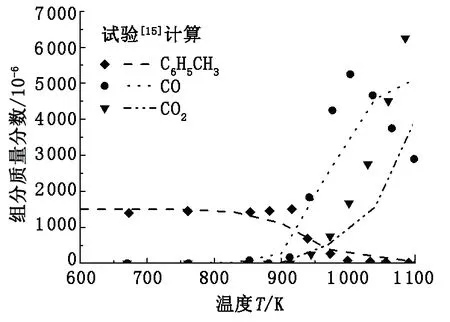
图11 主要组分含量的计算值与试验值对比Fig.11 Comparison of main mass fraction for calculated and experimental data
2.3 HCCI发动机
为了进一步了解简化机制在HCCI发动机中的预测性能,与Metcalfe[14]详细机制进行了对比。图12为两种机制的预测结果。计算中使用的发动机参数与2.2节相同,图12(a)是当量比0.25,进气压力0.1 MPa,不同进气温度时的缸内峰值温度和峰值压力;图12(b)是进气温度500 K,当量比0.25,不同进气压力时的计算结果;图12(c)是进气温度500 K,进气压力0.1 MPa,不同当量比时的计算结果。从图12中可以看出,进气温度增加,峰值温度明显升高,峰值压力有所降低;进气压力增加,峰值温度无明显变化,而峰值压力明显升高;当量比增加,峰值温度和峰值压力都会增大。在文中的计算工况下,简化机制的预测值与详细机制计算结果吻合良好。
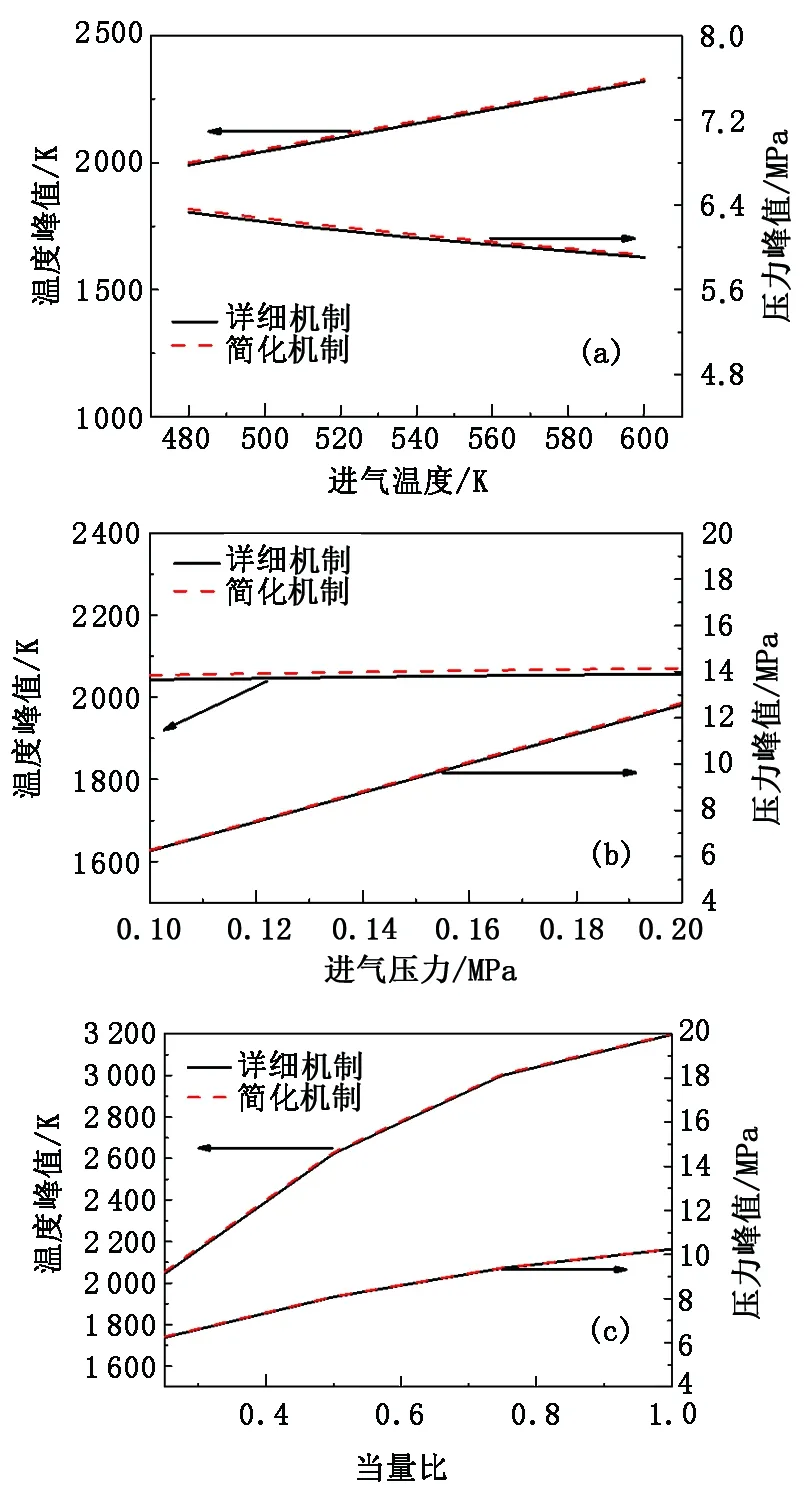
图12 简化模型与详细模型峰值温度、压力计算对比Fig.12 Comparison of peak temperature and pressure for reduced and detailed kinetic models
3 结 论
(1)构建的甲苯简化反应动力学模型包括48个组分和176个反应,模型得到广泛验证。
(2) 甲苯被OH基氧化脱氢的反应,C6H5CH3+OH=C6H5CH2+H2O,在浓混合气条件下抑制系统反应的进行,而在稀燃时会促进系统氧化反应,增加系统温度。
(3)苯甲基除了直接氧化为苯甲醛(C6H5CHO),还有一条重要间接反应途径:通过C14H14路径生成。
(4)与O-OC6H4O2相关的反应对着火有重要影响,C6H4CH3与O2形成O-OC6H4CH2的过程随温度升高延迟着火作用增强。

