放线菌产杀虫物质的初步鉴别及其活性评价
张遵霞 张亚妮 方伟 张志刚 王开梅 万中义


摘要:从中国四川乐山地区采集的土样中分离到1株放线菌HBERC-21542,农药活性测定发现其发酵粗提物对农业害虫具有很好的杀虫活性。对HPLC半制备组分进行农药活性测定结果表明,其杀虫活性成分出峰时间在14~19 min。根据HPLC-MS图谱特征确定了活性物质的分子离子峰及分子量,结合UV吸收光谱及文献数据,初步确定其为聚醚化合物费棱西霉素A。对发酵提取物进行HPLC制备后,获得了纯度在90%左右的纯品,在50 μg/mL浓度下,其对小菜蛾、棉铃虫的杀虫效果达到90%~100%。
关键词:天然产物;杀虫活性;放线菌;费棱西霉素A
中图分类号:S476 文献标识码:A 文章编号:0439-8114(2018)07-0061-04
DOI:10.14088/j.cnki.issn0439-8114.2018.07.014
Identification and Evaluation of a Natural Product with Insectcidal Activity Produced by an Actinomycetes Strain
ZHANG ZUN-xia, ZHANG Ya-ni, FANG Wei, ZHANG Zhi-gang, WANG Kai-mei, WAN Zhong-yi
(Hubei Biopesticide Engineering Research Center/The Branch Center of Biopesticide, Hubei Agricultural Sciences and Technology Innovation Center, Wuhan 430064, China)
Abstract: During the screening process of natural products produced by actionmycetes,a strain HBERC-21542 was isolated from soil samples collected in Leshan district,Sichuan province. The fermentation extract exhibited strong insectcidal activities against some insects such as Plutella xylostell,Helicoverpa armigera,etc. It was determined by components bioassay that the active compounds were in between 14~19 min in HPLC profile,and the active compound was identified as Ferensimycin A based on MS,UV absoption spectrum and natural product dictionary. Pure compound of 90% was obtained by preparative HPLC,and the lethal rate was 90%~100% at 50 μg/mL against Plutella xylostell,Helicoverpa armigera.
Key words: natural products;insectcidal activity;actinomycetes;Ferensimycin A
在生物源农药的研究及开发工作中,放线菌产生的活性天然产物是其重要来源。在国内市场上,农用抗生素占生物源农药市场份额的90%左右[1]。天然产物的重要性在于,一方面,它们可经过发酵、提取及剂型化等后处理过程制成生物农药,如现在广泛使用的生物农药阿维菌素、多杀菌素、井冈霉素、农抗120等[2];另一方面,以天然产物为模板,对其结构进行优化改造,是研发高效、低毒、绿色农药的另一途径,如阿米西达,就是以真菌产生的Strobilurin[3]为先导化合物经人工改造而获得的。
HBERC-21542是湖北省生物农药工程研究中心在农药活性天然产物筛选过程中,从四川乐山地区采集的土样中分离到的1株放线菌,其发酵提取物经室内生物测定,对多种农作物害虫靶标具有良好的杀虫活性,对发酵提取物进行HPLC半制备及自动收集,获得了不同时间流出的样品共36份,经生物测定,确定其活性成分在14~19 min。对提取物的HPLC-MS图谱分析后,确定了目标产物的紫外吸收波长及分子量,结合天然产物数据库比对,初步鉴定出活性产物的化学结构,并采用纯品进行了室内活性评价,以期为生物源农药的开发提供参考。
1 材料与方法
1.1 材料
1.1.1 菌种 放线菌HBERC-21542,分离自四川乐山地区采集的山地渣土,由湖北省生物农药工程研究中心分离保藏。
农药活性测定用虫:小菜蛾(Plutella xylostell)、棉铃虫(Helicoverpa armigera)、蚜虫(Aphis craccivora)。农药活性测定用草:浮萍(Lemna minor)、油菜(Brassica campestris)、狗芽根[Cynodon dactylon(Lynn.)]。
1.1.2 培養基
1)斜面培养基:ISP-2培养基。采用18 mm×180 mm玻璃试管,每管装琼脂培养基8~10 mL。
2)种子培养基:同ISP-2,不加琼脂,另加入2~4滴豆油作消泡剂。采用500 mL带挡板三角瓶,每瓶装培养基100 mL,121 ℃灭菌30 min。
3)发酵培养基:主要成分为葡萄糖、棉子蛋白、酵母浸粉等。采用500 mL带挡板三角瓶,每瓶装培养基100 mL,121 ℃灭菌30 min。
1.1.3 主要设备及软件、数据库 LYO-0.8型冰冻干燥机(上海东富龙科技有限公司生产);Büchi Evaprator R-200型旋转蒸发仪、Waters高效制备液相色谱仪(Waters 2525泵,带2767自动收集系统,2996二极管阵列式检测器)、Waters 2695高效液相色谱仪(Waters 2996二极管阵列式检测器)、Micromass Quattro micro ?誖质谱仪(电喷雾离子源ESI、正负离子模式);Masslynx V 4.1液质联用分析软件,查普曼(Chapman)天然产物数据库2003版。
1.1.4 主要化学试剂 乙腈、甲醇、乙酸,色谱纯(天津基准化学试剂有限公司);乙酸乙酯(西陇化工股份有限公司)。
1.2 方法
1.2.1 摇瓶发酵 在严格无菌条件下,从琼脂斜面取8~10 mm2的一块菌苔转移至种子摇瓶中,置旋转式摇床上28 ℃,150 r/min,振荡培养72~96 h,然后按10%(V/V)的接种量转接至发酵培养基中,在旋转式摇床上,28 ℃,150 r/min振荡培养100~120 h,即完成发酵。
1.2.2 发酵液的冻干及提取 将发酵液转移至不锈钢冻干杯中,置冻干机中冰冻干燥,冻干条件为 -40 ℃预冻2 h,冷阱预冷至-45 ℃以下,开启真空泵升华。真空度为10~30 Pa,升温速率为2~3 ℃/h,极限温度升为37 ℃。取出冻干粉后,小心转移至三角瓶中,先用少量50%(V/V)甲醇-水湿润,再加入100 mL乙酸乙酯,于摇床上180 r/min振荡萃取1 h,分离出酯相,旋蒸,除去溶剂,再以少量甲醇溶解后,送HPLC-MS分析。
1.2.3 生物活性测定 取1份发酵提取物,加入100 μL乙醇溶解,再加入900 μL去离子水,定容至1 mL。小菜蛾及棉铃虫采用24孔板进行农药活性测定,方法为涂布法。蚜虫农药活性测定采用浸叶法。组分农药活性测定采用相同的农药活性测定靶标及方法。
1.2.4 提取物的液质联用分析及制备 分析色谱柱为美国Sunfire C18柱,150 mm×2.1 mm(i.d),粒径3.5 μm,柱温40 ℃,进样量为2 μL,流动相为去离子水和色谱纯乙腈,梯度洗脱。半制备色谱柱为美国Sunfire OBD C18柱,250 mm×19 mm,粒径为10 μm,柱温为室温,进样量为800 μL,流动相为去离子水、乙腈,另加少量乙酸。质谱检测条件:电喷雾电离(ESI),毛细管电压为3.5 kV,锥孔电压为70 V,离子源温度为100 ℃,干燥气温度为300 ℃,脱溶剂气体流速为500 L/h,锥孔气体流速为50 L/h。
1.2.5 提取物的初步鉴别 根据半制备组分农药活性测定结果,确定活性成分的出峰时间,从HPLC图谱中,取得活性物质的紫外吸收光谱,从而确定吸收峰的波长。从ESI图谱中可判定目标产物的分子离子峰。将吸收峰波长及分子量输入Chapman天然产物数据库,可查询同该物质性质相同或相近的化合物名称及其化学结构,并有理化及生物学性质作比对,从而确定活性化合物的种类及其化学结构。
1.2.6 化合物纯品的制备 采用制备型 HPLC,每次进样量800 μL,流动相为乙腈和去离子水,加入少量乙酸,梯度洗脱,采用自动收集器收集目标组分,合并后用氮吹仪吹干。化合物纯度测定采用HPLC-MS分析。
1.2.7 化合物纯品的杀虫活性评价 称取纯度在90%以上的化合物纯品1 mg,加入100 μL乙醇溶解,其浓度为10 mg/mL,再以纯水稀释至1 000、333、100、50 μg/mL,采用涂布法进行农药活性测定,3次重复。
2 结果与分析
2.1 HBERC-21542粗提取物农药活性
由表1可知,在A、B培养基上,发酵提取物均有杀虫活性,但A培养基发酵提取物活性略差,这是由于在A培养基发酵条件下,该化合物很少或不产生的缘故。
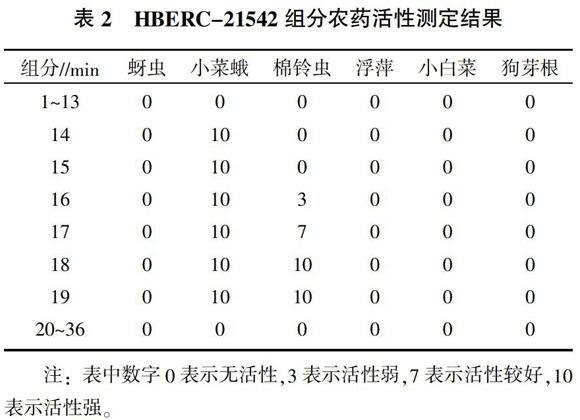
2.2 HBERC-21542提取物组分农药活性测定
从表2中可以看出,具有杀虫活性的组分出现在14~19 min,其余组分无活性。因此,判定活性峰应在15 min前后。
2.3 HBERC-21542提取物的HPLC-MS及紫外吸收光谱
由图1可知,10.63 min的峰为培养基杂峰,14.00 min为另一化合物的紫外吸收峰,活性化合物出现在15.17 min,而其正负离子流出现在15.26 min。
从图2可以看出,保留时间为15.17 min的化合物紫外吸收峰在195 nm,属末端吸收,可以认为此化合物在紫外区没有明显的吸收。
2.4 HBERC-21542活性产物的质谱图
从质谱图(图3)中可以看出,在正负离子流模式中,质量为627及629的两个质谱峰符合分子离子峰的特征,即其质荷比分别为M+1及M-1,次高峰687符合M-1+CH3COOH(627+60=687)的特点。在高质荷比区,分别有1 255及1 257质量数的离子出现,其丰度较低,可以判定其为二聚体。根据质谱图的上述特征,可以确定该化合物的分子量约为628 D。
2.5 活性化合物的初步鑒定
将化合物分子量及紫外吸收峰波长输入Chapman化合物数据库查询,条件为分子量介于627至629,紫外吸收峰值波长λ=0(0表示无紫外吸收峰即末端吸收)。查询得到两个化合物Feresinmycin A[4,5]和lysocellin[6],这两种化合物实际上是同一化合物的不同名称。因此,HBERC-21542的主要活性物质为费棱西霉素A。该化合物分子式为C34H60O10,分子量为628.842,结构式如图4所示。
2.6 活性物质纯品的杀虫活性评价
由表3可知,从室内农药活性测定结果来看,该化合物对小菜蛾和棉铃虫均有很强的杀虫活性。
3 讨论
在农药活性放线菌资源的筛选过程中,湖北省生物农药工程研究中心发现许多具有杀虫及抗真菌活性的天然产物,如尼日利亚菌素、猎神霉素等,它们均具有聚醚类结构。聚醚类抗生素对动物球虫类具有很强的杀虫活性,如莫能菌素等,常用作饲料添加剂,很少见到聚醚类抗生素作为农药使用的报道,惟一报道的是南昌霉素[7],它对很多农业害虫具有明显的防治效果。
结果表明,聚醚类抗生素对农业害虫具有较好的杀虫活性,另有试验结果证实,此类抗生素也具有相当广谱的抗真菌活性,因此,聚醚类抗生素具有开发成为农用抗生素的潜力。
参考文献:
[1] 邱德文.我国生物农药现状分析与发展趋势[J].植物保护,2007(5):27-32.
[2] 朱昌雄,宋 渊.我国农用抗生素的现状与发展趋势探讨[J].农药市场信息,2007(4):17-18.
[3] ANKE T,OBERWINKLER F,STEGLICH W,et al. The strobilurins——New antifungal antibiotics from the basidiomycete Strobilurus tenacellus[J].J Antibiot (Tokyo),1977,30(10):806-810.
[4] KUSAKABE Y,MIZUNO T,KAWABATA S,et al. Ferensimycins A and B. two polyether antibiotics. Taxonomy,fermentation,isolation,characterization and structural studies[J].J Antibiot(Tokyo),1982,35(9):1119-1129.
[5] WESTLEY J W,LIU C M,BLOUNT J F,et al. Isolation and characterization of four polyether antibiotics,X-14889A,B,C,and D,closely related to lysocellin and the ferensimycins[J].J Antibiot(Tokyo),1993,46(2):280-286.
[6] EBATA E,KASAHARA H,SEKINE K,et al. Lysocellin,a new polyether antibiotic.I. Isolation,purification,physico-chemical and biological properties[J].J Antibiot(Tokyo),1975,28(2):118-121.
[7] 歐阳谅,涂国全,高勇生,等.南昌链霉菌新种及其产生的两种杀虫抗生素[J].江西农业大学学报,1993(S4):148-153.

