研究血氧探头的结构形式对脉搏血氧饱和度测量的影响
邵秀稳 覃启路 张文忠 陆宇飞 郭嘉杰 万福瑞
1 广东省医疗器械质量监督检验所 深圳检验室 (广东 深圳 518000)2 深圳安维森实业有限公司 (广东 深圳 518000)3 广东省食品药品监督管理局审评认证中心 (广东 广州 510080)
血氧饱和度(SaO2)是指人体内进行氧化反应的血红蛋白占总量的比例,是诊断循环类、心血管类和呼吸类疾病的重要参数[1]。目前常见的检测方法分有创法和无创法,前者常被作为血氧饱和度检测的金标准;后者一般采用脉搏血氧仪设备对患者血氧浓度进行持续监测。脉搏血氧仪设备一般包括脉搏血氧仪主机和血氧探头。血氧探头由发光管和接收管组成,测量时发光管发射的红光和红外光线穿透动脉血管,被含氧血红蛋白和还原血红蛋白吸收[2]。吸收的光量随动脉血液做脉动变化,未被吸收的光线被接收管接收。经过光电转换,并经过主机内的标定曲线,电信号转化为血氧数值显示在仪器上。因此任何可以影响接收管接收光信号的因素都会影响测量结果。
本课题来源于实际工作,在日常注册检验中,检验人员常遇到血氧探头生产企业欲对不同结构形式探头之间的型号申请覆盖,如指夹式、指套式、一体缠绕式不同包裹方式中,选取一种作为主检型号,对其他两种型号申请型号覆盖。为了探讨在其他条件一致,仅包裹方式不同对SpO2测量值的影响,本课题组进行了该临床试验的研究。
1.资料与方法
1.1 临床资料
试验采用Nellcor生产的550型台式血氧监测仪,以及深圳安维森实业有限公司为本次试验特制的指夹式CF-3212-9型、指套式USL-3212-9型和一体缠绕式WP-3212-9型血氧探头进行试验。这三种血氧探头与测试部位接触的材料均为同颜色同材质的灰色硅胶材料,发光管、接收管等其他参数完全一致,仅包裹方式不同,探头样品如图1所示(注:CF-3212-9探头内部与皮肤接触处颜色与其他两种型号相同;测试过程中探头和被测手指加盖遮光罩)。
麻醉师将动脉插管放置在每个受试者的左手腕或右手腕中桡动脉里。操作人员将采集的动脉血液样品在OSM-3多波长血气分析仪(Hemoximeter,Radiometer,Copenhagen)上进行氧饱和度浓度的分析。
前2个血样是在受试者处于正常空气环境呼吸下采集的。之后低氧状态的每个平台都是通过控制受试者呼吸气体内中的氮气、空气和二氧化碳的比例,将受试者体内的氧气水平诱导至不同浓度(70%~100%)的预设平台进行采集,短暂的低血氧(50%~70%大约10min)不会危及健康受试者的心血管系统[3]。在进行不同浓度的控制时,采用气控调节监控系统(由Nellcor N560台式血氧监测仪、原装Nellcor血氧探头、计算软件及其他监护及显示配件组成)进行监控。采集前,必须保证平台的稳定性,每个血氧浓度平台上的稳定性要保持在30s左右,直至2个血样采集结束。每一轮6个浓度梯度,采集12个血样,两轮共24个血样。
1.2 方法

图1.血氧探头
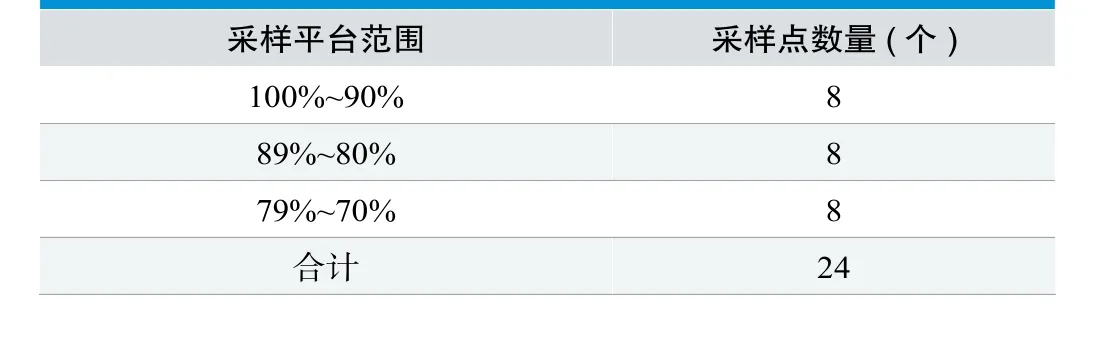
表1.血氧饱和度采样平台范围及采样点数量
纳入10~12名健康成人受试者,同时包含男性和女性,且为不同肤色(至少有两名具有黑色素沉淀的受试者或者该类受试者至少达到15%),参考相关标准[4]中的方法进行试验。每名受试者在表1中的3个血氧饱和度平台范围分别提供8个血样,即每名受试者共提供24个血样,12名受试者共提供288个血样,数据采用手动记录。
所纳入数据的血氧饱和度范围应均匀分布在70%~100%,即对于表1中列出的3个平台范围,每一平台范围包括大约96个数据。对于每一名受试者,其每一血氧饱和度范围的测量值至多为8个,以保证所采集的样本具有足够的代表性。
对于每名受试者均进行以下系列降低血氧饱和度的操作,每次操作首先从室内空气环境中自然浓度开始,然后将保持在各个低于室内氧气浓度的稳定氧浓度水平,血氧浓度目标数值如下:
第一轮:当前脉搏氧值(呼吸室内气体浓度下)、92%、87%,82%、78%、74%。
第二轮:100%(呼吸纯氧浓度下)、90%、85%、80%、75%、72%。
试验开始后,降低吸入氧浓度,然后通过观察气控调节监控系统的脉搏氧饱和度值和潮气末氧分压曲线的平稳情况,以判断是否达到稳定预期指标平台,稳定后(气控调节监控系统的读数在45s变动不超过1%,则认为这个平台是稳定的)才可以采样。当指标平台稳定后,先抽取废血约0.5mL,再抽取约1mL血样,抽样结束,记录550型台式血氧监测仪的SpO2数值;30s后再抽取约1mL血样,再记录550型台式血氧监测仪的SpO2数值。应及时用血气分析仪分析血样的SaO2值,并记录该值及其编号。
重复以上试验步骤,但需将SpO2降低到各个低血氧目标值(以保证受试者安全为前提),为了保持血氧探头部位动脉氧饱和度SaO2达到稳定平衡,所有血氧饱和度从一个平台改变到下一个平台时,应该至少稳定45s。
由于在这类实验中血氧中心值是持续变化的。血液在人体内循环需要时间,因此血氧饱和度在不同的时间,不同的测量部位是不同的,在30s内产生差异是正常现象。为了减少这些生理因素对数据的影响,需要确认每次血样采集是在同一个平台上进行,血气分析仪的读数与采集同时间的550型监测仪读数进行对比。如果在一平台上的两个血样,在血气分析仪上的数值变化超出2%,则对应的血样数值将被认为无效。
1.3 观察指标
根据ISO 80601-2-61:2011中201.12.1.101.2.2(国内等同YY 0784-2010《医用电气设备 医用脉搏血氧仪设备基本安全和主要性能专用要求》第50.101.2.2)进行数据分析,得到平均偏差Mean Bias(B)和准确度Accuracy(Arms)的统计结果。
平均偏差代表整体数据的偏移,用公式(1)表示:
准确度定义为测量值(SpO2i)与参考值(SRi)之差的均方根,用公式(2)表示:
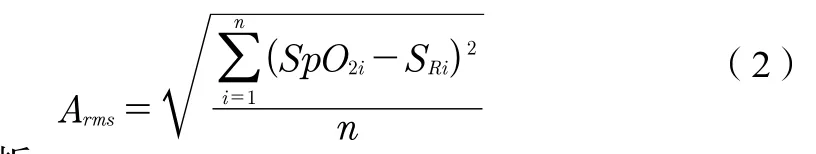
1.4 统计学分析
将血氧探头测得的SpO2与同步采集的动脉血的血气分析仪结果对比,进行统计分析和处理。
计算结果使用表格显示,表格中列明每个型号血氧探头分别在血氧范围80%~100%,70%~100%,70%~80%,80%~90%和90%~100%的平均偏差和准确度(均方根)等指标。
2.结果
本次受试对象为12名健康成人,其中8名男性,4名女性;5名白色皮肤,4名棕色皮肤,3名黑色皮肤。在本实验中,共采集了286个血样(第1名受试者在第一轮最后两个低血氧浓度时状态不佳,未进行2个血样的采集),其中第3名受试者的第1、2个血样,第10名受试者的第5、6个血样,第11名受试者的第11、12个血样,第12名受试者的第19、20个血样的血氧饱和度变化超出2%被排除;共排除8个读数,采集的有效读数为278个。统计结果见表2。
从表2中可以看出,指夹式、指套式和一体缠绕式血氧探头在70%~80%这个区间偏差较大,直接导致70%~100%区间的偏差增大。指夹式血氧探头在70%~100%的平均偏差和准确度分别为-2.30%和3.80%;指套式血氧探头在70%~100%的平均偏差和准确度分别为-3.66%和5.09%;一体缠绕式血氧探头在70%~100%的平均偏差和准确度分别为-1.52%和3.46%。
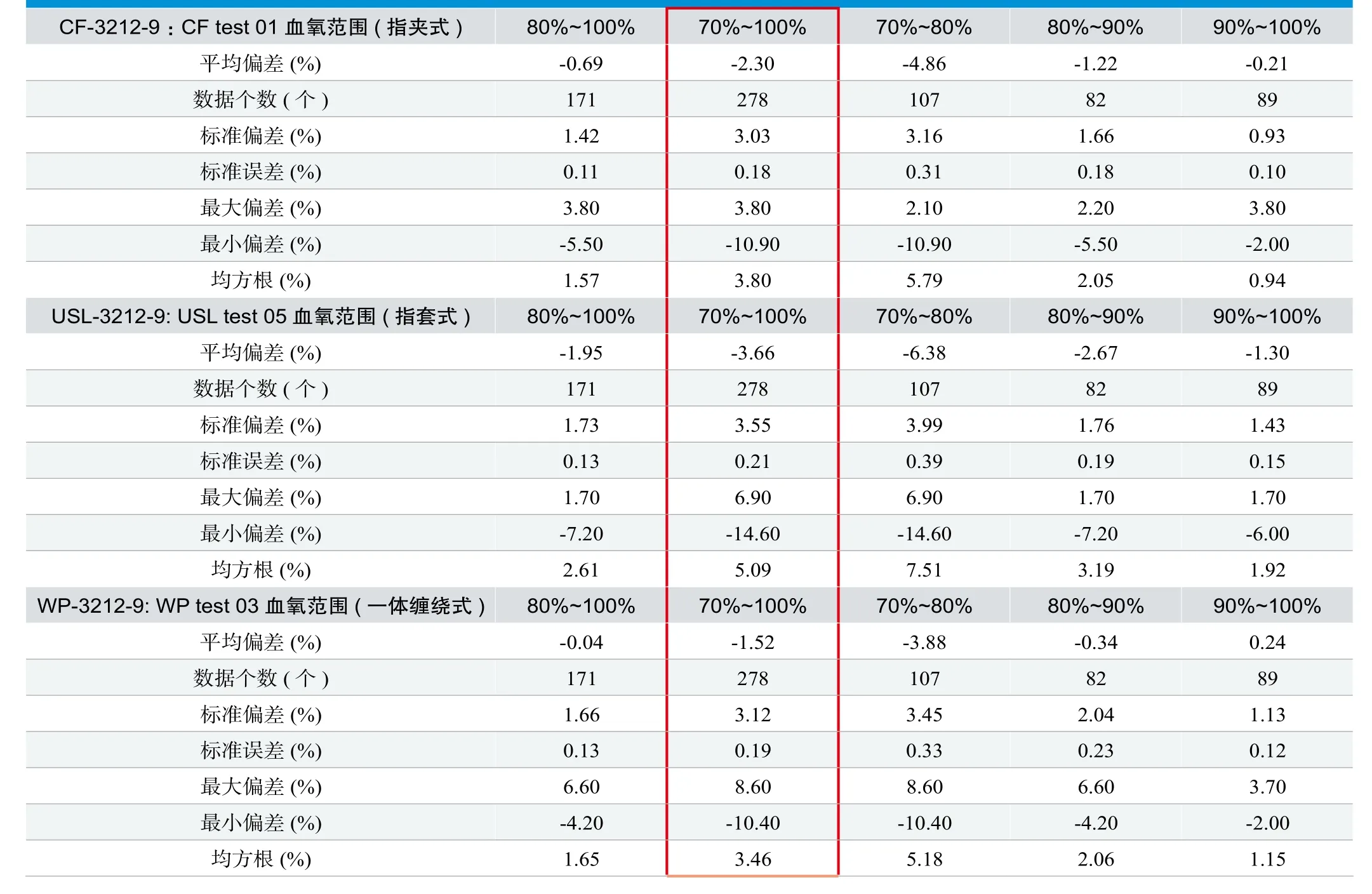
表2.三种型号血氧探头试验数据分析结果
3.讨论
如果血氧探头具有相同的组成材料和光电元器件,并且具有相同的结构形式、适用人群、与人体贴合方式、使用部位、规格参数和性能指标,则血氧探头可视为相似的[5]。从目前我国法规文件可知结构形式是设计血氧探头时要考量的重要因素之一。
从临床试验原始数据以及表2中数据分析结果均可以看出其他条件相同的情况下,三种不同结构形式的血氧探头测试结果是有差异的。指夹式和一体缠绕式数据相近,指套式测试结果与前两者相差较大。在SpO2测量过程中,探头内部被测手指周围的灰色硅胶材料对光有一定程度的吸收[6]。指套式血氧探头因自身结构原因,手指周围的硅胶面积较大;而其他两种血氧探头的硅胶面积较小且接近,测试结果也相近。在发光管发射光信号相同的条件下,三种血氧探头内部手指周围硅胶材料面积不同导致对光的吸收也不同,因此会造成接收管接收的光信号不同。
由血氧探头的工作原理可知,接收管接收的光信号变化是造成读数变化的主要原因。通过临床试验数据分析不难发现,血氧探头的不同结构形式影响接收管对光的接收量,进而对SpO2测量值有不同的影响。
[1]李皙茹.基于光电容积描记法的人体生理参数动态测量技术研究[D].中国科学技术大学,2017.
[2]国家食品药品监督管理总局.脉搏血氧仪注册技术审查指导原则(2017年修订版)[S].2017.
[3]Bickler PE, Feiner JR, Lipnick MS, et al.Effects of Acute, Profound Hypoxia on Healthy Humans: Implications for Safety of Tests Evaluating Pulse Oximetry or Tissue Oximetry Performance[J].Anesthesia & Analgesia,2017,124(1):146-153.
[4]国家食品药品监督管理局.YY 0784-2010,医用电气设备 医用脉搏血氧仪设备基本安全和主要性能专用要求[S].北京:中国标准出版社,2010.
[5]国家食品药品监督管理总局.脉搏血氧仪设备临床评价技术指导原则[S].http://samr.cfda.gov.cn/WS01/CL1421/144676.html.2016-02-19.
[6]https://baike.baidu.com/item/太阳光/10471684?fr=aladdin[OL].

