阿司匹林肠溶片2015年药典微生物限度检查法的建立及方法学验证
(云南省药物研究所 云南 昆明 650111)
杜春华 李东娴 和东阳 普冰清 牛延菲 游燕(通讯作者)
阿司匹林,主要成分为2-(乙酰氧基)苯甲酸,最早用于解热、镇痛、抗炎,在临床上,能够对于感冒发热、头痛牙痛以及关节风湿疾病等患者起到较好的镇痛效果,类别为:解热镇痛、非甾体抗炎药、抗血小板聚集药[1]-[4]。根据2015版药典要求,为了确认所采用的方法适合用于某制剂的微生物限度检查,必须对相应检验方法进行方法学验证。李秋菲等[5]按照中国药典2005年版一部对阿司匹林缓释片的微生物限度建立并验证了检查方法,发现其具有很强的抑菌作用,现在笔者通过2015年新版药典建立阿司匹林肠溶片微生物限度检查方法及方法验证。
1.仪器与材料
1.1 仪器
隔水式电热恒温培养箱(型号:GSP-9160MBE,上海博迅实业有限公司),生化培养箱(型号:LRH-150,上海一恒科学仪器有限公司),匀浆仪(型号:JT-C,漯河海德实验设备有限公司),二级生物安全柜(型号:BSC-1100ⅡB2-X,济南鑫贝西生物技术有限公司)
1.2 试药
1.2.1 供试品 阿司匹林肠溶片。
1.2.2 培养基
胰酪大豆胨液体培养基,批号170310;胰酪大豆胨琼脂培养基,批号1706282;沙氏葡萄糖琼脂培养基,批号170608;沙氏葡萄糖液体培养基,批号3106032;
麦康凯琼脂培养基,批号160303;麦康凯琼液体培养基,批号161228;pH 7.0 无菌氯化钠-蛋白胨缓冲液,批号1705184。(沙氏葡萄糖液体培养基来源于广东环凯微生物科技有限公司,其余培养基均来源于北京三药科技开发公司。)
1.2.3 pH试纸 pH精密试纸(6.4-8.0)、pH广泛试纸(1-14)均购于上海三爱思试剂有限公司。
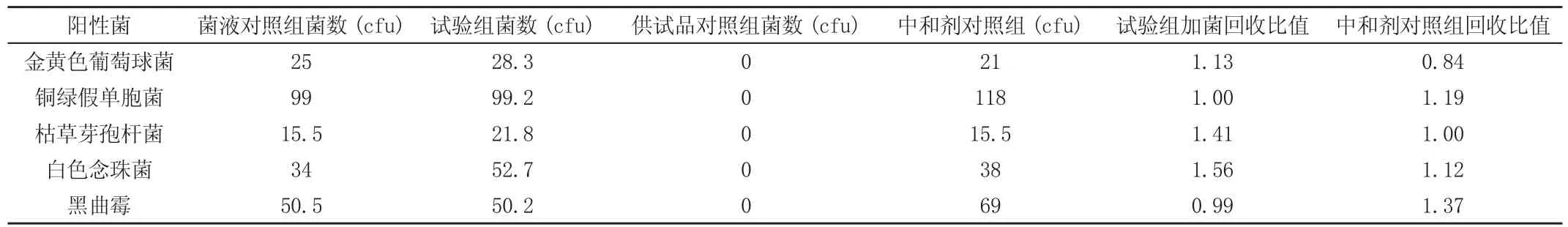
表1 需氧菌总数计数方法学验证结果

表2 霉菌和酵母菌总数计数方法学验证结果
1.3 试验菌株
铜绿假单胞菌[CMCC(B)10104]、金黄色葡萄球菌[CMCC(B)26003]、枯草芽孢杆菌[CMCC(B)63501]、黑曲霉[CMCC(F)98003]、白色念珠菌[CMCC(F)98001],上述5种菌种都来源于中国食品药品检定研究院。
2.方法与结果
阿司匹林肠溶片按《中国药典》2015版规定,需检查需氧菌总数,霉菌和酵母菌总数,控制菌检查大肠埃希菌。
2.1 菌液制备
金黄色葡萄球菌、铜绿假单胞、枯草芽孢杆菌、白色念珠菌、黑曲霉的的制备参照新版药典通则1105。制成每1ml含菌数小于100cfu的菌悬液。
2.2 供试液制备
取供试品10g,放入已灭菌的匀浆杯中,加入pH7.0无菌氯化钠-蛋白胨缓冲液50ml,匀浆至供试品均匀分散,用30%碳酸钠溶液,广泛和精密pH试纸调节供试品溶液pH至6.7,然后加缓冲液补足至100mL,即得1∶10的供试液。再逐级稀释为1∶20供试液。
3.方法适用性试验
3.1 需氧菌总数计数方法适用性试验
试验组:取1∶20供试液9.9ml于灭菌试管中,加入制备好的5种阳性菌液0.1ml,使其终浓度为每1ml含菌落数小于100cfu的菌液,从试管中吸取1ml注入灭菌平皿中,立刻倾注胰酪大豆胨琼脂培养基,待其凝固后,倒置于恒温培养箱中30~35℃培养48h。每个菌种平行制备2个平皿,测定试验组的菌落数。
供试品对照组:取1∶20供试液9.9ml于灭菌试管中,加缓冲液0.1ml,后续操作同试验组。
菌液对照组:取pH7.0氯化钠-蛋白胨缓冲液9.9ml于灭菌试管中,加入制备好的5种阳性菌液0.1ml,其余按试验组操作。
中和剂组:取30%碳酸钠稀释剂1ml,平行制备2个平皿,倒入胰酪大豆胨琼脂培养基混匀。
中和剂对照组:取30%碳酸钠稀释剂溶液9.9ml,加入试验菌悬液0.1ml,摇匀,其余按试验组操作。
阴性对照组:取pH7.0氯化钠-蛋白胨缓冲液1ml至平皿中,平行制备2个平皿,倾注胰酪大豆胨琼脂培养基。
计数方法适用性试验中,试验组菌落数-供试品对照组菌落数/菌液对照组菌落数的比值应在0.5~2范围内;中和剂对照组的菌落数与菌液对照组的菌落数的比值应在0.5~2范围内,结果见表1。
3.2 霉菌和酵母菌总数计数方法适用性试验
取1∶10供试液9.9ml于灭菌试管中,加入制备好的白色念珠菌、黑曲霉菌液0.1ml,其余操作同需氧菌总数计数方法适用性试验,培养基为沙氏葡萄糖琼脂,培养温度20~25℃,培养时间为72h,结果见表2。
3.3 控制菌检查方法的验证
试验组:取调过pH值的1∶10的供试液10mL至100mL胰酪大豆胨液体培养基中,再加入小于100cfu 的大肠埃希菌 1mL,其余操作和结果判断按2015版药典通则1106进行。阴性对照组:取pH7.0氯化钠-蛋白胨缓冲液 1mL 按大肠埃希菌检查法操作。试验组应检出大肠埃希菌,阴性对照组不得检出。试验结果表明,大肠埃希菌检查可采用常规法。
4.讨论
新版药典要求将试验菌加入供试液中,进行挑战试验,从而更加客观地考察了微生物在整个试验过程中所受的影响[6]。本研究采用30%碳酸钠溶液调节供试液的pH值呈中性后,取试验要求浓度的供试液9.9ml于灭菌试管中,加入制备好的试验菌菌液0.1ml,使其终浓度为每1ml含菌落数小于100cfu的菌液进行后续试验,通过三次验证的试验结果表明,药典规定验证用5种试验菌株的比值均在0.5~2范围内,阿司匹林肠溶片微生物限度检查可依据上述试验方法进行。
《中国药典》2015年版提出[7],若试验中使用了中和剂,那么应设立中和剂对照组,以此来确认所使用的中和剂不影响污染微生物的生长。本研究中采用了30%碳酸钠溶液作为中和剂,用于调节其pH值,可以消除供试品的抑菌性。笔者在做试验设计时,做了中和剂组和中和剂对照组,且二者的菌落数比值在0.5~2之间,说明30%碳酸钠稀释剂不影响污染微生物的生长。
[1] CHAN T-A,MORIN P J,VOGELSTEIN B,et al. Mechanisms underlying nonsteroidal antiinflammatory drug-mediated apoptosis[J].Proc Natl Acad Sci US A,1998, 95(2):681-686.
[2]李才正,苗佳.阿司匹林的临床应用进展[J].华西医学,2012,27(7):988-991.
[3]许桂萍,马热也木·克日木.阿司匹林的药理特性及其临床应用[J].中国农村卫生2015(14):28-29.
[4]国家药典委员会.中国药典[S].二部.北京:中国医药科技出版社,2015:545.
[5]李秋菲,周志云,罗世书.阿司匹林缓释片微生物限度检查方法验证[J].安徽医药,2008,12(12):1240-1241.
[6]徐晓洁,冷佳蔚,王志宏,丁勃.具有抗菌活性的中药固体制剂微生物限度检查计数方法研究[J].中国药事,2015,29(9):946-950.
[7]国家药典委员会.中国药典[S].四部.北京:中国医药科技出版社,2015:142.

