奥曲肽联合奥美拉唑治疗肝硬化并上消化道出血的临床效果
尹琴琴
(成都军区总医院消化内科 四川 成都 610081)
肝硬化是临床内科常见进行性发展疾病,实则为纤维性、弥漫性肝实质病变,而上消化出血是肝硬化晚期严重并发症之一,出血量大常表现出黑便、呕血等症状,病情紧急而凶险,死亡率高。肝硬化病机复杂,而临床治疗合并上消化道出血的关键措施在于尽早止血,同时配合肝脏病变基础治疗[1-3],本文将探析对肝硬化合并上消化道出血患者应用奥曲肽、奥美拉唑联合疗法的临床效果,特择取2015年5月—2018年1月期间入我院接受治疗的84例肝硬化合并上消化道出血患者进行了研究分析,现报道如下。
1.对象和方法
1.1 对象
取2015年5月—2018年1月期间入我院接受治疗的84例肝硬化合并上消化道出血患者,其中男45例,女39例,年龄33~74岁,平均年龄(53.56±13.55)岁;呕血量700~1200(950±130)ml;肝硬化程度按Child-Pugh分级,其中A级患者20例、B级45例、C级19例;肝硬化类型分布:酒精性10例、肝炎后60例、血吸虫性4例、胆源性10例,所有患者住院前二十四小时内均存在黑便、呕血症状,经临床明确诊断为“肝硬化并上消化道出血”。根据临床不同药物治疗方案将其化为联合组(44例,奥曲肽、奥美拉唑联合治疗)和对照组(40例,常规垂体后叶素治疗)两个组别,两组对象肝硬化程度、呕血量、一般资料对比,差异无统计学意义(P>0.05),组间有可比性。
1.2 方法
所有患者治疗前均接受系统检查,包括尿常规、心电图、肝功、肺功、肾功等,确诊后接受常规综合治疗,措施有给氧、禁食、血容量补充、抗感染、保肝等,以此为基础,对照组给予患者常规垂体后叶素治疗,垂体后叶素注射液(注射剂;国药准字H2026637;生产企业:南京新百药业有限公司)10U溶入20ml 50%浓度的葡萄糖注射液中,静脉注射给药,之后以每分0.2~0.4u的速度电脑输液持续泵入给药,维持时间72小时。另外给入奥美拉唑治疗,奥美拉唑(规格 40mg;国药准字H20046453;生产企业:锦州九泰药业有限责任公司)40mg溶入100ml 0.9%生理盐水中,静脉滴注给药,每天两次,持续使用72h,共计给药6次。联合组给予患者奥曲肽、奥美拉唑联合治疗,奥美拉唑用法用量同对照组,奥曲肽(国药准字H20041558;吉林一心制药股份有限公司出品)0.1mg溶入20ml 0.9%浓度生理盐水中,缓慢推注给药,之后72小时电脑输液持续泵注给入,剂量控制在每小时25ug[4-5]。治疗过程中严密观察止血情况,必要时需及时采取其他更有效的治疗方案,记录不良反应。
1.3 观察指标
记录分析止血时间、住院时间、止血后48h内再出血率和不良反应发生情况。总疗效判定:显效,治疗2d后止血,无呕血,抽出胃液检测色泽基本呈澄清状,大便色泽改变,血压、脉搏等体征恢复正常;有效经3d治疗症状及体征有一定改善;治疗≥5d仍有少量再出血状况,大便检查呈阳性,生命体征不稳定,胃液抽出检查色泽呈淡红色或咖色。
1.4 统计学方法
将数据纳入SPSS19.3统计软件分析,计数资料比较“t”检验,并以(±s)“平均值±标准差”表示;或纳入卡方以“χ2”比较,百分比表示,若P值低于0.05则为有统计学意义。
2.结果
2.1 总疗效对比
研究结果显示联合组患者治疗总有效率86.4%明显高于对照组的67.5%(P<0.05),见表1。

表1 疗效对比情况[n(%)]
2.2 住院指标对比
联合组患者止血时间及住院时间均较对照组更短(P<0.05),见表2。
表2 住院指标(±s)
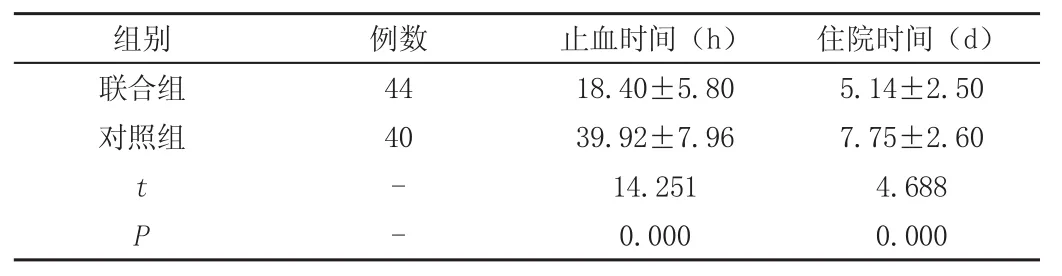
表2 住院指标(±s)
组别 例数 止血时间(h) 住院时间(d)联合组 44 18.40±5.80 5.14±2.50对照组 40 39.92±7.96 7.75±2.60 t-14.251 4.688 P-0.000 0.000
2.3 不良反应及事件情况对比
联合组患者止血48h内再出血率%明显低于对照组的%(P<0.05);此外,两组患者均未出现严重不适,仅个别病例表现出轻微胸闷、腹部不适症。
3.讨论
肝硬化并上消化出血病情凶猛,可直接威胁患者生命安全,作为肝硬化严重并发症,上消化道出血的关键因素为食管-胃底静脉曲张破裂,常合并胃黏膜损伤、消化性溃疡,是肝硬化失代偿期高压门脉侧支循环建立、开放的最后结果,为控制病情有效止血是关键,而基于病理治疗的重要环节是降低门静脉及其周边侧支循环血管压力[6-9]。
奥曲肽为人工合成八肽化合物,与十四肽人生长抑素类似,治疗肝硬化上消化道出血药理作用和天然激素基本一致,而且在胰高血糖素、生成素及胰岛素的抑制作用中效果更强。和生产抑素一样它能抑制LH对GnRH的反应,内脏血流降低其中尤其对门脉血流有减少效果,压力下降利于上消化道止血,此外药理能有效抑制胃泌素、5-HT、糜蛋白酶、血管活性肠肽、胰高血糖素、血管活性肠肽和胃动素,从抑制胃酸分泌入手,促进了胃溃疡面愈合,进而降低上消化道再出血发生率[10-11]。奥美拉唑是一种消旋混合物,目的性强,能针对性降低胃酸分泌,是胃壁细胞中酸泵的一种特殊抑制剂,它呈弱碱性,补入患体后迅速在酸性环境的胃部浓缩转化成活性物质,抑制K+-ATP质子泵、H+。两种药物联用能起到抑制胃酸分泌,释放活性物质,促进溃疡面愈合等效果[12-15]。本次研究结果显示,与对照组相比,联合组患者平均止血时间更短、住院时间短、疗效更优、止血后48h内再出血率更低 (P<0.05),可见奥曲肽联合奥美拉唑治疗止血疗效迅速;此外两组患者均未出现严重不良反应,用药安全性也是值得肯定的。
综上,奥曲肽联合奥美拉唑治疗肝硬化并上消化道出血止血迅速,可促进管壁恢复,减少再次出血概率,而且患者不良反应少,有效性、安全性兼顾,临床应用价值高。
[1]王磊,赵培西,朱彦荣,等.奥美拉唑、埃索美拉唑与泮托拉唑治疗上消化道出血的成本-效果分析[J].中国医院用药评价与分析,2010,10(1):42-44.
[2]张健,吴友伟,史丽萍,等.奥曲肽联合奥美拉唑治疗肝硬化并上消化道出血的疗效评价[J].实用临床医药杂志,2013,17(19):97-99.
[3] Lee DY,Kim JW,Lee MG et al.Pharmacokinetic interaction between oltipraz and omeprazole in rats: Competitive inhibition of metabolism of oltipraz by omeprazole via CYP1A1 and 3A2, and of omeprazole by oltipraz via CYP1A1/2,2D1/2, and 3A1/2.[J].European journal of pharmaceutical sciences,2007,32(4/5):328-339.
[4]阮旭东.奥曲肽联合奥美拉唑治疗肝硬化并上消化道出血[J].中国基层医药,2012,19(18):2781-2782.
[5]贺延新,宋晓华,李敏,等.奥曲肽并奥美拉唑治疗肝硬化并上消化道出血的效果[J].青岛大学医学院学报,2010,46(6):543-544.
[6] Salimi,A.,Enferadi,Z.,Noorbakhash,A.et al.Sensitive amperometric detection of omeprazole and pantoperazole at electrodeposited nickel oxide nanoparticles modified glassy carbon electrode[J].Journal of solid state electrochemist ry,2012,16(4):1369-1375.
[7]潘宏强,唐国文,蔡政友,等.垂体后叶素联合奥曲肽治疗肝硬化并上消化道出血的疗效[J].实用临床医学,2014,15(1):10-12.
[8]羊海峰.奥曲肽联合奥美拉唑治疗肝硬化并上消化道出血的疗效分析[J].中外医学研究,2015,(20):46-47.
[9]郭映泉.观察奥曲肽并奥美拉唑治疗肝硬化并上消化道出血的效果[J].医药前沿,2014,(14):273-274.
[10]田芸.肝硬化并上消化道出血予奥美拉唑联合奥曲肽治疗的探讨分析[J].中国医药指南,2013,(17):237-237,238.
[11]李利平,程继华.奥美拉唑联合综合护理干预治疗上消化道出血的疗效观察[J].中国医院用药评价与分析,2016,16(9):1201-1202.
[12]乔进朋,鲁力锋,王晓燕,等.奥美拉唑治疗非静脉曲张性上消化道出血的疗效观察[J].中国医院用药评价与分析,2009,9(4):311-312.
[13]李萍,邱忠伟.泮托拉唑治疗消化性溃疡合并上消化道出血的疗效观察[J].中国医院用药评价与分析,2016,16(9):1214-1216.
[14]钟华,钟冬梅.泮托拉唑联合奥曲肽治疗非静脉曲张性上消化道出血临床研究[J].中国医院用药评价与分析,2009,9(4):300-301.
[15] Zhang,W,Nan,FT,Guo,P et al.Simultaneous determination of tolbutamide, omeprazole,midazolam and dextromethorphan in human plasma by LC-MS/MS-A high throughput approach to evaluate drug-drug interactions[J].Journal of chromatography,B.Analytical technologies in the biomedical and life scienc es,2010,878(15/16):1169-1177.

