氢气对大鼠脑缺血/再灌注损伤线粒体功能的影响机制
张鑫磊 陈盼 夏裕宁 李雪梅 戴春光 谭永星桂林医学院研究生院(广西桂林 5400);桂林医学院附属医院护理部,重症医学科(广西桂林5400)
脑缺血/再灌注(I/R)损伤是临床常见的具有严重危害的病理生理过程,其损伤机制十分复杂,其中ROS自由基的大量生成及释放是造成细胞损伤的主要因素,并引起一系列的反应。线粒体是细胞内重要的细胞器,I/R发生时,线粒体结构破坏、功能受损,启动了线粒体途径的凋亡[1];其功能和结构的研究对于临床上I/R损伤的防治具有重要意义,并已成为当前该领域的研究热点之一。氢气是一种重要的生理性调节因子,研究[2]证实其在细胞和器官水平上具有明确的抗氧化应激、抗凋亡作用;本研究拟用大鼠局灶性脑I/R损伤模型,观察腹腔注射纯H2后对大鼠脑I/R后神经功能缺损评分及缺血皮质区神经细胞ROS生成率、线粒体膜电位水平变化、通透性转换孔(MPTP)开放度和线粒体肿胀度等影响,探讨氢气对大鼠脑I/R损伤脑皮质区线粒体功能和结构的调控机制与氧化应激时ROS生成率的相关性。
1 材料与方法
1.1 材料
1.1.1 实验动物 成年健康雄性SPF级SD大鼠,体质量为(230±10)g,由桂林医学院实验动物中心提供,许可证号:SCXK(桂)2013⁃0001。
1.1.2 氢气制备 使用纯水氢气发生器(济南浩伟实验仪器有限公司,型号SPE⁃300)产氢,电解纯水后氢气氧气比例为2∶1。
1.2 方法
1.2.1 动物模型制备及处理 随机将大鼠分为假手术组(Sham)、脑I/R组(MOD组)、氢气治疗组(H2组)。应用Longa等的方法改良,使大鼠大脑中动脉阻塞形成实验所需模型。此模型采用左侧颈内动脉线栓法。手术采用4%水合氯醛400 mg/kg腹腔注射麻醉。90 min后拔出栓线至颈外动脉残端内进行再灌注24 h。Sham组除不插入栓线外其余操作同上。H2组于拔出栓线时腹腔注射10 mL氢气,后每隔12 h注射1次。
1.2.2 神经功能缺损评分 采用Longa等的5级4分法进行神经功能缺损评分并记录神经功能症状,0分:正常,无神经损伤症状;1分:提尾时右侧前肢不能完全伸展;2分:行走时向右侧转圈;3分:行走时向右侧跌倒;4分:不能自发行走,意识水平下降。1~3分即为制模成功。
1.2.3 皮质区缺血神经细胞线粒体的提取 每组8只,I/R手术24 h后麻醉状态下用冰生理盐水经心脏灌注后取脑,按照线粒体提取试剂盒(索莱宝)步骤进行操作,整个提取过程在0~4℃下进行,线粒体含量以分离出的胞浆蛋白含量表示。提取出的线粒体进行后续检测。
1.2.4 ROS生成率测定 按照活性氧检测试剂盒(碧云天)操作。用荧光酶标仪进行检测(Tecan,In⁃finite F500)荧光强度变化情况(测定5~10 min,激发波长499 nm,发射波长521 nm)。测试过程保持37℃恒温。以荧光强度(RFU)来表示生成速率。
1.2.5 JC⁃1法测定△ψm水平变化 按照线粒体膜电位检测试剂盒(JC⁃1)说明操作,用荧光酶标仪进行检测,激发波长484 nm,发射波长590 nm,以荧光强度(RFU)来表示各组膜电位水平。同时将此样本用倒置荧光显微镜进行荧光拍照,正常线粒体内,JC⁃1聚集在线粒体基质中形成聚合物,聚合物发出强烈的红色荧光;不健康的线粒体由于膜电位的下降或丧失,JC⁃1只能以单体的形式存在于胞浆中,产生绿色荧光。
1.2.6 MPTP开放度测定 按照纯化线粒体膜通道孔红色荧光检测试剂盒(GENMED)说明操作,用荧光酶标仪进行检测,激发波长540 nm,发射波长580 nm,以荧光强度降低来表明MPTP增强。
1.2.7 线粒体肿胀度的测定 将提取的线粒体悬液分装出数份,加入蔗糖溶液,充分混匀后7 000g,4℃,离心10 min后去上清,重复洗涤1次。加入1 mL蔗糖溶液,混匀后移入清洁的比色杯中,再加入1 μL 200 mmol/L的CaCl2溶液充分混匀。用荧光酶标仪进行检测在单波长540 nm处每隔30 s连续监测3 min,记录数值。
1.3 统计学方法 实验结果用SPSS 18.0进行统计分析处理,所得的数值均以±s表示。各组间数据进行单因素方差分析比较,两两比较应用最小显著性差异法(LSD)检验。P<0.05为差异有统计学意义。
2 结果
2.1 SD大鼠神经功能缺损症状及评分 Sham组的大鼠无行为学异常,行动敏捷,反应正常;MOD组的大鼠精神不振,前进时向右侧转圈跛行,反应迟钝;H2组的大鼠行动较MOD组敏捷,行走较快且不转圈,反应较快,神经功能缺损评分明显低于MOD组(P<0.01)。见表1。
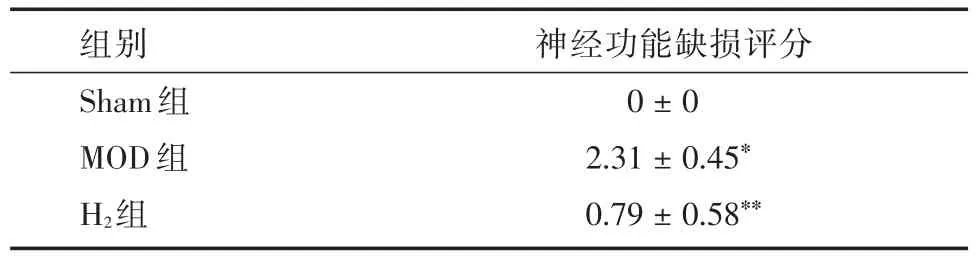
表1 各组大鼠神经功能缺损评分(n=6)Tab.1 Neurological deficit scores of rats in each group
2.2 ROS生成率 荧光强度的大小代表ROS的生成率,结果显示,与Sham组相比,MOD组ROS水平明显升高(P<0.01);与MOD组相比,H2组ROS水平有明显降低(P<0.01),见图1。
2.3 线粒体肿胀度的水平 线粒体肿胀时540 nm处吸光度下降,结果显示,与Sham组相比,MOD组线粒体肿胀度升高(P<0.01);与MOD组相比,H2组线粒体肿胀度降低(P<0.01),见图2。
2.4 △ψm水平及MPTP开放度 荧光强度的大小代表△ψm水平及MPTP开放度的高低,结果显示,与Sham组相比,MOD组△ψm水平降低(P<0.01)、MPTP开放度升高(P<0.01);与MOD组相比,H2组△ψm水平升高(P<0.01)、MPTP开放度降低(P<0.01),见图 3、4。荧光拍照显示,与Sham组相比,MOD组红色荧光减弱,绿色荧光增强;与MOD组相比,H2组红色荧光增强,绿色荧光减弱,见图5。
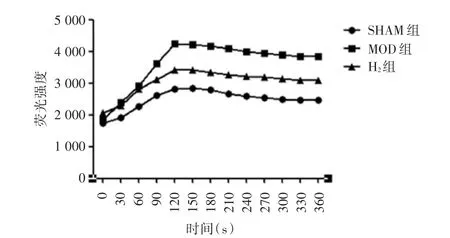
图1 R O S生成率Fig.1 Active oxygen generation rate
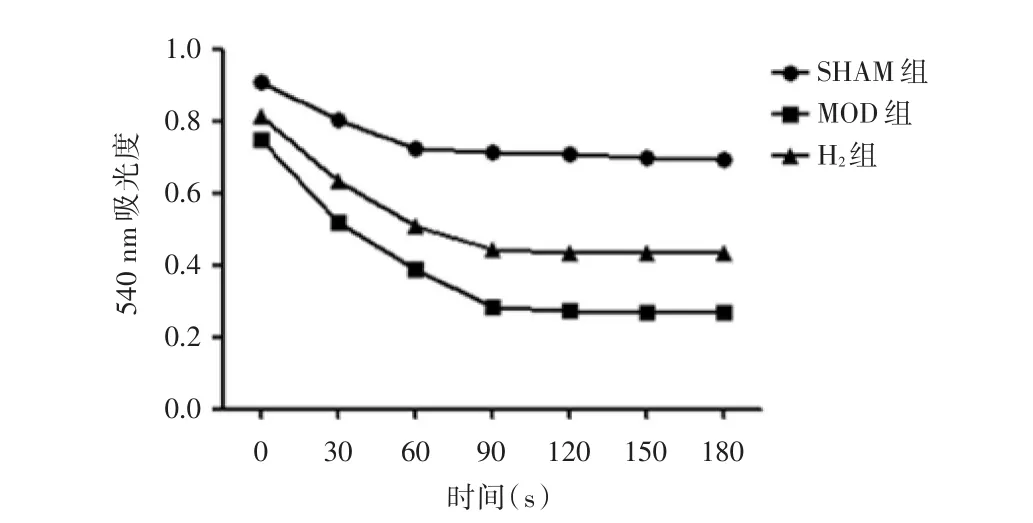
图2 线粒体肿胀度Fig.2 Mitochondrial swelling degree

图3 线粒体膜电位 图4 线粒体荧光拍照 图5 MPTP开放度Fig.3 Mitochondrial membrane potential Fig.4 Mitochondrial fluorescence photography Fig.5 Opening degree of mitochondrial permeability transition pore
3 讨论
目前研究发现[3-4],正常生理状态下ROS生成率处于低水平,当I/R使脑细胞产生损伤时ROS自由基的大量生成及释放引起氧化应激损伤;I/R同时可引起线粒体功能受损,最终造成细胞凋亡,但其具体机制及与ROS生成率的关系尚不明确。为探讨大鼠脑I/R皮质区神经细胞线粒体结构功能异常是否由过量的ROS引发和H2对神经细胞线粒体结构功能的保护作用机制。本研究拟采用大鼠局灶性脑I/R损伤模型,观察应用H2后对大鼠脑I/R后神经功能缺损评分及缺血皮质区神经细胞线粒体功能的影响。
线粒体作为细胞呼吸和物质氧化的中心,在各种细胞过程中发挥关键作用[5-7]。研究[8]表明,正常生理状态下,线粒体膜的完整性维持着△ψm及MPTP开放度处于正常水平。△ψm是由线粒体膜内负外正的电位差特性形成,其在维护线粒体内外物质平衡及保持线粒体正常功能方面发挥着重要作用。△ψm是线粒体合成ATP的动力,一旦△ψm消散和(或)电子传递受阻导致△ψm下降,可使细胞不能合成足够的ATP而无法完成正常的生命活动[10]。MPTP是反映线粒体功能及结构完整性的重要指标,防止其大量开放可有效预防脑I/R引起的神经细胞结构损伤及功能损害,现已逐渐成为关注的热点[11]。同时线粒体通常被认为是在I/R时ROS产生的主要场所,脑I/R损伤初期即有大量的ROS生成[9];本研究结果显示,Sham组没有发生I/R,ROS处于正常水平,未产生氧化应激损伤,线粒体功能指标△ψm,MPTP开放度,肿胀度都处于正常水平。MOD组因发生I/R,ROS生成率升高产生氧化应激损伤;同时△ψm,MPTP开放度,肿胀度都发生改变,线粒体功能受损。因此笔者猜测I/R时引起ROS升高,过量的ROS自由基破坏了线粒体膜,引起线粒体功能受损,△ψm水平下降,MPTP开放增加,线粒体发生肿胀。因此减少ROS的生成,维护线粒体结构完整性,稳定△ψm水平,抑制并阻断病理状态下MPTP不可逆的长时程开放,是脑保护的重要环节。
H2是一种重要的生理性调节因子,能通过气体扩散穿过血脑屏障和细胞膜及细胞器膜到达线粒体,具有明确的选择性抗氧化等脏器保护作用。国内外研究表明[12-15],呼吸氢气或注射饱和氢气生理盐水均可通过抗炎、抗氧化和抗凋亡等作用对大鼠脑缺血缺氧和脑创伤,以及对心脏、肺脏、肾脏I/R损伤产生明显保护作用。本实验采用电解水制取H2并直接腹腔注射,相比于呼吸氢气或静脉注射饱和氢气生理盐水效果更加确切,可控性更好。H2主要作用是选择性清除自由基,减少ROS的产生。活性氧具有很强的氧化还原作用,可以和细胞的各种成分发生相互作用,引起一些膜和酶的功能改变[16],尤其是线粒体膜损伤,导致细胞损伤,最终导致MPTP开放增加。所以应用氢气治疗后可以减少氧化应激的损害,从而使线粒体膜的破坏程度降低维持其完整性。实验结果中,使用氢气治疗后与MOD组相比,ROS生成率明显降低,膜电位明显升高,MPTP开放度降低,线粒体肿胀度降低,起到了保护线粒体功能的作用。本研究同时引入缺损功能评分检测,可以更直观地分析大鼠I/R损伤线粒体功能下降后在行为上的变化,以及氢气治疗后在行为表现上的改善效果。
综上所述,I/R同时腹腔注射纯氢气可改善大鼠I/R后的神经功能评分,对I/R损伤后的大鼠有明确的保护作用。其机制可能通过减少ROS生成,减轻氧化应激损伤,维持了线粒体膜完整性从而增强△ψm的稳定性限制线粒体MPTP开放,进而维持线粒体结构完整及功能稳态等有关。同时本研究仅从单方面分析了线粒体损伤的机制,存在许多不足,下一步将从细胞自噬方面来分析线粒体损伤的更多可能的机制。
参考文献
[1]FAIZI M,SEYDI E,ABARGHUYI S,et al.A Search for Mito⁃chondrial Damage in Alzheimer′s Disease Using Isolated Rat Brain Mitochondria[J].Iran J Pharm Res,2016,15(Suppl):185⁃195.
[2]袁楠楠,夏裕宁,张鑫磊,等.氢气对大鼠全脑缺血再灌注损伤海马CA1区神经元的保护作用[J].实用医学杂志,2016,32(6):870⁃874.
[3]JANKAUSKAS S S,ANDRIANOVA N V,ALIEVA I B,et al.Dysfunction of kidney endothelium after ischemia/reperfusion and its prevention by mitochondria⁃targeted antioxidant[J].Bio⁃chemistry(Mosc),2016,81(12):1538⁃1548.
[4]WANG Z,KANG B,LI W,et al.Hydrogen sulfide protects car⁃diomyocytes against apoptosis in ischemia/reperfusion through MiR⁃1⁃regulated histone deacetylase 4 pathway[J].Cell Physiol Biochem,2016,41(1):10⁃21.
[5]DYMKOWSKA D.Oxidative damage of the vascular endotheli⁃um in type 2 diabetes⁃the role of mitochondria and NAD(P)H oxidase[J].Postepy Biochem,2016,62(2):116⁃126.
[6]BIAAS A J,SITAREK P,MIKOWSKA J,et al.The role of mito⁃chondria and oxidative/antioxidative imbalance in pathobiology of chronic obstructive pulmonary disease[J].Oxid Med Cell Longev,2016,2016:7808576.
[7]GUEGUEN N,DESQUIRET V,LEMAN G,et al.Resveratrol directly binds to mitochondrial complex I and increases oxida⁃tive stress in brain mitochondria of aged mice[J].PLoS One,2015,10(12):e0144290.
[8]崔耀梅,程慧娴,曾宪明,等.富氢液对大鼠脑缺血/再灌注损伤后海马线粒体通透性转换孔及细胞凋亡的影响[J].中国药理学通报,2012,28(6):853⁃857.
[9]LI H,SUN J J,CHEN G Y,et al.Carnosic acid nanoparticles suppress liver ischemia/reperfusion injury by inhibition of ROS,Caspases and NF⁃κB signaling pathway in mice[J].Biomed Pharmacother,2016,82:237⁃246.
[10] ALIZADEH R,NAVID S,ABBASI N,et al.The effect of amino⁃guanidine on sperm motility and mitochondrial membrane poten⁃tial in varicocelized rats[J].Iran J Basic Med Sci,2016,19(12):1279⁃1284.
[11] TAMARA A,OLGA K,YULIA B,et al.Effect of the CRAC peptide,VLNYYVW,on mPTP Opening in rat brain and liver mitochondria[J].Int J Mol Sci,2016,17(12):2096.
[12] STOJANOVIC M,ZIVKOVIC V,SREJOVIC I,et al.The role of hydrogen sulfide in homocysteine⁃induced cardiodynamic effects and oxidative stress markers in the isolated rat heart[J].Physi⁃ol Int,2016,103(4):428⁃438.
[13] GAO Y,YANG H,FAN Y,et al.Hydrogen⁃Rich saline attenu⁃ates cardiac and hepatic injury in doxorubicin rat model by in⁃hibiting inflammation and apoptosis[J].Mediators Inflamm,2016,2016:1320365.
[14] 谭永星,夏裕宁,袁楠楠,等.PI3K/Akt/GSK⁃3β信号通路在氢抑制局灶性脑缺血再灌注诱发大鼠神经元凋亡中的作用[J].中华麻醉学杂志,2016,36(9):1058⁃1062.
[15] 刘宁,王薇,张蕊,等.富马酸氯马斯汀在肺缺血/再灌注损伤中对TLR4表达的影响[J].实用医学杂志,2016,32(18):2988⁃2991.
[16] MADUNGWE N B,ZILBERSTEIN N F,FENG Y,et al.Criti⁃cal role of mitochondrial ROS is dependent on their site of pro⁃duction on the electron transport chain in ischemic heart[J].Am J Cardiovasc Dis,2016,6(3):93⁃108.

