COMPASS系统在头颈部肿瘤调强放疗计划验证中的应用
彭莹莹,张书旭,张全彬,张国前,王琳婧
广州医科大学附属肿瘤医院 放疗中心,广东 广州 510095
引言
随着调强适形放疗技术的广泛应用,其质量保证和质量控制的实施变得尤为重要,剂量验证是调强放疗用于临床不可或缺的步骤[1-2]。传统的点剂量验证和二维平面剂量验证是目前常用的剂量验证方法[3-4]。因调强适形放疗技术的复杂性,还需对其进行三维剂量验证,进一步提高验证精度。COMPASS三维剂量验证系统能实现基于测量的照射野通量在病人CT图像上重建剂量分布,反映患者三维解剖结构上的真实受照情况。本文使用COMPASS三维剂量验证系统对头颈部肿瘤调强放疗计划进行剂量验证,探讨COMPASS系统在调强放疗剂量验证中的应用价值。
1 材料与方法
1.1 主要设备
Varian直线加速器,Varian Varis网络系统,Philips公司的Pinnacle V9.10放射治疗计划系统,IBA公司的COMPASS三维剂量验证系统(包括用于数据采集的带角度传感器的Matrixx二维电离室矩阵,固体水和用于剂量计算和分析的软件)。
1.2 计划设计
筛选8例头颈部肿瘤患者。男5例,女3例,年龄41~68岁,中位年龄54岁。其中鼻咽癌4例,胶质瘤2例,上颌窦癌2例。所有入组患者进行CT扫描后经网络传输至Pinnacle V9.10计划系统中,勾画大体肿瘤靶区GTV和临床靶区CTV,正常组织包括脊髓、脑干、晶体、腮腺。制订调强适形放疗计划,将放疗计划以Dicom格式分别传输至IBA COMPASS系统和Varian Varis网络中。
1.3 COMPASS系统进行剂量测量
(1)将Matrixx二维电离室矩阵采用Matrixx专用机头固定托架固定在机架上,加3 cm固体水于Matrixx表面作为剂量建成。
(2)在加速器上固定角度传感器用于测量Matrixx得到的每帧通量所对应的加速器机架角度。
(3)测量本底,使用6 MV X射线进行预照射后,重新测量本底。
(4)进行几何位置校准和绝对剂量校准。
(5)采集各个子野的照射野通量,测量时采用“Beam triggered”数据采集模式。
1.4 COMPASS软件分析
在COMPASS软件系统中的Patient 3D Dosimetry模块中对数据进行分析。计划系统传输的计划剂量为计划系统剂量,基于测量的照射野通量在患者CT图像上重建的剂量分布为重构剂量。针对患者的各感兴趣区域对比计划和实测两者的剂量体积直方图并进行三维Gamma分析。Gamma分析误差限定条件为3 mm/3%。
1.5 统计学分析
采用SPSS 13.0统计分析软件对数据进行分析。数值以(±s)表示。
2 结果
所有8例患者计划系统剂量和COMPASS实测重构剂量两者之间的靶区剂量差异及Gamma通过率,见表1。可以看出大体肿瘤靶区和临床靶区的Gamma通过率平均值均在95%以上。各靶区的计划系统剂量和重构剂量在D99、Dmean和D1的差异平均值均<3%。
表1 计划系统和COMPASS实测的靶区剂量差异(±s,%)
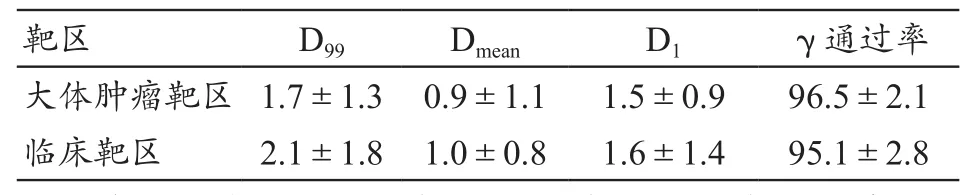
表1 计划系统和COMPASS实测的靶区剂量差异(±s,%)
?
计划系统剂量和重构剂量两者之间的危及器官剂量差异及Gamma通过率,见表2。可以看出脊髓和脑干的Gamma通过率平均值均在95%以上。脊髓和脑干的剂量差异平均值均<10%。
表2 计划系统和COMPASS实测的危及器官剂量差异(±s,%)

表2 计划系统和COMPASS实测的危及器官剂量差异(±s,%)
危及器官 D99 Dmean D1 γ通过率脊髓 5.1±2.2 4.9±3.1 4.8±3.5 97.1±3.7脑干 6.4±3.7 7.0±4.9 6.5±4.3 95.9±3.2
选取1例患者数据进行说明,计划系统剂量和COMPASS测量重构剂量的剂量分布图及两者之间的Gamma分析,见图1。对比图1a和b可以看出计划系统和COMPASS实测剂量两者之间的剂量学差异较小。该例患者靶区和危及器官的剂量体积直方图对比,见图2。虚线为计划系统剂量,实线为重构剂量。
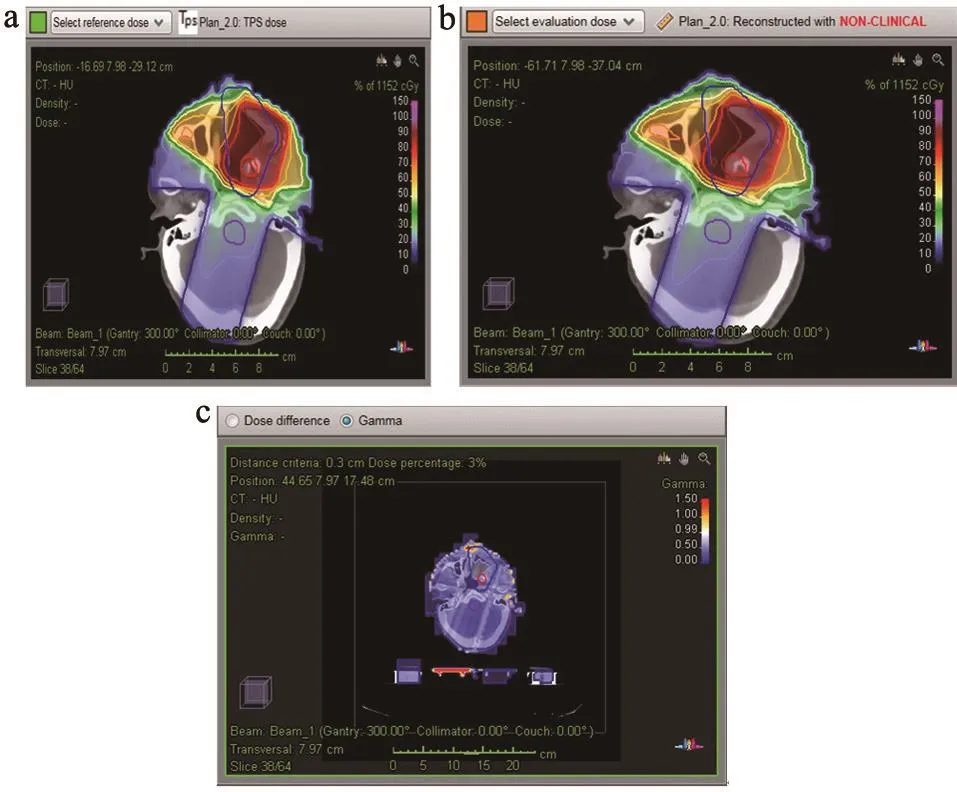
图1 计划系统和COMPASS实测的剂量分布及Gamma分析
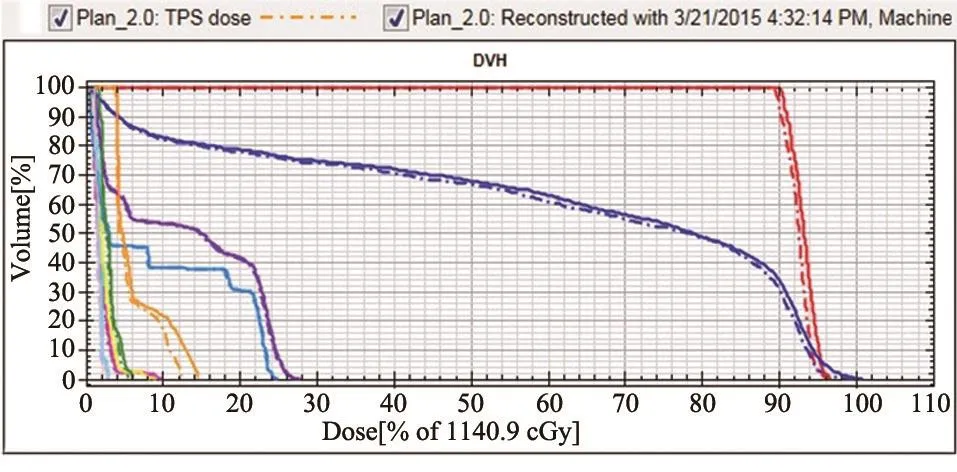
图2 计划系统和COMPASS实测的剂量体积直方图
3 讨论
相对于常规放射治疗和三维适形放疗技术,调强适形放疗技术能达到提高靶区剂量的同时更好的保护正常组织的效果。调强适形放疗技术具有靶区剂量精确,周围正常组织受照量小,靶区剂量分布均匀的特点,其应用越来越广泛。调强放疗技术治疗方式复杂,治疗过程中有很多不确定因素影响,调强计划实施的剂量是否准确与最终的治疗效果直接相关。因此,在治疗前进行剂量验证是必不可少的关键步骤。
目前,调强放疗剂量验证主要采用点剂量验证和二维平面剂量验证两种方式。使用单个指形电离室和剂量仪测量的单点绝对剂量测量结果准确,但获取的信息较少,不能很好的满足临床要求。二维平面剂量分为慢感光胶片和二维电离室矩阵测量,测量选定平面的相对剂量分布。胶片测量空间分辨率高,但费时费力,且测量结果受其他因素影响较大。二维电离室矩阵测量简便快捷,但Matrixx电离室矩阵两个探头间距为7.6 mm[5-6],受电离室矩阵排列间距的限制导致空间分辨率低,且仅能看到某一层面的平面剂量分布。因调强放疗技术的特点及复杂性,还需进行三维剂量验证以提高验证精度。
COMPASS三维剂量验证系统是一种基于测量的照射野通量在病人CT图像上重建三维剂量分布,反映患者三维解剖结构上的真实受照情况的剂量验证系统。与二维剂量验证相比,其结合了患者的解剖结构,并采用与临床治疗相同的照射方式进行验证,可以得到更丰富的三维剂量分布信息。张秀春等[7]对比分析了三维水箱测量和COMPASS系统测量的百分深度剂量、输出因子、离轴曲线等数据,结果显示出较好的一致性且平均偏差在2.5%以内,验证了COMPASS数据模型的可靠性。邢晓汾等[8]使用胶片和指形电离室对COMPASS系统的点剂量和平面剂量分布进行了测试验证,结果显示其剂量精度可满足调强放疗计划验证的要求。这都表明COMPASS系统可以作为可靠的临床剂量验证工具。
本文结果显示,肿瘤靶区的计划剂量和COMPASS实测剂量间Gamma通过率平均值均在95%以上。各靶区的计划系统剂量和重构剂量在D99、Dmean和D1的差异平均值均<3%。脊髓和脑干的Gamma通过率平均值均在95%以上。脊髓和脑干的剂量差异平均值均<10%。COMPASS系统剂量重构精度与治疗计划系统的精度较接近。Boggula等[5]对5例前列腺病例VMAT计划采用COMPASS系统进行了三维剂量验证,结果显示患者计划系统剂量和COMPASS测量结果两者靶区的D95和Dmean平均差异均小于2%。柏朋刚等[9]使用COMPASS系统验证了8例鼻咽癌容积旋转调强计划,结果显示8例患者靶区计划系统剂量和COMPASS测量结果的D95平均偏差均小于3%、Dmean均小于1%,靶区的Gamma通过率均大于95%。褚薛刚等[10]研究了COMPASS系统在8例宫颈癌病例的IMRT计划三维剂量学验证中的应用,结果显示Gamma通过率都在95%以上,靶区D95、Dmean、D2偏差均在3%以内。邢晓汾等[11]对12例食管癌病例采用COMPASS系统进行了三维剂量验证,结果显示COMPASS重建剂量和计划剂量有很好的吻合性。这都与本文结果一致。
COMPASS软件具有独立剂量计算功能,可根据探测器调试中预设的机器参数、计划系统传输的RT计划以及其射野模型进行剂量计算,通过比较计划系统剂量和COMPASS直接计算剂量可以检测放疗计划系统的计划计算精度,可作为第三方验证工具。COMPASS可实现计划系统传输剂量、COMPASS基于实测进行重构的剂量以及COMPASS直接计算剂量三者之间的三维Gamma分析,更进一步,具有剂量体积直方图分析功能。我们将在后续研究中对3种剂量进行对比分析。
相对于传统的二维剂量验证,三维剂量验证可以提供病人解剖结构上真实的三维剂量分布,能展示病人肿瘤和正常组织的实际受照情况。因此COMPASS系统是安全可靠的放疗质控设备,可以在病人的三维解剖结构上展示真实的剂量分布信息。
[参考文献]
[1] Ezzell GA,Galvin JM,Low D,et al.Guidance document on delivery, treatment planning, and clinical implementation of IMRT: report of the IMRT Subcommittee of the AAPM Radiation Therapy Committee[J].Med Phys,2003,30(8):2089-2115.
[2] Leybovich LB,Sethi A,Dogan N.Comparison of ionization chambers of various volumes for IMRT absolute dose verification[J].Med Phys,2003,30(2):119-123.
[3] Bucciolini M,Bounamici FB,Casati M.Verification of IMRT fields by film dosimetry[J].Med Phys,2004,31(1):161-168.
[4] Poppe B,Blechschmidt A,Kollhoff R,et al.Two-dimensional ionization chamber arrays for IMRT plan verification[J].Med Phys,2006,33:1005-1015.
[5] Boggula R,Jahnke L,Wertz H,et al.Patient-specific 3D pretreatment and potential 3D online dose verification of Monte Carlo calculated IMRT prostate treatment plans[J].Int J Radiat Oncol Biol Phys,2011,81(4):1168-1175.
[6] Dobler B,Streck N,Klein E,et al.Hybird plan verification for intensity-modulated radiation therapy (IMRT) using the 2D ionization chamber array I’m RT Matrixx-a feasibility study[J].Phys Med Biol,2010,55(2):N39-N55.
[7] 张秀春,胡彩容,陈开强,等.COMPASS验证系统在放射治疗中的应用研究[J].肿瘤预防与治疗,2012,25(5):273-279.
[8] 邢晓汾,褚薛刚,崔桐,等.调强放疗三维验证系统精度测试及临床应用研究[J].中华放射医学与防护杂志,2014,34(6):427-430.
[9] 柏朋刚,李奇欣,陈开强,等.COMPASS系统在鼻咽癌容积旋转调强剂量验证中的应用[J].中华放射医学与防护杂志,2012,32(3):304-307.
[10] 褚薛刚,邢晓汾,崔桐,等.CompassR在宫颈癌调强放疗三维剂量验证中的应用研究[J].中华放射医学与防护杂志,2015,35(7):548-549.
[11] 邢晓汾,褚薛刚,郑旭亮,等.Compass®在食管癌IMRT三维剂量验证中应用研究[J].中华放射肿瘤学杂志,2015,24(3):327-330.
[12] 陈旭明,姚升宇,许奕.宫颈癌调强放疗的三维剂量验证[J].中国医疗设备,2017,32(2):74-76.
[13] 林海磊,黄邵敏,邓小武,等.基于解剖在线测量调强放疗的三维剂量验证系统的测试与应用[J].中华放射肿瘤学杂志,2012,21(3):271-275.
[14] Boggula R,Lorenz F,Mueller L,et al.Experimental validation of a commercial 3D dose verification system for intensity modulated arc therapy[J].Phys Med Biol,2010,55(19):5619-5633.
[15] Nakaguchi Y,Araki F,Ono T,et al.Validation of a quick threedimensional dose verification system for pre-treatment IMRT QA[J].Radiol Phys Technol,2015,8(1):73-80.
[16] Lin H,Huang S,Deng X,et al.Comparison of 3D anatomical dose verification and 2D phantom dose verification of IMRT/VMAT treatments for nasopharyngeal carcinoma[J].Radiat Oncol,2014,9(1):1-7.