星点设计-效应面法优化苍桂颗粒提取工艺△
高梦洁,贾春燕,姜林*
(1.新疆医科大学中医学院,新疆 乌鲁木齐 830011;2.新疆医科大学附属中医医院 药学部,新疆 乌鲁木齐 830000)
过敏性鼻炎是鼻炎中最常见的类型,我国过敏性鼻炎的患病率近年来也有显著增加,可能与经济发展、工业化进程加速、生活方式改变有关。尽管过敏性鼻炎不会危及生命,但会影响生活质量,造成个人及社会的经济负担,儿童会因此影响学习成绩,严重者出现阻塞性睡眠呼吸障碍,甚至影响到颌面部发育[1]。因而对过敏性鼻炎作出正确的诊断,进行有效地预防及治疗就显得尤为重要。苍桂汤是新疆医科大学附属中医医院主任中药师李风森教授临床应用多年,在呼吸科得到广泛应用,治疗过敏性鼻炎疗效显著的处方。此药方传统剂型为汤剂,携带不便,易霉变,故拟将其改为颗粒剂,使其便于携带,质量稳定。本方由白芷、苍耳子、桂枝、辛夷等8味药组成,其中白芷、苍耳子、辛夷合而为君药,桂枝、荆芥为臣药,因白芷中的有效成分欧前胡素难溶于水,故在本方中以打粉加入。选择君药苍耳子和辛夷中的绿原酸、木兰脂素以及臣药中桂枝所含的桂皮醛为指标,优化本方提取工艺。且木兰脂素、绿原酸和桂皮醛相配合,均有治疗鼻炎的作用[2-4]。由于金黄色葡萄球菌、绿脓杆菌、乙型溶血性链球菌、肺炎链球菌、变形杆菌等为致鼻炎的主要菌种,故通过体外抑菌实验所得到的抑菌作用评分为药效学指标,结合化学成分指标,最终确定本方的提取工艺。本实验以综合评分(木兰脂素、绿原酸、桂皮醛、抑菌作用评分)为评价指标,采用响应面法优化提取工艺,为该制剂的工业化大生产提供实验依据。
1 仪器与材料
高效液相色谱仪(美国Waters 公司,PAD 检测器,Waters2695);AG-135电子天平(瑞士梅特勒-托利多仪器有限公司);超纯水仪(Millipore公司,Direct-QTM5);超声清洗仪(上海科导超声仪器有限公司);低温冷却液循环泵(郑州长城科工贸有限公司);可控温电热套(山东城华鲁电热仪器有限公司);电热恒温水浴锅(北京市永光明医疗仪器有限公司);电热恒温培养箱(上海市跃进医疗器械一厂,HH.B11.420)。
木兰脂素、桂皮醛,绿原酸(批号分别为110882-201607、110710-200714、110753-200413,供定量测定用,中国食品药品检定研究院);甲醇、乙腈为色谱纯;其他试剂均为分析纯;胰酪大豆胨液体培养基、胰酪大豆胨琼脂培养基(产品编号分别为HB4114-19、HB0177-1,青岛高科园海博生物技术有限公司)。
药材饮片均购自新疆维吾尔自治区中医医院,经李永和主任中药师鉴定,均符合2015 年版《中国人民共和国药典》相关项下的要求。实验用菌均购自新疆维吾尔自治区药物研究所。
2 方法与结果
2.1 木兰脂素含量测定
2.1.1 色谱条件与系统适应性 Symmetry C18色谱柱(150 mm×4.6 mm,5 μm);流动相:乙腈-四氢呋喃-水(35∶1∶64);流速:1.0 mL·min-1;柱温:30 ℃;检测波长:278 nm;进样量为20 μL。在此条件下样品中木兰脂素能达到良好的分离,理论板数按木兰脂素峰计算不低于3000[5-6]。
2.1.2 供试品溶液制备 取本方10倍量水提液50 mL,置分液漏斗中,用乙酸乙酯振摇萃取3次,分别为20、20、10 mL,合并萃取液,挥干,用适量甲醇溶解后,转入5 mL容量瓶中,用甲醇定容至刻度,摇匀,滤过,取续滤液,即得[7]。
2.1.3 对照品溶液的制备 取木兰脂素对照品适量,精密称定,加甲醇制成每l mL含0.18 mg的溶液,即得。
2.1.4 阴性供试品溶液制备 称取处方量缺辛夷药材,其他操作同2.1.2,结果见图1。
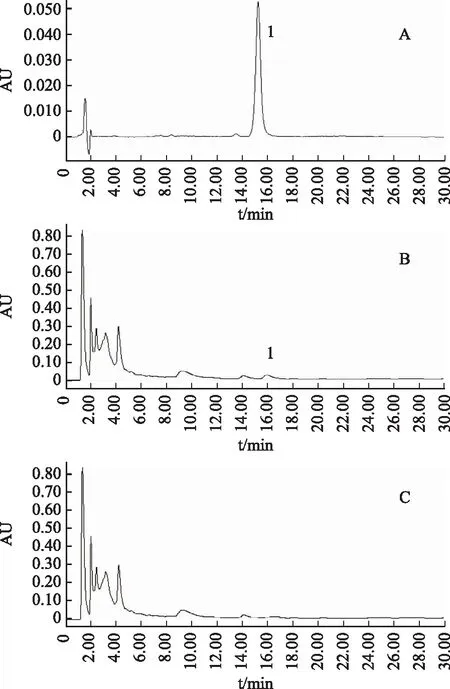
注:A.木兰脂素对照品;B.样品;C.阴性样品。图1 木兰脂素HPLC图
2.1.5 标准曲线的制作 精密称取木兰脂素对照品适量,精密称定,加入适量甲醇(色谱纯),配置成一定浓度的储备液;精密梯度吸取5个不同体积的储备液,分别置于相同体积容量瓶中,加甲醇(色谱纯)稀释至刻度,摇匀,即得。得标准曲线为Y=116 447.45X+1 127.9,r=0.998 2。
2.1.6 精密度试验 精密吸取对照品溶液,取对照品溶液按2.1.1项下色谱条件连续进样6次,计算木兰脂素峰面积的RSD为0.81%,表明仪器精密度良好。
2.1.7 重复性试验 用同一供试品溶液连续进样6次,每次进样量20 μL,根据结果计算重复性RSD为0.57%。
2.1.8 稳定性试验 取供试品溶液,分别在0、2、4、6、8、12、24 h测定样品木兰脂素峰面积,RSD为1.25%。
2.1.9 加样回收率试验 取已知浓度的待测溶液6份,精密加入2.5 mg的木兰脂素对照品,按2.1.2项下方法制备供试品溶液,按2.1.1项下色谱条件进行含量测定,其平均回收率为103.4%,RSD为2.24%。
2.2 桂皮醛含量测定
2.2.1 色谱条件与系统适应性 Symmetry C18色谱柱(150 mm×4.6 mm,5 μm);流动相:乙腈-水(32∶68);流速:l.0 mL·min-1;柱温:30 ℃;检测波长:290 nm;进样量为10 μL。理论板数按桂皮醛峰计算应不低于3000[8]。
2.2.2 供试品溶液的制备 取本方10倍量水提液,离心,取上清液5 mL,用甲醇定容于10 mL量瓶中,滤过,取续滤液即得。
2.2.3 对照品溶液的制备 取桂皮醛对照品适量,精密称定,加甲醇制成每l mL含0.4 mg的溶液。
2.2.4 阴性供试品溶液制备 称取处方量缺桂枝药材,其他操作同2.2.2,结果见图2。
2.2.5 标准曲线的制作 精密称取桂皮醛对照品适量,精密称定,加入适量甲醇(色谱纯),配置成一定浓度的储备液;精密梯度吸取5个不同体积的储备液,分别置于相同体积容量瓶中,加甲醇(色谱纯)稀释至刻度,摇匀,即得标准溶液。标准曲线为Y=525 491.8X-179 850.8,r=0.999 7。
2.2.6 精密度试验 精密吸取对照品溶液,取对照品溶液按2.2.1项下色谱条件连续进样6 次,计算桂皮醛峰面积的RSD为0.55%,表明仪器精密度良好。
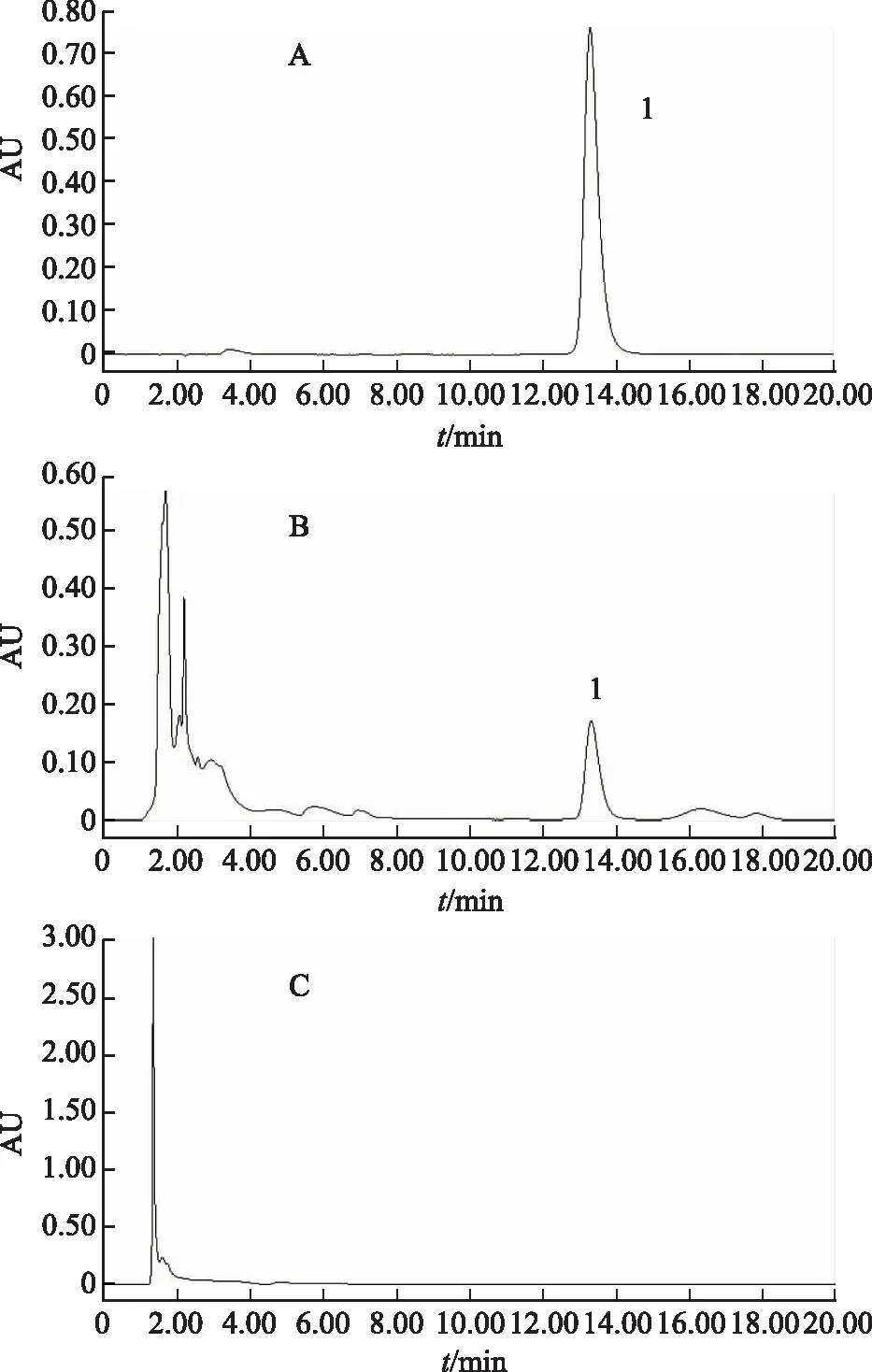
注:A.桂皮醛标准品;B.样品;C.样品阴性。图2 桂皮醛HPLC图
2.2.7 重复性试验 用同一样品连续进样6次,每次进样量10 μL,根据结果计算重复性RSD为0.33%。
2.2.8 稳定性试验 取同供试品溶液,分别在0、2、4、6、8、12、24 h测定样品桂皮醛峰面积,RSD为1.95%。
2.2.9 加样回收率试验 取已知浓度的待测溶液6份,精密加入3.3 mg的桂皮醛对照品,按2.2.2项下方法制备供试品溶液,按2.2.1项下色谱条件进行含量测定,其平均回收率为99.24%,RSD为2.78%。
2.3 绿原酸的含量测定
2.3.1 色谱条件与系统适应性 Symmetry C18色谱柱(150 mm×4.6 mm,5 μm);流动相:乙腈-0.4%磷酸(10∶90);流速:1.0 mL·min-1;柱温:30 ℃;检测波长:327 nm;进样量为10 μL。在此条件下样品中绿原酸能达到良好的分离,理论板数按绿原酸峰计算不低于3000[8]。
2.3.2 供试品溶液的制备 取本处方10倍量水提液,离心,取上清液10 mL,水浴蒸干,用甲醇5 mL溶解,滤过,取续滤液,即得。
2.3.3 对照品溶液的制备 取绿原酸对照品适量,精密称定,加甲醇制成每1 mL含60 μg的溶液,即得。
2.2.4 阴性供试品溶液制备 称取处方量缺苍耳子药材,其他操作同2.2.2,结果见图3。
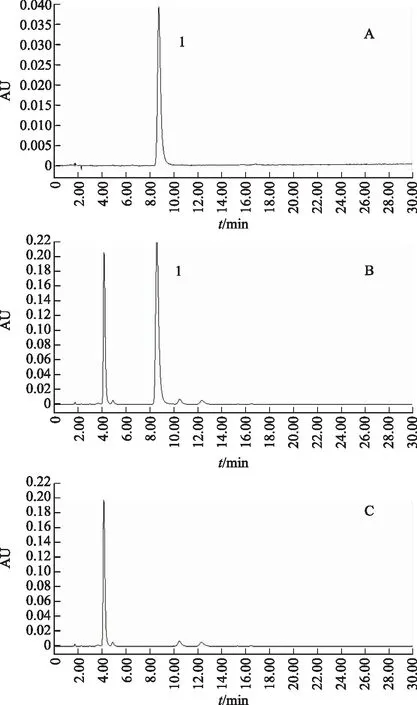
注:A.绿原酸对照品;B.样品;C.样品阴性。图3 绿原酸HPLC图
2.3.5 标准曲线的制作 精密称取绿原酸对照品适量,精密称定,加入适量甲醇(色谱纯),配置成一定浓度的储备液;精密梯度吸取5个不同体积的储备液,分别置于相同体积容量瓶中,加甲醇(色谱纯)稀释至刻度,摇匀,即得标准溶液。标曲为Y=1 221 440.541X+10 511.648 65,r=0.999 7。
2.3.6精密度试验 精密吸取对照品溶液,取对照品溶液按2.3.1项下色谱条件连续进样6次,计算绿原酸峰面积的RSD为0.18%,表明仪器精密度良好。
2.3.7重复性试验 用同一样品连续进样6次,每次进样量10 μL,根据结果计算重复性RSD为1.61%。
2.3.8 稳定性试验 取同供试品溶液,分别在0、2、4、6、8、12、24 h测定样品绿原酸峰面积,RSD为1.38%。
2.3.9 加样回收率试验 取已知浓度的待测溶液6份,精密加入9.6 mg的绿原酸对照品,按2.3.2项下方法制备供试品溶液,按2.3.1项下色谱条件进行含量测定,其平均回收率为101.08%,RSD为2.75%。
2.4 单因素试验
2.4.1 浸泡时间的考察 将提取次数固定为2次,提取时间固定为1.5 h,加水倍数固定为10倍,分别考察浸泡时间0.5、1.0、1.5、2.0、2.5 h对综合评分的影响,结果各评价指标含量在0.5~1.0 h呈递增趋势,1.0~2.5 h无明显变化,故以1.0 h为最佳浸泡时间。
2.4.2 提取时间的考察 将提取次数固定为2次,加水倍数固定为10倍,浸泡时间固定为1.0 h,分别按0.5、1、1.5、2、2.5 h进行提取,结果在0.5~1.5 h内各评价指标含量呈增长趋势,1.5 h后呈下降趋势,故以1.5 h为最佳提取时间。
2.4.3 加水倍数的考察 将提取次数固定为2次,浸泡时间固定为1.0 h,提取时间固定为1.5 h,分别按8、10、12、14、16倍进行提取,结果各评价指标含量在8~10倍呈递增趋势,10~16倍呈递减趋势,故以10倍为最佳提取倍数。
2.4.4 提取次数的考察 将加水倍数固定为10倍,浸泡时间固定为1.0 h,提取时间固定为1.5 h,分别按1次、2次、3次进行提取,结果各评价指标含量在提取1~3次呈增加趋势,但2次和3次相差不大,结合实际生产情况选取2次为最佳提取次数。单因素数据见表1。
2.5 体外抑菌实验
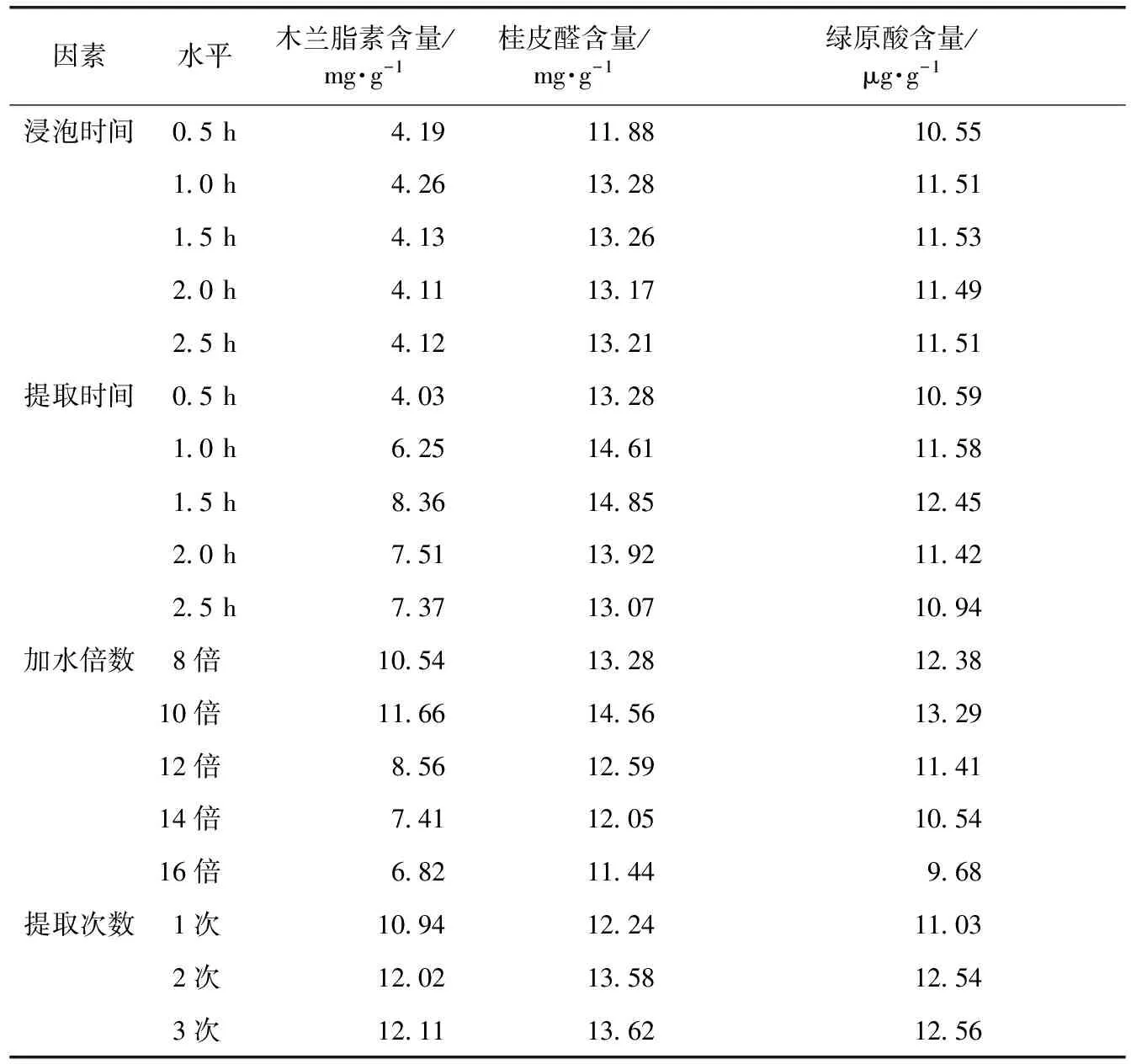
表1 单因素试验结果
按照单因素筛选出的结果提取药液,即浸泡时间1 h,提取时间1.5 h,10倍量水提取2次。以培养基将药液稀释成为每mL含总药材4、2、1、0.5、0.25、0.125、0.063 g共7个浓度,经高压消毒后,将活化的细菌(金黄色葡萄球菌、绿脓杆菌、乙型溶血性链球菌、肺炎链球菌、变形杆菌)加入上述培养基中,另设空白对照(有菌无药)管。因药物加入培养基后颜色太深,无法观察其混浊程度,影响结果判断,故恒温培养24~48 h后,将各管培养物划线接种于平板培养基上,再次培养24~48 h,观察实验菌生长情况,确定无菌生长的药物浓度即为最低抑菌浓度(MIC)[9-10]。将恒温培养24~48 h后的培养物涂布于琼脂培养基平板上,再次培养24~48 h,观察平板上菌落形成单位(CFU)。CFU≤5的浓度为杀菌浓度,记“-”号,CFU>5的浓度为无杀菌作用,记“+”号。以产生杀菌作用的最小浓度为最低杀菌浓度(MBC)。结果,本品对金黄色葡萄球菌、绿脓杆菌、乙型溶血性链球菌、肺炎链球菌、变形杆菌的最低抑菌浓度分别为2、2、2、2、2 g·mL-1,最低杀菌浓度分别为4、2、2、2、2 g·mL-1,结果见表2。证明本品具有一定的抑菌作用,可进入星点设计,进行提取工艺的优选。

表2 体外抑菌实验
2.6 提取工艺优选
2.6.1 响应面试验设计 在单因素试验基础上,选择浸泡时间、提取时间和加水倍数作为影响因素,固定提取次数为2次。抑菌作用需将提取液均浓缩至药物浓度2 g·mL-1,然后以涂布后所增长的菌落数进行数据处理(菌落数为0记为100分,菌落数多致无法计算记为1分,100-菌落数/100,即将分值正向化处理后得出每种提取工艺对5个菌抑菌作用的平均值,计算抑菌作用评分)后带入星点设计,综合评分(木兰脂素、桂皮醛、绿原酸含量,抑菌作用评分)为评价指标(根据本方中各化学指标对本方药效贡献程度的大小以及本方主要药效学指标的综合考虑,决定其权重系数分别为30%、20%、20%、30%),采用Design-Expert8.0.4软件Central Composite试验设计的方案进行研究,筛选最佳提取条件[11-12]。结果见表3~4。
2.6.2 模型的拟合采用 ANOVA对各因素进行多元二次回归,得到二次拟合方程为Y=82.68-0.73A-4.10B+9.36C-0.51AB-7.50×10-3AC+1.41BC-1.16A2-1.68B2-7.18C2。对其进行方差分析,可知B、C、B2、C2具有显著性影响,失拟项>0.05,表明失拟项不显著,相关系数r=0.970 1,表明回归方程拟合度较好,试验误差小,可用该模型对不同条件下的试验结果进行测定。根据回归分析结果,利用软件进行响应面分析,结果见图4。

表3 响应面试验设计及结果
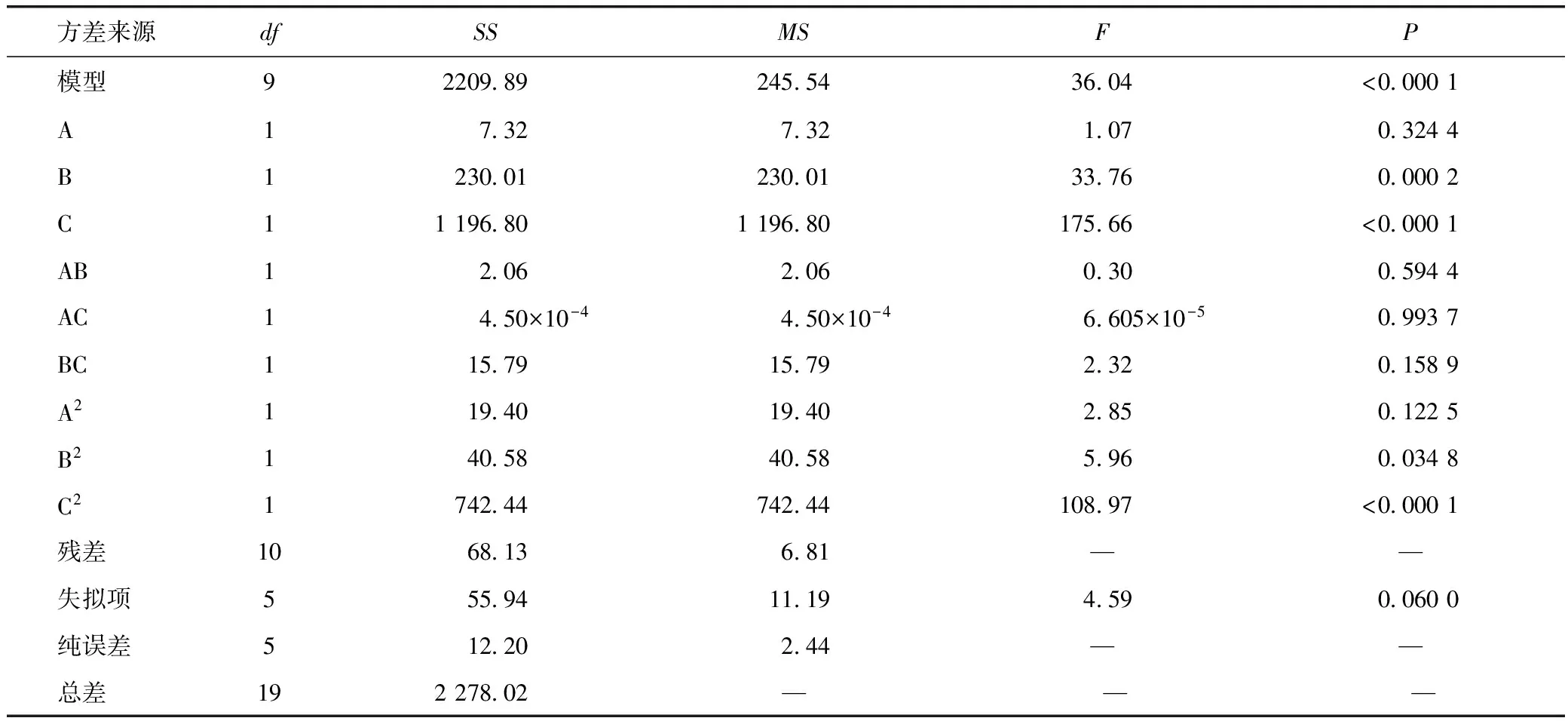
表4 方差分析
注:“—”为无法比较。

注:A.浸泡时间和水提倍数对综合评分的影响;B.水提倍数和提取时间对综合评分的影响;C.浸泡时间和提取时间对综合评分的影响。图4 提取工艺中各因素对综合评分的影响
2.6.3 验证试验 通过对实验数据的综合分析,可知最优工艺为浸泡56.96 min,加8.05倍量水提取2次,每次76.71 min。考虑到实际生产需要,将提取工艺定为浸泡60 min,加8倍量水提取2次,每次80 min。再进行3次验证试验,结果木兰脂素平均含量为9.58 mg·g-1;桂皮醛平均含量为11.33 mg·g-1;绿原酸平均含量为11.49 μg·g-1;抑菌作用平均评分为88.11%。综合评分与预测值的偏差为0.47%,表明该二项式模型拟合效果良好,可信度高。按最终提取工艺提取本方,做体外抑菌实验,进行涂布和划线,结果本品对金黄色葡萄球菌、绿脓杆菌、乙型溶血性链球菌、肺炎链球菌、变形杆菌的最低抑菌浓度分别为2、2、2、2、2 g·mL-1,最低杀菌浓度分别为4、2、2、2、2 g·mL-1。
3 讨论
本文通过单因素考察筛选出各因素的最佳范围进入星点试验,再通过星点设计,对提取工艺进行优化。本方为治疗鼻炎的经验方,以君药和臣药中主要成分为化学成分指标;所选取的5种菌是导致鼻炎的主要菌种,通过体外抑菌实验确定了本方对这5种菌具有一定的抑菌作用,故将抑菌作用评分作为本方的药效学指标。将药效学指标和化学成分指标相结合,综合评价提取工艺,进一步优化了本方的提取方法,这是本文的一个创新点,同时也为中药复方提取工艺的筛选提供了新思路。
[1] 温丽慧,杨正光,吕忠,等.低温等离子体治疗过敏性鼻炎32例报告[J].右江民族医学院学报,2008,30(1):103-104.
[2] 朱雄伟,杨晋凯,胡道伟.辛夷成分及其药理应用研究综述[J].海峡药学,2002,14(5):5-7.
[3] 甘晨曦,谢强,邓铮铮,等.谢强应用桂枝汤治疗鼻炎的合理用药经验[J].实用中西医结合临床,2013,13(4):69-70.
[4] 严永旺,肖兰,周旭,等.绿原酸的药理作用及药用研发对策[J].中国药房,2017,28(19):2729-2732..
[5] 曾江洪,刘灿辉.鼻炎糖浆质量标准研究[J].中国药业,2011,20(9):16-17.
[6] 李亚山,王立兴.高效液相色谱法测定鼻康喷雾剂中木兰脂素的含量[J].海峡药学,2011,23(12):59-60.
[7] 蒋华科,陈纯,陈玉秀,等.高效液相色谱法测定鼻敏方胶囊中木兰脂素的含量[J].中南药学,2007,5(4):335-337.
[8] 国家药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2015.
[9] 周龙强,饶伟源,李茂,等.苍鹅鼻炎片的药效学研究[J].中药药理与临床,2004,20(4):38-41
[10] 金桂芳,张文军,谭毓治.鼻炎滴剂抗炎消肿药效学研究[J].广东药学院学报,2009,25(3):295-298
[11] 张雪峰,杨轲,欧燕,等.星点设计-效应面法优化天山雪莲提取物磷脂复合物制备工艺[J].中草药,2014,45(16):2326-2332.
[12] 刘志雯,张玲玉,刘潇,等.响应面法优化葛黄片提取工艺[J].中成药,2017,39(4):838-841.

