pH响应型空心微球在CSTR中的振荡行为
路兴杰,赵 芳,谷田平,张 柯,闫继伟,朱永宏
(1.河南省计量科学研究院,河南郑州 450002;2.河南出入境检验检疫局,河南郑州 450002)
刺激响应型微球[1-3]会根据所受刺激信号做出相应的响应行为,在体积和形态等方面发生变化,即“智能响应型行为”,比如pH、温度、光、生物分子响应性[4-8]等。此种特性为研究生化传感器、药物输送系统、纳米计算机和生化分离等智能生化系统[9-15]提供重要启示。刺激响应型微球在许多领域存在巨大的潜在用途吸引了广泛关注,成为近年来的研究热点。
传统刺激响应型微球[16-19]大多采用无规共聚法和核壳结构法获得。其实心结构的阻尼特性导致刺激响应行为不够明显,过程的可逆性差,甚至失去了二次响应性。另外,在实验过程中外部环境的刺激因素多为单次、单向刺激,与实际的生化环境相差甚远。基于上述情况的考虑,我们首先采用模板自由基聚合法,将含有pH响应官能团的丙烯酸(AAc)与异丙基丙烯酰胺(NIPAm)接枝共聚,合成膨胀收缩比更大的空心结构pH响应性P(NIPAm-co-AAc)微球。然后将合成的空心微球与BrO3--SO32--H+[20]这一pH振荡体系相混耦合。该pH振荡体系的特点是:1)振荡的温度区间主要是室温范围,与人体温度接近,也与所合成空心微球临界相转变温度接近。2)pH振荡幅度比较大(3.5~7.5)。3)体系在振荡反应过程中停留在高pH和低pH的时间相对较长,有利于微球充分膨胀收缩。
耦合体系在pH振荡过程中,空心微球表面的羧基也同时发生质子化和非质子化的过程,电荷密度随之发生变化,这样微球就会产生周期性的膨胀收缩,这是一个化学能转变为机械能的过程。为了使耦合体系能持续反应下去,本实验选取连续流动搅拌反应器(CSTR)作为反应器,通过物料的不断流入、流出,可以使反应远离平衡态,长时间稳定进行。为了考查空心pH响应型微球耦合pH振荡反应动力学行为,我们搭建了能在线实时监测耦合体系动力学行为的动态光散射系统(DLS)和pH监测系统。
1 实验
1.1 空心微球的合成及其粒径pH响应性测试
图1为空心微球合成路线示意图[21],首先取2.5 mL正硅酸四乙酯和50 mL乙醇混合加入反应器,室温条件下搅拌3 min(500 r/min)。再取1.4 mL去离子水与4 mL氨水混合,搅拌3 min(500 r/min)。然后将上述氨水溶液加入反应器中,快速搅拌3 min(750 r/min),使溶液充分混合,再温和搅拌(500 r/min)。反应24 h后,向反应器中加入2 mL硅烷偶联剂KH-570(MPS),温和搅拌(500 r/min),再反应 24 h。对反应24 h后的溶液进行离心分离,弃上层清液。用无水乙醇洗泡产物,超声波振荡分离,再次离心分离,弃上层清液。换用去离子水洗泡产物,离心分离2次。产物进行冷冻干燥,得到表面改性的SiO2纳米粒子。
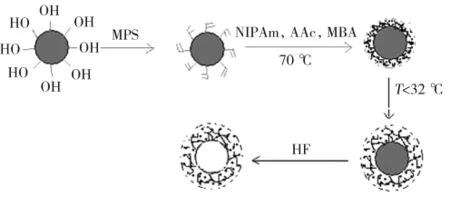
图1 空心微球合成路线示意图Fig.1 Synthetic schematic diagram of hollow microsphere
将0.2 g改性SiO2纳米粒子与2.5 g N-异丙基丙烯酰胺(NIPAm)、2.5 g N,N’-亚甲基双丙烯酰胺(MBA)交联剂溶于175 mL的去离子水中,超声振荡使其完全溶解,氮气保护下缓慢搅拌30 min,充分除去反应器中的氧气。加入适量丙烯酸(AAc),再将0.25 g KPS溶于25 mL水中(预先通氮气除氧)加入反应器中引发单体聚合,升温至70℃,反应6 h。反应结束后,在磁力搅拌下自然冷却至室温。之后再加入75 mL质量分数为20%的氟化氢(HF)溶液以溶解SiO2,静置过夜。将所得溶液离心分离,弃上层清液。再用去离子水重新分散产物,再离心分离2次。用截止相对分子质量为14 000的透析袋透析7 d,每天超纯水换水3次。对透析后的产物进行冷冻干燥,就得到纯净的pH响应型空心微球。
将纯化的空心微球0.05 g混于200 mL超纯水中,通过HCl和NaOH溶液来调节其pH值,pH复合电极e-corder数据记录仪相连,以监测反应中pH变化情况。微球粒径的变化通过搭建的DLS在线实时监测,整个DLS由BI-DLS检测器(美国Brookhaven)、BI-9000数字相关器(美国Brookhaven)和氩离子激光器构成,激光波长为532 nm,检测角度为90°。
1.2 CSTR中空心微球耦合pH振荡反应动力学行为测试
耦合体系动力学测试装置如图2所示。耦合反应在CSTR中进行,有效反应体积为22 mL,外包恒温水套(温控精度为±0.1℃),由2个独立的储液瓶分别供料,一个储液瓶中装有浓度为0.050 mol/L的Na2SO3和0.001 25 mol/L的H2SO4的混合溶液,另外一个储液瓶中为0.050 mol/L的NaBrO3和空心微球混合溶液。CSTR顶部安装一个pH复合电极,一个数显温度计,以监测反应过程体系的pH值和温度变化。微球粒径的变化通过搭建的DLS在线实时监测。通过精密蠕动泵驱动,2根进料管分别独立进料,在输入CSTR前预混合。耦合体系通过磁力搅拌来确保混合均匀,搅拌速度为900 r/min。为了避免干扰DLS测量,通过程序软件控制,反应过程中每隔30 s,持续搅拌、供料120 s,在搅拌、供料停止的30 s过程中进行动态光散射测量。反应过程中pH随时间变化过程通过e-corder数据记录仪记录在电脑上。微球粒径的实时变化情况也通过DLS数字相关器记录在电脑上。
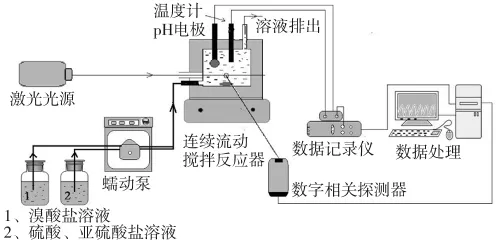
图2 CSTR动力学测试装置图Fig.2 Schematic diagram of CSTR for kinetic test
2 结果与讨论
2.1 空心微球pH响应性能
调节耦合体系pH值从2.5增大到9.5,微球粒径随pH的变化情况如图3所示。由图可以看出,随着pH值的增大,微球粒径先减小后增大。这是由于在所合成的无规共聚物微球中,响应性官能团—COOH主要分布在聚合物表面,聚合物在水中时表面羧基会发生解离,生成羧酸根离子(—COO-)和氢离子(H+),呈离解平衡状态,该平衡态受混合体系pH值的影响。当pH值较小时(3.5~5.5),使阴离子静电场得到平衡,以致分子链表面电荷排斥力作用减弱,共聚物链发生蜷曲,粒径减小,溶解性变差;当pH值足够小时(小于3),羧基不电离,氢键稳定,使网络紧密呈收缩状态,微球进一步发生团聚现象,粒径反而又增大了。当pH值较大时(大于羧基的电离常数pKa=4.28),聚合物链上的同性电荷(—COO-)数目就会增加,阴离子之间的排斥力增强使得共聚物链在水溶液中呈伸展状态,溶解性增强,导致粒径的增大。当继续增大pH值(大于6),微球分子链上的羧基与碱作用形成羧酸盐,增加了微球粒子的亲水性,大分子之间疏水缔合作用减小,大分子链段处于伸展状态而自由运动,以致无相分离现象出现,粒径保持稳定。
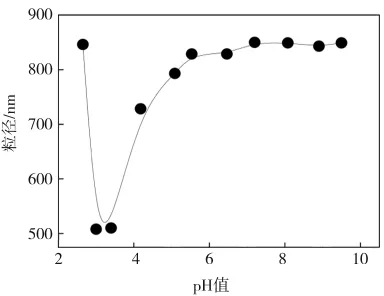
图3 空心微球粒径随pH的变化情况Fig.3 pH dependence of diameter of hollow microsphere
空心微球粒径的pH脉冲响应性如图4所示。调节环境介质的pH值在高低之间变化,当溶液介质pH值呈现脉冲式振荡变化时,微球粒径随pH也呈现脉冲式振荡,在pH=6.5时,粒径充分膨胀;pH=3.5时,微凝胶粒径充分收缩,溶胀收缩比:
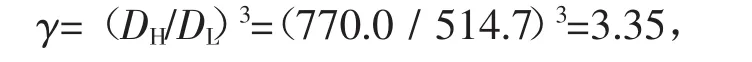
式中DH、DL分别为空心微球处于高pH(6.5)和低pH(3.5)条件下的粒径值。空心微球粒径随pH值变化的脉冲式振荡体现出良好的智能响应特性。

图4 空心微球粒径的pH脉冲响应性Fig.4 pH pulse responsibility of hollow microsphere
2.2 空心微球耦合pH振荡反应体系动力学行为
将空心微球在CSTR中与BrO3--SO32--HSO3-这一pH振荡反应体系混合,BrO3--SO32--HSO3-体系主要反应过程方程式如下:
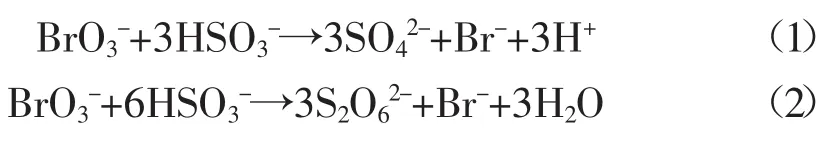
反应过程(1)是产生H+的过程,此过程导致体系pH值减小;反应过程(2)是消耗H+的过程,此过程导致体系pH值增大。反应过程中当H+消耗到一定水平会触发反应(1)开始并逐步占据主导地位;反之,当H+浓度上升到一定程度,会触发反应(2)开始,消耗H+的反应开始占据主导地位。周而复始,体系的H+浓度周期性增大、减小,即体系pH值在低值和高值之间交替振荡进行,体系关键参数呈现出类似于仿生化环境的自发振荡变化。
CSTR中空心微球粒径与耦合体系pH同步振荡情况如图5所示,耦合体系pH值与粒径值振荡动力学行为能保持同步进行。在测量pH值振荡的同时也在线实时测量了微球粒径的变化情况。
当pH维持在高位(6.5~7.5)时,微球充分膨胀,粒径维持在700~800 nm左右,当pH振荡到低位(3.5~4.5)时,微球充分收缩,粒径维持在450~500 nm左右,粒径振荡与pH振荡实时同步。pH振荡体系提供化学能驱动空心微凝胶体系实时地膨胀收缩,整个过程是一个化学能转变为机械能的过程。

图5 CSTR中空心微球粒径与耦合体系pH的同步振荡情况Fig.5 Synchronous oscillations of diameter of hollow microsphere and pH of coupling system in CSTR
在低pH值区域出现了幅度较小的复杂振荡。而在高pH值区域,pH则相对稳定。 这是由于pH响应性微球表面的pH响应性官能团—COOH耦合非线性化学反应过程造成的,因为—COOH的pKa=4.28,正好处在振荡过程中的低pH值区域(3.5~4.5),—COOH发生质子化和非质子化过程。对H+来说,这又是一个正负反馈过程,并且在此pH条件下,空心微球呈收缩状态,聚合物空间网络结构也会影响质子的反应扩散,所以pH受到影响发生微振荡。在高pH值区域,pH远远大于—COOH的pKa值,羧基早已非质子化,主要以—COO-形式存在,耦合体系趋于均相化,在此范围内不对非线性体系的pH产生反馈影响。
CSTR中耦合体系振荡周期随温度变化曲线如图6所示,随着温度的不断升高,耦合体系的振荡周期逐渐减小,可由阿伦尼乌斯公式得到解释,温度升高导致体系反应速率加快了。也可由经典的关于凝胶聚合物的Flory-Rehner理论[22]得到解释,其理论认为耦合体系的化学势由各物质的混合化学势和聚合物支链弹性化学势构成。温度升高直接导致耦合体系的化学势相应增大,反应趋势增强,速率增大,反应周期相应减小了。
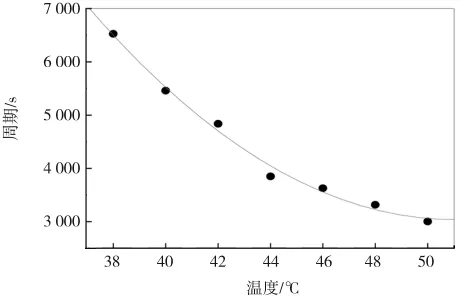
图6 CSTR中耦合体系振荡周期随温度变化曲线Fig.6 Oscillation period of coupling system mearured at different temperature in CSTR
3 结论
通过模板自由基聚合法获得的空心微球具有良好的生化响应特性:1)微球粒径可以随所处环境的pH值变化而变化,并能呈现脉冲式响应特性。2)在CSTR中将空心微球与pH振荡体系BrO3--SO32--H+混合作用,在维持CSTR进料、出料平衡条件下,空心微球粒径膨胀、收缩与体系pH值增大、减小保持长时间同步变化。整个实验是化学能驱动机械能转变的过程。其空心结构可进一步包埋特定生化药物成分,微球在响应环境变化的同时,通过膨胀收缩行为,达到定向释放的功能。能够被调制的响应性空心微球耦合非线性化学反应系统为研究生化传感器、药物输送系统、纳米计算机等提供有益启示。
参考文献(References):
[1]刘瑞,郝红,梁珊珊,等.聚合物微凝胶研究进展[J].离子交换与吸附,2012,28(6):570-576.
[2]王龙海,宏春雁.响应性支化聚合物的合成、组装及其生物医药应用[J].高分子学报,2017,2(6):200-213.
[3]LIU L,ZEN J,ZHAO XB,et al.Independent temperature and pH dual-responsive PMAA/PNIPAM microgels[J].Colloids and Surfaces.2017,526(3):48-55.
[4]王世杰,黄雯,王磊.pH响应性高分子的合成及表征研究进展[J].高分子通报,2016,(4):61-79.
[5]陈韩婷,樊晔,方云.全亲水无规共聚物的pH和温度双重刺激响应性水相自组装[J].物理化学学报,2014,30(7):1290-1296.
[6]LIU XY,YANG J,YAN WX,et al.Thermoreversible thickening and self-assembly behaviors of pH/temperature dually responsive microgels with interpenetrating network strcture[J].J Donghua University,2014,31(3):312-315.
[7]KIM J,NAYAK S,LYON L A.Bioresponsive hydrogel microlenses[J].J Am Chem Soc,2005,127(26):9588-9592.
[8]SEIFFERT S.Sensitive microgels as model colloids and microcapsules[J].Journal of Polymer Science Part A Polymer Chemistry,2014,52(4):435-449.
[9]NAYAK S,LEE H,CHMIELEWSKI J,et al.Folate-mediated cell targeting and cytotoxicity using thermoresponsive microgels[J].J Am Chem Soc,2004,126(33):10258-10259.
[10]SUZUKI D,KAWAGUCHI H.Stimuli-sensitive core/shell template particles for immobilizing inorganic nanoparticles in the core[J].Colloid Polym Sci,2006,284(12):1443-1451.
[11]ZHOU X F,SU F Y,TIAN Y Q,et al.Dually fluorescent core-shell microgels for rationetric imaging in live antigen-presenting cells[J].Plos One,2014,9(2):8815-88191.
[12]MOLINA M,MAZDAK A B,BALACH J,et al.Stimuli-reponsive nanogel composites and their application in nanomedicine[J].Chem Soc Rev 2015,44(6):6161-6186.
[13]朱颖.pH/温度双重响应抗肿瘤药物微球的制备和研究[J].天津医科大学学报,2016,22(4):354-358.
[14]杨年旺,陈涛,傅佳骏.智能纳米容器对缓蚀剂酸/碱双刺激的响应释放性能[J].高等学校化学学报,2014,35(5):971-975.
[15]ZHANG Y J,GUAN Y,LUO Q F,et al.Applications of thermosensitive PNIPAM microgels in biomedical field[J].Polymer Bulletin,2013,126(1):26-39.
[16]宋一凡,柴云,张普玉.刺激响应性聚合物载药纳米胶束研究进展[J].化学研究,2016,(27)5:655-659.
[17]吕英海,郭续娟,牟宗凯,等.pH值/盐浓度双重敏感性SPM水凝胶微球性能分析[J].功能材料,2015,46(18):18057-18060.
[18]徐甜甜,徐昆,周超,等.温敏型微球表面接枝交联复合凝胶的制备及性能[J].高等学校化学学报,2016,37(5):996-1002.
[19]刘维俊,黄永民,刘洪来.温度、pH敏感性核壳结构微凝胶的制备及性质[J].化学学报,2007,65(2):91-94.
[20]TIBOR G,Szántó,GYULA R.pH oscillations in the BrO3--SO32--HSO3-reaction in a CSTR[J].J Phys Chem A,2005,109(24):5398-5402.
[21]STOBER W,FINK A.Controlled growth of monodisperse silica spheres in the micron size range[J].J Colloid Interface Sci,1968,26(1):62-69.
[22]SHIBAYAMA M,TANAKA T.Small angle neutron scattering study on poly (N isopropyl acrylamide) gels near their volume phase transition temperature[J].J Phys Chem,1992,97(9):6829-6841.

