基于萘酰亚胺的功能凝胶因子的合成及其凝胶性能
饶亚沙,杨新国,邱欢,沈启立,李文露
基于萘酰亚胺的功能凝胶因子的合成及其凝胶性能
饶亚沙1, 2,杨新国1, 2,邱欢1, 2,沈启立1, 2,李文露1, 2
(1. 湖南大学 材料科学与工程学院,湖南 长沙,410082; 2. 湖南大学 湖南省喷射沉积技术及应用重点实验室,湖南 长沙,410082)
以三聚氯氰为原料合成一种含有酰胺结构的三嗪中间体,与1,4,5,8-萘四甲酸二酐缩合得到萘酰亚胺衍生物NDI-M,运用1HNMR,13CNMR和红外光谱等手段对NDI-M的化学结构进行确认。采用试管倒转法考察NDI-M的凝胶性能;利用扫描电镜(SEM)观测NDI-M凝胶的微观形貌;通过紫外−可见吸收光谱和荧光光谱等研究NDI-M凝胶的光物理性能。研究结果表明:NDI-M在甲苯、二甲苯、乙酸丁酯和甲基丙烯酸丁酯等有机溶剂中均可形成热可逆的凝胶,除在乙酸丁酯中其临界凝胶浓度(CGC)为30 mmol/L外,在其他溶剂中均为20 mmol/L,且在不同的溶剂中形成的凝胶形貌结构有所差别;与溶液的光谱性质相比,形成凝胶后NDI-M的Stokes位移显著增大,不同凝胶的光谱性质表现出明显差异。
萘酰亚胺;小分子有机凝胶;三嗪
小分子有机凝胶因子(low molecular-mass organic gelator,LMOG)是一类能够在较低浓度下使有机溶剂胶凝的小分子有机化合物[1−2]。近年来,将特殊功能基团引入小分子有机凝胶因子制备功能凝胶材料被广泛关注[3−6]。萘酰亚胺是一类具有良好化学稳定性和性能优异的光电功能材料。通过化学修饰,可以使萘酰亚胺衍生物的光谱横跨整个紫外−可见光区,展示出丰富的功能特性[7],如SURARU等[8−11]合成了多种含萘酰亚胺基团的凝胶因子,得到纳米级的纤维网络状结构的凝胶材料,而且具有特殊的自分类现象,在分子识别方面显示出广阔的应用前景。尽管三嗪类衍生物分子之间可以形成二重氢键作用,表现出具有较强的氢键组装能力,但由于其分子间作用有限,通常只能与另一具有互补氢键作用的组分构成双凝胶组分,使其应用受到很大限制,如DAS等[12−14]设计合成了含有双三嗪基团的偶氮苯类小分子有机凝胶因子,发现在所研究的溶剂中均不能形成凝胶,只能与巴比妥酸衍生物共组装形成双组分凝胶,因此,如何利用三嗪基团的组装特性构筑一类基于萘酰亚胺的单组分功能凝胶因子存在一定困难。本文作者利用三嗪衍生物的分子结构可灵活设计的特点,在三嗪环上引入酰胺基团,再对萘酰亚胺进行化学修饰得到一类单组分功能凝胶因子。该化合物能在多种溶剂中形成热可逆凝胶,并表现出特殊的凝胶性能,为进一步发展功能凝胶材料提供了一定的依据。
1 实验
1.1 试剂与仪器
试剂为:1,4,5,8-萘四甲酸二酐,购于TCI公司;三聚氯氰,购于Alfa Aesar公司;月桂酸甲酯(AR),乙二胺(AR),己二胺(AR),均购于国药化学试剂有限公司;N,N-二正丁基-1,4,5,8-萘酰亚胺(NDI-B),由本实验室提供。对于其他试剂,若没有特殊说明,均为分析纯试剂。
仪器为:INOVA−400型核磁共振分析仪(美国Varian公司);Nicolet−460 型红外光谱仪(美国Nicolet 公司);Shimadzu UV−2550紫外−可见光谱仪(日本Shimadzu公司);JSM−6700F 型场发射扫描电子显微镜(日本Jeol公司);Elementar varioⅢ元素分析仪(德国Elementar 公司);SWG−X4 显微熔点测定仪(上海精密科学仪器有限公司)。
1.2 实验过程
NDI-M的合成见图1。

图1 NDI-M的合成
1.2.1 化合物Ⅰ的合成
在250 mL三口烧瓶中,加入100 mL乙醇和88 mL(1.28 mol)乙二胺,然后将40 mL(0.16 mol)月桂酸甲酯缓慢滴加至三口烧瓶中,升温至80 ℃回流7 h。反应结束后,减压蒸馏(90 ℃/−0.075 MPa)出未反应的乙二胺,静置,过滤,取滤液,蒸干溶剂,得到白色固体。用石油醚重结晶得23.36 g白色固体,产率为53.20%,溶点(m.p.)为122~125 ℃[15]。
1.2.2 化合物Ⅱ的合成
在冰浴条件下,将80.0 mL无水氯仿,2.32 g (0.012 5 mol)三聚氯氰和4.5 mL(0.025 0 mol) N,N-二异丙基乙胺(DIPEA)加入250 mL三口烧瓶中,然后缓慢滴加溶有6.20 g(0.025 0 mol)化合物Ⅰ的20.0 mL无水氯仿,滴加完后继续搅拌反应约30 h。将反应溶液冷却后倒入250.0 mL乙醇中,过滤,滤饼用蒸馏水洗涤,再用甲醇洗涤,干燥,得白色粉末5.94 g,产率为80.20%,溶点(m.p.)为129~130 ℃。1HNMR (400 MHz,CDCl3)(×10−6):6.64(d, 2H),6.12(d,2H,频率= 4 Hz),4.40(m, 4H),3.55(m, 4H),2.15(m, 4H),1.35(m, 38H),0.87(t, 6H,=6 Hz)。IR(KBr, cm−1):3 294(N—H),2 920(—CH2—),1 648(C=O),1 556(N—H),1 296(C—N)。
1.2.3 化合物Ⅲ的合成
将5.94 g(0.01 mol)化合物Ⅱ,2 mL(0.01 mol)DIPEA和23.23 g(0.20 mol)己二胺加入到150 mL四氢呋喃中,加热至回流,TLC控制反应进程,约 24 h后终止反应,蒸出大部分溶剂。将剩余的反应液倒入大量蒸馏水中析出沉淀,过滤,得白色蜡状固体,真空干燥,得白色固体5.94 g。产率为88.50%,m.p.116~117 ℃。1HNMR (400 MHz,CDCl3)(×10−6):6.50(s,3H),5.68(s,2H),4.28(s,2H),3.53(s,10H),2.18(s,4H),1.79(s,6H),1.43(m,40H),0.88(t,6H)。IR(KBr,cm−1):3 446(NH2),3 290(N—H),2 917(—CH2—),1 640(C=O),1 264(C—N)。
1.2.4 化合物NDI-M的合成
将0.48 g(0.001 8 mol)化合物Ⅳ和2.43 g(0.003 6 mol)化合物Ⅲ加入至150 mL乙二醇单甲醚中,回流12 h。反应结束后,倒入大量蒸馏水中析出沉淀,过滤,滤饼用蒸馏水洗涤,干燥,用柱层析(淋洗剂是三氯甲烷与甲醇的体积比即三氯甲烷/甲醇=20的混合溶液)分离后得红色固体1.44 g,产率为52.40%。1HNMR (400 MHz,CDCl3)(×10−6):8.75(s,4H),6.65(s,4H),5.51(s,6H),4.18(s,4H),2.2(m,20H),1.00~1.90(m,96H),0.8(t,=6.8 Hz,12H)。13C NMR (101 MHz,CDCl3)173.69,160.38,158.15,126.25,121.94, 35.66,32.10,27.23,24.97,24.86,24.68,21.74,21.09,18.01,9.45.IR(KBr,cm−1):3 219(N—H),2 920(CH3),2581(—CH2—),1705(C=O),1 519(N—H),1 261(N—C)。
1.3 凝胶的制备
取一定量的凝胶因子溶于不同的溶剂(1 mL)中配置成一定浓度的溶液,加热至凝胶因子溶解后置于室温下自然冷却。当体系在倒置情况下没有发生流动时,即认定为形成凝胶。
1.4 临界凝胶浓度的测定
采用试管倒置法测定,从1 mmol/ L开始测试,直至能在室温下形成稳定凝胶为止的浓度,并将该浓度定义为该凝胶因子在该溶剂中的临界凝胶浓度。
1.5 临界凝胶温度的测定
采用试管倒转法测定,在直径为10 mm的试管中形成一定浓度凝胶,并在室温下保持12 h。将试管置于恒温水浴锅中,以0.5 ℃/次升温,每次升温后保持恒温2 min。最终以试管底部的凝胶在试管倒转后发生流动时的温度定为临界凝胶转变温度。
2 结果与讨论
2.1 凝胶行为
NDI-M在常用溶剂中的凝胶性质见表1。NDI-M在不同溶剂中形成的凝胶见图2。从图2可见:NDI-M在甲苯、二甲苯和甲基丙烯酸丁酯中可形成不透明的橘红色凝胶;凝胶在加热至临界凝胶温度时,失去凝胶特性,重新加热溶解、冷却可重新恢复其凝胶特性,具有热可逆性;在正己烷、环己烷、甲基环己烷、丙酮、甲醇和乙醇中均不能溶解;在三氯乙烯、四氯乙烷、二氧六环、乙酸乙酯和DMF中溶解后,冷却后析出沉淀;在二氯甲烷、三氯甲烷和四氢呋喃中形成溶液;在苯乙烯和乙酸丁酯中形成不稳定的聚集体;当浓度达30 mmol/L后,在乙酸丁酯中可以形成稳定的凝胶;另外,NDI-M在不同有机溶剂中形成的临界凝胶浓度和临界凝胶温度都不同。这些结果表明:在形成凝胶的过程中,由于溶剂的极性不同,溶剂与凝胶因子之间的相互作用对凝胶性能有重要的影响。

表1 NDI-M的凝胶性质
注:S代表溶液;P代表沉淀;Go代表不透明凝胶;IS代表不溶物;CGC代表临界凝胶浓度;g为凝胶温度gel。

图2 NDI-M在不同溶剂中形成的凝胶
2.2 凝胶的聚集态结构
图3所示为NDI-M在不同溶剂中形成的凝胶SEM图像。从图3可见:在二甲苯 (图3(a))和甲苯(图3(b))等芳香族溶剂中均形成团状聚集体,其中在二甲苯中的聚集体纤维直径较细小,且结构更规整;在甲基丙烯酸丁酯(图3(c))和乙酸丁酯(图3(d))中形成类纤维网络状的聚集体,但规整度较差,甲基丙烯酸丁酯中的聚集体纤维直径较小。这表明同种凝胶因子在不同溶剂中形成的聚集体的微观结构不同,这可能是因为溶剂种类不同,溶剂与凝胶因子之间的作用方式 不同。
2.3 光物理性能
图4(a)所示为NDI-M和参比物NDI-B的三氯甲烷溶液(5×10−5mol/L)的紫外−可见吸收光谱,两者吸收峰的性状非常类似,其3个特征峰分别约在380,360和340 nm处,为NDI-M和NDI-B分子中萘酰亚胺基团沿着分子长轴方向的 π-π*跃迁特征吸收峰[16];另外,与NDI-B相比,NDI-M的0-1与0-2峰强度比值较小。进一步从NDI-M和NDI-B的三氯甲烷溶液的荧光光谱(图4(b))可以看出:NDI-B的特征发射峰出现在410 nm和437 nm处[17],这表明NDI-M在三氯甲烷溶液中分子间可能存在一定程度的电子相互作用。进一步考察NDI-M凝胶的光谱性质(图5(a)和图5(b))发现:与溶液的紫外−可见吸收光谱相比,NDI-M凝胶中的萘酰亚胺基团的吸收峰均发生一定程度红移,峰型变宽,且0-2峰的吸收强度明显大于0-1峰的吸收强度;与溶液的荧光光谱相比,NDI-M的凝胶的荧光光谱表现出截然不同的性质,除了在450~550 nm荧光发射峰之外,还伴随有590~610 nm的肩峰,且随着溶剂不同,Stokes位移程度不同,这表明形成凝胶的NDI-M中的萘酰亚胺基团之间有一定程度的聚集,这可能是因为其聚集方式受到酰胺基团的氢键作用的牵制而表现出这种特殊的光电性质。

图3 NDI-M在不同溶剂中形成的凝胶的SEM图像
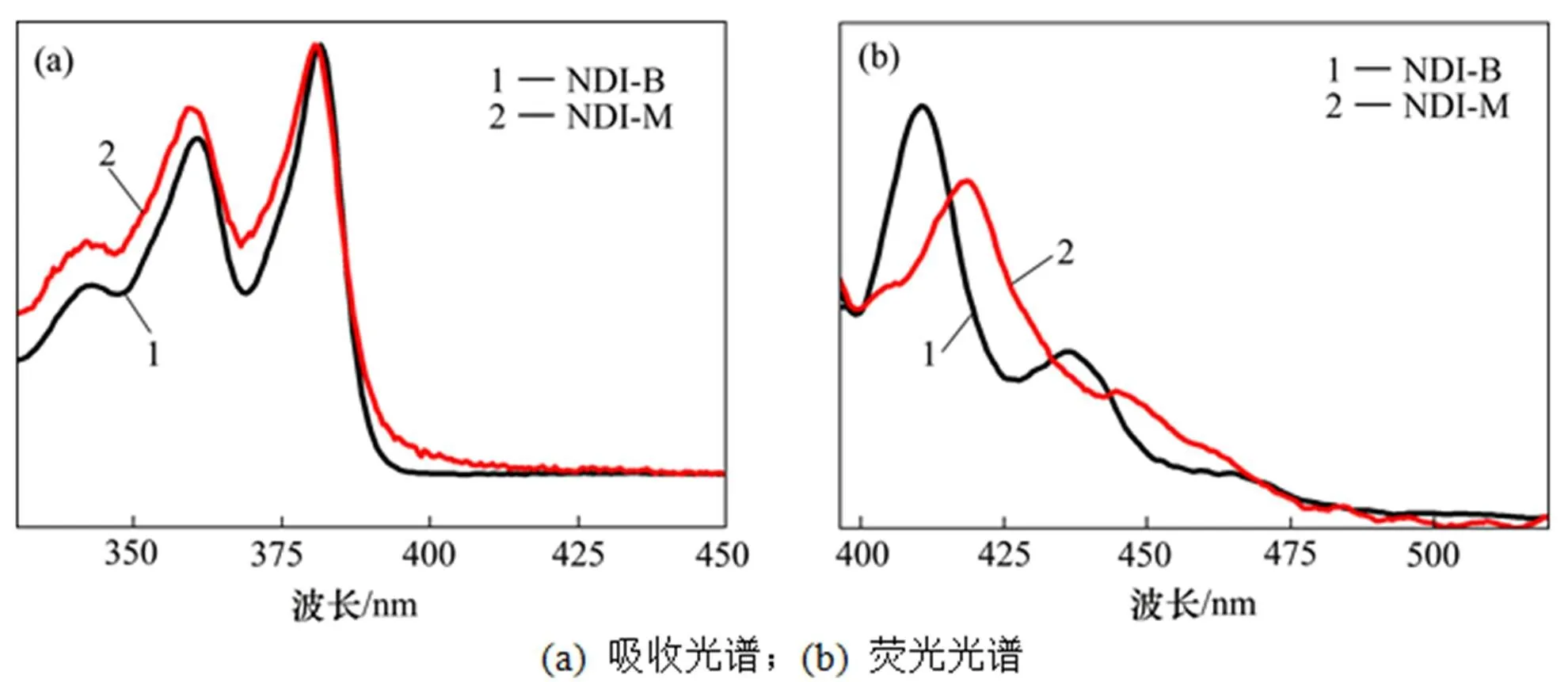
图4 NDI-B和NDI-M的三氯甲烷溶液(5×10−5 mol/L)的吸收光谱和溶液的荧光光谱(激发波长为380 nm)

图5 NDI-M在不同溶剂中形成的凝胶的吸收光谱和荧光光谱(激发波长为380 nm)
3 结论
1) 合成了一种含有萘酰亚胺基团的功能凝胶因子NDI-M,在甲苯、二甲苯、乙酸丁酯和甲基丙烯酸丁酯等有机溶剂中可形成热可逆凝胶。
2) 溶剂种类对NDI-M凝胶的微观形貌和临界凝胶转变温度有一定的影响。在甲苯、二甲苯中形成的凝胶为团状结构,其临界凝胶转变温度低;在甲基丙烯酸丁酯和乙酸丁酯中形成的凝胶为类纤维状的聚集结构,其临界凝胶转变温度较高。
3) NDI-M形成凝胶后其荧光发射峰红移至450~550 nm之间,并伴有590~610 nm的肩峰,其Stokes位移显著增大,且随着溶剂不同,其Stokes位移程度不同,表明在凝胶中NDI-M分子间存在不同的堆积模式。
[1] TERECH P, WEISS R G. Low molecular mass gelators of organic liquids and the properties of their gels[J]. Cheminform, 1998, 97(8): 3133−3160.
[2] SANGEETHA N M, MAITRA U. Supramolecular gels: functions and uses[J]. Cheminform, 2005, 34(10): 821−836.
[3] LEE S, OH S, LEE J, MALPANI Y, et al. Stimulus-responsive azobenzene supramolecules: fibers, gels, and hollow spheres[J]. Langmuir, 2013, 29(19): 5869−5877.
[4] REN Xiangyu, YU Wei, ZHANG Zijian, et al. Gelation and fluorescent organogels of a complex of perylenetetracarboxylic tetra acid with cationic surfactants[J]. Colloids and Surfaces A, 2011, 375(1/2/3): 156−162.
[5] MARTINZEZ-CALVO M, KOTOVA O, MOBIUS M E, et al. Healable luminescent self-assembly supramolecular metallogels possessing lanthanide (Eu/Tb) dependent rheological and morphological properties[J]. Journal of the American Chemical Society, 2015, 137(5): 1983−1992.
[6] BABU S S, PRAREEN V, AJAYAGHOSH A. Functional π‑gelators and their applications[J]. Chemical Reviews, 2014 , 114(4): 1973−2129.
[7] 申剑磊, 杨新国, 黄燎, 等. 新型三嗪桥连的双1, 8-萘酰亚胺衍生物的合成及其光物理行为[J]. 物理化学学报, 2012, 28(8): 1992−1999. SHEN Jianlei, YANG Xinguo, HUANG Liao, et al. Synthesis and photophysical behavior of two novel bis(1, 8-naphthalimides) containing triazine spacers[J]. Acta Physico-Chimica Sinica, 2012, 28(8): 1992−1999.
[8] SURARU S L, WURTHER F. Strategies for the synthesis of functional naphthalene diimides[J]. Angewandte Chemie International Edition, 2014, 45(39): 7428−7448.
[9] MOLLA M R, GHOSH S. Structural variation on self-assembly and macroscopic properties of 1,4,5,8-naphthalenediimide chromophores[J]. Chemistry of Materials, 2011, 23(23): 95−105.
[10] MOLLA M R, GHOSH S. Hydrogen bonding-mediated J-aggregation and white-light emission from a remarkably simple, single-component, naphthalenedimide chromophre[J]. Chemistry, 2012, 18(5): 1290−129.
[11] DAS A, GHOSH S. Generalized supramolecular strategy for self-sorted assembly between donor and acceptor gelator[J]. Chemical Communications, 2011, 47(31): 8922−8924.
[12] DAS A, RAHAMAN M, GHOSH S. Comprarative self-assenbly studies and self-sorting of tow structurally isomeric naphthalenediimide(NDI)-gelators[J]. Journal of Chemical Sciences, 2011, 123(6): 963v973.
[13] YAGAI S, MONMA Y, KAWANCHI N, et al. Supramolecular nanoribbons and nanoopes generated from hydrogenbonded supramolecular polymers containing perylene bisimide chromophores[J]. Organic Letters, 2007, 9(6): 1137−1140.
[14] YAGAI S, KARATSU T, KITAMHRA A. Melamine- barbiturate/cyanurate binary organogels possessing rigid azobenzene-tether moiety[J]. Langmuir, 2005, 21(24): 11048−11052.
[15] 丁立伟, 杨新国, 钟文斌, 等. 含蜜胺基团的新型苝酰亚胺染料的合成及纳米纤维的构筑[J]. 高等学校化学学报, 2013, 34(5): 1277−1283. DING Liwei, YANG Xinguo, ZHONG Wenbin, et al. Synthesis of a new perylene bisimide dye containing melamine moieties and construction of well-defined nanofiber[J]. Chemical Journal of Chinese Universities, 2013, 34(5): 1277−1283.
[16] GUO Le, MA Xiaochen, FANG Huaquan, et al. A general and mild catalytic-alkylation of unactivated esters using alcohols[J]. Angewandte Chemie, 2015, 54(13): 4023−4027.
[17] LICCHELLI M, LINATI L, BIROLI A O, et al. Metal induced assembling/disassembling of fluorescent naphthalene-diimide derivatives signalled by excimer emission[J]. Chemistry, 2002, 8(22): 5156−5169.
(编辑 陈灿华)
Synthesis and gel properties of functional gelators based on naphthalene-diimide
RAO Yasha1, 2, YANG Xinguo1, 2, QIU Huan1, 2, SHEN Qili1, 2, LI Wenlu1, 2
(1. College of Materials Science & Engineering, Hunan University, Changsha 410082, China; 2. Key Laboratory for Spray Deposition Technology & Application of Hunan Province, Hunan University, Changsha 410082, China)
A new triazine intermediates with amide group was synthesized from cyanuric chloride, and NDI-M was obtained by condensation of the intermediates and 1,4,5,8-naphthalenetetracarboxylic dianhydride. The molecular structure of NDI-M was confirmed by1HNMR,13CNMR and FTIR. Gel properties were tested by the stable-to-inversion of vial method, and micromorphology of gels was observed by SEM. Photophysical properties were investigated by UV-Vis absorption spectrum and fluorescence spectrum. The results show that NDI-M can form thermal reversible gels in solvents, such as toluene, xylene, butyl methacrylate and butyl acetate. All critical gelation concentrations(CGC) reach 20 mmol/L but butyl acetate is 30 mmol/L. Gels present different microstructures in various solvents. Compared with the spectral properties of the solution,the stokes shift of gels significantly increases and the spectral properties of gels formed in various solvents show obvious differences.
naphthalimide; low molecular-mass organic gelator; triazine
O648.17
A
10.11817/j.issn.1672-7207.2018.03.007
1672−7207(2018)03−0560−06
2017−03−10;
2017−05−08
国家自然科学基金资助项目(50573019,51273061);湖南省自然科学基金资助项目(2016JJ2027) (Projects(50573019, 51273061) supported by the National Natural Science Foundation of China; Project(2016JJ2027) supported by the Natural Science Foundation of Hunan Province)
杨新国,博士,副教授,从事有机/高分子功能材料的制备与应用研究;E-mail: xgyang@hnu.edu.cn

