腹腔镜下射频消融治疗小肝癌的临床疗效分析
张发鹏,袁荣发,张引,余晓雯,王文龙,欧阳永鹏,伍明明,罗志强
(南昌大学第二附属医院 肝胆外科,江西 南昌 330006)
射频消融(radiofrequency ablation,RFA)是继手术切除和肝移植之后小肝癌(small hepatocellular carcinoma,SHCC)的又一种根治性治疗手段[1-3],且具有微创、风险小、可重复性高等特点[4-6],一般在CT引导下经皮射频消融(percutaneous radiofrequency ablation,PRFA),但对于特殊部位(靠近膈顶、胃、胆囊及肝表面等)的肿瘤往往易出现副损伤或消融不彻底[7],而腹腔镜下射频消融(laparoscopic radiofrequency ablation,LRFA)可有效弥补上述不足。笔者通过比较我院LRFA、PRFA、手术切除3种方式治疗小肝癌的治疗效果、术后恢复情况、3年复发率、无瘤生存率及总生存率,评估LRFA在小肝癌治疗中的疗效,现报告如下。
1 资料与方法
1.1 一般资料
选择2011年8月—2013年10月南昌大学第二附属医院收治的90例原发性肝癌患者[按卫生部原发性肝癌诊疗规范(2011年版)制定的原发性肝癌诊断标准]纳入本研究。入选标准:⑴ 初发的原发性肝癌,未接受过任何抗癌治疗;⑵ 肿瘤直径≤5 cm,无子灶,无血管及远处转移;⑶ 肝功能Chlid-Pugh A级或B级,或经护肝治疗后达到该标准。排除标准:⑴ 有血管或邻近组织器官侵犯;⑵ 有淋巴或远处转移;⑶ 有凝血功能障碍;⑷ 有手术或视频消融的其他禁忌证。90例患者分别行LRFA(肿瘤均位于肝脏表面,LRFA组)、CT引导PRFA(PRFA组)、开腹手术切除(手术切除组),每组各30例。3组患者性别、年龄、肿瘤直径等术前一般资料比较,无统计学差异(均P>0.05)(表1)。
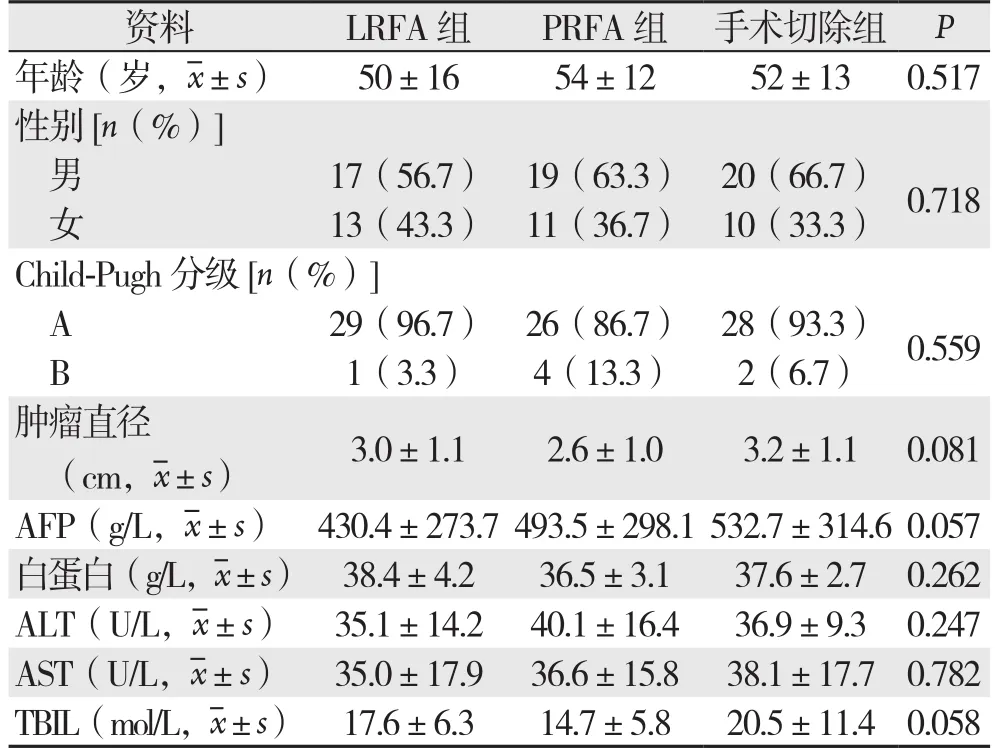
表1 患者一般资料(n=30)Table 1 General clinical characteristics of the patients (n=30)
1.2 治疗方法
LRFA:全身麻醉,均采用三孔法。⑴ 腹腔镜下先探查腹腔,确定肿瘤部位及是否转移;⑵ 充分显露肿瘤,必要时游离相应的肝周韧带;⑶ 射频电极针(StarBurstXL/25 cm,RITA公司,美国)在腹腔镜直视下穿刺病灶布针,按说明书操作2~3次、均多方位布针进行消融。消融的范围包含肿瘤和其周边0.5~1.0 cm的肝组织范围。每次消融后常规原针道消融避免出血及肿瘤种植。CT引导下PRFA:采用腹壁局部麻醉,常规消毒铺巾,在CT引导下将电极插入肝脏肿瘤中心,按说明书操作进行消融,消融范围同射频消融组。在CT监控下观察肿瘤病灶获完全消融。开腹手术切除:采用气管插管全身麻醉,开腹后先探查腹腔,结合术中B超明确病灶部位及范围,根据肝功能情况行规则性或不规则性肝切除方法行肿瘤根治性切除,切除范围至少包括肿瘤周围2 cm非瘤肝组织。
1.3 观察指标及随访
⑴ 术前及术后第1、3、7天肝功能变化;⑵ 术前及术后1、2个月AFP的变化;⑶ 手术时间;⑷ 术中出血量;⑸ 围手术期并发症;⑹ 住院时间;⑺ 肿瘤清除程度:在治疗后1个月行肝脏增强CT检查,结合AFP判断肿瘤是否完全清除(complete response,CR);⑻ 复发情况:所有患者于术后或射频后1个月行肝脏增强CT及血AFP检查,定期随访,术后第1年每3个月复查1次B超及血AFP,术后第2、3年每半年复查1次B超及血AFP;⑼ 无瘤生存率和总生存率。
1.4 统计学处理
采用SPSS 23.0软件来进行所有的统计分析。对于计量资料,使用Gaussianity检验来确保数据的同质性,数据表达为均数±标准差(±s),由单变量ANOVA比较。ANOVA检验的同时,3组数据的两两比较由LSD或Bonferroni检验实现。对于不符合正态分布的多组样本之间比较采用了Wilcoxon秩和检验。对于定性(分类)资料,采用Pearson χ2检验。用Kaplan-Meier法计算生存率,Log-rank检验比较无瘤生存率和总生存率。P<0.05为差异有统计学意义。
2 结 果
2.1 术后AFP及肝功能变化
术后1个月3组AFP浓度均明显低于术前(均P<0.05);术后2个月AFP浓度均恢复至正常水平;治疗后3组同期AFP比较,差异均无统计学意义(均P>0.05)。术后各组第1、3天肝功能指标均较术前明显升高(均P<0.05),术后第7天ALT、AST、TBIL均有所回落,LRFA组和PRFA组与术前比较,无统计学差异(均P>0.05),而手术切除组与术前比较,差异有统计学意义(P<0.05)。术后ALT、AST、TBIL同期比较,LRFA组和PRFA组无统计学意义(均P>0.05),而手术切除组明显高于其他两组(均P<0.05)(表2)。
表2 术后各组AFP及肝功能指标比较(n=30,±s)Table 2 Comparison of postoperative AFP levels and liver function parameters among the 3groups (n=30, ±s)
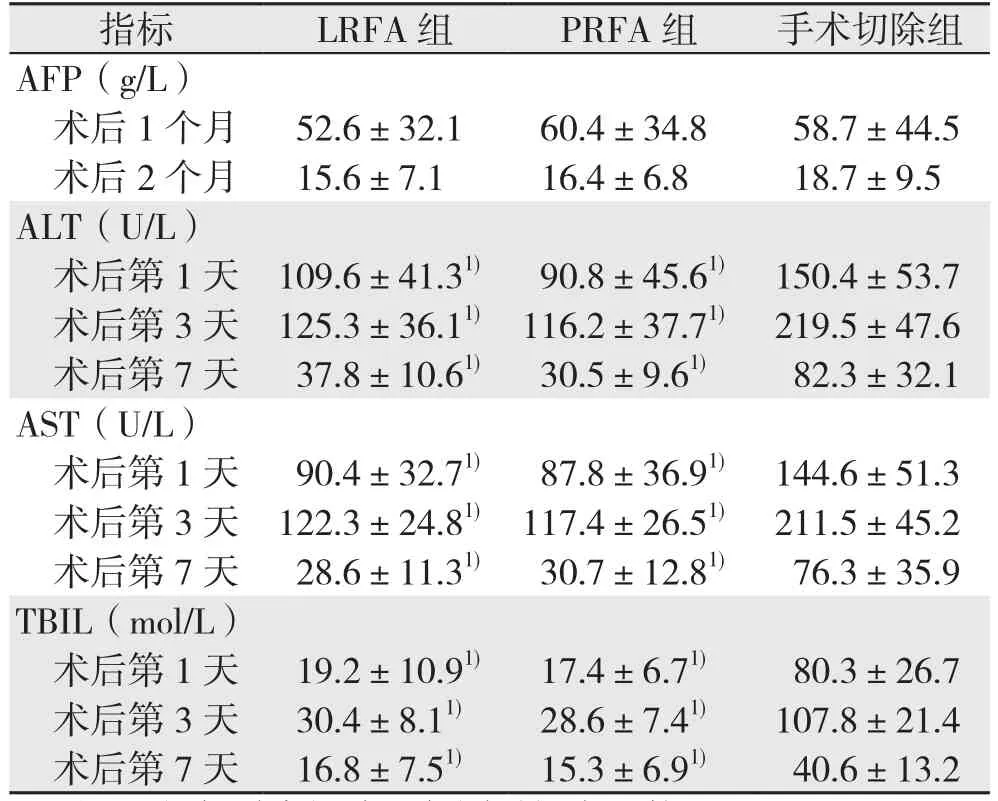
表2 术后各组AFP及肝功能指标比较(n=30,±s)Table 2 Comparison of postoperative AFP levels and liver function parameters among the 3groups (n=30, ±s)
注:1)与手术切除组与同时间点比较,P<0.05Note: 1) P<0.05 vs. surgical resection group of the same time point
指标 LRFA组 PRFA组 手术切除组AFP(g/L)术后1个月 52.6±32.1 60.4±34.8 58.7±44.5术后2个月 15.6±7.1 16.4±6.8 18.7±9.5 ALT(U/L)术后第1天 109.6±41.31) 90.8±45.61) 150.4±53.7术后第3天 125.3±36.11) 116.2±37.71) 219.5±47.6术后第7天 37.8±10.61) 30.5±9.61) 82.3±32.1 AST(U/L)术后第1天 90.4±32.71) 87.8±36.91) 144.6±51.3术后第3天 122.3±24.81) 117.4±26.51) 211.5±45.2术后第7天 28.6±11.31) 30.7±12.81) 76.3±35.9 TBIL(mol/L)术后第1天 19.2±10.91) 17.4±6.71) 80.3±26.7术后第3天 30.4±8.11) 28.6±7.41) 107.8±21.4术后第7天 16.8±7.51) 15.3±6.91) 40.6±13.2
2.2 围手术期并发症及其他结果
LRFA组和PRFA组的手术时间明显短于手术切除组(P=0.024),术中出血明显少于手术切除组(P=0.017),住院时间也明显短于手术切除组(P=0.031)。手术切除组术后并发症:胆瘘2例,肺部感染3例,胸腔积液2例,出血1例,腹腔积液1例,切口愈合不良1例;LRFA组术后并发症:发热1例,腹痛1例;PRFA组术后并发症:发热2例,腹痛4例,胸腔积液1例,皮肤灼伤1例。出现并发症患者经对症治疗后均完全缓解。3组间并发症的发生率差异有统计学意义(P=0.028),LRFA组并发症发生率明显低于PRFA组和手术切除组(P<0.05),而后两者之间差异无统计学意义(P>0.05)。术后1个月影像学及AFP结果表明LRFA组和手术切除组60例患者均达到CR,PRFA有4例未达到CR,2例进行了肝动脉栓塞化疗(TACE),2例进行了第2次PRFA治疗。PRFA组的肿瘤完全清除率明显低于其他两组,差异有统计学意义(P=0.016)(表3)。
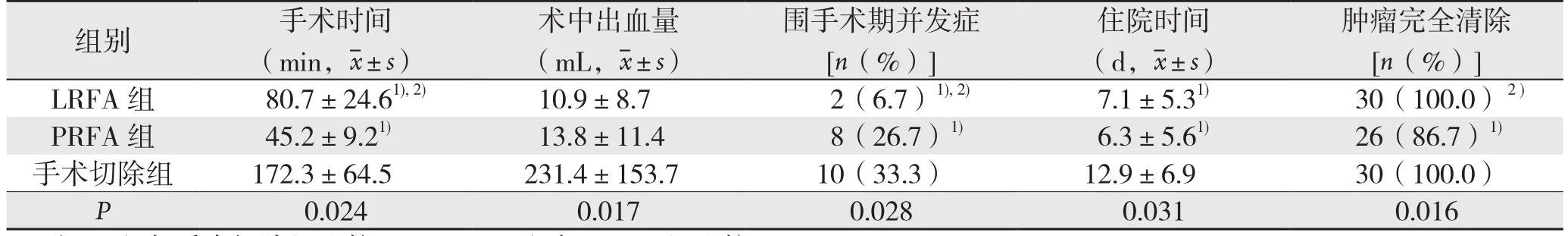
表3 各组围手术期指标比较(n=30)Table 3 Comparison of perioperative variables among the 3 groups (n=30)
2.3 无瘤生存率及复发情况
以36个月为随访期限,3组均无失访。LRFA组、PRFA组、手术切除组3年内复发率分别为33.3%、60.0%、26.7%,差异有统计学意义(P=0.021)。复发后将综合考虑患者的残余肝脏功能、肿瘤生长形态、大小、位置等方面的因素,选择手术、TACE、局部消融治疗以及姑息性镇痛等治疗。LRFA组、PRFA组、手术切除组的3年无瘤生存率分别为66.7%、40.0%、73.3%。3组的无瘤生存率采用Kaplan-Meier检验有统计学意义(χ2=8.480,P=0.014),PRFA组的无瘤生存率明显低于其他两组(图1)。PRFA组与LRFA组之间差异有统计学意义(χ2=3.925,P=0.048),同样与手术切除组比较时差异也具有统计学意义(χ2=7.265,P=0.007),而LRFA组和手术切除组之间差异无统计学意义(χ2=0.393,P=0.531)。
2.4 总生存率
在3年随访中,共1 4例患者死亡。LRFA组、PRFA组、手术切除组的3年总生存率分别为8 6.7%、7 6.7%、9 0.0%。采用Kaplan-Meier检验,3组的总生存率差异无统计学意义(χ2=2.396,P=0.302)(图2)。
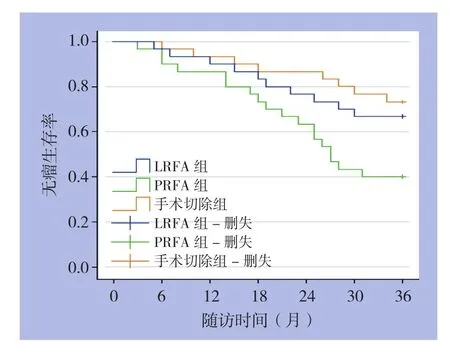
图1 各组3年无瘤生存率曲线Figure 1 The 3-year disease-free survival curves of the three groups
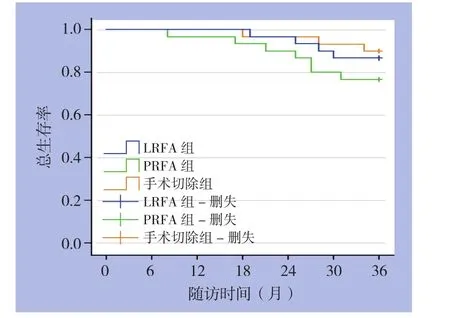
图2 各组的3年总生存率曲线Figure 2 The 3-year overall survival curves of the three groups
3 讨 论
肝癌是临床上常见的恶性肿瘤[8-9],目前其主要治疗方式[10-12]包括:手术切除、RFA、肝移植、TACE、无水酒精消融术(PEI)等,由于肝移植昂贵的治疗费用以及肝脏供体的短缺,肝移植无法广泛开展[13-14]。我国肝癌临床治疗中大多采取手术切除[15-16],且我国绝大部分肝癌患者合并不同程度的肝硬化,因此手术风险大,部分患者不能耐受手术,而射频消融则为此类患者提供了另一种根治性治疗方式。
RFA的直接作用是热毁损肿瘤组织[17-22],同时打破了肿瘤与宿主之间的动态平衡,激活机体局部和整体免疫系统,发挥独特抗肿瘤作用[23-25]。有研究[26-27]表明,肿瘤患者免疫功能低下和紊乱,而肿瘤细胞可以多种方式逃避免疫系统的监控。研究[28-30]表明患者术后免疫功能状况与肿瘤的复发、预后密切相关,射频消融术不仅能够清除病灶,还能够强化患者的免疫功能。因此RFA治疗肝癌,不仅仅是单纯物理性肿瘤消融,还可通过免疫增强获得全身治疗,是局部治疗和全身治疗的统一。由于射频消融毁损范围是以布针点为中心的球形区域,而要治疗体积较大或不规则生长的肿瘤,就需要多次烧灼[31-33]。PRFA治疗过程中高温产生蒸气及用二维影像技术的引导,使得其在治疗中很难区分已发生坏死的和残留的癌组织,也很难再精确穿刺定位进行多次消融。因此,传统的PRFA治疗肝肿瘤相对容易毁损不全和病灶残留,这在一定程度上增加了复发的风险[34]。相比于PRFA,LRFA可以在直视下进行操作及监测消融范围,准确定位肿瘤,灵活进行多点、多方位布针,达到肿瘤的完全毁损;同时,腹腔镜下可牵开肝脏周围组织及器官,充分暴露肿瘤,减少对周围组织的损伤,有效降低胆囊损伤、胃肠道损伤等并发症;此外,腹腔镜下易于识别和处理穿刺针道出血,清理腹腔内积血,减少腹腔感染。
由于医院当时未引进腹腔镜超声设备,故本次研究中LRFA组纳入的病例均为单发的位于肝脏表面的肝癌患者。本研究结果显示:PRFA组肿瘤完全清除率低于LRFA组,而围手术期并发症、复发率较LRFA高,且差异均具有统计学意义(P<0.05)。但术中出血量、术后肝功能、住院时间两组比较无统计学差异(P>0.05)。而LRFA组与手术切除两组之间复发率、3年无瘤生存率及总生存率之间差异均无统计学意义(P>0.05),但手术切除组术中出血量大,手术时间、术后住院时间明显较LRFA组长,患者术后肝功能恢复慢。因此,对于小肝癌治疗,LRFA具有创伤小、肝功能影响小优势,对于一些对于肝功能差、局部肝切除对肝功能打击较大和风险较高的肝癌患者,选择LRFA治疗可减小手术风险,同时又可达到与手术切除相同的根治性效果。
综上所述,本研究表明LRFA不仅具有术后恢复快、出血量少、住院日短等优点,其3年复发率、无瘤生存率及总生存率与手术切除无明显差异,可作为小肝癌的首选治疗方案之一。由于样本量少,随访时间短,还需要更多循证医学证据来进一步研究LRFA对于小肝癌的疗效。
[1] Ziemlewicz TJ, Wells SA, Lubner MG, et al. Hepatic Tumor Ablation[J]. Surg Clin North Am, 2016, 96(2):315–339. doi:10.1016/j.suc.2015.12.006.
[2] Miura JT, Johnston FM, Tsai S, et al. Surgical resection versus ablation for hepatocellular carcinoma ≤ 3 cm: a population-based analysis[J]. HPB (Oxford), 2015, 17(10):896–901. doi: 10.1111/hpb.12446.
[3] 崔芒芒, 朱晓琳, 张倜, 等. 射频消融治疗符合米兰标准的早期肝癌疗效分析[J]. 中国肿瘤临床, 2017, 44(11):539–543.doi:10.3969/j.issn.1000–8179.2017.11.256.Cui MM, Zhu XL, Zhang T, et al. Efficacy analysis of radiofrequency ablation in the treatment of early-stage hepatocellular carcinoma within the Milan criteria[J]. Chinese Journal of Clinical Oncology, 2017, 44(11):539–543. doi:10.3969/j.issn.1000–8179.2017.11.256.
[4] Xu Q, Kobayashi S, Ye X, et al. Comparison of hepatic resection and radiofrequency ablation for small hepatocellular carcinoma:a meta-analysis of 16,103 patients[J]. Sci Rep, 2014, 4:7252. doi:10.1038/srep07252.
[5] 白存海. 射频消融治疗单发小肝癌的效果及预后[J]. 中国现代普通外科进展, 2013, 16(9):722–723. doi:10.3969/j.issn.1009–9905.2013.09.015.Bai CH. Efficacy and outcomes of radiofrequency ablation for single small liver cancer[J]. Chinese Journal of Current Advances in General Surgery, 2013, 16(9):722–723. doi:10.3969/j.issn.1009–9905.2013.09.015.
[6] 曾鹏, 周乐杜, 王栋, 等. 射频消融治疗小肝癌疗效及预后因素分析[J]. 中国普通外科杂志, 2014, 23(7):904–909. doi:10.7659/j.issn.1005–6947.2014.07.008.Zeng P, Zhou LD, Wang D, et al. Radiofrequency ablation for small hepatocellular carcinoma: efficacy and prognostic factors[J].Chinese Journal of General Surgery, 2014, 23(7):904–909.doi:10.7659/j.issn.1005–6947.2014.07.008.
[7] 唐寒秋, 杨瑞. 腹腔镜下射频消融术对原发性肝癌的远期生存及安全性评价[J]. 医学综述, 2016, 22(11):2188–2191. doi:10.3969/j.issn.1006–2084.2016.11.032.Tang HQ, Yang R. Evaluation of the Long-term Survival and Safety of Laparoscopic Radiofrequency Ablation for Primary Hepatic Carcinoma[J]. Medical Recapitulate, 2016, 22(11):2188–2191.doi:10.3969/j.issn.1006–2084.2016.11.032.
[8] 张彪, 关连越, 付佩尧, 等. 射频消融、无水乙醇注射与手术切除治疗小肝癌疗效的Meta分析[J]. 中华肝胆外科杂志, 2015,21(11):729–732. doi:10.3760/cma.j.issn.1007–8118.2015.11.003.Zhang B, Guan LY, Fu PY, et al. Therapeutic effects of radiofrequency ablation, percutaneous ethanol injection or surgical resection on early stage hepatocellular carcinoma: a Metaanalysis[J]. Chinese Journal of Hepatobiliary Surgery, 2015,21(11):729–732. doi:10.3760/cma.j.issn.1007–8118.2015.11.003.
[9] Li L, Zhang J, Liu X, et al. Clinical outcomes of radiofrequency ablation and surgical resection for small hepatocellular carcinoma:a meta-analysis[J]. J Gastroenterol Hepatol, 2012, 27(1):51–58. doi:10.1111/j.1440–1746.2011.06947.x.
[10] Merchant N, David CS, Cunningham SC. Early Hepatocellular Carcinoma: Transplantation versus Resection: The Case for Liver Resection[J]. Int J Hepatol, 2011, 2011:142085. doi:10.4061/2011/142085.
[11] Lee KK, Kim DG, Moon IS, et al. Liver transplantation versus liver resection for the treatment of hepatocellular carcinoma[J]. J Surg Oncol, 2010, 101(1):47–53. doi: 10.1002/jso.21415.
[12] Zhu ZX, Huang JW, Liao MH, Zeng Y. Treatment strategy for hepatocellular carcinoma in China: radiofrequency ablation versus liver resection[J]. Jpn J Clin Oncol, 2016, 46(12):1075–1080.
[13] Omata M, Lesmana LA, Tateishi R, et al. Asian Paci fi c Association for the Study of the Liver consensus recommendations on hepatocellular carcinoma[J]. Hepatol Int, 2010, 4(2):439–474. doi:10.1007/s12072–010–9165–7.
[14] Benson AB 3rd, Abrams TA, Ben-Josef E, et al. NCCN clinical practice guidelines in oncology: hepatobiliary cancers[J]. J Natl Compr Canc Netw, 2009,7(4):350–391.
[15] 徐建波, 祁付珍, 许刚, 等. 原发性中小肝癌手术与射频消融治疗的疗效分析[J]. 现代肿瘤医学, 2013, 21(8):1822–1825.doi:10.3969/j.issn.1672–4992.2013.08.51.Xu JB, Qi FZ, Xu G, et al. Comparison of the efficacy of radiofrequency ablation and surgical resection for the treatment of small primary hepatocellular carcinoma[J]. Journal of Modern Oncology, 2013, 21(8):1822–1825. doi:10.3969/j.issn.1672–4992.2013.08.51.
[16] 荚卫东. 精准肝切除治疗肝细胞癌关键技术[J]. 中国普通外科杂志, 2014, 23(1):1–5. doi:10.7659/j.issn.1005–6947.2014.01.001.Jia WD. Key techniques in precise hepatectomy for hepatocellular carcinoma[J]. Chinese Journal of General Surgery, 2014, 23(1):1–5.doi:10.7659/j.issn.1005–6947.2014.01.001.
[17] Hu X, Zhang F, Liu XR, et al. Efficacy and potential microRNA mechanism for computed tomography-guided percutaneous radiofrequency ablation of primary lung cancer and lung metastasis from liver cancer[J]. Cell Physiol Biochem, 2014, 33(5):1261–1271.doi: 10.1159/000358694.
[18] 张雨康, 牛丽娟, 王勇. 射频消融在肝细胞肝癌临床治疗中的研究现状与进展[J]. 癌症进展, 2017, 15(1):15–17. doi:10.11877/j.issn.1672–1535.2017.15.01.05.Zhang YK, Niu LJ, Wang Y. Radiofrequency ablation in clinical treatment of hepatocellular carcinoma: current status and future directions[J]. Oncology Progress, 2017, 15(1):15–17. doi:10.11877/j.issn.1672–1535.2017.15.01.05.
[19] 姜川, 赵中伟, 朱锦德, 等. 射频消融与手术切除治疗小肝癌疗效比较[J]. 浙江医学, 2013, 35(11):1066–1067.Jiang C, Zhao ZW, Zhu JD, et al. Comparison of radiofrequency ablation and surgical resection in treatment of small liver cancer[J].Zhejiang Medical Journal, 2013, 35(11):1066–1067.
[20] 胡善雷. 经皮射频消融与手术切除治疗小肝癌的疗效对比分析[J]. 实用癌症杂志, 2015, 30(2):188–190. doi:10.3969/j.issn.1001–5930.2015.02.010.Hu SL. Comparison of effects of percutaneous radiofrequency ablation and surgical resection for small hepatocellular carcinoma[J]. The Practical Journal of Cancer, 2015, 30(2):188–190. doi:10.3969/j.issn.1001–5930.2015.02.010.
[21] Xu ZF, Xie XY, Kuang M, et al. Percutaneous radiofrequency ablation of malignant liver tumors with ultrasound and CT fusion imaging guidance[J]. J Clin Ultrasound, 2014, 42(6):321–330. doi:10.1002/jcu.22141.
[22] Yin T, Li W, Zhao P, et al. Treatment efficacy of CT-guided percutaneous microwave ablation for primary hepatocellular carcinoma[J] Clin Radiol, 2017, 72(2):136–140. doi: 10.1016/j.crad.2016.10.022.
[23] 梁博, 王国平. 微创介入疗法对肝癌患者 T细胞免疫功能的影响分析[J]. 实用癌症杂志, 2015, 30(4):488–490. doi:10.3969/j.issn.1001–5930.2015.04.005.Liang B, Wang GP. Effect of Minimally Invasive Interventional Therapy on T-cell Immunity in Patients with Hepatocellular Carcinoma[J]. The Practical Journal of Cancer, 2015, (4):488–490.doi:10.3969/j.issn.1001–5930.2015.04.005.
[24] 苗同国, 王立静, 马立伟, 等. 射频消融治疗对原发性肝癌患者T细胞免疫功能的影响[J]. 中国微创外科杂志, 2016, 16(6):538–540. doi:10.3969/j.issn.1009–6604.2016.06.017.Miao TG, Wang LJ, Ma LW, et al. Influence of Radio Frequency Ablation on T Lymphocyte Subsets in Patients with Primary Liver Cancer[J]. Chinese Journal of Minimally Invasive Surgery, 2016,16(6):538–540. doi:10.3969/j.issn.1009–6604.2016.06.017.
[25] 孙文兵. 浅述肝癌射频消融转化医学研究的几个重要问题[J].中华肝胆外科杂志, 2013, 19(11):804–807. doi:10.3760/cma.j.issn.1007–8118.2013.11.002.Sun WB. Some important issues in the translational medical research of radiofrequency ablation of liver cancer[J]. Chinese Journal of Hepatobiliary Surgery, 2013, 19(11):804–807.doi:10.3760/cma.j.issn.1007–8118.2013.11.002.
[26] 孔丽, 姚树坤, 刘金星, 等. 原发性肝癌患者细胞免疫功能变化及其与转归的关系[J]. 中华肝脏病杂志, 2005, 13(3):194–197.doi:10.3760/j.issn:1007–3418.2005.03.010.Kong L, Yao SK, Liu JX, et al. The prognostic value of cellular immunity function in patients with hepatocellular carcinoma[J].Chinese Journal of Hepatology, 2005, 13(3):194–197. doi:10.3760/j.issn:1007–3418.2005.03.010.
[27] Burke Schinkel SC, Carrasco-Medina L, Cooper CL, et al.Generalized Liver- and Blood-Derived CD8+ T-Cell Impairment in Response to Cytokines in Chronic Hepatitis C Virus Infection[J].PLoS One, 2016, 11(6):e0157055. doi: 10.1371/journal.pone.0157055.
[28] 杨闯, 张永川, 李华国, 等. 射频消融对原发性肝癌患者外周血T细胞亚群及NK细胞变化的影响[J]. 中国老年学杂志, 2014,(16):4489–4490. doi:10.3969/j.issn.1005–9202.2014.16.035.Yang C, Zhang YC, Li HG, et al. Influence of radiofrequency ablation on peripheral blood T subsets and NK cells in patients with primary hepatic carcinoma[J]. Chinese Journal of Gerontology,2014, (16):4489–4490. doi:10.3969/j.issn.1005–9202.2014.16.035.
[29] 陈余, 张建淮, 时汀, 等. 射频消融治疗对肝癌患者肝功能和免疫功能的影响[J]. 中国肿瘤临床与康复, 2014, 21(11):1374–1376.doi:10.13455/j.cnki.cjcor.2014.11.30.Chen Y, Zhang JH, Shi T, et al. Influence of liver function and immune function of hepatic cancer patients with radioactive interventional therapy[J]. Chinese Journal of Clinical Oncology and Rehabilitation, 2014, 21(11):1374–1376. doi:10.13455/j.cnki.cjcor.2014.11.30.
[30] 黄浩, 赵现伟, 谢斌, 等. 超声引导射频消融术治疗肝癌的疗效及对患者免疫功能、肝功能的影响[J]. 临床和实验医学杂志,2017, 16(9):892–895. doi:10.3969/j.issn.1671–4695.2017.09.018.Huang H, Zhao XW, Xie B, et al. Efficacy and influence of ultrasound-guided radiofrequency ablation on the immunological function and liver function of patients with hepatocellular carcinoma[J]. Journal of Clinical and Experimental Medicine, 2017,16(9):892–895. doi:10.3969/j.issn.1671–4695.2017.09.018.
[31] Beppu T, Nitta H, Tsukamoto M, et al. Percutaneous radiofrequency ablation-assisted laparoscopic hepatectomy[J]. Asian J Endosc Surg,2014, 7(2):188–192. doi: 10.1111/ases.12088.
[32] 独建库, 李冠海, 何伟华, 等. 经皮射频消融术与根治性切除术在小肝癌治疗中的疗效研究[J]. 临床军医杂志, 2012, 40(3):570–572. doi:10.3969/j.issn.1671–3826.2012.03.021.Du JK, Li GH, He WH, et al. The curative effect of percutaneous RFA and radical resection to small hepatocellular carcinoma[J].Clinical Journal of Medical Officers, 2012, 40(3):570–572.doi:10.3969/j.issn.1671–3826.2012.03.021.
[33] Livraghi T, Goldberg SN, Lazzaroni S, et al. Hepatocellular carcinoma: radio-frequency ablation of medium and large lesions[J].Radiology, 2000, 214(3):761–768.
[34] 马宽生. 对射频消融治疗肝肿瘤的一些思考[J]. 重庆医学, 2008,37(15):1644–1645. doi:10.3969/j.issn.1671–8348.2008.15.002.Ma KS. Some re fl ections on radiofrequency ablation in treatment of liver cancer[J]. Chongqing Medicine, 2008, 37(15):1644–1645.doi:10.3969/j.issn.1671–8348.2008.15.002.

