木制儿童用品中6种木材防腐剂的迁移规律研究
王志娟,赵而敬,张 庆,白 桦,吕 庆*
(1.中国检验检疫科学研究院 工业与消费品安全研究所,北京 100176;2.有研半导体材料有限公司,北京 100088)
木制儿童用品包括但不限于木制玩具、木制婴儿床等,因与儿童日常接触频繁,其化学安全性与儿童健康密切相关。木材防腐剂主要用于延长木材使用寿命,防止木材腐败、发霉和虫蛀[1]。然而,防腐剂大都是具有较高毒性的化学物质(如氯酚类化合物),对人体有内分泌干扰、致癌、致畸等危害[2-3],一些氯酚类化合物已被欧盟(EU)和美国环境保护署(EPA)列为优先控制污染物[4],并且欧盟玩具协调标准EN71-9[5]中对五氯苯酚等木材防腐剂作出1~10 mg/kg的限量要求。木材防腐处理一般采用压力处理法,而非化学键合[6],所以很容易在接触样品时通过口、皮肤等途径迁移到儿童体内,进而构成危害。
目前,国内外对木材防腐剂的研究主要集中于总量(即残留量)测定[7-10],关于防腐剂迁移量及迁移行为的研究鲜有报道[11-12],且未有木制儿童用品中防腐剂迁移的限量标准。已报道的迁移实验通常是将样品粉碎处理[13-14],处理方法简便快捷,并能快速地将样品中有害物质迁移出来。但是将样品粉碎后与儿童实际接触的样品状态(实际暴露场景)不一致,有研究表明防腐剂由木材样品向溶液中迁移时,主要是表面3 mm左右厚度层中的物质迁移出来[12]。本文通过搭建简易迁移装置,模拟实际暴露场景,基于建立的总量和迁移量测定方法,研究木制儿童用品中6种防腐剂的迁移规律及迁移率,为有效评估儿童用品中防腐剂的暴露风险提供基础数据,为我国制定相关标准及监管措施提供技术支持。
1 实验部分
1.1 仪器与试剂
TSQ8000 Evo 气相色谱-串联质谱仪(美国Thermo Fisher公司);CF16RXII离心机(日本Hitachi公司);SM2000 切割研磨仪(德国Retsch公司);固相萃取装置(美国Supelco公司);Oasis HLB固相萃取柱(6 mL,0.2 g,Waters公司);P300H型超声波清洗器(德国Elma公司);NTS-4000恒温水浴振荡器(日本Eyela公司);Syncore平行蒸发仪(瑞士Buchi公司)。
标准品:2,4-二氯苯酚、2,4,5-三氯苯酚、2,4,6-三氯苯酚、2,3,4,6-四氯苯酚、林丹、2,3,4-三氯苯酚(内标)均购自Accustandard公司,纯度≥98%;五氯苯酚购自Supelco公司,纯度≥99%。正己烷、乙酸乙酯、甲醇(色谱纯,美国Sigma公司);乙醇、冰乙酸、乙酸酐均为分析纯;实验用水为经Milli-Q制备的超纯水。
在超市和商场随机采购不同品牌的木制玩具样品,实验前用密封袋封好,以避免受到污染。
1.2 溶液配制
标准溶液配制:分别称取6种防腐剂标准品各100 mg于100 mL棕色容量瓶中,用乙醇-冰乙酸溶液(体积比9∶1)定容,配制成质量浓度1 000 mg/L的单标储备液,用单标储备液配制质量浓度100 mg/L的混合储备液。实验中用乙醇-冰乙酸溶液(9∶1)稀释成所需质量浓度的系列工作溶液。
内标溶液:称取50 mg 2,3,4-三氯苯酚于100 mL棕色容量瓶中,用乙醇-冰乙酸溶液(9∶1)定容,配制成500 mg/L的内标储备液,然后将其稀释成1 mg/L的内标工作溶液。
模拟唾液和汗液的配制参考欧盟DIN53160-2010标准[15-16]。
模拟唾液:分别称取0.17 g MgCl2·6H2O、0.15 g CaCl2·2H2O、0.76 g K2HPO4·3H2O、0.53 g K2CO3、0.33 g NaCl和0.75 g KCl,先将钾、钠盐溶于900 mL去离子水中,再加入MgCl2·6H2O和CaCl2·2H2O,全部溶解后用1%盐酸水溶液调至pH(6.8±0.1),然后用去离子水定容至1 L。避光保存,保证用前pH≈6.8±0.1。
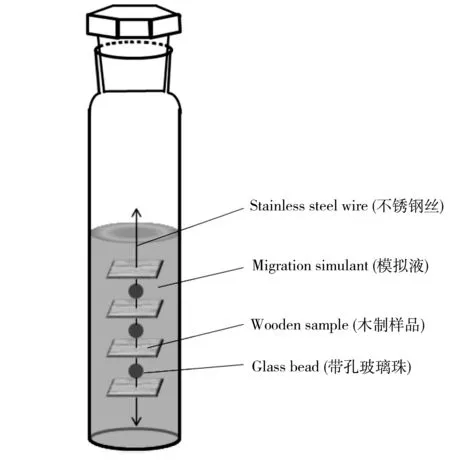
图1 自制迁移装置Fig.1 Illustration of self-made migration device
模拟汗液:分别称取5 g NaCl、1 g尿素、1 g 90%的乳酸于900 mL去离子水中,用1%氢氧化钠水溶液调至pH(6.5±0.1),然后用去离子水定容至1 L。避光保存,保证用前pH≈6.5±0.1。
1.3 阳性样品制备
将空白样品加工成长12 mm×宽15 mm×厚3 mm 的木片,然后将木片浸没在装有1 mg/L甲醇标准溶液的锥形瓶中(将100 mg/L混标储备液用甲醇稀释成1 mg/L),将锥形瓶密封后放置在旋转式混匀器中振摇24 h。然后将木片取出平铺在筛网上,置于通风橱中直至自然干燥,即得阳性样品。
1.4 样品前处理
总量测定:参见实验室前期文献[8]。
迁移量测定:迁移装置如图1所示,取木制样品光滑平整的部分,将其加工成长12 mm×宽15 mm×厚3 mm 的木片,在木片中间穿孔,用细不锈钢丝将4块木片串起,每两片中间以带孔玻璃珠间隔,以保证样品与模拟液充分接触。将制备好的样品放入50 mL比色管中,加入20 mL模拟液。将比色管密封后,放入37 ℃的恒温水浴振荡器中以100 r/min速度迁移,迁移时间2 min~96 h,获得迁移溶液。在迁移溶液中加入50 μL质量浓度为1 mg/L的内标工作溶液。然后在模拟唾液中加入1 mL乙酸酐进行衍生化,边振荡边放气,振荡1 min后置于摇床振荡5 min。模拟汗液中分别加入1 mL 0.1 mol/L碳酸钾溶液和1 mL乙酸酐进行衍生化。最后经5 mL正己烷液-液萃取,待上机分析。
1.5 仪器条件
色谱柱为HP-5MS(30 m × 0.25 mm × 0.25 μm);进样口温度290 ℃;载气为高纯氦气,流速1 mL/min;不分流进样,进样量2 μL;柱箱升温程序:初始温度60 ℃,以20 ℃/min升至200 ℃,再以25 ℃/min升至290 ℃,保持5 min。
传输线温度290 ℃,离子源温度300 ℃;EI电离,电离能量70 eV;采用SRM模式测定。优化的色谱及质谱参数如表1所示。
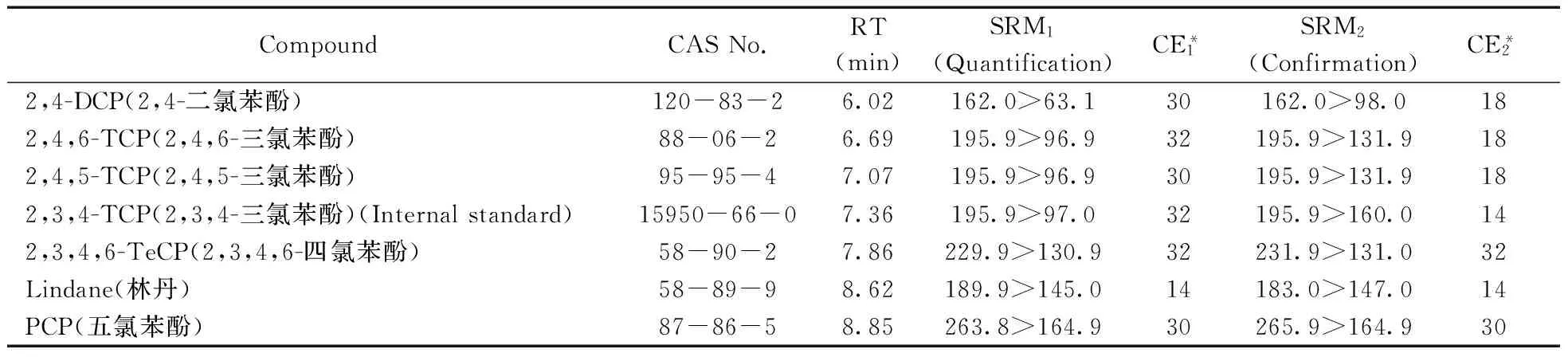
表1 6种防腐剂的色谱质谱参数Table 1 GC-MS/MS parameters of the target six preservatives
*collision energy(eV)
2 结果与讨论
2.1 总量及迁移量测定方法
总量测定方法参照实验室前期工作[8],方法对于2,4-DCP、2,4,6-TCP、2,4,5-TCP的定量下限为0.25 μg/kg(线性范围0.25~200 μg/kg),2,3,4,6-TeCP、林丹的定量下限为1 μg/kg(线性范围1~200 μg/kg),PCP的定量下限为2.5 μg/kg(线性范围2.5~200 μg/kg),各物质在其线性范围内相关系数均大于0.999 1。其中2,4-DCP、2,4,6-TCP、2,4,5-TCP的3个加标水平分别为0.25、2.5、50 μg/kg,2,3,4,6-TeCP和林丹的3个加标水平分别为1、10、50 μg/kg,PCP的3个加标水平分别为2.5、10、50 μg/kg,6种物质的平均加标回收率为90.2%~100.1%,相对标准偏差(RSD)为0.6%~6.1%(n=6)。应用此方法对16件木制玩具中防腐剂的初始含量进行测定,有检出的样品和物质如表2所示。其中2,4-DCP、2,4,6-TCP在6件样品中均有不同程度检出,检出量分别在1.13~6.08 μg/kg和0.25~8.27 μg/kg之间,低于目前欧盟的限量要求。

表2 木制玩具中木材防腐剂总量的测定结果Table 2 The residual amount determination results of preservatives in wooden toys
-:not detected
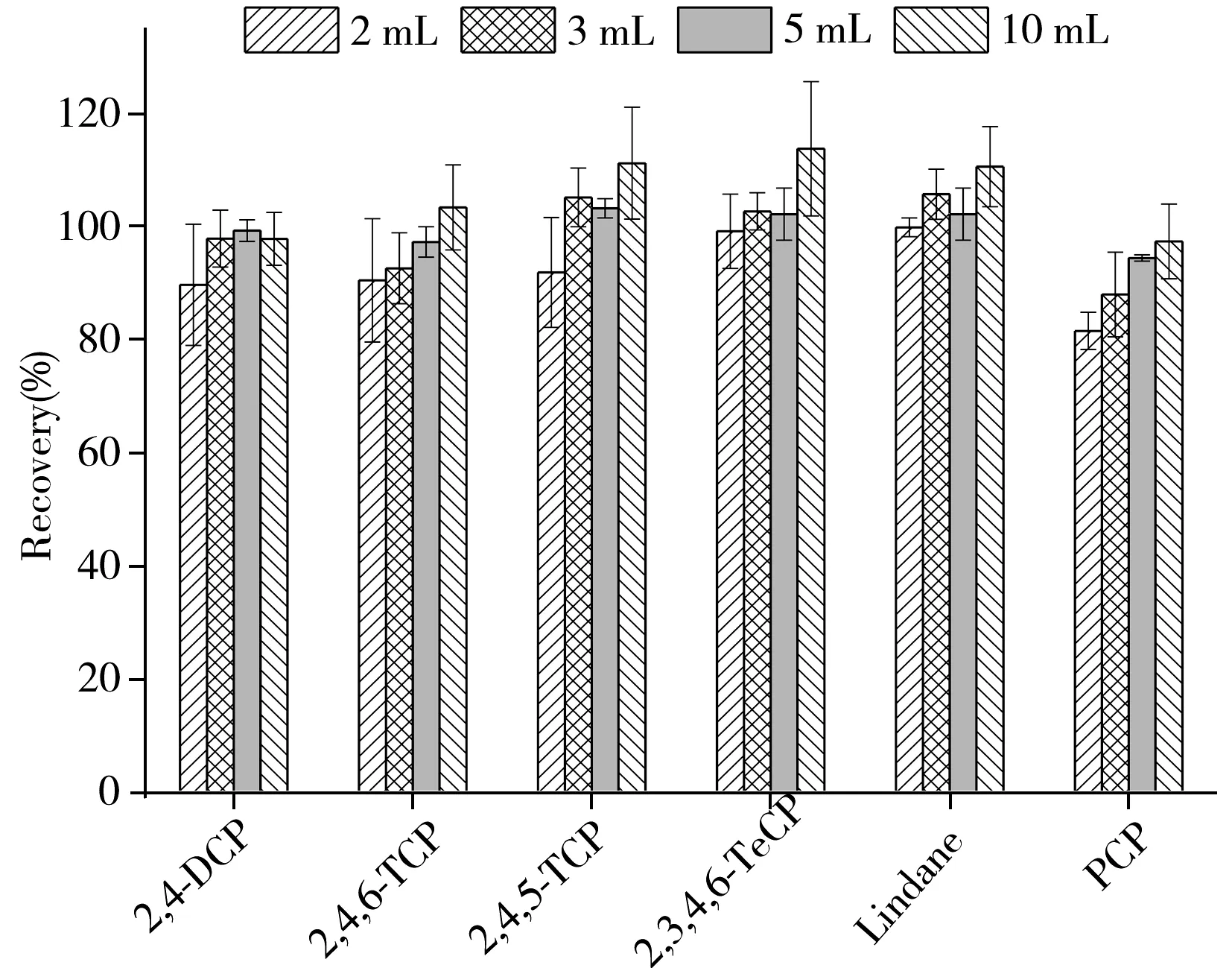
图2 不同体积正己烷对防腐剂的萃取效果Fig.2 Extraction effects of different volumes of n-hexane on preservatives
迁移量测定时,先将迁移溶液中目标物衍生化,然后进行液-液萃取。在20 mL模拟唾液中分别加入100 μL防腐剂混标(10 mg/L)和50 μL内标工作溶液(1 mg/L)作为迁移溶液,加入1 mL乙酸酐衍生化,然后以不同体积正己烷(2、3、5、10 mL)萃取目标物。结果如图2所示,溶剂体积为5 mL和10 mL时对6种物质的萃取率达到90%以上,综合考虑方法的灵敏度及取液方便性,最终选定5 mL正己烷萃取。对于模拟汗液,衍生化时只加入1 mL乙酸酐,2,4-DCP的回收率低于70%,当加入1 mL 0.1 mol/L碳酸钾溶液后再加入1 mL乙酸酐,2,4-DCP的回收率提高至93.0%~ 97.1%。此现象可能是由于模拟汗液中缺少碳酸根离子,而碳酸根的碱性介质是2,4-DCP衍生化的重要因素[2,17],因此对于模拟汗液,需先加入碳酸钾溶液后再衍生化。此方法在0.1~100 μg/L线性范围内的相关系数大于0.999 5,模拟唾液中3个加标水平的回收率为91.2%~117.7%,RSD≤6.4%(n=6),模拟汗液中3个加标水平的回收率为92.5%~114.4%,RSD≤9.7%(n=6)。
2.2 迁移规律探索
由于很难找到含有6种防腐剂的标准阳性样品,采用自制阳性样品的方法进行迁移规律研究。通过对16个木制玩具中防腐剂的总量测定,选出1个基质干净的空白样品按照“1.3”方法制备阳性样品。将制作好的阳性样品平分为3份,测得2,4-DCP、2,4,6-TCP、2,4,5-TCP、2,3,4,6-TeCP、林丹、PCP的平均含量分别为0.75、0.80、0.90、1.01、0.93、1.23 mg/kg,RSD小于15%,表明制作的阳性样品较为均匀,可以用于迁移规律的研究。其中,在同一添加量水平下,测得的6种目标物含量略有差异,此差异可能是在制作阳性样品过程中产生:即6种物质分子经甲醇渗透扩散至木材样品的情况有差别,且在平铺至通风橱自然干燥时,6种物质因沸点不同导致挥发损失的情况不同,由测定结果可知沸点较高的物质其测定结果也较大。
由于儿童通常会经皮肤和口接触儿童用品,为有效模拟儿童与样品的实际接触场景,探究6种防腐剂的迁移规律,将样品在模拟唾液和汗液中迁移2 min~96 h,迁移温度设置为人体温度37 ℃。简易迁移装置如图1所示,此装置可一次容纳多片样品,从而使得样品与模拟液的接触面积较大,迁移的物质量更多,进而降低迁移量测定的检出限。此外样品与迁移溶剂的接触面积基本固定,可保证每次实验操作的结果具有较好的重复性。
应用制作的阳性样品分别研究防腐剂在两种模拟液中随不同迁移时间的变化规律及对应的迁移率,迁移率定义为防腐剂迁移至模拟液的迁移量与其在样品中总量的百分比,按公式(1)进行计算。
(1)
式中:MR为防腐剂的迁移率;csimulant为防腐剂在迁移溶液中的质量浓度(mg/L);Vsimulant为迁移溶液的体积(L);csample为防腐剂在样品中的含量(mg/kg);msample为样品取样量(kg)。
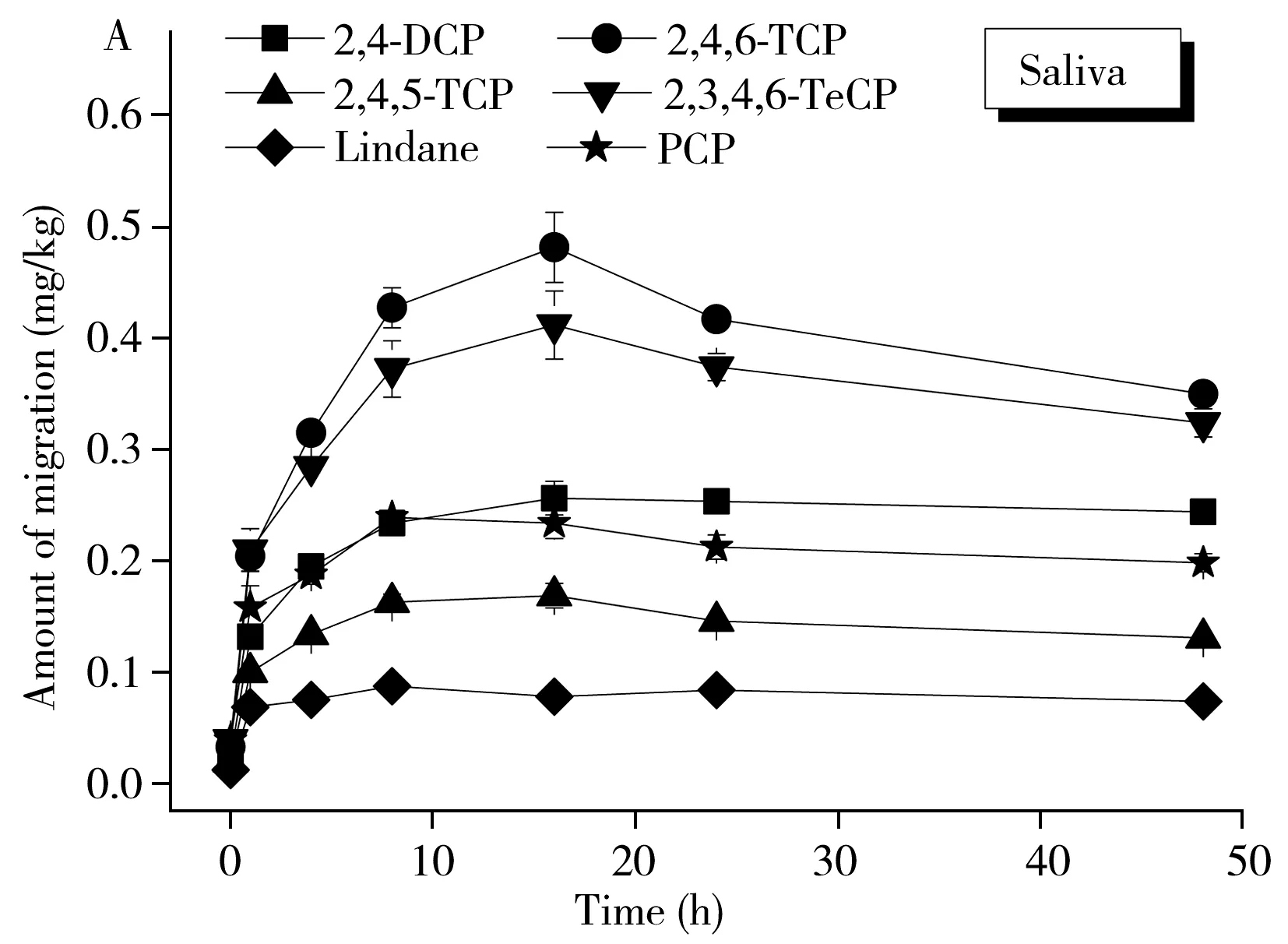
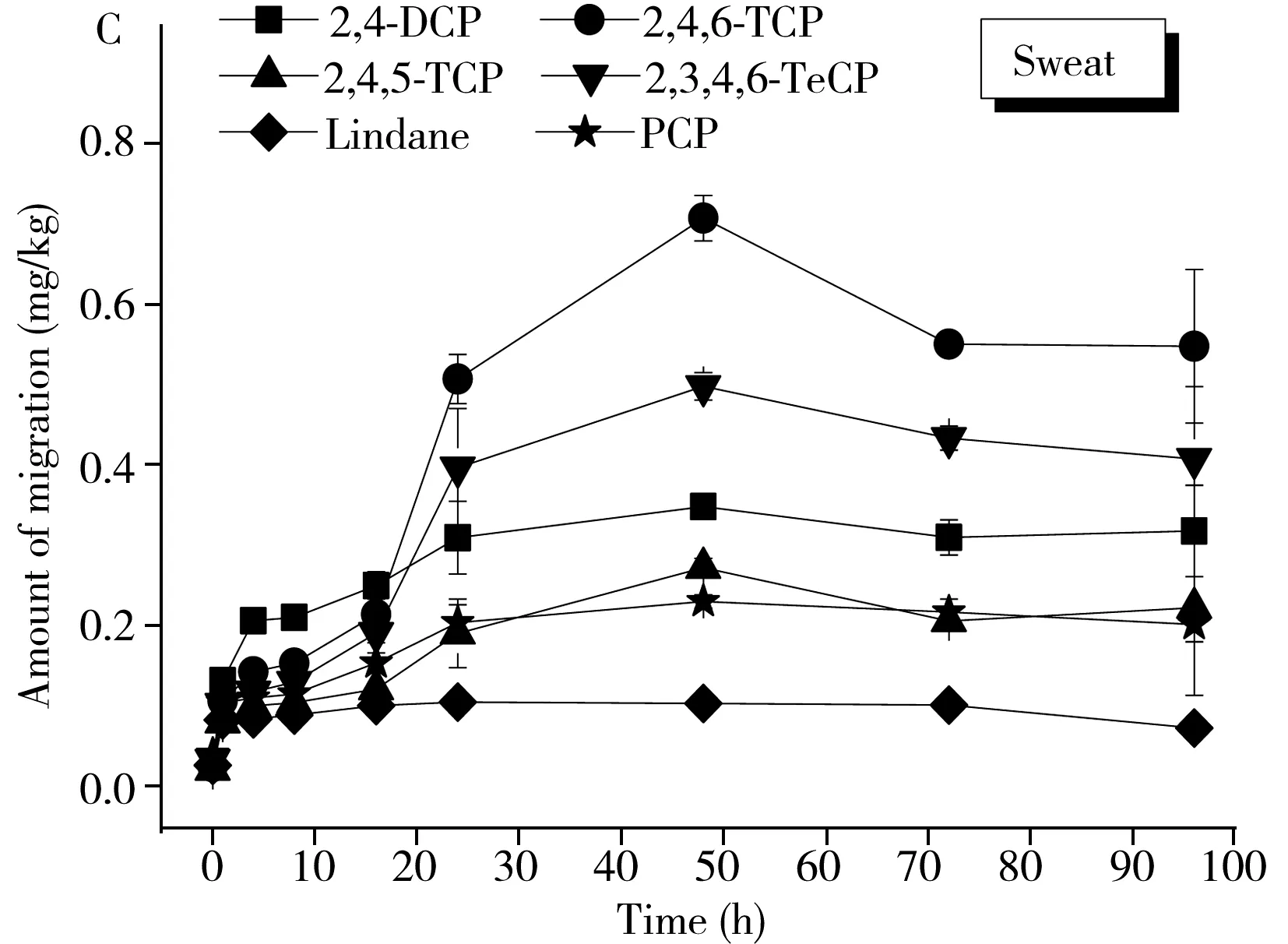
结果如图3所示,从图3A和C可知,6种防腐剂在模拟唾液和汗液中的迁移量均随着迁移时间的延长而逐渐增大,最后达到迁移平衡。防腐剂在模拟唾液中16 h左右即达到平衡,而在汗液中48 h左右才达到平衡,原因可能是由于两个模拟液的成分和pH值不同。图3B和D展示了6种防腐剂在两种模拟液中迁移率的变化,在迁移2 min~96 h范围内,防腐剂的迁移量随时间延长而逐渐增大,最终达到平衡,迁移率为2.1%~61.7%(唾液),2.2%~86.4%(汗液)。在样品与模拟液仅接触2 min时即有检出,迁移率分别为2.1%~4.2%和2.2%~3.3%。2,4,6-TCP在两种模拟液中的迁移率均高于其他物质,最大迁移率均大于50%,其他物质的最大迁移率为11.2%~46.1%。产生如此大的迁移率,究其原因:一是可能与目标物在水中的溶解性有关,如2,4,6-TCP溶解度为0.8 g/L,因而易于迁移到模拟液中;二是可能与木材疏松多孔的结构特性有关[18-19]。即各物质的迁移率大小可能是物质分子在模拟液中的溶解度和物质分子与木材结合能力相互作用平衡的结果,溶解度大有利于物质由木材样品迁移至溶液中,但由于木材为疏松多孔结构,物质分子与木材的吸附作用大则有利于溶液中的物质被吸附至木材样品;此外,迁移率大小还与模拟液的成分和pH值有关。
上述结果表明儿童在经口或手接触儿童用品时,木材防腐剂很可能在短时间内就迁移至人体中,进而对其身体健康产生危害。
2.3 实际样品测定
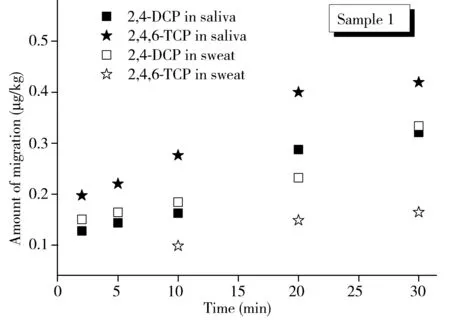
根据上述迁移规律的研究,发现木材防腐剂在短时间内就会有迁移,而且儿童每天持续接触样品的时间也较短,所以选定初始含量检出量较高的两个样品研究其在2~30 min的迁移行为(图4)。样品1和2在两种模拟液中均检出2,4-DCP和2,4,6-TCP,迁移量也随着迁移时间的延长而增加。样品1在模拟唾液中迁移2 min时,2,4-DCP和2,4,6-TCP即能被检出,迁移率分别为2.1%和2.4%。由于样品2中目标物的初始含量较低,仅2,4-DCP在模拟唾液中且迁移10 min时才有检出,在迁移10 min时2,4-DCP在唾液和汗液中的迁移率分别为10.1%和9.4%。
3 结 论
木制儿童用品中化学物质的迁移规律研究较少,而迁移危害对于消费者来说更接近于真实暴露场景。本文通过模拟实际接触环境,对自制阳性样品中6种防腐剂在模拟唾液和汗液中的迁移规律进行了研究。结果表明,由于氯酚类防腐剂的溶解性与在疏松多孔的木材中的相互分配平衡作用,导致防腐剂具有较大的迁移率,甚至在迁移2 min时即可检出。部分实际样品中检出了2,4-二氯苯酚和2,4,6-三氯苯酚,在儿童接触样品时,这些物质很可能在短时间随汗液或唾液迁移到身体中,对其健康构成危害。本研究可为相关暴露风险评估提供基础数据,为相关迁移实验提供借鉴。
[1] Konkler M,Morrell J J.J.Environ.Manage.,2017,203:273-277.
[2] Morais P D,Stoichev T,Basto M C P,Vasconcelos M T S D.Talanta,2012,89:1-11.
[3] Wang X X,Yang J,Xie S Y,Chen Y,Liu F L,Shen H Y,Xia Q H.J.Instrum.Anal.(王新鑫,杨军,谢晟瑜,陈扬,刘芳伶,沈昊宇,夏清华.分析测试学报),2015,34(11):1213-1219.
[4] Bagheri H,Mohammadi A,Salemi A.Anal.Chim.Acta,2004,513(2):445-449.
[5] BS EN71-9:2005.Safety of Toys-Part 9:Organic Chemical Compounds-Requirements.British Standard.
[6] Brocco V F,Paes J B,Costa L G,Brazolin S,Arantes M D C.JournalofCleanerProduction,2017,142:2093-2099.
[7] Ye X W,Niu Z Y,Yao P,Wang H H,Luo X,Xu H.J.Instrum.Anal.(叶曦雯,牛增元,姚鹏,王卉卉,罗忻,许辉.分析测试学报),2010,25(9):449-454.
[8] Lü Q,Li H Y,Li P,Li W T,Guo X Y,Wang Y,Bai H,Qi M L,Zhang Q.J.Chin.MassSpectrom.Soc.(吕庆,李海玉,李丕,李文涛,郭项雨,王烨,白桦,齐美玲,张庆.质谱学报),2013,34(6):321-329.
[9] Sarrión M N,Santos F J,Galceran M T.J.Chromatogr.A,2002,947(2):155-165.
[10] Becker R,Buge H G,Win T.Chemosphere,2002,47(9):1001-1006.
[11] Simonsen J,Chen H,Morrell J J,Freitag C,Clauson M.Holzforschung,2008,62(5):608-612.
[12] Lü Q,Guo X Y,Li H Y,Li P,Bai H,Qi M L,Zhang Q.Chin.J.Anal.Lab.(吕庆,郭项雨,李海玉,李丕,白桦,齐美玲,张庆.分析试验室),2014,33(6):678-683.
[13] Xu X X,Chen H L,Mao L S,Hu X N.FoodSci.(许欣欣,陈慧玲,毛丽莎,胡辛楠.食品科学),2016,37(14):193-197.
[14] Huang L N,Li H K,Yi L Z,Peng F,Li Q.J.Chin.MassSpectrom.Soc.(黄理纳,李函珂,蚁乐洲,彭峰,李琼.质谱学报),2016,37(5):453-464.
[15] DIN 53160-1:2010-10.Determination of the Colourfastness of Articles for Common Use-Part 1:Test with Artificial Saliva.German Standard.
[16] DIN 53160-2:2010-10.Determination of the Colourfastness of Articles for Common Use-Part 2:Test with Artificial Sweat.German Standard.
[17] Campillo N,Pealver R,Hernández-Córdoba M.J.Chromatogr.A,2006,1125:31-37.
[18] Yin J P,Yuan T Q,Lu Y,Song K L,Li H Y,Zhao G J,Yin Y F.CarbohydratePolymers,2017,155:163-172.
[19] Wang S,Liu M,Jia S S,Qing Y,Wu Y Q.JournalofCentralSouthUniversityofForestryandTechnology(王爽,刘明,贾闪闪,卿彦,吴义强.中南林业科技大学学报),2017,37(4):104-108.

