兽用烟酸阿莫西林可溶性粉的安全性试验
孟冬霞 ,武果桃 ,任 杰,卫顺生 ,孟 帆,赵 娟,马政禹,刘晓东,夏艳婷
(1.山西省农业科学院畜牧兽医研究所,山西 太原 030032;2.山西农业大学,山西 晋中 030801;3.甘肃省武乡县动物卫生监督所,山西 武乡 046300)
阿莫西林属半合成广谱抗生素,通过抑制细菌细胞壁的合成而起抗菌作用。用于敏感菌所致的肺部、尿道感染和革兰氏杆菌引起的某些感染等,例如牛巴氏杆菌病、乳腺炎、肺炎,犊、驹肺炎,猪传染性胸膜肺炎,鸡白痢、禽伤寒等。对肠球菌属和沙门氏菌的作用较氨苄西林强2倍。但由于阿莫西林水溶性不好,临床应用时易造成药物损失,无形中增加养殖成本。烟酸阿莫西林可溶性粉是由烟酸和阿莫西林研制而成的一种新型兽药制剂,提高了阿莫西林的溶解度和生物利用度,在兽医临床中有广阔的应用前景。为保证其在兽医临床中的安全应用,选用昆明系小鼠灌胃给药进行急性毒性试验、清洁级SD大鼠灌胃给药进行亚急性毒性试验,为临床用药奠定理论基础,为开展药效学研究提供科学依据。
1 材料
1.1 试验药物
烟酸原料药,含量99.8%,批号120203,天津中瑞药业有限公司生产;阿莫西林原料药,华北制药集团先泰药业有限公司生产,批号:101150510112;烟酸阿莫西林可溶性粉,为课题组自行研制而成,使用时用0.5%羧甲基纤维素钠配制成所需浓度。
1.2 主要试剂
羧甲基纤维素钠,成都市科龙化工试剂厂生产,批号:20130821;大、小鼠饲料,北京科澳协力饲料有限公司生产,批号:16043211、16063211;碱性磷酸酶(ALP)试剂盒(批号P1502011)、丙氨酸氨基转移酶(ALT)试剂盒(批号P1506011)、天冬氨酸氨基转移酶(AST)试剂盒(批号P1504021)、尿素(BUN)试剂盒(批号 P1411011)、尿酸(UA)试剂盒(批号P1412021)、肌酐(CREA)试剂盒(批号D1507091)、白蛋白(ALB)试剂盒(批号 L1505013)、总蛋白(TP)试剂盒(批号L1508013),试剂盒均为上海复星长征医学科学有限公司生产。
1.3 主要仪器
JMB30001型电子天平;石蜡包埋机,Histocentre 3,英国Shandon;石蜡切片机,Finesse 325,英国 Shandon;全自动组织脱水机,Excelsior,英国Shandon;荧光显微成像系统,BX53,日本Olympus公司;Konelab PRIME 30全自动生化分析仪(美国Thermo Fisher公司);HEMAVET 950全自动五分类动物血液分析仪(美国Drew Scientific公司)。JEM 1011显微镜。
1.4 试验动物
清洁级昆明系小鼠100只,体重18~22g,雌雄各50只,购自山西省肿瘤医院;清洁级SD大鼠40只,体重150~190g,雌雄各20只,购自山西医科大学实验动物中心;动物环境适应和检疫观察期为5d,检疫期内小鼠及大鼠皮毛光滑、行为及外观正常、无异常分泌物等,未发现异常动物。灌胃前14h禁食、不禁水,灌胃后3~4h恢复正常进食,常规饲养。
1.5 饲养条件
饲养室温度21.0±0.5℃,湿度66.7±3.9%,12h照明,12h黑暗。标准饲养笼内饲养,每笼5只,每周换笼2次。每日作业结束后清扫,擦拭笼架、台面,每周五用消毒液擦拭消毒,每周轮流更换消毒剂种类。垫料,大厂回族自治县陈府伊甸园垫料加工厂生产,经中国辐射防护研究院辐照中心钴-60辐照灭菌后使用。饮水,由饮水瓶供应经高压灭菌的自来水,自来水经国家城市供水水质监测网太原监测站检验(检测报告编号:W2015723),符合《生活饮用水卫生标准》(GB5749-2006)要求。每日更换饮水瓶,饮水瓶经清洗、高压灭菌后使用。
2 方法
2.1 急性毒性试验
2.1.1 预试验 用改良冠氏法进行LD50测定。取60只小鼠,随机分为6组,每组10只,雌雄各5只。各组小鼠分别按0.2mL/10g·bw的剂量灌服相应浓度的受试药液。受试药液浓度 分 别 为 1000mg/kg.bw、1500mg/kg.bw、2000mg/kg.bw、3000mg/kg.bw、5000 mg/kg.bw,空白组灌服同等剂量的蒸馏水。连续观察7d,记录小鼠的精神状态、食欲、活动状况、呼吸、粪便及死亡情况。第8d每组随机取2只处死剖检观察脏器、体腔积液等病理变化。
2.1.2 正式试验 根据预试验结果,进行最大给药量试验。选取40只小鼠,随机分为2组,每组20只,雌雄各半,试验组用5000mg/kg.bw灌胃给药1d,连续观察7d,详细记录小鼠反应情况。在观察期间保证食、水、温度等生活条件,严防非试验因素引起的死亡。第8d各组随机剖解2只,观察脏器病理变化。
2.2 亚急性毒性试验
将清洁级SD大鼠40只随机分为高、中、低剂量组及对照组,每组10只,雌雄各半,1~3组为试验组,每天同一时间灌胃给药,药物浓度分别为4800mg/kg.bw、2400mg/kg.bw、1200mg/kg.bw,4组为对照组,灌服蒸馏水。连续给药28d,观察并记录大鼠的生理行为,包括精神状态、饮食情况、活动状况、被毛光泽度腺体分泌、粪便性状及体重增长情况。在观察期间保证食、水、温度等生活条件,严防非试验因素引起的死亡。给药结束时各组随机取5只大鼠用水合氯醛麻醉,腹主动脉采血,进行血常规检验、血清生化指标测定,并进行解剖肉眼观察各脏器颜色、形状、大小等组织病变情况。取肝、双肾称重,计算脏器系数(脏器重量g/体重g);并每组随机选3只大鼠进行肝、肾病理组织学及超微结构检查。各组剩余的5只大鼠停止给药,进行恢复期试验。常规饲养10d,进行血常规检验、血清生化指标检测、脏器系数计算;每组随机取3只大鼠进行肝肾病理组织学及超微结构检查。
2.3 检测指标及方法
血液学指标:采用HEMAVET 950全自动五分类动物血液分析仪(美国 Drew Scientific公司)测定,测定方法见表2;血液生化指标均采用Konelab PRIME 30全自动生化分析仪(美国Thermo Fisher公司)测定,检测指标包括碱性磷酸酶、谷丙转氨酶、谷草转氨酶、尿素、尿酸、肌酐、白蛋白及总蛋白,测定方法见表3。
2.4 组织病理学及超微结构检查
试验结束后各组随机选取3只大鼠迅速剖杀,采集肝、肾参照文献[3]进行病理组织学及超微结构检查。
2.5 统计学分析
采用SPSS 17.0软件对试验数据进行统计分析,采用ANOVA程序进行方差分析和邓肯氏(Duncan)多重比较,试验数据以均值±标准差表示。
3 结果与分析
3.1 急性毒性试验结果
3.1.1 预试验结果 小白鼠给药7d内,各组精神状态良好,口及肛门无异常分泌物,皮毛洁净,呼吸正常,食欲及活动状态未见异常,未见中毒症状和死亡。测不出LD50。各组随机取2只小鼠处死进行病理剖检,未出现眼观病理变化。
3.1.2 最大给药量试验结果 小鼠经最大剂量5000mg/kg灌胃给药后,精神状态良好,被毛光泽洁净,采食、饮水、排便、排尿等均无异常,口、鼻、眼均无异常分泌物,无死亡现象。7d后各组随机剖检2只,均未见脏器有异常病理变化,
故LD50>5000mg/kg。据文献报道LD50为5000mg/kg时认为无毒性,故表明烟酸阿莫西林可溶性粉急性毒性分级属低毒级。

表1 烟酸阿莫西林对大鼠体重的影响

表2 烟酸阿莫西林对大鼠血液生理指标的影响(n=5)

表3 烟酸阿莫西林对大鼠血液生化指标及脏器系数的影响(n=5)

图1 对照组 肝脏组织切片HE×200
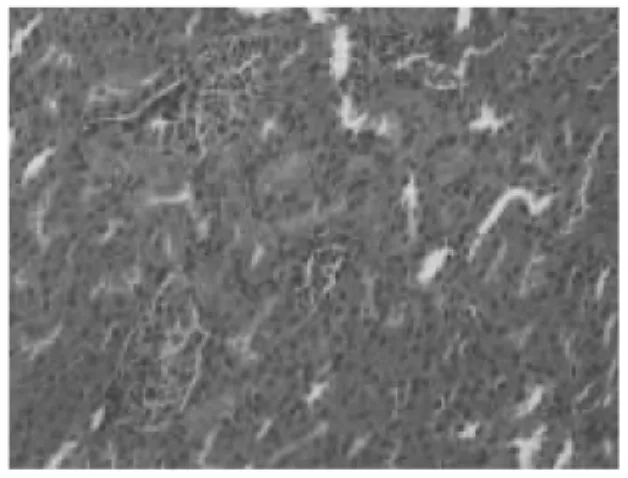
图2 对照组 肝脏组织切片HE×200

图3 高剂量肝脏组织切片肝脏中央静脉扩张,周围肝细胞肿胀 HE×200

图4 中剂量肝脏组织切片肝脏枯否氏细胞增生 HE×200
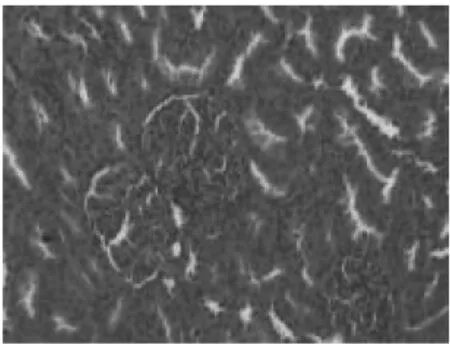
图5 高剂量组肾脏组织切片肾小球内细胞增生 HE×200
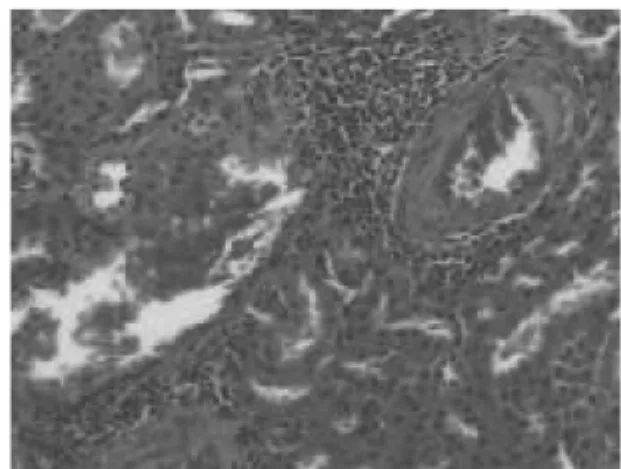
图6 中剂量组肝脏组织切片局部间质血管周围炎性细胞浸润HE×200

图7 对照组肝脏超微结构线粒体正常、嵴排列整齐,内外膜完整,内质网排列规则

图8 对照组肾脏超微结构微绒毛排列整齐

图9 高剂量组肝脏超微结构核规律,内外膜完整,线粒体形状规则,部分嵴断裂

图10 中剂量肝脏超微结构核完整,内质网排列整齐,个别线粒体变形,双层膜完整,少部分嵴断裂

图11 高剂量组肾脏超微结构核外膜肿胀,线粒体部分空泡化嵴断裂

图12 中剂量组肝脏超微结构核膜肿胀,微绒毛边缘有脱落现象
3.2 亚急性毒性试验结果
3.2.1 烟酸阿莫西林对大鼠生理行为及体重变化影响 试验组大鼠灌胃给药后生长良好,口、鼻、眼均无异常分泌物、体温、呼吸、脉博及排便均正常,饮食情况、精神状态、活动状况和被毛光泽度等与对照组无显著差异。给药期间,大鼠未出现死亡。体重变化情况见表1,由表1可知,各组大鼠均有不同幅度的体重增加,给药28d时,对照组及高、中、低剂量组分别增重 109.2g,101.5g、106g、108.9g,各试验组大鼠体重变化幅度与对照组相比,差异均不显著(p>0.05);停药10d时,对照组及高、中、低剂量组分别增重130.5g、126.7g、126.4g、129.2g,各试验组大鼠体重变化幅度与对照组相比,差异均不显著(p>0.05)。
3.2.2 烟酸阿莫西林对大鼠血液生理指标的影响 血常规测定结果见表2。由表2可知,给药28d时,高剂量组白细胞显著低于对照组(p<0.05),其余各组检测指标与对照组相比,差异均不显著(p>0.05)。停药10d时,各组检测指标与对照组相比差异均不显著(p>0.05)。表明长期大剂量口服烟酸阿莫西林可引起白细胞降低,但此不良反应在停药后即可消失。
3.2.3 烟酸阿莫西林对大鼠血液生化指标及脏器系数的影响 血液生化指标及肝、肾脏器系数测定结果见表3。由表3可知,给药28d时,高、中剂量组碱性磷酸酶、谷丙转氨酶、谷草转氨酶、肌酐、总蛋白均显著低于对照组(p<0.05);其它指标各试验组与对照组相比差异均不显著(p>0.05);停药10d时,各组生化检测指标及肝、肾脏器系数与对照组相比差异均不显著(p>0.05)。表明长时间大剂量用药,对肝、肾均有一定的影响,但这种影响停药后即可消失。
3.2.4 烟酸阿莫西林对大鼠病理组织变化及超微结构的影响 给药28d,各组随机剖解3只,心、肝、脾、肺、肾、胃和肠的形态、颜色、质地均未见异常。正常肝、肾组织切片见,高、中剂量组肝脏组织切片。高、中剂量组肾脏组织切片;正常肝、肾超微结构。高、中剂量组肝脏超微结构。高、中剂量组肾脏脏超微结构。停药10d,肝、肾组织切片及超微结构均未见异常。
4 讨论
4.1 急性毒性试验是安全性评价的重要内容。在本试验中,以最大给药浓度5g/kg.bw一次给药,小鼠无死亡现象,根据新兽药一般毒性试验技术要求,可初步判定烟酸阿莫西林毒性较低,较安全。
4.2 亚急性毒性试验过程中,连喂28d,大鼠的饮食、行为、排泄、精神状态、活动状况和被毛光泽度等与对照组无显著差异,体重也随天数增加而增加,增加幅度与对照组相比,差异不显著(p>0.05),表明烟酸阿莫西林对大鼠生长发育无抑制作用。
4.3 血液成份的检测是检验药物毒性的一个重要指标。连续给药28d,高剂量组大鼠白细胞显著低于对照组(p<0.05),停药10d,则差异不显著(p>0.05)。表明长期大剂量服用烟酸阿莫西林可引起白细胞降低,但停药后即可恢复正常。
4.4 谷丙转氨酶、谷草转氨酶、碱性磷酸酶、白蛋白、总蛋白是检查肝功能的重要指标。尿素氮、尿酸、肌酐是检查肾功能的主要指标。通过对大鼠给药后血液生化指标的测定,可以判断药物对机体脏器的毒性作用情况。动物的脏器重量与脏器指数是生物医学研究的重要基础指标,动物脏器重量与其指数的测定,既能反映脏器本身的结构改变,同时还可以反映生理性功能状态,如免疫功能、生殖功能等。脏器系数增大,反映该脏器肿大,病变可能为增生、充血、水肿等;脏器系数变小,可能反映脏器发育不良或萎缩等变化。不仅对动物饲养管理和生理状态具有指导意义,而且是进行毒理学、病理学研究和探讨发病机理等研究时选择动物的依据。本试验结果表明,大鼠长期大剂量使用该药,对心、肝、脾、肺、肾、胃和肠的形态、颜色、质地及肝、肾脏器系数影响不明显,对肝、肾代谢有一定的影响,但停药10d后不良反应即可消除。
4.5 脏器形态结构改变将直接影响机体的正常功能。本试验通过组织切片及电镜检查,为肝、肾细胞早期损伤的形态学改变提供依据。试验结果表明,长期大剂量使用,可对肝、肾有一定的损伤,但这种损伤可以通过机体自身恢复。
综上所述,无论从血液、生化指标还是从组织切片、电镜超微结构来看,长期大剂量使用烟酸阿莫西林对肝、肾均有一定的影响,建议临床使用时注意控制药物剂量和使用时间。
[1]陈杖榴,等.兽医药理学[M].北京.中国农业出版社,2009.
[2]沈建忠.动物毒理学[M].北京:中国农业出版社,2002:38-39.
[3]任杰,等.复方中药对热应激肉鸡肝细胞保护作用研究[J].中兽医医药杂志,2015(2):18-21.
[4]王占庆.丙磺舒对阿莫西林的急性毒性、组织分布及药代动力学的影响[D].长春:中国人民解放军军需大学,2002.
[5]李明雁,等.阿莫西林-泰乐菌素复方药物的安全性试验[J].中国兽医杂志,2010(9):66-68.
[6]陈华,等.SPF、清洁及普通级大鼠部分生物学特性的比较[J].中国实验动物学杂志,1999,9(1):28-33.
[7]王尧,等.不同月龄SPF级SD雌性大鼠主要脏器参数的研究[J]。四川生理科学杂志,2009,31(4):155-156.
[8]赵毓梅,等.给药方式对大鼠体重影响的研究[J]。中国热带学,2004,(2):202-203.

