小麦分子伴侣TaTCP22基因克隆及特性分析
胡晓薇+田原+乔梦+付金梅+张小红+闵东红
摘要: 非生物胁迫可引起蛋白的功能紊乱,维持蛋白的功能构象和阻止非天然蛋白的聚合,对于细胞存活很关键。伴侣素可以帮助蛋白质在胁迫条件下复性,在植物抵抗非生物胁迫中扮演着非常重要的角色。为分析伴侣素TaTCP22的分子特性,解析伴侣素的胁迫响应机制,以小麦的cDNA为模板扩增得到TaTCP22 ,利用生物信息学方法分析小麦TaTCP22 的分子特性,使用MEGA5对小麦TaTCP22蛋白序列及其同源序列进行多序列比对分析并构建同源物种间的系统进化树;利用GSDS和PHYRE2在线工具分别对小麦TaTCP22 基因结构和三级结构进行分析;从Phytozome数据库中获取小麦TaTCP22 上游2 000 bp序列作为启动子,用PLACE数据库对小麦TaTCP22 启动子的顺式作用元件进行分析;利用实时荧光定量PCR检测TaTCP22 在不同组织及在脱落酸(abscisic acid,简称ABA)、聚乙二醇(polyethylene glycol,简称PEG)、水杨酸(salicylicacid,简称SA)、氯化钠(NaCl)、低温胁迫处理下的表达量;利用In-Fusion技术构建TaTCP22 -16318GFP载体,采用PEG介导法将外源基因转到小麦原生质体中,在激光共聚焦显微镜下观察基因定位情况。小麦TaTCP22 全长1 643 bp,基因编码区包含UTR区和13个内含子以及13个外显子;启动子元件分析表明,TaTCP22 包含多种逆境胁迫应答元件;亚细胞定位结果表明,TaTCP22蛋白主要定位在细胞核、细胞膜和细胞质中;实时荧光定量PCR结果显示,TaTCP22在不同组织中的表达水平不同;TaTCP22 对于多种非生物胁迫均有不同程度的响应,说明TaTCP22 可能参与了多种胁迫应答途径。
关键词: 小麦;分子伴侣;TCP-1;胁迫响应;亚细胞定位
中图分类号: Q785;S512.101 文獻标志码: A
文章编号:1002-1302(2017)22-0027-05
小麦是主要的粮食作物之一,其生长发育、产量及品质受到干旱、低温、盐和病虫害等生物和非生物胁迫的极大限制。仅盐害就影响约20%的灌溉农业[1],因此揭示小麦抗逆的分子机制,对提高小麦产量和品质有重要意义。非生物胁迫通常造成蛋白质功能紊乱,维持蛋白质的功能结构域和阻止与非功能蛋白质聚合是细胞在非生物胁迫下存活的关键。热激蛋白/分子伴侣是一类在细胞中帮助其他蛋白折叠、组装、运输、降解的蛋白质,在非生物胁迫下,可帮助其他蛋白质复性。热激蛋白/分子伴侣可分为5类:HSP70家族、伴侣素(HSP60)、HSP90家族、Hsp100/Clp家族、小分子热休克蛋白家族[2-3]。TCP-1属于伴侣素(HSP60)家族,伴侣素广泛存在于生物界,被分为2类:GroE(Ⅰ型)和伴侣素CCT(Ⅱ型)[4]。Ⅰ型是在细菌、线粒体、叶绿体中发现的,Ⅱ型是在古细菌和真核生物的细胞质中发现的[5]。CCT是一种广泛存在于细胞浆中的异型寡聚蛋白,在肌动蛋白、微管蛋白的组装和折叠中发挥重要的作用,具有相同的双环背靠背垛叠结构(back to back stacked rings),由14~18个亚基组成,每个亚基的分子量约为60 ku。真核细胞的CCT由2个花托样结构构成,只有少数蛋白是与CCT结合的天然底物[6]。除哺乳动物睾丸中发现的一种组织特异性亚基类型CCTζ-2外,所有生物的CCT都由8个相同的亚基(α、β、γ、δ、ε、ζ、η、θ)构成[7]。Yamada等从红树林cDNA中克隆BsCCTα转化的大肠杆菌能增强对盐和渗透胁迫的忍耐性[8]。前期研究主要集中在CCT伴侣素的结构、功能及作用底物方面,且在动物中的研究较多,而对CCT在植物体中响应胁迫的功能研究较少。本研究从小麦中克隆到1个伴侣素基因TaTCP22,并对小麦TaTCP22 的生物学特性以及参与非生物胁迫的应答机制进行研究,为阐述CCT提高小麦抗逆性的分子机制提供理论依据。
1 材料方法
1.1 试验材料
小麦轮选987种子由西北农林科技大学小麦育种课题组提供。16318 GFP载体由笔者所在实验室保存。小麦播种在土中(蛭石、泥炭土体积比=1 ∶ 1),在温室适宜的条件中生长2周,取出后用蒸馏水将根冲洗干净,置于滤纸上进行干燥处理,将干燥后的整株放入液氮中冷冻10 min后取出并迅速保存到 -80 ℃ 冰箱中准备提取RNA。
1.2 方法
1.2.1 基因TaTCP22 的全长克隆
利用美国国立生物技术信息中心(NCBI)网站的相关程序对测序结果进行比对,找出小麦TaTCP22 基因的全长序列,利用DNAMAN设计正向引物5′-ATGGGCGGCCCAGGC-3′和反向引物5′-TTAAGGCTTGAGAGCAATCG-3′。以小麦cDNA为模板进行PCR扩增,扩增片段总长为828 bp,反应程序为95 ℃ 5 min;95 ℃ 45 s,60 ℃ 45 s,72 ℃ 1 min,30个循环;72 ℃ 10 min。对PCR产物进行琼脂糖凝胶电泳,并利用DNA纯化回收试剂盒(TaKaRa)进行胶回收。用Zero Back Fast Ligation Kit(TIANGEN) pZeroBack/blunt载体快速连接胶回收产物,利用热激法将连接产物转入大肠杆菌DH5α中,然后进行菌液PCR阳性鉴定,对阳性菌液进行测序,将其中正确的保菌备用。
1.2.2 进化树和基因蛋白序列分析
根据小麦TaTCP22蛋白序列进行同源性搜索,下载与小麦TaTCP22蛋白序列相似度>50%的其他物种蛋白序列。使用MEGA5对TaTCP22蛋白序列进行多序列比对分析,将分析结果使用邻接法生成系统进化树,其中Bootstrap值设为1 000。endprint
1.2.3 基因结构和三级结构预测
根据GSDS(http://gsds.cbi.pku.edu.cn/)在线工具对基因的结构进行分析,制作小麦TaTCP22 基因外显子-内含子结构示意图。利用PHYRE2(http://www.sbg.bio.ic.ac.uk/phyre2/html/page. cgi?id=index)在线工具对基因的三级结构进行预测。
1.2.4 启动子顺式作用元件分析
从基因组数据库Phytozome(http://www.phytozome.net/search.php)中选取基因起始密码子上游2 000 bp序列作为启动子区,利用植物顺式作用元件数据库PLACE26.0(http://www.dna.affrc.go.jp/PLACE/)分析基因的顺式作用元件。
1.2.5 亚细胞定位
利用In-Fusion技术构建TaTCP22 -16318GFP载体,利用聚乙二醇(PEG)诱导转化法将外源基因转到小麦原生质体中,25 ℃培养18 h,在激光共聚焦显微镜下观察其定位情况。
1.2.6 组织特异性及表达模式分析
分别取小麦品种轮选987的根、茎、叶、雌蕊、雄蕊、颖壳、胚性愈伤组织为试验材料,液氮速冻保存。对生长2周的小麦幼苗分别进行脱落酸 (ABA,200 μmol/L)和水杨酸(SA,1 mmol/L)、干旱(6% PEG)、低温(4 ℃)、NaCl(200 mmol/L)处理,并分别于处理后0、1、2、4、 8、12、24、48 h取样,液氮速冻后保存于-80 ℃冰箱备用。
用TRIzol试剂盒(北京康为世纪生物科技有限公司)提取总RNA,分别利用小麦不同组织和5种胁迫下的总RNA为模板,以SYBR Green染料法进行实时荧光定量PCR。用实时荧光定量PCR仪(Bio-Rad CFX96)进行PCR扩增,反应体系如下:2×Taq PCR Master Mix(含荧光染料)12.5 μL、10 μmol/L 引物各 1 μL、ddH2O 7.5 μL、cDNA模板3 μL。反应条件为95 ℃ 3 min;95 ℃ 10 s,58 ℃ 20 s,72 ℃ 30 s,40个 循环。PCR引物序列为F:5′-AGCCTGACCGCATCCTATTA- 3′,R:5′-AGCGACTTTGGCCTGAACT-3′。以小麦β-actin基因为内标,其引物序列为β-actin-F:5′-CTCCCTCACAA CAACCGC-3′和β-actin-R:5′-TACCAGGAACTTCCATA CCAAC-3′。采用2-ΔΔCT法计算基因表达量。
2 结果与分析
2.1 TaTCP22 的特性分析
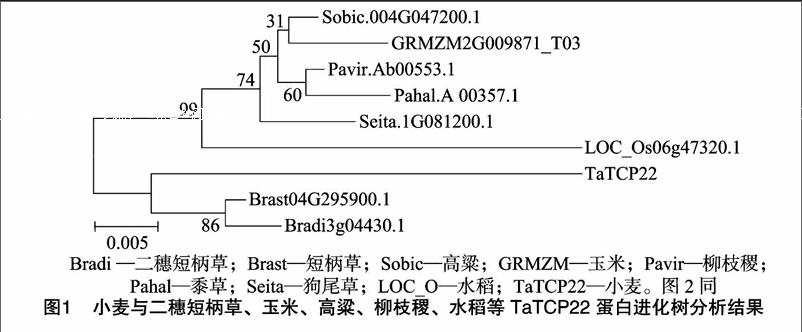
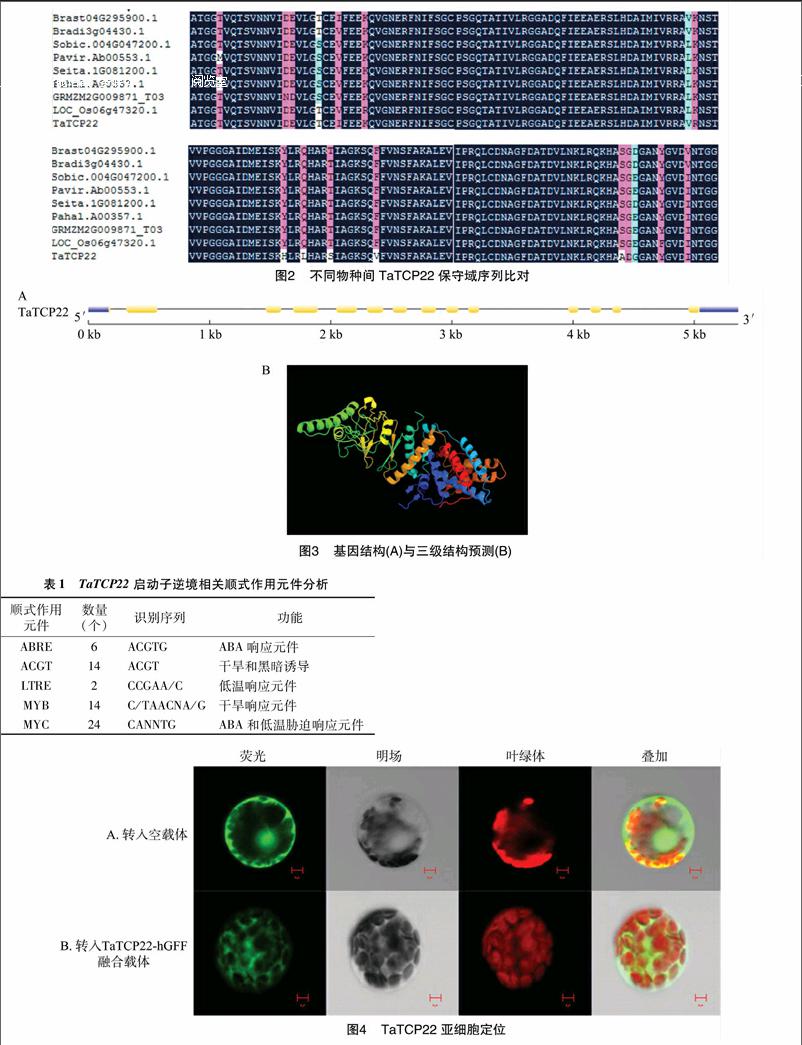
小麦TaTCP22 全长1 674 bp,编码557个氨基酸,其对应蛋白的分子量为60.0 ku,等电点为9.13。氨基酸序列分析发现,小麦TaTCP22蛋白包含1个Porin3保守域,属于Porin3转录因子家族第一大类。运用MEGA5软件对TaTCP22蛋白及其他物种中的同源蛋白做系统进化树分析(图1)。用DNAMAN分析二穗短柄草、玉米、高粱、柳枝稷、水稻等作物的蛋白保守域,图2结果显示,小麦TaTCP22与短柄草亲缘关系最近,亲缘关系越近,蛋白结构越相似。
从Phytozome基因组数据库中获得基因组序列和编码序列(coding sequence,简称CDS),对小麦TaTCP22外显子-内含子结构进行分析。图3结果表明,该基因编码区包含非编码区(untranslated region,简称UTR)和13个内含子以及13个外显子;对该蛋白的三级结构进行分析发现,小麦TaTCP22 三级结构预测的可信度为100%,包含18个α螺旋结构和19个β折叠结构。
2.2 启动子顺式作用元件分析
用PLACE在线工具分析小麦TaTCP22 启动子顺式作用元件,结果(表1)发现,该启动子区域中包含ABRE、ACGT、LTRE、MYB、MYC等逆境相关的顺式作用元件[9],其中MYC元件数量最多,为24个,其次为ACGT。据报道,这些元件在植物处于ABA、低温、干旱等胁迫响应中发挥作用[10-11]。
2.3 亚细胞定位
将TaTCP22与GFP蛋白融合的TaTCP22-hGFP融合表达载体和GFP空载体分别转入小麦原生质体中,在激光共聚焦显微镜下进行观察,结果显示,在转入空载体的小麦原生质体整个细胞中可见明亮的绿色荧光(图4-A),转入 TaTCP22-hGFP融合表达载体的小麦原生质体主要在细胞膜、细胞质和细胞核中可见绿色荧光(图4-B)。结果说明小麦TaTCP22主要分布在细胞膜、细胞质和细胞核中。
2.4 表达模式分析
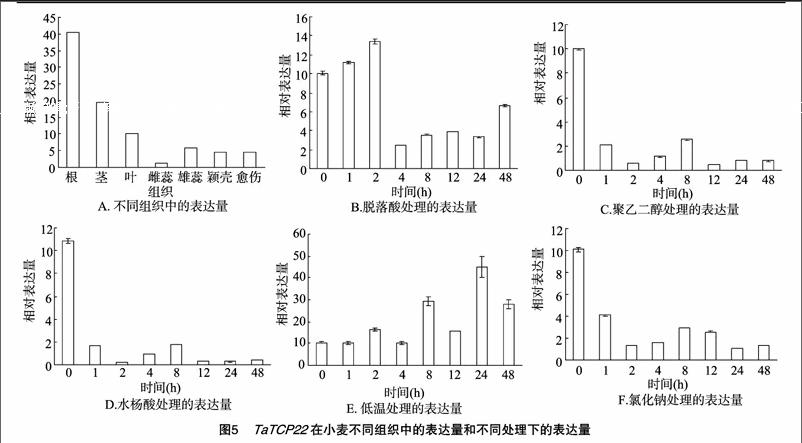
TaTCP22 在小麦组织中的特异性表达分析结果(图5-A)显示,TaTCP22 基因在根、茎、叶、雌蕊、雄蕊、颖壳、愈伤中都有表达,根中表达量最高,说明TaTCP22 主要在根中发挥作用。茎、叶中的表达量次之,雄蕊、愈伤和颖壳的表达量相似,雌蕊中表达量最少。
迄今为止,不同物种中鉴定出的大部分TaTCP22 基因参与[CM(25]了对生物和非生物逆境的响应。通过荧光定量PCR检测
ABA(200 μmol/L)和SA(1 mmol/L)、干旱(6% PEG)、低温(4 ℃)、NaCl(200 mmol/L)等不同胁迫处理下TaTCP22 基因的表达量,图5结果表明,PEG、SA、NaCl处理下TaTCP22 基因的表达量下调;4 ℃低温处理下,TaTCP22 在处理2 h后被诱导表达,2 h后表达量波动变化,24 h时表达量达到最大值。ABA处理下,TaTCP22 表达量在处理2 h达到最大值,之后都低于正常水平。上述結果表明,TaTCP22 基因的表达,受ABA、SA、干旱、低温和NaCl的诱导,在ABA、干旱、NaCl处理下的表达模式有些相似。endprint
3 討论
TCP-1广泛存在于真核及原核生物中,是一个典型的分子伴侣,受多种生物逆境和非生物逆境的诱导[12]。真核细胞中双环背对背堆叠的多聚体分子伴侣素(chaperonin)TRiC/CCT是最为复杂的分子伴侣,可以帮助5%~10%的胞质蛋白进行折叠[13-15],包括许多重要的结构和调节蛋白,如细胞骨架组成的微管蛋白和肌动蛋白、细胞周期调控蛋白CDC20和CDH1[16-17]。
TRiC/CCT蛋白质的折叠是依赖ATP[18-19]进行的。本研究中的TaTCP22 编码557个氨基酸,其保守域C端和N端包含β折叠结构,其顶端结构域包含1个螺旋突出结构域;赤道结构域形成1个环形接口,包含参与核苷酸表达的大部分残基,可与ATP结合并有微弱的ATP酶活性;中间区域形成的顶端表面口袋与核苷酸结合。CCT底物蛋白别构后形成单链,进入CCT中间内腔,与顶端结构域结合,形成复合物,该复合物与ATP结合后,可依赖ATP水解释放的能量改变CCT顶端结构螺旋突出结构域的构象,并带动环内构象的改变,完成蛋白质的折叠与组装[7,20]。
目前关于植物分子伴侣功能特性的研究是有限的,当植物遭受胁迫时,植物体内的酶和结构蛋白发生结构和功能的改变,因此细胞可在应激条件下维持蛋白质功能结构的构象,防止非天然蛋白质的聚集使得细胞在应激条件下的存活显得尤为重要[21]。为维持细胞间的稳态,sHsp、Hsp70可维持蛋白质的功能构象,阻止在胁迫下对细胞存活非常重要的蛋白质的聚合,Hsp60、Hsp70和Hsp90可维持非天然蛋白的复性。当聚合形成一些变性蛋白和错误折叠蛋白时,Hsp100/Clp蛋白可溶解错误蛋白,重新折叠形成有功能的蛋白,或通过蛋白酶降解这些蛋白[22]。本研究中,TaTCP22 基因在ABA和 4 ℃ 低温处理下被诱导表达,可能参与了维持一些非天然蛋白质复性的过程,推测其参与了胁迫应答。在啤酒酵母属中,CCTα在低温条件下,mRNA和蛋白的表达水平都提高了[23],这与本试验研究结果一致;将4 ℃条件下的酵母细胞转移至10 ℃条件下,其蛋白表达水平也明显提高,表明CCTα蛋白对于初期从低温恢复转至高温生长条件非常重要,与其他热激蛋白从高温恢复一致,猜测本试验中的TaTCP22 基因也有相似的功能。植物对干旱的胁迫响应分为ABA依赖和ABA不依赖2种途径,TaTCP22 基因对干旱表现为负调控,对ABA表现为正调控,说明该基因在干旱胁迫下不依赖ABA的信号途径。因此推测该基因可能参与了低温调控和非依赖ABA的干旱调控,在小麦适应非生物胁迫中起作用,为研究小麦的抗逆机制提供了帮助。
[HS2][HT8.5H]参考文献:
[1] Suarez C,Cardinale M,Ratering S,et al. Plant growth-promoting effects of Hartmannibacter diazotrophicus on summer barley (Hordeum vulgare L.) under salt stress[J]. Applied Soil Ecology,2015,95:23-30.
[2]Boston R S,Viitanen P V,Vierling E. Molecular chaperones and protein folding in plants[J]. Plant Molecular Biology,1996,32(1/2):191-222.
[3]Wang J,Martin E,Gonzales V,et al. Differential regulation of small heat shock proteins in transgenic mouse models of neurodegenerative diseases[J]. Neurobiol Aqing,2008,29:586-597.
[4]Kubota H,Hynes G,Willison K. The Chaperonin containing t-complex polypeptide-1(TCP-1)[J]. The FEBS Journal,1995,230(1):3-16.
[5]Ranson N A,White H E,Saibil H R. Chaperonins[J]. Biochemical Journal,1998,333:233-242.
[6]Ursic D,Sedbrook J C,Himmel K L,et al. The essential yeast TCP1 protein affects actin and microtubules[J]. Molecular Biology of the Cell,1994,5(10):1065-1080.
[7]Valpuesta J M,Martin-Benito J,Gomez-Puertas P,et al. Structure and function of a protein folding machine:the eukaryotic cytosolic chaperonin CCT[J]. Febs Letters,2002,529(1):11-16.
[8]Yamada A,Sekiguchi M,Mimura T,et al. The role of plant CCT alpha in salt- and osmotic-stress tolerance[J]. Plant and Cell Physiology,2002,43(9):1043-1048.
[9]Baker S S,Wilhelm K S,Thomashow M F. The 5′-region of Arabidopsis-thaliana cor15a has cis-acting elements that confer cold-,drought- and ABA-regulated gene-expression[J]. Plant Molecular Biology,1994,24(5):701-713.endprint
[10] Urao T,Yamaguchishinozaki K,Urao S,et al. An Arabidopsis myb homolog is induced by dehydration stress and its gene-product binds to the conserved MYB recognition sequence[J]. Plant Cell,1993,5(11):1529-1539.
[11]Abe H,Urao T,Ito T,Seki M,et al. Arabidopsis AtMYC2 (bHLH) and AtMYB2 (MYB) function as transcriptional activators in abscisic acid signaling[J]. Plant Cell,2003,15(1):63-78.
[12]Lopez T,Dalton K,Frydman J. The mechanism and function of group Ⅱ chaperonins[J]. Journal of Molecular Biology,2015,427(18):2919-2930.
[13]Yam A Y,Xia Y,Lin H T J,et al. Defining the TRiC/CCT interactome links chaperonin function to stabilization of newly made proteins with complex topologies[J]. Nature Structural and Molecular Biology,2008(15):1255-1262.
[14]Liang X H,Shen W,Sun H,et al. TCP1 complex proteins interact with phosphorothioate oligonucleotides and can co-localize in oligonucleotide-induced nuclear bodies in mammalian cells[J]. Nucleic Acids Res,2014,42(12):7819-7832.[HJ1.7mm]
[15]Wang S Q,Zhang W J,Yang K L,et al. Isolation and characterization of a novel Dehalobacter species strain TCP1 that reductively dechlorinates 2,4,6-trichlorophenol[J]. Biodegradation,2014,25(2):313-323.
[16]Yaffe M B,Farr G W,Miklos D,et al. TCP1 complex is a molecular chaperone in tubulin biogenesis[J]. Nature,1992,358:245-248.
[17]Vinh D B,Drubin D G. A yeast TCP-1-like protein is required for actin function in vivo[J]. Proc Natl Acad Sci U S A,1994,91(19):9116-9120.[HJ1.75mm]
[18]Frydman J,Nimmesgern E,Erdjument-Bromage H,et al. Function in protein folding of TRiC,a cytosolic ring complex containing TCP-1 and structurally related subunits[J]. EMBO J,1992,11(13):4767-4778.
[19]Spiess C,Meyer A S,Reissmann S,et al. Mechanism of the eukaryotic chaperonin:protein folding in the chamber of secrets[J]. Trends in Cell Biology,2004,14(11):598-604.
[20]Llorca O,Martin-Benito J,Grantham J,et al. The ‘sequential allosteric ring mechanism in the eukaryotic chaperonin-assisted folding of actin and tubulin[J]. EMBO Journal,2001,20(15):3893-4323.
[21]Wang W X,Vinocur B,Shoseyov O,et al. Role of plant heat-shock proteins and molecular chaperones in the abiotic stress response[J]. Trends in Plant Science,2004,9(5):244-252.
[22]Ben-Zvi A P,Goloubinoff P. Review:Mechanisms of disaggregation and refolding of stable protein aggregates by molecular chaperones[J]. Journal of Structural Biology,2001,135(2):84-93.
[23]Somer L,Shmulman O,Dror T,et al. The eukaryote chaperonin CCT is a cold shock protein in Saccharomyces cerevisiae[J]. Cell Stress & Chaperones,2002,7(1):47-54.endprint

