PVP联合RFA对骨质疏松性椎体压缩性骨折患者术后疼痛及生活质量的影响
李坤,梅继文,胡守力,孙海光
(吉林医药学院附属医院,吉林吉林132013)
PVP联合RFA对骨质疏松性椎体压缩性骨折患者术后疼痛及生活质量的影响
李坤,梅继文,胡守力,孙海光
(吉林医药学院附属医院,吉林吉林132013)
目的探讨经皮椎体成形术(PVP)联合射频消融术(RFA)对骨质疏松性压缩性脊柱骨折患者术后疼痛及生活质量的影响。方法选取骨质疏松性脊柱压缩性骨折患者77例,按治疗方法分为对照组35例、观察组42例。对照组单纯采用PVP,观察组在PVP基础上联合RFA。记录术中肺栓塞、骨水泥渗漏等并发症情况。术后1个月评价临床疗效。术前、术后l周、3个月、6个月及12个月时采用目测类比(VAS)评分及Barthel指数进行疼痛及生活质量评分。结果对照组、观察组有效率分别为91.43%、92.86%,两组有效率差异无统计学意义(P>0.05)。与治疗前比较,两组治疗后VAS评分均下降、Barthel指数均升高(P均<0.05)。观察组术后3个月、术后6个月及术后12个月时VAS评分均低于对照组,Barthel指数均高于对照组(P均<0.05)。两组术中均无肺栓塞等严重并发症发生。结论PVP联合RFA治疗骨质疏松性脊柱压缩性骨折可明显缓解患者术后疼痛,提高生活质量。
经皮椎体成形术;射频消融术;脊柱骨折;骨质疏松;压缩性骨折;疼痛;生活质量
随着人口老年化社会的到来,骨质疏松性脊柱压缩性骨折患者已呈高发态势[1]。随着经皮椎体成形术(PVP)治疗方法的出现,PVP治疗老年骨质疏松性椎体非压缩性骨折能迅速缓解疼痛,提高患者生活质量[2]。然而,单纯的PVP仍存在较多不足,如不能有效解决骨质疏松性骨骼疼痛以及手术后再次骨折等问题[3]。随着射频技术的发展,射频消融术(RFA)治疗脊柱压缩性骨折可以帮助减少难治性疼痛的发生率,从而提高远期疗效。本研究探讨PVP联合RFA治疗脊柱骨质疏松性压缩性骨折的安全性与临床疗效。现报告如下。
1 资料与方法
1.1 临床资料 选取2014年3月~2015年5月在我院治疗的骨质疏松性脊柱压缩性骨折患者77例,男37例、女40例,年龄(49.12±7.21)岁。椎体压缩程度25%~50%39例、>50%~75%38例。病变椎体单椎体41例、双椎体36例。病变部位T1118例、T1220例、L119例、L220例。均经X线、MRI检查证实。按治疗方法分为对照组35例、观察组42例。排除标准:肿瘤;存在PVP手术禁忌证;精神障碍或不能言语交流配合;因其他疾病长期口服止痛药以及激素类药物。两组性别、年龄、病情程度等差异无统计学意义。本研究取得患者及其家属知情同意。
1.2 治疗方法 ①对照组采用单纯PVP。患者俯卧在操作床上,皮肤消毒,铺无菌手巾,C型臂透视下确定病变椎体位置。以椎体椎弓根体表投影作进针点,采用1%利多卡因5 mL做全层浸润麻醉,经皮用3 mm钻头作椎弓根钻孔,自椎弓根影外上缘开始,直至椎体前中1/3交界处,取出钻头后穿入15G穿刺活检针。置入工作套管,调制好骨水泥至牙膏状,透视下通过注射器缓慢注射骨水泥,一般一个椎体4~6 mL,C臂下动态观察骨水泥的弥散情况,当骨水泥至椎体边缘时,立即停止注入。②观察组在PVP基础上联合RFA。手术在DSA引导下进行,患者俯卧于DSA操作床上,透视下定位并标记病变椎体,将电极片放置在双侧大腿或小腿内侧,使用绝缘垫来防止皮肤灼伤。DSA下将骨穿针按穿刺路径穿入椎体病变处,拔出穿刺针芯,透视下穿入射频电极针,根据椎体骨皮质后缘破坏程度和患者反应确定好温度和维持时间。椎体后缘骨皮质有破坏的温度设置在75 ℃,连接到射频发生器进行消融,若患者诉剧烈疼痛或有明显不适,应立即停止加热,以免损伤脊髓和周围神经。完成RFA后停止加热,射频发生器监视器显示温度降低后,拔出射频电极针,然后将骨穿刺针芯置入穿刺针套管内。透视下将骨穿针穿至直至椎体前中1/3交界处,拔出针芯,注射器缓慢注射骨水泥。术后CT复查检测骨水泥分布状况。
1.3 临床疗效评价 术后1个月时参照疼痛缓解分级评价疗效,完全缓解(CR)为疼痛症状完全消失,术后完全自理;部分缓解(PR)为疼痛缓解明显,偶有症状,无须使用口服止痛剂,生活大部分能自理;轻微缓解(MP)为时有疼痛症状,使用口服止痛剂能止痛,生活部分能自理;无效(NR)为疼痛无缓解,口服止痛剂不能完全止痛,须较强止痛。以CR+PR计有效率。
1.4 疼痛及生活质量评分 分别于术前、术后l周、3个月、6个月及12个月时,分别采用视觉模拟评分(VAS)及Barthel指数进行疼痛及生活质量评分。VAS由患者根据疼痛程度进行评分,分为0~10分,0分代表无疼痛,10分代表感觉最严重疼痛。Barthel指数总分100分,分数越低,生存质量越低。
1.5 术中并发症发生情况 记录术中肺栓塞、骨水泥渗漏等并发症情况。
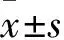
2 结果
2.1 两组临床疗效比较 对照组CR 24例、PR 8例、MP 2例、NR 1例,有效率为91.43%(32/35),观察组分别为33、6、2、1例及92.86%(39/42),两组有效率差异无统计学意义(P>0.05)。
2.2 两组不同时间点VAS比较 与治疗前比较,两组治疗后VAS均下降,观察组术后3个月、术后6个月及术后12个月时VAS均低于对照组(P均<0.05)。见表1。
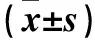
表1 两组不同时间点VAS比较
2.3 两组不同时间点Barthel指数比较 与治疗前比较,两组治疗后Barthel指数均升高,观察组术后3个月、术后6个月及术后12个月时Barthel指数均高于对照组(P均<0.05)。见表2。
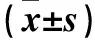
表2 两组不同时间点Barthel指数比较
2.4 并发症情况 两组术中均无肺栓塞等严重并发症发生。对照组术中1例椎体发生椎间盘渗漏,3例椎体发生椎旁渗漏,2例发生椎管内渗漏,其中l例患者有神经脊髓受压症状,应用激素、脱水对症治疗7 d后好转。观察组发生椎间盘渗漏3例,出现神经根压迫症状2例,神经根压迫症状2例。
3 讨论
随着国内人口老龄化进程的加快,骨质疏松性脊柱压缩性骨折的患者越来越多[4],成为导致老年性骨质疏松患者常见的骨折之一,表现为无明显外伤或由于轻微外伤作用下发生的胸腰部或者下腰部疼痛,活动时疼痛明显加重,如果引起神经症状可导致双下肢不全瘫、大小便失禁等,严重影响中老年人的生活质量[5]。目前传统保守治疗方法包括卧床、止痛、抗骨质疏松药物等治疗方法,传统的非手术治疗方法存在明显缺陷,无法早期解除疼痛[6]。而且老年人骨折后长期卧床易出现坠积性肺炎、下肢深静脉血栓、褥疮、泌尿系感染、畸形、骨质疏松加重等并发症[7],严重影响老年人的生活及治疗,甚至增加老年人口的病死率。手术是达到迅速缓解疼痛、增强椎体强度、恢复脊柱生理曲度和早期下床活动目的的有效方法[11]。目前PVP已经成为脊柱压缩性骨折的主要治疗方法之一。PVP通过直接往伤椎内注入骨水泥,具有微创、恢复伤椎强度、迅速缓解疼痛等诸多优点[8]。PVP能稳定骨折,防止病理性骨折和后突畸形,加固脊柱稳定性。然而其远期效果并不显著,可能与神经根出口处组织炎性渗出、粘连、反复刺激有关。目前对PVP治疗骨质疏松性脊柱压缩性骨折后,远期出现原骨折节段引起的难治性疼痛没有统一的认识和治疗方案。
近几年射频消融技术发展迅速[9]。研究发现,DSA引导下的RFA已经广泛应用于淋巴瘤、脊柱椎体转移瘤、骨质疏松及血管瘤等所致的椎体压缩性骨折的治疗[10]。目前RFA在骨质疏松性椎体压缩性骨折中减轻疼痛的机制尚不明确,可能原因有温热式射频通过微小震动使痛觉传导受抑制或中断,从而起到止痛的作用;另外可通过促进炎症水肿的吸收,缓解痉挛,达到止痛的目的。配合射频电流具有消融松解神经根周围组织粘连,解除神经根水肿,从而缓解疼痛的作用。两者联合治疗骨质疏松性椎体压缩性骨折的同时能够有效地加强脊柱的强度和硬度。本研究发现,两组有效率差异无统计学意义,观察组术后3个月、术后6个月及术后12个月时VAS评分均低于对照组,Barthel指数均高于对照组,提示PVP联合RFA在疼痛缓解及生活质量上均优于单纯采用PVP,表明PVP联合RFA治疗脊柱压缩性骨折提高了骨质疏松性脊柱压缩性骨折患者的生活质量,减轻了疼痛。
PVP目前仍存在一些并发症如复发等,特别是骨水泥渗漏可导致神经根疼痛、椎管受压以及肺梗死等严重并发症[12]。若RFA操作不当很容易导致术后感染、损伤血管等,温度过高可灼伤皮肤,严重时可引起肠麻痹、尿失禁或潴留等严重并发症。因此,选择射频针位置、有效射频温度和射频时间是积极预防射频并发症发生的重要措施。射频针的位置应位于椎体的中央,当椎体后缘骨皮质有灼伤或破坏时,将温度适当降低,调整穿刺针的位置,一般理想位置为椎体前中l/3处。本研究在DSA引导下,在PVP之前先进行RFA术,通过射频消融毁损椎体内静脉,减少了骨水泥外渗等并发症,术后两组均无肺栓塞等严重并发症,仅存在少数灼伤或骨水泥渗漏现象,表明安全性较高。
综上所述,PVP联合RFA治疗骨质疏松性脊柱压缩性骨折疗效满意,可明显缓解疼痛、提高生活质量,并具有较好的远期效果。
[1] 丁小方, 王元利, 王书堂,等. 阿仑膦酸钠治疗骨质疏松性脊柱压缩性骨折椎体成形术后残余疼痛的早期疗效观察[J]. 中华老年医学杂志, 2013,32(3):260-262.
[2] 朱新炜, 高浩源, 邱思强,等. PVP治疗老年骨质疏松性椎体非压缩性骨折的疗效观察[J]. 中国矫形外科杂志, 2013, 21(4):342-345.
[3] 刘冬斌,李辉,程志安,等. 经皮椎体成形术联合鲑鱼降钙素治疗骨质疏松椎体压缩性骨折的临床观察[J].亚太传统医药,2012,8(3):118-120.
[4] 张相伟, 孙建民, 崔新刚,等. 骨质疏松椎体压缩性骨折患者脊柱矢状面的失平衡[J]. 中国组织工程研究, 2014,18(26):4224-4228.
[5] 邹戟, 赵红卫, 陈卫东,等. 经皮椎体成形术与经皮椎体后凸成形术治疗骨质疏松脊柱压缩性骨折的临床对比分析[J]. 中国老年学杂志, 2012, 32(24):5581-5582.
[6] 张洋, 肖杰, 龙浩,等. 经皮椎体成形术治疗骨质疏松性胸腰椎压缩性骨折的疗效[J]. 贵阳医学院学报, 2014, 39(2):250-251.
[7] 郭永昌.PFNA治疗股骨转子间骨折的临床体会[J]. 中国保健营养月刊,2013,23(1):121-122.
[8] 肖海祥.经皮椎体成形术和后凸成形术治疗骨质疏松性椎体压缩性骨折的研究进展[J].中国矫形外科杂志,2013, 21(24):2490-2494.
[9] 王冠羽.腰椎间盘突出症低温双极射频消融术微创治疗的新进展[J].医学综述,2013,19(5):892-895.
[10] 张亚辉,刘鸣.经皮椎体成形术联合射频消融术治疗脊柱转移瘤[J].肿瘤基础与临床,2015,28(3):218-220.
[11] 胥琼华.骨质疏松性脊柱压缩骨折经皮椎体成形术护理探讨[J].按摩与康复医学,2012,3(1):169.
[12] 胡继红,王会,赵卫,等.射频消融联合椎体成形术治疗脊柱转移性肿瘤12例[J].介入放射学杂志, 2013, 22(7):563-566.
10.3969/j.issn.1002-266X.2017.46.026
R683.2
B
1002-266X(2017)46-0083-03
2017-05-20)

