一步法人类CYP2C19基因分型检测在临床中的应用及其意义
, ,, , , , ,*
(1.卡尤迪生物科技有限公司,北京,100081;2.中南大学湘雅医学检验所;3.中南大学湘雅医院临床药理研究所)
·技术与方法·
一步法人类CYP2C19基因分型检测在临床中的应用及其意义
李响1,刘宁1,肖乐东2,张伟3,李清3,李智3,杨坤1,谭志荣3*
(1.卡尤迪生物科技有限公司,北京,100081;2.中南大学湘雅医学检验所;3.中南大学湘雅医院临床药理研究所)
目的探索一步实时荧光PCR检测CYP2C19基因分型的方法。方法采用人类CYP2C19基因分型检测试剂盒(PCR-荧光探针法)对全血或人基因组进行一步法实时荧光PCR检测,同时采用焦磷酸测序和试剂盒进行对比。结果一步法检测结果准确性为100%。重复性检测显示,该法对各个基因型Ct值进行变异系数(CV值)的统计学分析,CV值均小于5%,对已知基因型的浓度的检测范围为0.2~125 ng,对杂合突变型基因组DNA(1 ng)和血液样本(十倍稀释)进行7次检测,变异系数(CV值)均小于5%,对特异性样品、EDTA抗凝样本、枸橼酸钠抗凝样本、乳糜血样本、血红素污染样本的基因型都有较好的检测效果。结论一步法检测方法准确性高,检测范围宽,重复性、特异性和灵敏度均能达到人基因组DNA样本的检测的水平,满足临床对人CYP2C19基因分型检测的目的。
CYP2C19基因分型; 氯吡格雷; 一步法实时荧光PCR; 个体化用药
近年来随着人类基因组学(genomics)的发展,药物基因组学(pharmacogenomics)领域得到了迅猛发展,越来越多的药物基因组生物标记物及其检测方法相继涌现。药物基因组学已成为指导临床个体化用药、评估严重药物不良反应发生风险、指导新药研发和评价新药的重要工具,药物反应相关基因及其表达产物的分子检测是实施个体化药物治疗(individualized treatment)的前提。目前美国食品药品监督管理局(FDA)和我国食品药品监督管理局(CFDA)都已批准了一系列的个体化用药基因诊断试剂盒。
氯吡格雷是一种抗血小板药物,广泛用于急性冠脉综合征(acute coronary syndrome,ACS)、缺血性脑血栓(acute ischemic stroke,AIS)、闭塞性脉管炎(thromboangitisobliterans,TAO)和动脉硬化及血栓栓塞引起的并发症。心脏支架手术后的患者需长期服用氯吡格雷以防止支架内再梗[1-2]。氯吡格雷主要经CYP2C19代谢活化后发挥抗血小板效应[3-4]。2010年3月,美国(FDA)宣布氯吡格雷抵抗的“黑框警告”,提醒应用氯吡格雷后出现心血管不良事件与CYP2C19功能缺失的等位基因有关。CYP2C19遗传变异可导致酶活性的个体差异,使人群出现超快代谢者(ultrarapid metabolizer,UM)、快代谢者(extensive metabolizer,EM)、中间代谢者(intermediate metabolizer,IM)和慢代谢者(poor metabolizer,PM)4种表型。CYP2C19*2(rs4 244_285,c.681G>A)和CYP2C19*3(rs4_986 893,c.636G>A)是中国人群中存在的2种导致CYP2C19酶缺陷的主要等位基因。美国FDA和美国心脏病学会建议,对于CYP2C19慢代谢基因型患者需考虑改变治疗方案[5]。
用于个体化用药基因检测的方法包括PCR-直接测序法、PCR-焦磷酸测序法、荧光定量PCR法、PCR-基因芯片法、PCR-电泳分析、PCR-高分辨率熔解曲线法、等位基因特异性PCR法、PCR-限制性片段长度多态性方法、原位杂交(ISH)等多种方法。其中,实时荧光PCR法灵敏度高,分型准确,操作简便快捷,所用仪器容易普及。目前CFDA已批准CYP2C9、VKORC1等多种基因多态性检测的PCR-荧光检测试剂盒。已获批的试剂盒大多采用全血基因组核酸提取,然后进行扩增检测的方法。本文采用一步法实时荧光PCR检测,对全血样本免核酸提取,直接进行CYP2C19基因分型检测,同时进行了同类试剂盒的对比验证以及分析性能的验证,为临床实现快速便捷的床边检测提供了新的思路和方法。
1 资料与方法
1.1检测对象61例未知基因型的临床全血样本(EDTA或枸橼酸钠抗凝),受试者选择标准:(1)年龄18~75岁;(2)男女不限;(3)心脑血管以及外周动脉疾病患者;(4)无研究者认为的不宜参加本试验的其他情况。
1.2方法
1.2.1 检测方法 采用人类CYP2C19基因分型检测试剂盒(PCR-荧光探针法)[卡尤迪生物科技(北京)有限公司],取49.8 μL PCR反应液分装到0.2 μL PCR管,然后加入0.2 μL待测样本(全血或人基因组),放入实时荧光定量PCR仪(Mini8 Plus)[卡尤迪生物科技(北京)有限公司]进行检测。
1.2.2 对照方法 焦磷酸法测序(中南大学湘雅医学检验所)及已获cFDA批准的人类CYP2C19基因多态性检测试剂盒(武汉友芝友医疗科技股份有限公司)。取临床全血样本(约200 μL)进行人基因组提取,然后进行浓度测定,调整核酸浓度至说明书要求的范围内,取20 ng基因组DNA进行焦磷酸测序及实时荧光定量PCR检测。全部检测时间约4~5 h。
1.3性能分析
1.3.1 准确性分析 对54例未知基因型的临床样品同时进行一步法检测,以及焦磷酸测序(中南大学湘雅医学检验所)和已获cFDA批准的人类CYP2C19基因多态性检测试剂盒(武汉友芝友医疗科技股份有限公司)的检测,对检测结果进行准确性分析。
1.3.2 重复性分析 对三个已知基因型(分别为野生型、杂合突变型及纯合突变型)的血液样本,一例杂合突变型的基因组DNA样本分别进行5次重复性检测,对各位点进行CV值的统计分析。
1.3.3 检测范围分析 对一个杂合突变型的基因组DNA进行梯度稀释,浓度分别为125、25、5、1、0.2 ng,分别进行检测分析。
1.3.4 灵敏度分析 对杂合突变型基因组DNA(1 ng)和血液样本(十倍稀释),对每个样本进行7次检测,然后进行统计学分析。
1.3.5 特异性分析 对三个已知基因型(分别为野生型、杂合突变型及纯合突变型)的基因组DNA样本进行检测分析。
1.3.6 抗干扰性分析 对4个未知基因型的血液样本,分别为EDTA抗凝样本,枸橼酸钠抗凝样本,乳糜血样本,血红素污染样本,进行一步法检测及对比方法的检测,对检测结果进行分析。
2 结 果
准确性分析结果显示,三种方法的检测结果完全符合,包含了CYP2C19*2/*3的三种基因型,一步法检测结果准确性为100%。重复性分析结果见表1,CV值均小于5%。对已知基因型的不同浓度的检测范围参考品(*2/*3均为GA基因型)进行检测后,从0.2~125 ng每个浓度的样品都能被正确的检测出来(表2)。杂合突变型基因组DNA检测其CYP2C19*2的G/A基因型的CV值分别为4.06%/4.04%,CYP2C19*3的G/A基因型的CV值分别为0.33%/0.33%。血液样本CYP2C19*2的G/A基因型的CV值分别为2.46%/2.48%,CYP2C19*3的G/A基因型的CV值分别为3.56%/3.51%。CV值均小于5%。对特异性样品进行检测后,每个样品的基因型都能被正确的检测出来。对EDTA抗凝样本,枸橼酸钠抗凝样本,乳糜血样本,血红素污染样本进行检测后,每个样品的基因型都能被正确的检测出来,且与对照试剂盒检测结果一致。但对于血红素污染参考品,其CT值超过43,视为检测失败。故初步认为本试剂盒不适用于发生严重溶血的血红素污染样本。由于样本量小,还需进一步增加血红素污染样本检测数量,来判断本方法是否适用于溶血样本。
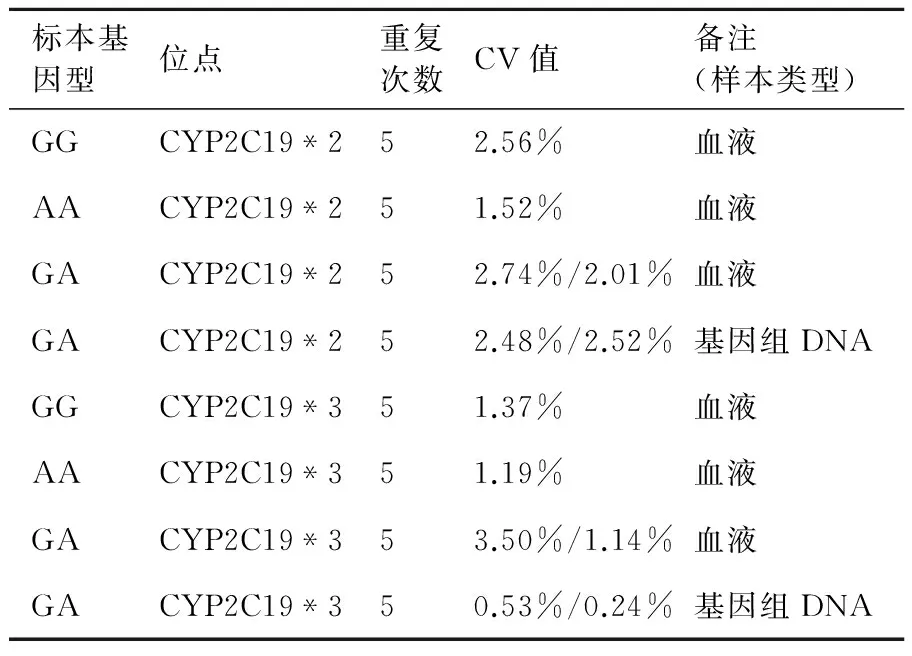
表1 一步法检测重复性分析

表2 不同浓度CYP2C19*2和CYP2C19*3检测的Ct值
3 讨 论
本文发现,采用实时荧光PCR方法,对临床全血样本直接进行人CYP2C19*2/*3基因分型一步法检测准确性高,检测范围宽,重复性、特异性和灵敏度均能达到人基因组DNA样本的检测的水平,满足临床对人CYP2C19基因分型检测的目的。与对比试剂盒相比,一步法检测免除了核酸提取,一方面缩短了临床样本的检测时间,减少检测成本,有利于检测报告的及时快速的发出,另一方面减少了临床检验人员的操作步骤,避免了操作误差和污染的引入,方便临床应用的推广,提高检测结果的可靠性和准确性。一步法检测所需样本量少(仅需0.2 μL血液),静脉血及指尖血均可以满足检测的需要,患者接受度高,临床检验人员操作方便。综上所述一步法个体化用药分子诊断因为耗时短,且操作简单,免去了对人员过高经验和专业的要求,因此可以应用于在医院科室的床旁检测(POCT)。该方案的可靠性和有效性已经经过实验验证。参照本文的操作和质控规范,即可较好地保证一步法检测在床旁检测方面的顺利开展。
Mega等[6]研究结果显示,至少携带1个CYP2C19功能缺失型等位基因的受试者(CYP2C19*2或*3携带者),导致氯吡格雷药物活性代谢物水平降低,容易出现氯吡格雷抵抗,PCI术后支架内血栓形成风险增高。对于PCI高危患者,CYP2C19基因检测是有必要的。对于“氯吡格雷抵抗”临床上可采用增加剂量或同类药物替代或联合用药的治疗策略[7-8]。因此,通过对CYP2C19基因检测基础上指导PCI术后氯吡格雷抗血小板治疗是减少血栓形成事件发生的有效途径之一,特别对冠心病高危人群具有特殊意义[9]。
[1] Desta Z,Zhao X,Shin JG,et al.Clinical significance of the cytochrome P450 2C19 genetic polymorphism [J].ClinPharmacokinet,2002,41(12):913-958.
[2] Paré G,Mehta SR,Yusuf S,et al.Effects of CYP2C19 genotype on outcomes of clopidogrel treatment[J].N Engl J Med,2010,363(18):1704-1714.
[3] Han Y,Lv HH,Liu X,et al.Influence of genetic polymorphisms on clopidogrel responseand clinical outcomes in patients with acute ischemic stroke CYP2C19 genotype on clopidogrel response [J].CNS Neurosci Ther,2015,21(9):692-697.
[4] Saab YB,Zeenny R,Ramadan WH.Optimizing clopidogrel dose response:a new clinical algorithm comprising CYP2C19 pharmacogenetics and drug interactions [J].Ther Clin Risk Manag,2015,11:1421-1427.
[5] Scott SA,Sangkuhl K,Stein CM,et al.Clinical pharmacogenetics implementation consortium guidelines for CYP2C19 genotype and clopidogrel therapy [J].ClinPharmacol Ther,2013,94(3):317-323.
[6] Mega JL,Close SL,Wiviott SD,et al.Cytochrome P-450 polymorphismsand response to clopidogrel [J].N Engl J Med,2009,360(4):354-362.
[7] Horenstein RB,Madabushi R,Zineh I,et al.Effectiveness of clopidogrel dose escalationto normalize active metabolite exposureand antiplatelet effects in CYP2C19 poor metabolizers [J].J Clin Pharmacol,2014,54(8):865-873.
[8] Lin R,Zhang L,Zhang P,et al.Influence of CYP2C19 loss-of-function variants on the metabolism of clopidogrelin patients from north-western China [J].J Clin Pharm Ther,2015,40(3):308-314.
[9] Zhang HZ,Kim MH,Guo LZ,et al.CYP2C19 but not CYP2B6,CYP3A4,CYP3A5,ABCB1,PON1 or P2Y12 genetic polymorphism impacts antiplatelet response after clopidogrel inKoreans [J].Blood Coagul Fibrinolysis,2017,28(1):56-61.
Clinicalapplicationandsignificanceofone-stephumanCYP2C19genotypedetection
LI Xiang,LIU Ning,XIAO Ledong,et al
(CoyoteBioscienceCo,Ltd,Peking,Beijing100081,China)
ObjectiveTo verify the analysis capabilities of one-step real-time PCR method in the directly detect CYP2C19 gene classification.MethodsUsing one-step real-time fluorescent PCR detection with human CYP2C19 genotyping kit (Coyotebio) to detect whole blood or genome,and compared with the pyrosequencing method and other qPCR kit.
ResultsAccuracy of one-step real-time PCR is 100%.The coefficient of variation (CV) of repeatability for all genotypesare was less than 5%.To detect known genes of different concentration,each sample can be detected correctly.Genomic DNA of hybrid mutation type (1 ng) and blood samples (10 times dilution),7 times repeating detection,the coefficient of variation (CV) of sensitivity are less than 5%.For EDTA anticoagulant samples,the samples of sodium citrate anticoagulation,chyle blood samples,heme pollution samples,each sample genotypes can be correctly detected.ConclusionOne-step detection method is of high accuracy and wide detection range,repeatability,sensitivity and specificity all can reach the level of genome DNA test samples.So one-step detection method could meet the clinical CYP2C19 gene classification testing purpose.
CYP2C19 genotyping; clopidogrel; One-step real-time fluorescent PCR; personalized medicine
10.15972/j.cnki.43-1509/r.2017.04.024
2016-11-05;
2017-05-01
长沙市科技局一般平台项目(K1403075-61);中南大学研究生创新课题(2016zzts522);湖南省科技厅省重点研发计划应用基础研究重点项目(2016JC2063).
*通讯作者,E-mail:tanzr@163.com.
R96
A
蒋湘莲)

