雾化吸入阿米卡星在气管支气管结核患者体内的药物分布特点
张亮 周秋云 陆磊 王洁 于俊 丁红梓
雾化吸入阿米卡星在气管支气管结核患者体内的药物分布特点
张亮1周秋云1陆磊1王洁1于俊2丁红梓1
目的 讨论气管支气管结核( EBTB) 患者接受雾化吸入或静滴阿米卡星治疗后,气道分泌物及血浆中阿米卡星的分布特点。方法 20例患者分为两组( 每组10例) ,分别接受雾化吸入阿米卡星200 mg和静滴阿米卡星200mg,1次/d;5天后,患者分别在治疗结束后0、2、6、8、12、24 h 检测气道分泌物和血浆中阿米卡星的浓度。结果 雾化吸入组气道分泌物中的药物浓度峰值中位数为0.3836μg·mL-1(0.1725-0.5269μg·mL-1) ,血浆中药物浓度峰值中位数为22.87μg·mL-1(15.53-30.12 μg·mL-1);静脉给药组气道分泌物药物浓度峰值中位数为0.3836μg·mg-1(0.1725-0.5269μg·mg-1),血浆中药物浓度峰值为22.87μg·mL-1(15.53-30.12 μg·mL-1)。结论 与静滴相比雾化吸入阿米卡星气道分泌物中的药物浓度远高于常见的MIC,而血浆中药物浓度却远低于其毒性浓度,雾化吸入阿米卡星治疗EBTB可能为一种安全有效的治疗方法。
气管支气管结核;雾化吸入;药物分布特点
气管支气管结核(end bronchi tuberculosis, EBTB)是支气管、支气管黏膜和黏膜下层受到结核分枝杆菌侵犯而发生的一致疾病。支气管内膜血液循环不充分,常规的全身给药方式不能达到治疗浓度,如增加给药剂量会增高不良反应发生率。所以,全身治疗的基础上结合雾化吸入是目前临床上较常用的疗法[1-2]。雾化吸入疗法是呼吸系统疾病常见的治疗手段。它通过雾化装置将药液转变为直径1- 5μm的雾粒, 能够到达肺泡[3]。目前普遍认为雾化吸入疗效好的原因为:①雾化吸入可能会提高局部的药物浓度; ②肺部病灶处通常存在黏膜的充血水肿、坏死等小血管被破坏的现象。这一现象造成局部的血液循环受限, 全身药物到达局部的量有限; 而雾化吸入理论上可以解决这一问题[4-6]。本研究观察雾化吸入阿米卡星治疗气管支气管结核后气道分泌物和血浆中药物分布的特点,从而阐明雾化吸入药物在肺部的药代动力学特点。
资料与方法
2015.1-2015.10入住我院结核科并诊断为气管支气管结核的20例患者,入选标准为:①无其他系统严重并发症、继发症;②初始治疗方案中包含阿米卡星的结核病住院患者;③男女不限,年龄介于20-70周岁;④评估患者气道分泌物量>2mL/4h。排除如下患者:妊娠、肝肾功能不全、白细胞缺乏。
仪器与试剂
一、仪器 LC-20AB 高效液相色谱系统( 检测器为SPD-M20A,日本岛津);WH-2 涡旋仪(上海沪西分析仪器厂有限公司);Bioprap-24低温组织匀浆机(杭州奥盛);FB224 电子分析天平(上海舜宇恒平科学仪器有限公司,精度:0.1 mg);TG1650-WS 高速离心机(上海卢湘仪);微量移液器 (Eppendorf,德国)。
二、试药 阿米卡星标准品(纯度为99.8%,Sigma Aldrich 公司,美国), 四氢呋喃(Merck,德国,色谱纯),庚烷磺酸钠、无水硫酸钠、磷酸二氢钠(国药集团,均为分析纯,中国)。水为自制双蒸水。
给药与样品采集
20例患者平均分为两组,1组给予阿米卡星(上海现代哈森药业有限公司)200mg加入250mL生理盐水中静脉滴注,1次/天,平均滴注时间为147.8±11.2min;另一组给予阿米卡星200mg加入5mL生理盐水中雾化吸入,1次/天,平均雾化时间为26.5±5.9min。两组患者在治疗前各项指标均无明显差异。第5天后在静脉滴注和雾化结束后 0、2、6、8、12和24 h 6个时间点经中心静脉留取血样2mL,3000r/min离心后取1mL血浆储存; 同时,先用漱口溶液漱口,以清除口腔内细菌后,深呼吸数次后用力咳出气管深处的痰液于无菌集痰器内,然后与血浆储存于-70℃低温下保存。
浓度检测
一、色谱条件 色谱柱:Waters Xselect-HSS T3 (250mm×4.6mm,5μm),流动相:取庚烷磺酸钠7.5mmol和无水硫酸钠20.0g,加pH=3.0的磷酸缓冲液250mL和四氢呋喃15mL,用水稀释至1000mL,柱温:40℃,流速:1mL/min,进样体积100μL,检测波长:220nm[7]。
二、血浆样品检测 取血浆样品300 μL 放入2 mL 离心管中,涡旋混匀2min,加乙腈700 μL,旋涡混合3 min,16 000 r·min-1离心5 min,取上清液经0.45 μm 滤膜过滤后转移至自动进样瓶,进样100μL检测。
三、 分泌物样品检测 称取分泌物样品200mg,置于2.5mL 离心管内,精密加入生理盐水2mL,进行匀浆,后吸取匀浆液1mL,旋涡混旋2min,12000r/min离心2min,取上清液500μL与等体积水混匀后放入自动进样瓶中,进样100μL检测。
结 果
一、气道分泌物中的药物分布
雾化吸入组浓度在雾化后即达到峰值,Cmax中位值为397.86μg·mg-1( 237.85-539.2μg·mg-1) ,以后随着时间延长,其浓度逐渐下降,24 h浓度达到最低,Cmin中位值为4.667μg·mg-1( 2.961-7.897μg·mg-1),阿米卡星AUC0-24h为989.2 μ·hr·mL-1( 526.8-1512.4) ; 静脉给药组药物浓度峰值出现在给药后2h,Cmax中位值为0.09457μg·mg-1( 0.07987-0.1498μg·mg-1),8h的浓度中位值0.07833μg·mg-1(0.06898-0.09858μg·mg-1)。8h后的浓度低于检测限无法测得.阿米卡星AUC0-24h为3.43 μ · hr ·mL-1( 2.18-4.21),(见图1A、1B)。
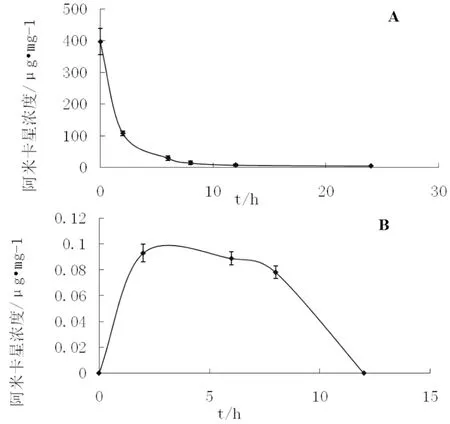
图1 气道分泌物中阿米卡星浓度
A:雾化吸入(nebulized);B:静脉给药(intravenous)
二、血浆中药物药物分布
雾化吸入组阿米卡星浓度峰值出现在雾化结束后,Cmax中位值为为0.3836μg·mL-1(0.1725-0.5269μg·mL-1),以后随着时间延长其浓度逐渐下降,24 h浓度达到最低,Cmin中位值为0.1565μg·mL-1(0.09459-0.2172μg·mL-1),阿米卡星AUC0-24h为3.97 μ · hr ·mL-1( 2.76-4.55) ; 静脉给药组药物浓度峰值亦出现在给药后,Cmax中位值为22.87μg·mL-1(15.53-30.12 μg·mL-1)。此后随着时间其浓度逐渐下降,24 h左右药物浓度达最低,Cmin中位值4.81μg·mL-1(1.36-8.53 μg·mL-1)。阿米卡星AUC0-24h为76.61μ·hr·mL-1( 47.72-97.87),(见图2A、2B)。
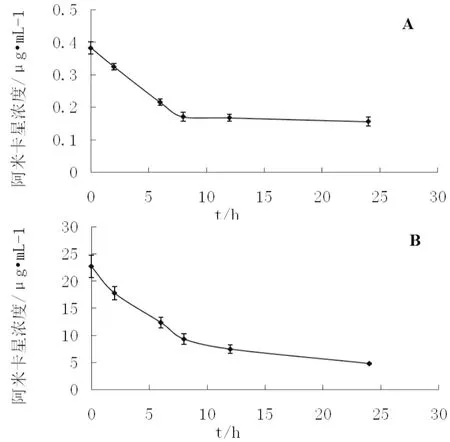
图2 血浆中阿米卡星浓度
A:雾化吸入(nebulized);B:静脉给药(intravenous)
讨 论
雾化吸入使药物可与局部组织直接接触, 希望在不显著改变全身血药浓度的情况下使局部药物浓度显著增高,直接增强杀菌效果, 从而增强疗效,降低全身不良反应。但迄今为止缺少雾化吸入药物在气道内分布和代谢的研究。无法得知通过局部药物浓度是否可以通过雾化吸入提高并维持较长时间。
WHO将阿米卡星归类为第二组抗结核药,其抗结核疗效肯定。但其缺点是组织穿透力弱。相关研宄表明静脉使用时上皮细胞衬液中的药物浓度仅为血清药物浓度的12%和32%,而这一浓度仅大约为抗结核杆菌MIC(最低有效抑菌浓度,4-8μg·mL-1)的10倍以下[8-9]。这样的浓度可能在病灶中难以发挥作用,从而增加治疗的困难。如果可以使气道中的药物浓度维持在MIC值的20-200倍,就可以极大提高有效率和治愈率[10]。
从本试验的结果来看,雾化吸入组中无论是血浆还是气道分泌物中药物都很快的达到峰浓度。由于雾化是局部给药,气道内的药物浓度在给药的同时就达到了峰值397.86μg·mg-1,远高于常见的MIC,推测这可能会取得较好的临床疗效。通过图1可以看出结束治疗后数小时下降的也较快,分析可能是因为随着时间的延长药物逐渐透过黏膜进入了血液;同时吸入了生理盐水后可促进排痰,使药物被排出体外。对于血浆中的药物分布来说,由于肺泡拥有极大的表面积,吸收和进行换气的效率很高。所以通过雾化吸入的途径几乎不需要吸收过程就可以达到峰值,但是峰浓度只有0.3897μg·mL-1,远低于静脉给药途径。虽然吸收的峰值较低,但由于长时间不断有药物透过黏膜进入血液,所以浓度下降的相对较慢。
静脉给药组中的气道分泌物药物峰浓度峰值0.09457μg·mg-1仅是雾化给药组的1/4000,且8h后就几乎没有分布了。说明通过静脉给药途径很难在支气管、支气管黏膜和黏膜下层达到理想的分布浓度。而在15.53-30.12 μg·mL-1之间的血浆浓度也属于正常范围[11]。
通过实验可以看出雾化吸入确是可以达到远高于全身药物浓度的局部治疗浓度。且雾化吸入抗生素也已经被允许用于治疗多重耐药菌所致的呼吸机相关性肺炎[12-13]。但需要强调的是目前临床使用的雾化吸入药物都是静脉用剂型,静脉剂型的pH值、渗透压、加入的药用辅料等可能未必适合雾化。不排除在雾化过程中产生一定的刺激性或出现相关副作用。因此,必须要严密关注雾化吸入过程,最好能够开发出可供雾化吸入的新剂型。
[1] 段明珉,王仁仪,陈国华.雾化吸入抗结核药物强化治疗气管支气管结核痰涂(+)患者23例临床观察[J].中国卫生产业, 2011,8(11):14,16.
[2] 梁改清.抗结核药物雾化吸入在支气管内膜结核患者中的应用及效果观察[J].齐鲁护理杂志,2012,18(19):117-118.
[3] 杨荣,蒋剑滔,李粼.雾化吸入抗结核药物治疗气管支气管结核患者的疗效分析[J].中国民族民间医药, 2013, 22(8): 94.
[4] Palmer LB,Smaldone GC,Chen JJ,et al.Aerosolized antibiotics and ventilator-associated tracheobronchitis in the intensive care unit[J].Crit Care Med,2008,36(7):2008-2013.
[5] Hallal A, Cohn SM, Namias N, et al.Aerosolized tobramycin in the treatment of ventilator-associated pneumonia: a pilot study [J].Surg Infect (Larchmt),2007,8(1):73-82.
[6] 郑丽华.雾化吸入疗法治疗肺结核病的临床疗效观察[J].中国医药科学,2015,5(20):167-169.
[7] 张亮,侯文洁,周秋云,等.HPLC-UV 法检测人血浆中阿米卡星的浓度[J].中南药学,2015,13(10):1048-1050.
[8] 朱海洋,高红伟.雾化吸入给药治疗气管支气管内膜结核的疗效分析[J].中国实用医药,2015,10(10):217-218.
[9] Boselli E,Breilh D,Djabarouti S,et al.Reliability of mini-bronchoalveolar lavage for the measurement of epithelial lining fluid concentrations of tobramycin in critically ill patients[J].Intensive Care Med,2007, 33(9):1519-1523.
[10] Luyt CE,Clavel M,Guntupalli K,et al.Pharmacokinetics and lung delivery of PDDS-aerosolized amikacin(NKTR-061) in intubated andmechanically ventilated patients with nosocomial pneumonia[J].Crit Care,2009,13(6):R200.
[11] 王传海,张业新,耿朝晖.阿米卡星血药浓度对呼吸道感染菌耐药性的影响[J].蚌埠医学院学报,2012,37(1):91-92.
[12] 牟照红,张家丽,许辉.雾化吸入阿米卡星治疗多重耐药铜绿假单胞菌呼吸机相关肺炎效果观[J].中国医药导报,2015,12(27):165-168.
[13] Peleg AY,Hooper DC.Hospital-acquired infections due to gram-negative bacteria[J].N Eng J Med,2010,362(19):1804-1813.
Characteristics of drug distribution of nebulized amikacin in patients with EBTB
ZHANGLiang,ZHOUQun-yun,LULei,WANGJie,YUJun,DINGHong-zi
DepartmentofPharmacy,NanjingChestHospital,Nanjing,Jiangsu210029,China
Objective To discuss the characteristics of drug distribution of amikacin in airway secretions and plasma, after receiving treatment of nebulized amikacin or intravenous amikacin in patients with EBTB. Methods 20 patients were randomly divided into two groups. The group A received nebulized amikacin 200mg, once a day, and the group B received intravenous amikacin 200mg, once a day. After 5 days, the concentration of amikacin in airway secretions and plasma was detected in 0, 2, 6, 8, 12, 24h when the treatment was finished. Results According to the nebuilized group, the median peak concentration of drug in air secretions was 0.3836μg·mg-1(0.1725-0.5269μg·mg-1), the median peak concentration of drug in plasma was 22.87μg·mL-1(15.53-30.12 μg·mL-1). According to the intravenous group, the median peak concentration of drug in air secretions was 0.3836μg·mg-1(0.1725-0.5269μg·mg-1). The median peak concentration of drug in plasma was 22.87μg·mL-1(15.53-30.12 μg·mL-1). Conclusion Compared with the intravenous group, the nebulized group has much higher concentration of amikacin in airway secretions than its usual MIC, meanwhile the concentration of plasma is far below its toxic concentration. Nebulized amikacin maybe is an effective treatment for EBTB.
EBTB; nebulized; characteristics of drug distribution
10.3969/j.issn.1009-6663.2017.01.013
常州四药医院药学研究基金(No 2014YX013)
210029 江苏 南京,南京市胸科医院1.药学部、2.结核科
丁红梓,E-mail:xkyydhz@163.com
2016-04-28]

