液化糖对林可霉素发酵大生产中成本的影响
李 强,秦宝福,马清进,王 莉,万 丹,翟 莉
(1.西北农林科技大学,陕西 西安 7121001;2.天方药业有限公司,河南 驻马店 463000)
液化糖对林可霉素发酵大生产中成本的影响
李 强1,2,秦宝福1,马清进2,王 莉2,万 丹1,2,翟 莉2
(1.西北农林科技大学,陕西 西安 7121001;2.天方药业有限公司,河南 驻马店 463000)
在林可霉素大生产中通过淀粉双酶法生产液化糖替代原材料及补料过程中使用的葡萄糖,目的是降低发酵生产中的成本。
液化糖;林可霉素;大生产;葡萄糖
1962年由Mason等首次从林可链霉菌(Streptomyces lincolnensis)培养液中获得林可霉素[1](1incomycin)。林可霉素具有较好的抗革兰阳性菌的能力,它与已知的抗生素间不存在交叉耐药性,并且毒性很低,主要用于由革兰阳性菌引起疾病的临床治疗,林可酰胺类抗生素已成为临床应用上主要的抗生素之一[2]。本文通过淀粉采用双酶法[3]生产液糖替代林可霉素原材料中的葡萄糖成为了研究的对象,淀粉转化为液化糖运用到发酵大生产中从而降低生产成本。
1 仪器与材料
1.1 仪器设备
赛多利斯pH计,180T发酵罐,150T转糖罐,滴定管,1200型高效液相色谱仪。
1.2 菌种
林肯链霉菌 由天方药业有限公司提供。
1.3 培养基
淀粉、葡萄糖、冷轧黄豆粉、硫酸铵、硝酸铵、氯化钠、磷酸二氢钾、玉米浆、碳酸钙、有机消泡剂。
以上原材料都有天方药业有限公司提供。
2 过程与方法
2.1 淀粉通过打料管道打入到转糖罐,调节pH值5.8~6.3,然后加入淀粉酶,运用蒸汽升温到60℃然后保温1h,然后升温到90℃保温10min保温,结束后,开盘管水降温至60±2℃,倒入糖化酶和泡敌,然后60℃保温。
2.2 转糖罐的液化糖测出其还原糖,然后加水使其达到补糖罐所需还原糖,然后升温至116~118℃保温保压15-20min,保压结束后降温至30℃,作为备用为发酵罐补糖。
2.3 检测方法:斐林试剂法测定总糖与还原糖[4]
2.3.1 还原糖测定
取一定量的发酵液过滤,取滤液1mL(含糖量较高时可适当稀释)于100mL的三角瓶中,加入10mL去离子水稀释,摇匀后准确加入20mL的斐林试剂,煮沸3min(需准确计时),冷却后加入3mol/L的盐酸溶液,立刻用0.1mol/L的硫代硫酸钠溶液滴定至淡黄色,加入1mL的淀粉指示剂,继续滴定到蓝色褪去为止,读数R1。用不加样品的一组作为对照,重复操作将其读数记为R0,将R0-R1的值查糖表即可得还原糖值。
2.3.2 pH值测定
接通电源将酸度计预热10分钟。酸度计预热时间到后,使用复合电极,将电极用纯化水冲洗干净,并用干净的滤纸将其擦干,先用pH值为4.01的标准溶液标定,冲净擦干电极后,再用pH值为6.86的标准溶液进行标定后将电极冲净擦干。开始测定培养液的pH值,将电极插入未知溶液内,稍稍摇动烧杯,置"范围"开关于被测溶液可能的pH值范围,此时仪器指示的pH值,即为未知溶液的pH值。测量完毕,清洗电极,应将电极浸泡于3mol/L KCl溶液中。
2.3.3 生物效价测定法
高效液相色谱法。林可霉素标准品购于中国药品生物制品鉴定所。
3 结果与讨论
碳源主要用于构成菌体细胞和作为菌体代谢产物的碳素来源,并为微生物的生长繁殖和代谢活动提供能源[5]。葡萄糖作为工业发酵中一种最易利用的碳源,在林可霉素的发酵中具有重要的作用。
3.1 在发酵培养基配方中都含有葡萄糖,因此可以用转化的液化糖替代原材料中的葡萄糖成分。通过连续三批发酵培养基加入中葡萄糖和连续三批发酵培养基中加入液化糖测得消后还原糖做对照。

表1 发酵培养基中葡萄糖及液化糖消后测得的还原糖的对照
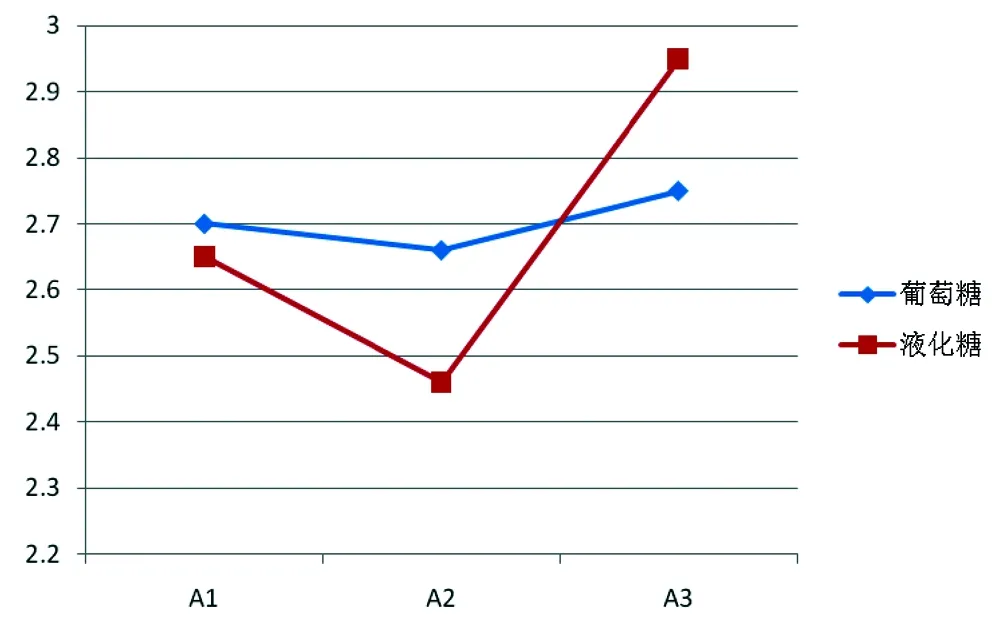
从图中来看培养基中葡萄糖换成液化糖后还原糖指标明显波动很大,这样会照成菌种生长不稳定,因此大生产中不建议用这种方法。
3.2 在林可霉素发酵过程中补糖是必不可少的,因此对于大生产来说控制住成本就等控制了价格,通过一批通过双酶法生产的液化糖所用的淀粉(在生产中一般还原糖转化率为95%以上)转化为糖的单价与葡萄糖的单价做对比,见表2,同时对发酵生产中三批用葡萄糖作为补糖原料和三批用液化糖作为补糖原料最终效价做对比,见表3。

表2 若一个转糖罐投入60t淀粉 t
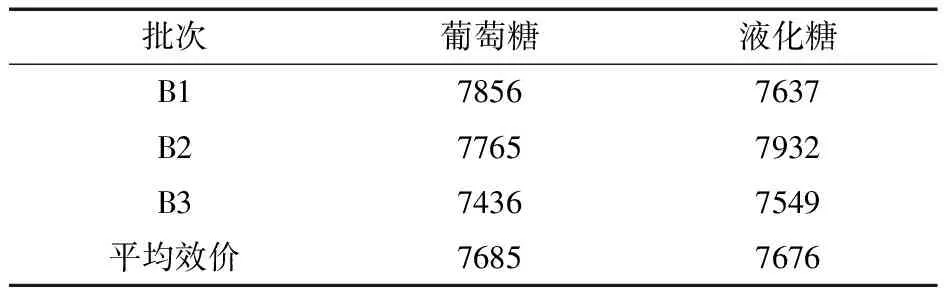
表3 补糖罐中加入葡萄糖与加入液化糖所用淀粉效价对比
从两表中可以看出在林可霉素发酵大生产中液化糖价格明显有优势,同时对发酵效价影响不是很大。
3.3 讨论
通过在基础培养基中及补糖中用液化糖代替葡萄糖进行林可霉素发酵的实验,发现在基础培养基中用液化糖代替葡糖糖进行发酵,还原糖指标明显波动很大,这样会照成菌种生长不稳定;在补糖罐中用液化糖代替葡萄糖糖进行发酵,最终放罐平均发酵效价影响不大,但是使用液化糖代替葡萄糖进行林可霉素的发酵,可降低生产林可霉素的成本,提高效率及产能,今后将在生产上对该工艺进行验证及完善。
[1] 周 徟, 亓平言.林可霉素提取过程生产现状和研究进展[J].国外医药抗生素分册,1992.20(2):61-63.
[2] Chang F N. Lincomycin[M]// Hahn F E .Mechanism of Action of Antibacterial Agents.New York: Springer,1979:127-134.
[3] 林亲录,周丽君,符 琼.淀粉转化生产葡萄糖工艺研究进展[J].食品工业科技, 2011 (4) :412-414 .
[4] 北京大学生物系生化教研室. 生物化学实验指导[M]. 北京: 高等教育出版社, 1986: 92-96.
[5] 何建勇.发酵工艺学[M].2版. 北京:中国医药科技出版社,2009:55.
2017-09-22
李 强(1982—),河南泌阳人,学士学位,助理工程师,主要从事微生物发酵工艺优化研究;通讯作者:秦宝福(1968—)),西北农林科技大学生命科学学院副教授,主要从事微生物资源、发酵工程等领域的研发工作。
TQ465
A
1008-021X(2017)22-0104-01
(本文文献格式:李强,秦宝福,马清进,等.液化糖对林可霉素发酵大生产中成本的影响[J].山东化工,2017,46(22):104,107.)

