雷帕霉素自乳化缓释微丸的研究
李红桥,卢振,杨林,王雨来*
(1. 鄂东医疗集团黄石市中心医院(湖北理工学院附属医院)药学部,湖北 黄石 43500;2. 肾脏疾病发生与干预湖北省重点实验室,湖北 黄石 43500)
雷帕霉素自乳化缓释微丸的研究
李红桥1,2,卢振1,2,杨林1,2,王雨来1,2*
(1. 鄂东医疗集团黄石市中心医院(湖北理工学院附属医院)药学部,湖北 黄石 43500;2. 肾脏疾病发生与干预湖北省重点实验室,湖北 黄石 43500)
以溶解度结合伪三元相图法,筛选与优化雷帕霉素液体自乳化处方。以羟丙甲基纤维素钠为主要骨架型缓释材料,采用挤出滚圆法制备一种新型的固体自乳化给药系统——雷帕霉素自乳化缓释微丸,并对其重分散性和体外释药进行了研究。结果表明:液体自乳化给药系统的处方是:Capmul MCM(油相)∶辛酸癸酸聚乙二醇甘油酯(表面活性剂)∶聚氧乙烯醚-35蓖麻油(表面活性剂)∶二乙醇单乙基醚(助表面活性剂)= 30∶28∶28∶14。制备成的缓释微丸的目标收率为(92.8±2.51)%,遇到重分散后的粒径是35.5±0.5 nm,在体外释药中表明微丸具有良好的缓释性能。以上表明:采用该方法为雷帕霉素的临床应用提供一种良好的应用方法。
雷帕霉素;自乳化给药系统;微丸;缓释;羟丙甲基纤维素钠
雷帕霉素是一种三烯大环内酯类的新型免疫抑制剂,由于具有强大的免疫抑制作用和较小的神经和肾毒性[1],因而在临床上广泛应用于器官移植和风湿性关节炎等自身免疫性疾病[2],但是雷帕霉素极微溶于水、口服生物利用度低、对胃酸敏感和治疗窗口窄导致不良反应较严重等原因[3],严重限制了该药在临床上的疗效发挥,因此改善雷帕霉素溶出度及提高生物利用度对临床的应用尤为重要。
自乳化缓释微丸是液体自乳化给药系统采用辅料固化成直径约为1 mm,一般不超过2.5 mm的小球状的缓释制剂[4]。它既能够保持液体自乳化给药系统和缓释微丸的改善溶解度、提高生物利用度及缓慢释放药物的优点,又能够克服液体自乳化给药系统运输、贮存和胶囊壳发生反应等缺点[5,6]。因此,本文以微晶纤维素、羟丙甲基纤维素钠、乳糖为辅料固化雷帕霉素液体自乳化给药系统,制备成新型的雷帕霉素自乳化缓释微丸,并考察了微丸释药性能。
1 实验部分
1.1 药品与试剂
Capmul MCM(美国Abite公司);聚氧乙烯醚-35-蓖麻油(CremophorEL)、聚乙二醇硬脂酸酯(Soutol HS-15)(德国BASF公司);二乙二醇单乙基醚(Transcutol® P)、辛酸癸酸聚乙二醇甘油酯(Labrasol)(法国Gattefossé公司);雷帕霉素原料药(批号 060705,福建省科瑞药业有限公司);甲醇、乙腈(色谱纯,美国Fisher公司);聚氧乙烯失水山梨醇单月桂酸酯(分析纯,国药集团化学试剂有限责任公司);微晶纤维素(MCC)(101型,批号:160523,陕西省西安北方惠安化学工业有限公司);乳糖(江苏省常州朗生生物工程有限公司);羟丙甲基纤维素钠(HPMC)(K4M,中国上海卡乐康公司);水为纯净水;其余试剂均为分析纯。
1.2 仪器
激光粒度分析仪(Zetasizer Nano ZS,英国马尔文公司);集热式恒温加热磁力搅拌器(DF-101S,河南郑州长城科工贸有限公司);台式微量高速离心机(H1650-W,湖南长沙市湘仪离心机仪器有限公司);安捷伦1200高效液相色谱系统,配备有四元泵、紫外检测器、自动进样器、化学工作站;水浴恒温振荡器(SHA-B 型,江苏省荣华仪器制造有限公司)。多功能滚圆机(CGC-350,中国重庆市英格造粒包衣技术有限公司);集热式恒温加热磁力搅拌器(DF-101S,河南省郑州长城科工贸有限公司);轴向单螺杆挤出机(E-50,中国重庆市英格造粒包衣技术有限公司)。
1.3 方法
1.3.1 雷帕霉素液体自乳化辅料的优化
通过测定雷帕霉素在不同辅料中的溶解度来优化辅料。将过量的雷帕霉素原料药分别添加到装有油,表面活性剂,助表面活性剂的离心管中,密封涡旋5 min后,置于(40±1)℃恒温箱中水浴50 min并将制备完毕的混合物置于(37±1)℃恒温摇床震荡72 h后,将混合物于12 000 r·min-1下离心5 min,精密吸取上清液,经流动相稀释至一定浓度后,用高效液相色谱法检测,计算雷帕霉素在各辅料中溶解度。其中色谱条件为:色谱柱:Ultimate ODS色谱柱(250 mm×4.6 mm,5 μm);柱温50 ℃;流动相为乙腈-甲醇-水=45∶34∶21(体积比);流速为 1.0 mL·min-1;检测波长为278 nm;进样量为20 μL。
1.3.2 伪三元相图的优化
采用伪三元相图法研究液体自乳化给药系统的处方配制比例。将表面积活性剂与助表面活性剂按设定好的比例混匀,作为混合乳化剂。精密称取油相与混合乳化剂,混合表面活性剂与助表面活性剂的质量比值(Km)为 1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1的比例分别混匀,在温度为(25±1)℃下用纯水滴定,在滴定过程中所产生的变化,仔细观察,并记录体系变化临界值时候的用水量,绘制伪三元相图。
1.3.3 自乳化效率的考察
取伪三元相图中面积最大而且能继续稀释的处方,加入100 mL水中,在磁力搅拌器中(温度:(25±1)℃)充分搅拌使混合均匀,记录从开始加入到形成稳定乳剂的时间,并对形成稳定乳剂的外观进行评级。
1.3.4 载药能力的测定
取伪三元相图中面积最大而且能继续稀释的处方,加入过量的雷帕霉素原料药,密封后涡旋,(40±1)℃水浴50 min,为了使充分溶解,并置于恒温(37±1)℃摇床平衡震荡72 h后,将混合物于5 000 r·min-1下离心10 min,精密吸取上清液,经流动相溶液溶解后用高效液相色谱法检测,计算各处方的最大载药量。
1.3.5 乳滴粒径的测定
取伪三元相图中面积最大而且能继续稀释的处方,在磁力搅拌器(37±1)℃搅拌下缓慢滴加到100 mL蒸馏水中,使其形成稳定的乳剂后,平衡30 min,采用激光纳米粒度仪测定粒径。
1.3.6 自乳化缓释微丸的制备
按照处方量称取帕霉素液体自乳化给药系统30%、微晶纤维素19%、羟丙甲基纤维素钠20%、乳糖 31%和精密量取水6 mL,将固体辅料按质量从小到大等量滴加,使混合均匀。再加入雷帕霉素液体自微乳化给药系统,快速搅拌,混合均匀,即得到外观略有潮湿的混合物;加入适量的纯化水制备软材,将软材加入到微丸机中,以挤出速度为 65 r·min-1挤出,挤出完毕后,迅速加入到滚圆机中以650 r·min-1的速度滚圆 3 min,收集所有制备的微丸于(40±1)℃的恒温烘干机中恒温干燥24 h。
1.3.7 自乳化缓释微丸的粒径分析和目标收率
采用筛分法测定缓释微丸的粒径分布范围,分别收集大于16目、16~24目、24~40目和小于40目的缓释微丸,称重,计算不同粒径范围的收率,其中16~24目为目标收率。

1.3.8 雷帕霉素自乳化微丸的重分散性
分别取 100 μL的液体自乳化给药系统和 100 mg自乳化缓释微丸加入到20 mL的磷酸盐缓冲液(pH 6.8)中,在磁力搅拌器(37±1)℃中快速搅拌24 h,使缓释微丸充分裂解,待稳定后,在离心机以5 000 r·min-1离心5 min后,取上层液体,用纳米激光粒度仪测定形成乳液的粒径和多分散系数。1.3.9 雷帕霉素自乳化缓释微丸体外释药研究
在同等条件下,制备三批雷帕霉素自乳化缓释微丸。精密称取适量填充于胶囊中,使每一粒胶囊含雷帕霉素约1 mg,参照《中国药典》2015版第二部中附录XC溶出度装置第三法进行实验,将胶囊装入沉降篮中,以900 mL的磷酸盐缓冲液(pH6.8)为释放介质,温度为(37±1)℃,转速为100 r·min-1,进行实验,每隔30 min取样4 mL直至8 h,并及时在操作容器中补充空白介质4 mL,将取样的溶液至于离心管中,在6 000 r·min-1的离心机中离心5 min后,取上清液过0.22μm的水溶性滤膜,取续滤液进行测定,计算累积释放度。
2 实验结果
2.1 雷帕霉素在不同辅料的溶解度
根据雷帕霉素在各辅料中的溶解度大小依次选择液体自乳化给药系统各处方的辅料,各数据见表1。
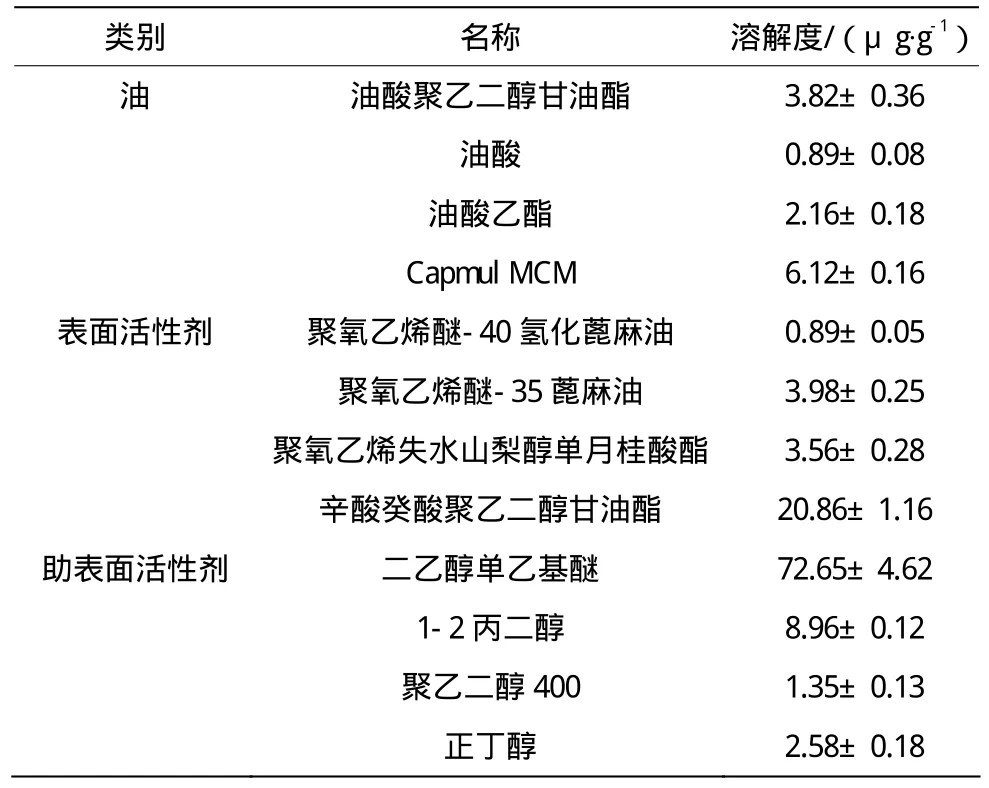
表1 雷帕霉素在油、表面活性剂、助表面活性剂的溶解度Table 1 Solubility of rapamycin in various oils, surfactants and co-surfactants
其中油相中Capmul MCM的溶解度最大,所以选择Capmul MCM 为油相。在表面活性剂中辛酸癸酸聚乙二醇甘油酯的溶解度最大,但是由于其是乳化能力不强,所以选择其次较大聚氧乙烯醚-35-蓖麻油作为混合表面活性剂,在助表面活性剂中二乙醇单乙基醚的溶解度最大,所以确定二乙醇单乙基醚为助表面活性剂。综上所述,雷帕霉素自乳化处方选择Capmul MCM为油相,聚氧乙烯醚-35-蓖麻油和辛酸癸酸聚乙二醇为混合表面活性剂,二乙醇单乙基醚为助表面活性剂。
2.2 三元相图的绘制
根据实验,绘制的伪三元相图如图1所示,结果表明:Km为4∶1时自能无限稀释的处方面积较其他比例大,所以选择 Km 为4∶1。
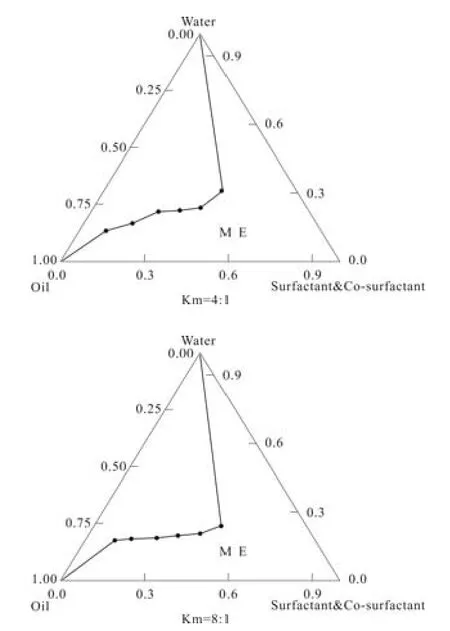
图1 不同比例伪三元相图Fig.1 Different proportions of pseudo-ternary phase diagrams
2.3 自乳化效率、载药能力、乳滴粒径测定
依据伪三元相图的结果,结合溶解度优化结果、粒径的大小和均一性、自乳化时间等(表 2)考虑到自乳化粒径大能太大和处方中表面活性剂比例不宜过高,确定液体液体自乳化给药系统的处方为Capmul MCM(油相)∶聚氧乙烯醚-35蓖麻油(表面活性剂)∶辛酸癸酸聚乙二醇甘油酯(表面活性剂)∶二乙醇单乙基醚(助表面活性剂)= 30∶28∶28∶14。
2.4 自乳化缓释微丸的粒径分析和目标收率
采用筛分法测定粒径分布,结果显示:未见直径大于2.0 mm者,直径为1.2~2.0 mm的微丸占总量(12.5±0.25)%;直径为 1.0~1.2 mm 的占总量(63.5±1.25)%,直径为 0.8~1.0 mm 的占总量(16.8±0.69)%(n=3),直径<0.8 mm 的占总量(7.2±0.32)%,粒径较均匀,符合微丸的规定。所以采用该制备工艺,雷帕霉素自乳化缓释微丸的目标收率为(92.8±2.51)%(n=3)。
2.5 自乳化微丸的重分散性
由表3可见,自乳化缓释微丸遇水重分散后形成乳剂的粒径稍有增大,但是仍在规定的范围内,这表明自乳化微丸基本保持了液体自乳化的特性;但,粒多分散系数也稍有增大,原因可能是:自微乳给药系统在溶剂中乳化的过程中受到辅料的影响,多分散系数增加,导致粒径稍大。
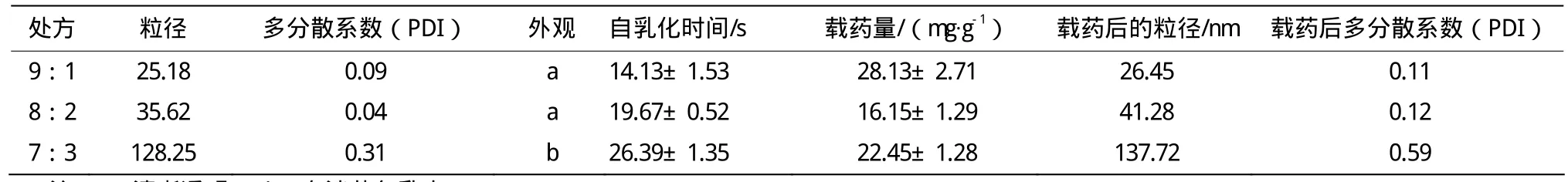
表2 不同自乳化处方的自乳化时间、乳化前后乳剂的多分散系数外观、乳化前后乳剂的粒径和载药量的测定结果(n=3)Table 2 Self-emulsifying time of different self-emulsifying prescriptions, appearance of polydispersity of emulsions before and after emulsification, determination of particle size and drug loading of emulsions before and after emulsification(n=3)
表3 前后粒径和多分散系数对比(,n = 3)Table 3 Droplet size with polydispersity index of reconstituted micro-emulsion(,n = 3)
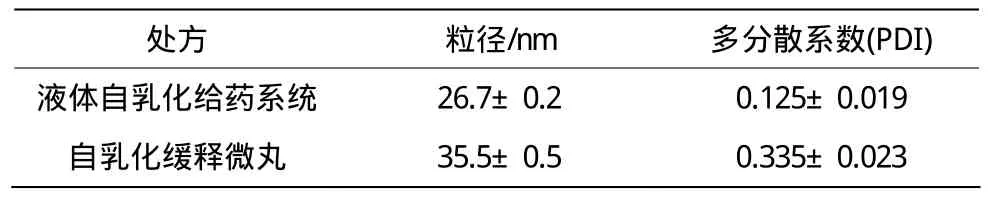
表3 前后粒径和多分散系数对比(,n = 3)Table 3 Droplet size with polydispersity index of reconstituted micro-emulsion(,n = 3)
处方 粒径/nm 多分散系数(PDI)液体自乳化给药系统 26.7±0.2 0.125±0.019自乳化缓释微丸 35.5±0.5 0.335±0.023
2.6 雷帕霉素自乳化缓释微丸体外释药研究
依据缓释制剂的要求[7]:在t=120 min时,释放度约为30%,t=240 min时,释放度约为50%,t=480 min,释放度大于80%。根据图2,雷帕霉素自乳化缓释微丸在120 min时候,释放度为31.54±3.12%,在240 min时候,释放度为51.25±4.76%,在480min时,释放度为83.16±4.52%,均符合缓释制剂的要求。这可能是在微丸中清斌甲基纤维素钠具有强大的吸收能力,形成厚厚的凝胶层,溶蚀慢,从而导致药物的缓慢释放[8]。

图2 三批缓释微丸的释药曲线(n=3)Fig.2 Drug release curves of three batches of sustained-release pellets
3 结 论
采用高效液相色谱法测定雷帕霉素在各辅料中的溶解度,来优化液体自乳化给药系统中的辅料。以伪三元相图法结合自乳化效率、微乳的粒径来确定液体自乳化给药系统的处方及比例是:Capmul MCM(油相)∶辛酸癸酸聚乙二醇甘油酯(表面活性剂)∶聚氧乙烯醚-35蓖麻油(表面活性剂)∶二乙醇单乙基醚(助表面活性剂)= 30∶28∶28∶14。将液体自乳化给药系统 30%、微晶纤维素19%、羟丙甲基纤维素钠20%、乳糖 31%和水6 mL制备成自乳化缓释微丸,粒径较均匀,符合微丸的规定且收率为(92.8±2.51)%,在磷酸盐缓冲液(pH 6.8)中,粒径和多分散系数稍有增大,但在允许的范围内;体外释药研究表明;该微丸具有良好的缓释性能。
采用该方法制备雷帕霉素自乳化缓释微丸,既能够保持口服制剂的优点,有可能提高雷帕霉素的溶出度和生物利用度,为雷帕霉素的临床应用提供一种新的方法。
[1]Yue Y,Tao C,Yang HY,et al.Preparation of mesoporous silica nanoparticles in different pore size and its use in the solidification of sirolimus loaded self -microemulsifying drug delivery system [J]. Acta Pharm Sin,2017,52 (6): 985-911.
[2]Chatel MA, Larkin DFB. Sirolimus and mycophenolate as combination prophylaxis in corneal transplant recipients at high rejection risk [J]. Am J Ophthalmol, 2010, 150: 179-184.
[3]刘志宏,胡雄伟,陶春,等. 西罗莫司国体自乳化给药系统的研究[ J] . 药学实践杂志,20016, 34 (2): 142-147.
[4]宦娣,易涛,刘颖,等.挤出滚圆法制备吲哚美辛缓释微丸[J].中国药房,2010,22 ( 17) : 1583-1586.
[5]吴昊,张晶,宋洪涛.西罗莫司纳米脂质载体固化制剂的制备[J].中国医药工业杂志,2012,43 (7):562-567.
[6]Li GL, Fan YT, Zhang YH, et al. In vitro and in vivo evaluationof total flavones of hippophae rhamnoides self-microemlsifying drug delivery system [J]. Acta Pharm Sin, 2012, 47: 1055−1062.
[7]崔福德. 药剂学[M]. 第6版. 北京:人民卫生出版社,2007:440+447.
[8]沈丽琳. 羟丙甲纤维素在药物制剂方面的应用与研究[J]. 中国药业,2007,16(12):64-67.
Study on Rapamycin Self-emulsifying Sustained Release Pellets
LI Hong-qiao1,2,LU Zhen1,2,YANG Lin1,2,WANG Yu-lai1,2*
(1. Huangshi Central Hospital of Edong Healthcare Group, Affiliated Hospital of Hubei Polytechnic University, Hubei Huangshi 435000, China;2. Hubei Key Laboratory of Kidney Disease Pathogenesis and Intervention, Hubei Huangshi 435000, China)
The rapamycin liquid self-emulsifying drug delivery system was screened out and optimized by solubility test and pseudo-ternary phase diagram. Sodium hydroxypropyl methylcellulose was used as the main framework for sustained release material. A novel solid self-emulsifying drug delivery system,rapamycin self-emulsifying sustained release pellet was prepared by extrusion-spheronization method, its dispersibility and release in vitro were also studied.The result indicated that, the liquid formulation of self-emulsifying drug delivery system was as follows: Capmul MCM (oil phase): labrasol (surfactant): castor oil polyoxyethylene ether-35 (surfactant): diethylene monoethyl ether(cosurfactant) = 30:28:28:14. The target yield of prepared sustained-release pellet was(92.8±2.51)%, and the particle size after re-dispersion was (35.5±0.5)nm. The release test of pellet in vitro showed that the pellet had good sustained-release properties. The results above indicated that this method can provide a good way for clinical application of rapamycin.
Rapamycin; Self-emulsifying drug delivery system; Pellets; Sustained release; Methylcellulose
R945
A
1671-0460(2017)11-2266-04
黄石市科技局医疗卫生领域项目(HSYL2015000085); 黄石市科技局医疗卫生领域项目(HSYL2016000087)。
2017-08-12
李红桥(1986-),男,湖北黄冈人,药师,硕士,2013年毕业于西南大学药物分析专业,研究方向:从事固体自乳化给药系统研究。E-mail:lixiaoganggg@163.com。
王雨来(1972-),男,主任药师,研究方向:临床药学。E-mail:452411085@qq.com。
——雷帕霉素

