不同算法模型在宫颈癌根治术后固定野调强放射治疗中剂量学分析
葛 双 郗会珍 王 寻 叶书成* 马 俊 陈长建 朱培军 杨君东 程淑媛
不同算法模型在宫颈癌根治术后固定野调强放射治疗中剂量学分析
葛 双①郗会珍①王 寻②叶书成①*马 俊①陈长建①朱培军①杨君东①程淑媛①
目的:比较宫颈鳞癌根治术后患者在固定野调强放射治疗(FF-IMRT)计划设计时采用各向异性分析算法(AAA)和笔形束卷积(PBC)算法的剂量学差异。方法:随机选取10例术后接受放射治疗的宫颈鳞癌患者的定位CT影像资料,分别采用Varian Eclipse放射治疗计划系统(TPS)提供的AAA和PBC两种剂量算法模型,对七野均分的同一调强计划(IMRT)进行剂量计算,并用电子射野影像装置(EPID)进行剂量验证,比较两种算法模型的剂量-体积直方图(DVH)图上靶区、小肠、结肠、直肠、膀胱、股骨头等危及器官(OARs)的吸收剂量与体积参数和机器跳数(MU)、验证结果γ通过率等参数的差异。结果:两种算法模型得到靶区的平均剂量(Dmean)与最大剂量(Dmax)PBC算法略高于AAA,适形度指数(CI)和靶区剂量均匀性指数(HI)的AAA结果均好于PBC算法,MU的AAA略高于PBC算法。小肠的V15、Dmean、50%的覆盖体积受照的最小剂量(D50%),结肠的Dmean、D50%,膀胱的V30、V40、V45、Dmean、D50%,左、右股骨头的Dmean的AAA的结果均高于PBC算法;结肠的Dmax,直肠的Dmean、Dmax、D50%和V45的PBC算法略高于AAA。平均差异除直肠的V45和结肠的V40(21.38%,3.59%)较大外,其余参数的偏差在0.07%~1.70%之间,相同角度射野两种算法的γ通过率结果均>98%,差异无统计学意义(t=-0.886,t=0.424,t=0.261,t=-1.426,t=0.284,t=-0.552,t=0;P>0.05)。结论:在宫颈癌根治术后,七野调强放射治疗计划中两种算法获得的靶区和OARs的剂量学参数存在一定的差异,但均可满足临床要求,且剂量验证通过率差异无统计学意义。两种算法均可应用于临床,但在直肠保护、降低放射性直肠损伤发生率方面,AAA要好于PBC算法。
宫颈癌;各向异性分析算法;笔形束卷积算法;调强放射治疗;剂量学;医用直线加速器
宫颈癌是近年来发展中国家妇女中最常见的妇科恶性肿瘤,其中90%为鳞状细胞癌,严重影响着患者的身心健康和生活质量[1]。目前针对早期宫颈癌(IBIIA)的治疗主要采用根治性子宫切除术及盆腔淋巴结清扫术的方法,为了降低复发的高危因素影响,行全盆腔辅助放射治疗,以提高患者总的生存率[2-4]。
近年来,伴随放射治疗设备的不断升级,调强放射治疗技术被广泛应用于宫颈癌放射治疗中,与传统放射治疗相比,其能有效实施靶区处方剂量,同时降低周围重要器官的受照剂量及发生并发症的可能性,但对靶区和危及器官(organ at risk,OARs)剂量计算的准确性有更高的要求[5]。计划系统内剂量计算的准确性与临床肿瘤放射治疗效果和毒性反应有着密切的关系,直接影响肿瘤控制概率(tumor control probability,TCP)以及正常组织并发症概率(normal tissue complications probability,NTCP)。因此,针对相同优化条件的放射治疗计划,在剂量计算时,选取不同的剂量算法模型,可能导致靶区及重要器官剂量分布计算结果的差异。国际辐射单位与测量委员会(International Commission on Radiation Units and Measurements,ICRU)24报告[6]指出,5%的剂量误差就会导致TCP的10%~20%的变化,而NTCP会有更大的变化[7]。
本研究探讨了各向异性分析算法(anisotropic analytical algorithm,AAA)和笔形束卷积(pencil beam convolution,PBC)算法在10例宫颈鳞癌患者根治术后七野FF-IMRT计划中靶区和OARs的剂量学差异,并采用电子射野影像装置(EPID)剂量学验证系统对两种算法的γ通过率进行测量,为临床实践提供剂量学参考和指导。
1 材料与方法
1.1 病例材料
选取2016年4月至2017年1月在济宁医学院附属医院肿瘤放疗科接受放射治疗的10例宫颈鳞癌根治术患者的CT影像资料,患者年龄34~76岁,平均年龄50.1岁。按国际妇产科协会(FIGO)分期,10例患者ⅠB1期3例,ⅠB2期3例,ⅡA期4例。手术方式均为广泛子宫、双附件切除和盆腔淋巴结清扫术。术后病理为中、低分化鳞状细胞癌,存在高危因素,需行全盆腔放射治疗。
1.2 仪器设备
医用电子直线加速器(美国 瓦里安Ix)、大孔径CT模拟定位机(荷兰 飞利浦Brilliance)、电子射野影像装置(EPID)和Varian Eclipse计划系统。
1.3 定位CT图像采集
所有患者均采用仰卧位,腹盆腔体模固定,双手抱肘(右手在上,左手在下)置于额头,通过三维定位激光来确保患者的正中位、水平位与CT定位床板平行。嘱咐患者在CT模拟机定位前排尽小便,口服800~1000 ml温开水,开始憋尿以保证中等程度的膀胱充盈,1 h后开始扫描采集CT图像。数据采集应用Philips Brilliance大孔径CT模拟定位机,CT扫描同时静脉注射碘海醇90 ml进行影像对比增强,注射速率2.5~3.0 ml/s。CT扫描的层厚和间隔均为5 mm,范围自腰2椎体上缘至坐骨结节下5 cm,获得的CT图像传输至Varian Eclipse放射治疗计划系统(treatment planning system,TPS)。
1.4 靶体积及OARs的勾画和处方剂量
将采集的CT图像在TPS计划系统进行三维重建处理后,根据美国放射治疗肿瘤学组(RTOG)宫颈癌术后靶区勾画指南和ICRU 83号报告[8]勾画靶区、膀胱、直肠、小肠等OARs。临床肿瘤靶体积(clinical target volume,CTV)包括阴道上段1/2及残端、阴道旁软组织和盆腔淋巴引流区域(髂内外、骶前、闭孔淋巴结、髂总淋巴结)。将CTV边界在三维上均匀外扩5~10 mm得到计划靶体积(planning target volume,PTV),同时需要勾画的OARs包括膀胱、小肠、结肠、直肠及双侧股骨头。处方剂量满足95%PTV接受4500 cGy,分25次,每次180 cGy。
1.5 计划设计
在TPS计划系统中对10例患者均采取固定射野逆向调强(FF-IMRT)方式制定治疗计划,照射方式为七野等中心照射,入射角分别为0°、51°、102°、153°、204°、255°和306°。
(1)优化限制条件的设置:处方剂量均设定为4500 cGy,要求95%PTV接受4500 cGy,5%PTV接受4700 cGy。
(2)计划优先(Priority)顺序:为CTV>PTV>直肠>膀胱>小肠和结肠>股骨头(膀胱D50%<4500 cGy,直肠V45<50%,小肠和结肠Dmax<4800 cGy,双侧股骨头D40%<1800 cGy)。射线质选取VARIAN ix直线加速器提供的6 MV的X射线,剂量率设置为400 MU/min。对同一个计划,设置相同的优化和归一参数,选取AAA和PBC两种剂量算法模型分别进行剂量计算。
1.6 剂量验证
在TPS中通过Portal Dosimetry模块对两种剂量算法的放射治疗计划分别生成剂量验证计划(Verification Plan),射野角度全部归零,将其传输到VARIAN加速器配备的电子射野影像装置(EPID)进行二维剂量学验证。Gamma分析中设置约束条件限值为:剂量容度(Dose Tolerance)为3%,距离偏差(DTA)<3 mm,以感兴趣区域内γ值<1为通过,要求通过率好于95%,即为测量结果与计划系统计算结果一致。
1.7 计划评估及剂量学评价
评价指标的参数通过靶区和OARs的剂量-体积直方图(DVH)进行比较,参数包括最小剂量(Dmin)、最大剂量(Dmax)、平均剂量(Dmean)、95%的PTV覆盖体积受照的最小剂量(D95%)、靶区剂量均匀性指数(homogeneity index,HI)、适形度指数(conformity index,CI),小肠、结肠、直肠和膀胱的受照射剂量分别>15 Gy、30 Gy、40 Gy和45 Gy的体积占危及器官总体积的百分比(V15、V30、V40和V45),50%的覆盖体积受照的最小剂量(D50%),左、右股骨头5%的覆盖体积受照的最小剂量(D5%),其HI计算为公式1:

而CI计算为公式2:

式中D2%为2%的PTV覆盖体积受照的最小剂量,D98%为98%的PTV覆盖体积受照的最小剂量,D50%为50%的PTV覆盖体积受照的最小剂量,VTV95%为95%等剂量线所包绕的PTV的体积,VTV为PTV的总体积,V95%为95%等剂量线所包绕的总体积。HI值越小,剂量跌落区越陡,靶区内剂量变化梯度越小,表示靶区剂量分布均匀性越好;CI值范围是0~1,值越大,表示适形度越好。正常组织的分析指标是受到特定剂量水平照射的体积百分比,越接近于1,表示靶区剂量分布的适形度越好。
1.8 统计学方法
数据结果采用SPSS 17.0软件进行统计学分析,对得到的两种剂量算法模型的各剂量学参数结果采用配对t检验分析,以P<0.05为差异有统计学意义;平均偏差(DP)为两种算法平均值的差值与AAA平均值的百分比。
2 结果
2.1 靶区剂量学参数及MU的差异
CTV和PTV的Dmean与Dmax的PBC算法均略高于AAA,差异有统计学意义(t=-6.621,t=-4.061;P<0.05),平均差异最大为0.96%,Dmin差异无统计学意义(t=0.986,t=1.523;P>0.05),PTV的95%覆盖体积受照的D95%差异无统计学意义(t=0.623,P>0.05),AAA的CI和HI均好于PBC算法,差异有统计学意义(t=2.552,t=-14.036;P<0.05);MU的AAA(1580±99.03)略高于PBC算法(1563±97.04),差异有统计学意义(t=7.373,P<0.05),见表1。
2.2 OARs剂量学参数的差异
小肠的V15、Dmean和D50%的AAA结果高于PBC算法,平均偏差分别为0.64%、0.81%与1.24%,差异有统计学意义(t=2.56,t=2.576,t=2.78;P<0.05);V30和V40差异无统计学意义(t=0.274,t=-0.079;P>0.05);结肠的Dmean和D50%的AAA结果略高于PBC算法,平均偏差为0.6%和1.2%,差异有统计学意义(t=2.61,t=2.413;P<0.05);Dmax的PBC算法略高于AAA,平均偏差为0.84%,差异有统计学意义(t=-3.34,P<0.05);V15、V30和V40差异无统计学意义(t=2.142,t=-0.796,t=-2.069;P>0.05);直肠的Dmean、Dmax、D50%和V45的PBC算法结果均高于AAA,其中除V45平均偏差较大为21.38%外,其余分别为1.05%、0.88%和0.97%,差异有统计学意义(t=-4.77,t=-3.201,t=-3.383,t=-4.427;P<0.05);膀胱的V30、V40、V45、Dmean和D50%的AAA算法结果略高于PBC算法,平均偏差最大为1.54%,差异有统计学意义(t=0,t=0.001,t=0.024,t=0,t=0;P<0.05);Dmax差异无统计学意义(t=-0.75,P>0.05);左、右股骨头的Dmean的AAA结果略高于PBC算法,差异有统计学意义(t=8.343,t=6.591;P<0.05);Dmax与D5%差异无统计学意义(t=1.665,t=0.821,t=1.98,t=2.232;P>0.05),见表2。
表1 AAA与PBC算法靶区剂量学参数的差异(±s)
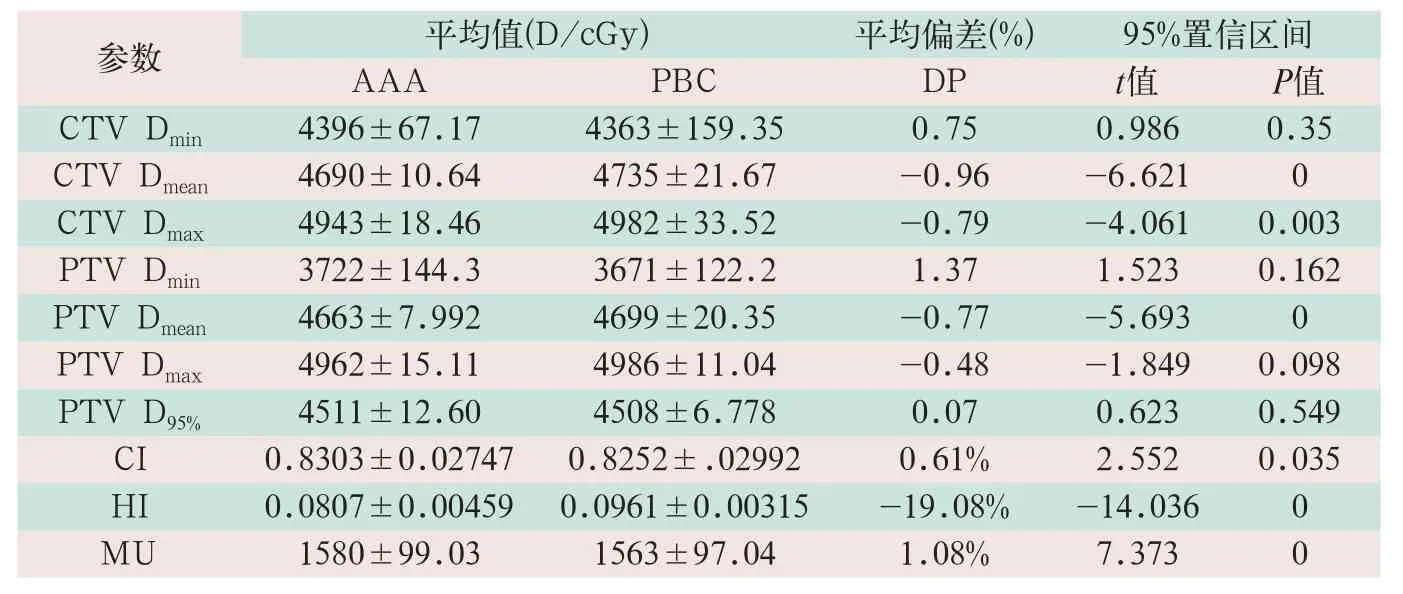
表1 AAA与PBC算法靶区剂量学参数的差异(±s)
表2 两种算法OARs剂量学参数的差异(±s)
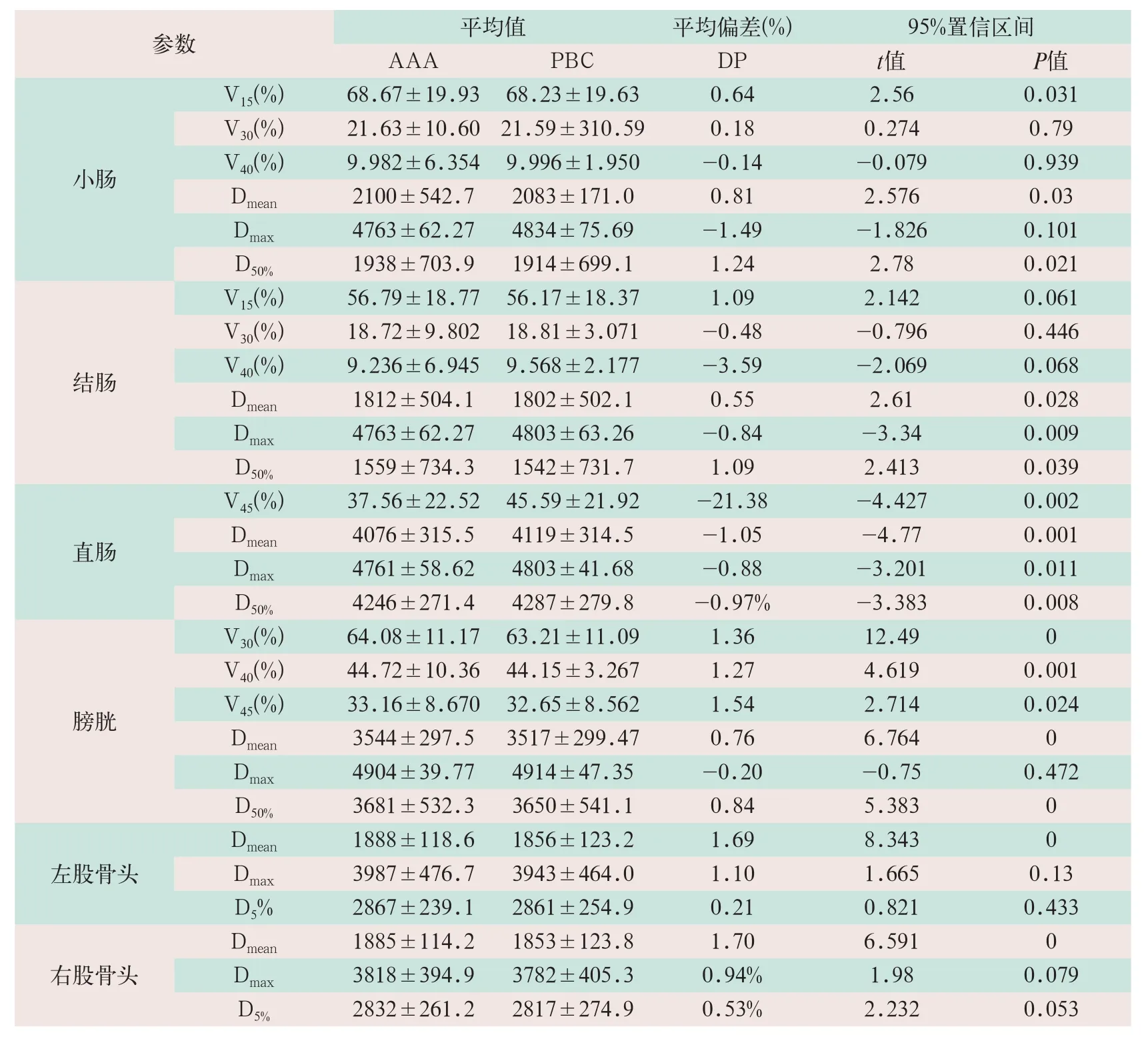
表2 两种算法OARs剂量学参数的差异(±s)
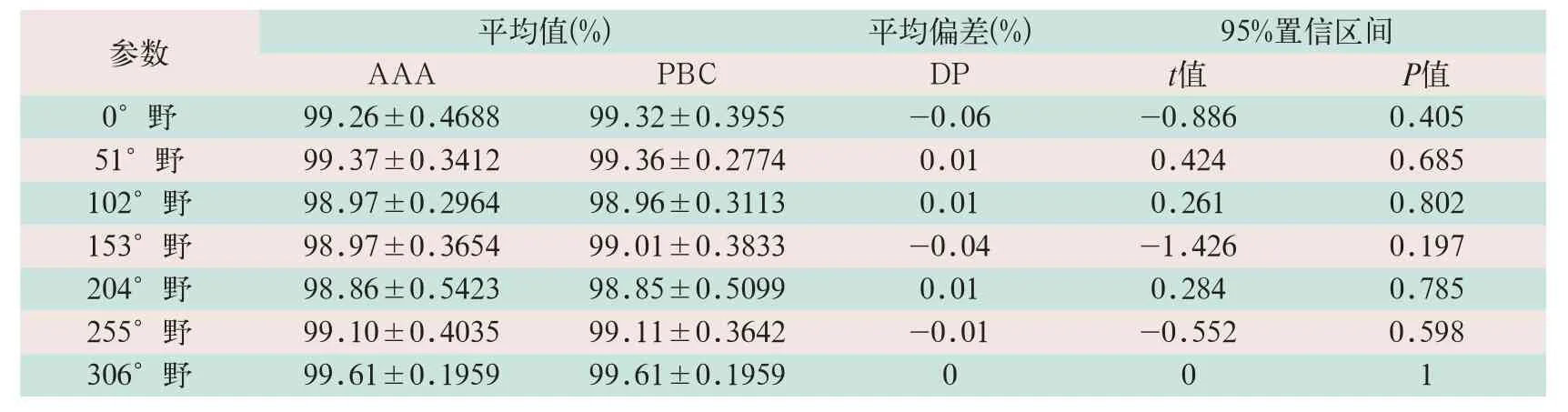
表3 不同角度7射野两种算法通过率的差异
2.3 EPID剂量验证通过率的差异
采取相同角度单一射野验证结果进行比较,7个射野两种算法各自的γ通过率结果均>98%,平均差异非常小,两种算法总的通过率为99.16%和99.17%,差异无统计学意义(t=-0.886,t=0.424,t=0.261,t=-1.426,t=0.284,t=-0.552,t=0;P>0.05),见表3。
3 讨论
放射治疗计划系统中不同的剂量算法其计算原理不同,PBC和AAA均是基于模型的算法,模型建立的准确性将直接影响到剂量计算的精度[9]。PBC算法是一维能量非局部沉积算法,是基于笔形束核的卷积模型,采用了快速傅立叶变换,深度方向和侧向电子密度修正在卷积过程中不考虑,因此对光子穿过不同电子密度组织时的二次建成效应体现较弱,但基本可以满足剂量计算准确性的要求[10-11];AAA模型的建立考虑了原射线、电子线污染以及散射线的影响,是三维的PBC叠加算法[12-15]。对于侧向不均匀组织进行了等效电子密度的修正,在不均匀介质中的剂量计算更准确,也更接近于测量值[16]。
对于AAA与PBC算法的剂量学对比的研究国内外均有相关文献报道,主要集中于肺癌、鼻咽癌等部位的剂量学差异。Fogliata等[17]和张富利等[18]提出肺癌PBC算法和AAA的HI及CI无差异,但是肺的指标差异显著,AAA计算结果受呼吸影响的幅度小于PBC算法,因此采用AAA更好。张先稳等[19]报道,鼻咽癌AAA与PBC算法相比,靶区的HI及CI的Dmean更有优势,脑干、脊髓、晶体以及视神经的最大剂量值均更低。结果均显示出在低密度区域或空腔部位AAA精度好于PBC算法,但针对两种算法模型在宫颈癌术后患者治疗计划方面的剂量学差异研究不多。
宫颈癌术后患者解剖结构复杂,靶区体积大,周围的膀胱、小肠、直肠等OARs紧密包绕靶区,极易受到过量照射,因此有必要开展AAA与PBC算法针对宫颈癌术后患者剂量学差异的研究,探讨较优的剂量算法。
本研究结果表明,两种算法模型得到的靶区的Dmean、Dmax,小肠的V15、Dmean、D50%,结肠的Dmean、D50%,膀胱的V30、V40、V45、Dmean、D50%,左、右股骨头的Dmean,结肠的Dmax,直肠的Dmean、Dmax、D50%、V45等剂量学参数PBC算法与AAA结果相差不大,平均偏差均<2%,其原因是由于宫颈癌根治术后靶区位于盆腔较深区域,与周围组织密度相差不大,造成组织间剂量跌落效应变小,AAA的优势不明显;直肠的V45和结肠的V45平均差异较大,分别为21.38%和3.59%,PBC算法明显高于AAA,主要原因是直肠的大部分和结肠的一部分是包含到靶区内,造成PBC算法趋向于过高估计靶区内低密度组织的吸收剂量,与谭丽娜等[12]的报道一致。靶区的CI和HI的AAA结果要略优于PBC算法;MU的AAA略高于PBC算法1.08%,两者计划实施的时间相差不大。电子射野影像装置(EPID)的验证实际测量结果与两种算法的计算结果γ通过率均>98%,相差不明显,无统计学意义。
综上所述,在宫颈癌根治术后调强放射治疗计划中两种算法获得的靶区和OARs的剂量学参数差异不大,并且剂量验证通过率差异无统计学意义。两种算法均可以应用于临床,但在降低放射性直肠损伤毒性,保护直肠方面,AAA要好于PBC算法。
[1]高强,邱杰,全红,等.不同铅门宽度和螺距对宫颈癌放射治疗计划设计的影响研究[J].中国医学装备,2015,12(12):47-51.
[2]Tsai CS,Lai CH,Wang CC,et al.The prognostic factors forpatients with early cervical cancer treated by radical hysterectomyand postoperative radiotherapy[J].Gynecol Oncol,1999,75(3):328-333.
[3]Papp Z,Csapó Z,Mayer A,et al.Wertheimoperation:5-yearsurvival of 501 consecutive patients with cervical cancer[J].OrvHetil,2006,147(12):537-545.
[4]夏怡,李云海,赵森,等.宫颈癌术后适形调强放疗与三维适形放疗同步化疗的对比研究[J].中国癌症杂志,2012,22(2):142.
[5]吴建亭,狄慧,施春明,等.两种算法在宫颈癌术后调强放疗中的剂量学比较研究[J].肿瘤预防与治疗,2017,30(1):39-42.
[6]ICRU.Determination of absorbed dose in a patient irradiated by beams of X or Gamma rays in radiotherapy procedures(ICRU report 24)[EB/OL].http://www.icru.org,1976.
[7]Bufacchi A,Nardiello B,Capparella R,et al.Clinical implications in the use of the PBC algorithm versus the AAA by comparison of different NTCP models/parameters[J].Radiat Oncol,2013,8(1):164.
[8]ICRU.Prescribing,recording,and reporting photonbeam intensity-modulated radiation therapy(IMRT)(ICRU83)[J].J ICRU,2010,10(1):1-106.
[9]李小波.组织不均匀条件对调强计划系统计算模型精度影响的研究[D].北京:清华大学,2012.
[10]Panetteri V,Barsoum P,Westermark M,et al.AAA and PBC calculation accuracy in the surface build-up region in tangentialbeam treatments.Phantom and breast case study with the Monte Carlo code PENELOPE[J].Radiother Oncol,2009,19(3):1221-1228.
[11]Carlaprile PF,Venencia CD,Besa P,et al.Comparisonbetween measured and calculated dynamic wedge dose distributionsusing the anisotropic analytic algorithm and pencil-beam convolution[J].J Appl Clin Med Phys,2006,8(1):47-54.
[12]谭丽娜,石梅,柴广金,等.食管癌调强放疗计划中AAA算法与PBC算法的对比研究[J].中国医学物理学杂志,2012,29(1):3092-3095.
[13]李金伟,肖海,王蓉,等.鼻咽癌调强放疗中解剖位置变化对剂量分布的影响[J].中国当代医药,2016,23(20):66-68.
[14]Carlaprile P,Venencia CD,Besa P.Comparison between measured and calculated dynamic wedgedose distributions using the anisotropic analytic algorithm and pencil-beam convolution[J].J Appl Clin Med Phys,2007,8(1):47-54.
[15]刘晓静,张西志,李军,等.胸中段食管癌旋转容积调强与固定野动态调强放疗的剂量学研究[J].实用癌症杂志,2011,26(6):630-633.
[16]张先稳,张西志,花威,等.AAA算法和PBC算法在食管癌调强放疗中的验证评估[J].实用癌症杂志,2013,28(3):282-284.
[17]Fogliata A,Nicolini G,Vanetti E,et al.The impact of photon dose calculation algorithms on expected dose distributionsin lungs under different respiratory phases[J].Phys Med Biol,2008,53(9):2375-2390.
[18]张富利,王军良,盛红国,等.PBC算法与AAA算法在肺癌调强放疗中的剂量学比较[J].中国医学物理学杂志,2011,28(3):2588-2590.
[19]张先稳,桂龙刚,张西志,等.不同剂量算法在鼻咽癌调强放疗中的剂量学研究[J].医疗装备,2017,30(1):30-32.
Dosimetric analysis of different algorithms model in fixed field IMRT after radical operation of cervical squamous carcinoma
GE Shuang, CHI Hui-zhen, WANG Xun, et al
Objective:To compare the dosimetric difference of patients with cervical squamous carcinoma in application of fixed-fields IMRT(FF-IMRT) between anisotropic analytical algorithm(AAA) and pencil beam convolution(PBC)algorithm.Methods:The location CT images of 10 patients with cervical squamous carcinoma who
radiotherapy post-operation were randomly selected in the research. Each IMRT that was averaged by seven-fields was calculated by AAA and PBC, respectively, that were provided by varian eclipse TPS. And the electronic portal imaging device (EPID)was applied to verify the dosage. The adsorbed dose, volume parameter, MU, the passing rate of γon series of organ at risks (OARs), that included of target region, small intestine, colon, rectum, bladder and femoral head, on the dosevolume histogram (DVH) of the two algorithm model were compared.Results:Dmeanand Dmaxof the target region of PBC algorithms were slightly higher than those of AAA algorithms, while CI and HI of AAA algorithms were better than that of PBC algorithm, and the MU of AAA was slightly higher than that of PBC algorithm. For V15, Dmean, D50%of small intestine, Dmean, D50%of colon, V30, V40, V45, Dmean, D50%of bladder, Dmeanof double femoral head, all of results of AAA are higher than that of PBC algorithm. Dmax of colon, Dmean, Dmax, D50%and V45of rectal of PBC algorithms were slightly higher than that of AAA. The average differences of most of parameters were between 0.07% and 1.70% except V45(21.38%) of rectum and V40(3.59%)of colon. The pass rates of γ of the two algorithms at same field were higher than 98%, and the difference between them were not statistically significant (t=-0.886, t=0.424, t=0.261, t=-1.426, t=0.284,t=-0.552, t=0, P>0.05).Conclusion:There are some differences in the dosimetric parameters of the target region and OARs which are obtained from two algorithms in seven fields FF-IMRT of post radical operation of cervical squamous carcinoma, but all of them can meet the clinical requirements and the difference of the pass rate of dose verification is not statistically significant. Therefore, both of algorithms can be used in clinical practice. However, in these aspects of protecting rectum and reducing the incidence of radioactive rectal injury, AAA is better than PBC algorithm.
Cervical squamous carcinoma; Anisotropic analytical algorithm; Pencil beam convolution algorithm;Intensity modulated radiotherapy; Dosimetry; Medical linear accelerator
Department of Tumor Radiotherapy, Affiliated Hospital of Jining Medical University,Jining 272000, China.
1672-8270(2017)11-0034-06
R814.2
A
10.3969/J.ISSN.1672-8270.2017.11.0010

葛双,男,(1989- ),硕士,物理师。济宁医学院附属医院肿瘤放疗科,研究方向:肿瘤放射治疗物理学。
①济宁医学院附属医院肿瘤放疗科 山东 济宁 272000
②济宁医学院附属医院医学影像中心 山东 济宁 272000
*通讯作者:18678766862@163.com
China Medical Equipment,2017,14(11):34-39.
2017-07-05

