高乌头药材常规项检查及高乌甲素、冉乌头碱含量测定
张立军 戴海蓉 樊秦 夏鹏飞 沈秉学 李芸


摘要:目的 对高乌头药材进行常规项检查并测定高乌甲素、冉乌头碱含量,为建立高乌头药材质量标准提供参考。方法 采集不同产地高乌头药材,采用薄层色谱法进行定性鉴别,按药典水分测定法(烘干法)、灰分测定法、浸出物测定法测定水分、灰分和浸出物,采用HPLC测定高乌甲素和冉乌头碱含量。结果 薄层色谱斑点清晰,分离度好;暂定高乌头药材中水分、总灰分及酸不溶性灰分分别不得过11.0%、12.0%、7.0%,水溶性浸出物和醇溶性浸出物分别不少于18.2%、10.6%;高乌头药材中冉乌头碱和高乌甲素含量分别不少于0.125%、0.815%。结论 本研究所建立的方法准确可靠,可用于高烏头药材质量评价。
关键词:高乌头;常规检查;高效液相色谱法;高乌甲素;冉乌头碱
DOI:10.3969/j.issn.1005-5304.2017.11.015
中图分类号:R284.1 文献标识码:A 文章编号:1005-5304(2017)11-0063-04
Routine Examination of Aconitum sinomontanum Nakai and Content Determination of Lappacontine and Ranaconitine ZHANG Li-jun1, DAI Hai-rong1, FAN Qin2, XIA Peng-fei2, SHEN Bing-xue1, LI Yun1 (1. Gansu University of Chinese Medicine, Lanzhou 730000, China; 2. Key Laboratory of Chemistry and Quality for Traditional Chinese (Tibetan) Medicines of Colleges of Gansu Province, Lanzhou 730000, China)
Abstract: Objective To study the routine examination of Aconitum sinomontanum Nakai and determine the contents of lappacontine and ranaconitine; To provide basis for establishing the quality standard of Aconitum sinomontanum Nakai. Methods Aconitum sinomontanum Nakai were collected from different areas. A method of TLC was used for qualitative discrimination. The methods in the Chinese Pharmacopoeia were adopted for the determination of moisture content, ash content and extractives. Determination of lappacontine and ranaconitine were performed by HPLC. Results The TLC showed that the spots were clear and the separation was good. Individual provisional standards: the moisture, total ash and acid-insoluble ash content of Aconitum sinomontanum Nakai were not more than 11.0%, 12.0%, and 7.0%, respectively; water soluble and alcohol soluble extractives were not less than 18.2% and 10.6%, respectively. The content of ranaconitine and lappacontine in Aconitum sinomontanum Nakai were not less than 0.125% and 0.815%, respectively. Conclusion The method established by the study is accurate and reliable, and can be used for quality evaluation of Aconitum sinomontanum Nakai.
Key words: Aconitum sinomontanum Nakai; routine examination; HPLC; lappacontine; ranaconitine
高乌头为毛茛科乌头属植物高乌头Aconitum sinomontanum Nakai的根,又名麻布七、辫子七、破骨七等,是我国甘肃等中西部地区民间习用中药,也是著名“七药”之一[1],具有祛风除湿、理气止痛、活血散瘀的功效,用于治疗风湿痹痛、关节肿痛、跌打劳伤等。现代药理研究表明,高乌头具有镇痛、抗炎、解热、局部麻醉、抗心律失常、抗氧化、杀虫等广泛的药理作用[2-4],临床上常用于治疗类风湿关节
基金项目:国家自然科学基金(81560650);甘肃省自然科学基金(1107RJZA242)
通讯作者:李芸,E-mail:liyunherb@163.com
炎及局部镇痛[5-6]。高乌头的主要活性成分为二萜生物碱[7],其中以高乌甲素和冉乌头碱的含量最高[8],而活性成分之一高乌甲素已开发出不同剂型并应用于临床[9]。
高乌头为我国特有植物,在北方地区有着丰富的资源分布,目前甘肃地区引种驯化成功、大量生产和应用,现已成为甘肃地产大宗商品药材。高乌头收载于《甘肃省中药材标准》(2009年版)[10],现有的标准尚不完善,既无常规项检查,也无含量测定项。为此,本试验采用常规项检查及高乌甲素、冉乌头碱含量对其进行质量评价,以保证临床用药安全有效,并为高乌头药材质量标准的制订和完善提供参考。
1 仪器与试药
BT125D电子天平(赛多利斯科学仪器有限公司);KQ3200DB超声波清洗器(昆山市超声仪器有限公司);FW-400A高建万能粉碎机(北京科伟永兴仪器有限公司);DHG-9240A型电热恒温鼓风干燥箱(上海一恒科技有限公司);RJX-4-9型号箱形电阻炉(天津实验电炉厂);HHS-11S数显恒温水浴锅(上海宜昌仪器纱筛厂);Agilent 1100 Series型高效液相色谱仪,DAD检测器(美国Agilent科技有限公司);SHB-3循环水多用真空泵(郑州杜甫仪器厂);PHS-430型pH计(方舟电子科技有限责任公司);旋转蒸发仪、称量瓶、干燥器、无灰滤纸等。
高乌甲素对照品(甘肃神龙药业股份有限公司,批号20001001,HPLC纯度≥97.50%),冉乌头碱对照品(成都克洛玛生物科技有限公司,批号150404,HPLC纯度≥98.00%);甲醇、三乙胺均为色谱纯,三氯甲烷、氨水、正己烷、异丙醇、乙酸乙酯、95%乙醇为分析纯。
高乌头药材分别购于甘肃、青海等地,经甘肃中医药大学药学院杨扶德教授鉴定为毛茛科乌头属植物高乌头Aconitum sinomontanum Nakai的干燥根,样品信息见表1。
2 方法与结果
2.1 薄层鉴别
取高乌头药材粉末2 g(过4号筛),精密称定,置具塞锥形瓶中,加氨试液3 mL,再加入异丙醇-乙酸乙酯(1∶1)混合溶液50 mL,称定质量,超声处理(功率300 W,频率40 kHz,水温25 ℃以下)30 min,放冷,补足减失的质量,摇匀,过滤,取续滤液25 mL,40 ℃以下减压回收溶剂至干,残渣加入甲醇3 mL,溶解,密塞,摇匀,作为供试品溶液。另取冉乌头碱、高乌甲素对照品,分别加甲醇溶解,制成每1 mL含1 mg的溶液,作为对照品溶液。按照薄层色谱法试验,分别吸取冉乌头碱、高乌甲素对照品、供试品溶液各5 ?L,点于同一硅胶GF254薄层板上,以正己烷-三氯甲烷-乙酸乙酯-甲醇(5∶6∶8∶1.5)为展开剂,置氨蒸气饱和20 min后展开,取出,晾干,分别置紫外光灯(254、365 nm)下检视(温度18~30 ℃,湿度45%~60%)。结果供试品色谱中,在与对照品相应的位置上,显相同颜色的斑点。
2.2 检查
2.2.1 水分测定 取高乌头药材粉末4 g(过4号筛),平行3份,精密称定,按照2015年版《中華人民共和国药典》四部通则0832水分测定项下第二法(烘干法)进行测定。
2.2.2 总灰分测定 取高乌头药材粉末4 g(过4号筛),平行3份,置炽灼至恒重的坩埚中,称定质量,按照2015年版《中华人民共和国药典》四部通则2302总灰分测定项下方法测定。如果供试品不易灰化,可将坩埚放冷,加热水或10%硝酸铁溶液2 mL,使残渣湿润,然后置水浴上蒸干,残渣继续炽灼,至坩埚内容物完全灰化。
2.2.3 酸不溶性灰分测定 取“2.2.2”项下所得的灰分,按2015年版《中华人民共和国药典》四部通则2302总灰分测定项下酸不溶性灰分测定法测定。
2.2.4 浸出物测定
2.2.4.1 水溶性浸出物 取高乌头药材粉末4 g(过4号筛),平行3份,精密称定,按照2015年版《中华人民共和国药典》四部通则2201水溶性浸出物测定项下热浸法进行测定。
2.2.4.2 醇溶性浸出物 取高乌头药材粉末4 g(过4号筛),平行3份,精密称定。分别用45%、55%、65%、75%、85%、95%乙醇作为溶剂,按照2015年版《中华人民共和国药典》四部通则2201醇溶性浸出物测定项下热浸法进行测定,计算得醇溶性浸出物含量分别为33.9%、28.9%、24.1%、19.5%、17.4%、12.5%。可见,随着乙醇浓度的降低,醇溶性浸出物较多,但同时溶出的杂质也多;95%乙醇浸出物较少,不能完全提取出高乌头中的各类成分。综合以上因素,选用稀乙醇(47.5%)作溶剂测定样品中的醇溶性浸出物,一方面能够溶出高乌头中各类主要成分,另一方面便于用市售的95%乙醇配制成稀乙醇。
取高乌头粉末约4 g(过4号筛),平行3份,精密称定,以稀乙醇作为溶剂,按上述操作方法进行测定。
2.3 指标成分含量测定
2.3.1 色谱条件 采用DIKMA Spursil C18色谱柱(4.6 mm×250 mm,5 ?m);流动相A为三乙胺水溶液(pH 9.3~9.6)、B为甲醇,梯度洗脱(0~30 min,5%~35%B,流速0.4 mL/min;30~70 min,30%~100%B,流速0.4 mL/min;70~80 min,100%B,流速0.4 mL/min;80~85 min,100%B,流速1.0 mL/min);检测波长308 nm;柱温35 ℃。
2.3.2 对照品溶液的制备 分别取冉乌头碱、髙乌甲素对照品,精密称定,加甲醇溶解并定容,制成冉乌头碱和高乌甲素对照品溶液,再分别精密量取上述2种对照品溶液适量,配制混合对照品溶液(冉乌头碱0.172 5 mg/mL,高乌甲素0.375 0 mg/mL)。在上述色谱条件下,冉乌头碱与高乌甲素能够很好地分离,色谱图见图1。
2.3.3 供试品溶液的制备 取高乌头药材粉末1 g(过4号筛),精密称定,置于具塞锥形瓶中,加氨试液3 mL,再加入异丙醇-乙酸乙酯(1∶1)混合溶液50 mL,称定质量,超声处理(频率50 kHz,水温25 ℃)30 min,放冷,补足减失的质量,摇匀,过滤,精密量取续滤液10 mL,40 ℃以下减压回收溶剂,残渣加甲醇溶解,定容至25 mL,密塞,摇匀,进样前用0.45 ?m微孔膜过滤,作为供试品溶液。
2.3.4 线性关系考察 分别精密吸取混合对照品溶液0.5、1、2、4、6、8、10 ?L进样分析,测定峰面积,以峰面积对进样量进行线性回归。结果表明,高乌甲素在0.187 5~3.750 ?g范围内线性关系良好,回归方程Y=1158.8X+2.128,r=0.999 9;冉乌头碱在0.086 25~1.725 0 ?g范围内线性关系良好,回归方程Y=1195.3X-2.035,r=0.999 8。
2.3.5 精密度试验 精密吸取对照品混合溶液20 ?L,按上述色谱条件进样分析,连续进样5次,结果冉乌头碱、高乌甲素峰面积的RSD分别为0.76%、0.98%,表明仪器的精密度良好。
2.3.6 稳定性试验 取同一供试品溶液,分别于0、3、6、9、12、24 h按上述色谱条件进样测定,记录冉乌头碱、高乌甲素峰面积,结果峰面积的RSD分别为2.36%、1.51%,表明24 h内样品的稳定性良好。
2.3.7 重复性试验 取同一批次样品粉末,平行称取5份,按供试品溶液的制备方法进行制备,按上述色谱条件进行测定,计算样品中高乌甲素和冉乌头碱的含量,结果高乌甲素和冉乌头碱含量的RSD分别为2.51%、1.62%,表明本法有良好的重复性。
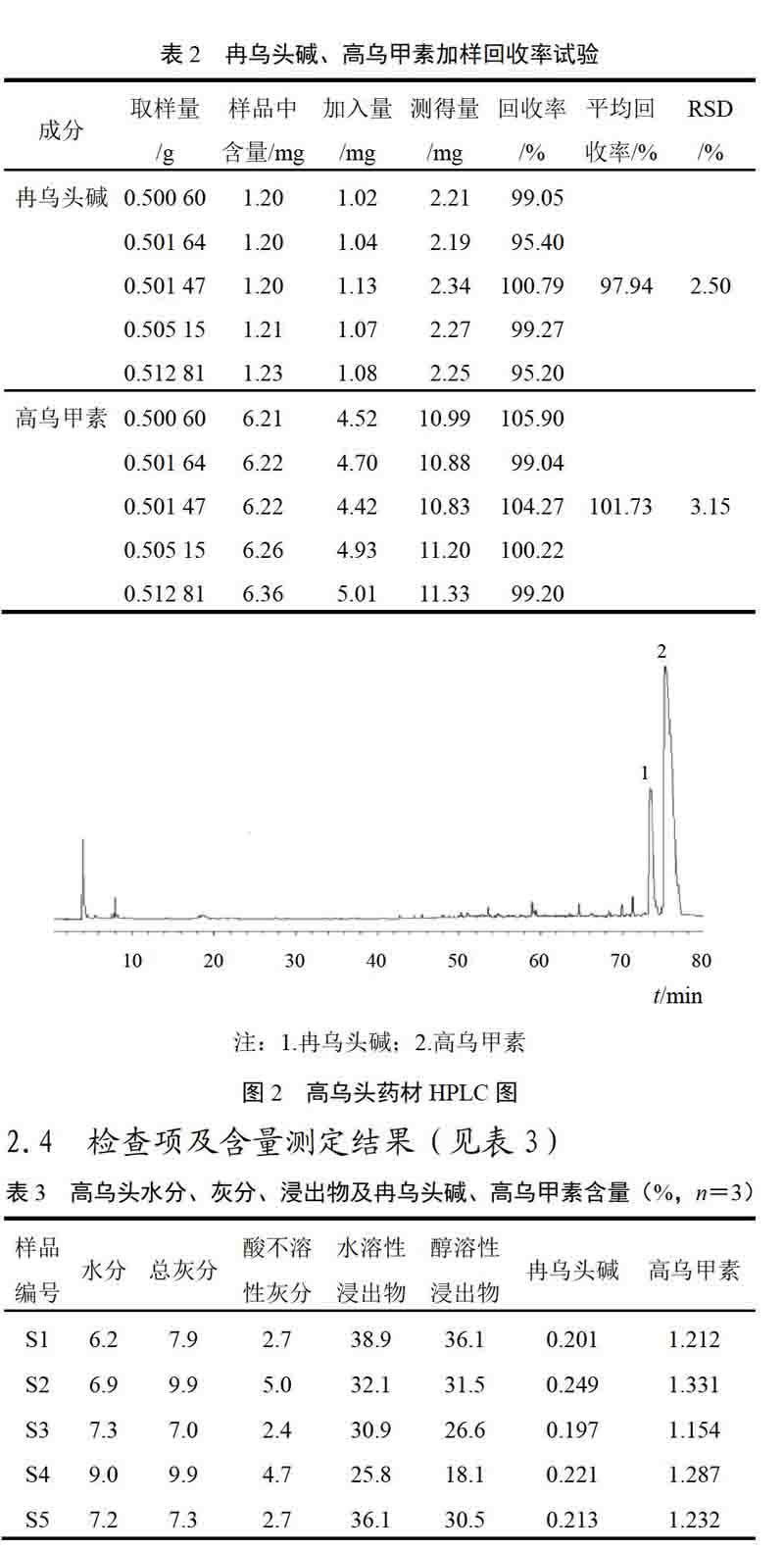
2.3.8 加样回收率试验 取已知含量的高乌头药材粉末0.5 g(高乌甲素含量为1.240%,冉乌头碱含量为0.239%),共5份,精密称定,分别加入与其含有等量的高乌甲素和冉乌头碱对照品,按供试品溶液制备方法制备,依法测定,计算高乌甲素和冉乌头碱的平均回收率均分别为97.94%、101.73%,RSD分别为2.50%、3.15%,表明本方法回收率良好,结果见表2。
2.3.9 样品含量测定 取5批次高乌头药材供试品溶液,分别精密吸取20 ?L注入液相色谱仪,记录色谱图,并按外标法以峰面积计算样品中高乌甲素、冉乌头碱的含量,色谱图见图2。
2.4 检查项及含量测定结果(见表3)
以统计学方法分析数据,设定高乌头药材水分、总灰分、酸不溶性灰分、水溶性浸出物、醇溶性浸出物、冉乌头碱及高乌甲素的上下限,计算公式如下[11-12]:
上限μ= +(t×s)/√n+MU,下限μ= -(t×s)/√n-MU
式中,—x为样本均数;t为置信水平为99%的t值(单侧),t(0.01,4)=4.604;s为样本标准偏差;n为样本批数;MU是不确定度评估,水分MU=0.126 0—x,总灰分MU=0.052 0—x,酸不溶性灰分MU=0.070 2—x,水溶性浸出物MU=0.127 5—x,醇溶性浸出物MU=0.141 5—x,冉乌头碱MU=0.223 5—x,高烏甲素MU=0.231 5—x。
水分:μ= +(t×s)/√n+MU=7.320+ (4.604×1.033)/√5+0.9221=10.369
总灰分:μ= +(t×s)/√n+MU=8.400+ (4.604×1.407)/√5+0.437=11.734
酸不溶性灰分:μ= +(t×s)/√n+MU=3.500+ (4.604×1.243)/√5+0.246=6.305
水溶性浸出物:μ= -(t×s)/√n-MU=32.760- (4.604×5.030)/√5-4.177=18.226
醇溶性浸出物:μ= -(t×s)/√n-MU=28.560- (4.604×6.755)/√5-4.041=10.611
冉乌头碱:μ= -(t×s)/√n-MU=0.216- (4.604×0.021)/√5-0.048=0.125
高乌甲素:μ= -(t×s)/√n-MU=1.243- (4.604×0.068)/√5-0.288=0.815
可知,高乌头药材的水分、总灰分及酸不溶性灰分应分别不得过11.0%、12.0%、7.0%,水溶性浸出物、醇溶性浸出物应分别不少于18.2%、10.6%;按干燥品计算,高乌头药材中冉乌头碱与高乌甲素的含量应不少于0.125%、0.815%。
3 讨论
高乌头是一味民间常用中药,一直以来,有关其质量控制方面的研究鲜有文献报道。现有的质量标准指标过于简单,不能很好地控制其质量。本课题首次从常规检查和定量分析角度对高乌头进行了质量评价研究,为新版《甘肃省中药材标准》中高乌头药材标准的完善提供依据。
薄层鉴别试验分别考察了正己烷、二甲苯、三氯甲烷、乙酸乙酯、甲醇等多种溶剂展开系统,曾用三氯甲烷-甲醇-氨水(7∶2∶0.50)、二甲苯-甲醇(5∶1)等,经过多次试验和筛选,最终确定上述展开条件,结果表明该条件具有分离度好、斑点清晰、简便易行等特点,可用于高乌头药材的薄层鉴别分析。
本试验建立了HPLC同时测定高乌头药材中冉乌头碱、高乌甲素的方法。该方法专属性强、灵敏度高、重复性好,可用于评价高乌头药材的质量。同时,试验采用药典方法对不同批次高乌头药材中水分、总灰分、酸不溶性灰分、水溶性浸出物和醇溶性浸出物进行测定,得出了较为准确的数据,为建立药材标准提供依据。
高乌头在功效上与同科同属的乌头(川乌、草乌)作用相当,但高乌头不含极毒的双酯型乌头碱类成分,临床应用相对乌头更加安全。乌头可以引起动物心律失常[13],而高乌头则具有抗乌头碱心律失常的作用。高乌头一直作为地方用药,究其原因,一方面是其标准不够完善,另一方面是产量较低、使用范围小,未能引起重视。如果解决以上问题,高乌头很有可能代替乌头药材,载入药典标准。
参考文献:
[1] 高学敏,谢晓林,党学德.中国七药:下卷[M].西安:陕西出版集团陕西科技出版社,2013:405.
[2] 魏华波,张宝华,谭兵,等.氢溴酸高乌甲素的药理作用及临床应用研究进展[J].重庆医学,2014,43(20):2660-2662.
[3] 宋晓峰,陆丽华,冯国祥,等.硬膜外氢溴酸高乌甲素复合曲马多用于剖宫产术后镇痛的效果评价[J].现代实用医学,2011,23(2):196-197.
[4] VAKHITOVA Iu V, FARAFONTOVA E I, KHISAMUTDINOVA R Iu, et al. To the mechanisms of antiarrhythmic action of Allapinine[J]. Russian Journal of Bioorganic Chemistry,2013,39(1):105-116.
[5] 李曉华,刘红.麻布七风湿药酒治疗类风湿性关节炎临床观察[J].湖北民族学院学报:医学版,2000,17(1):28-29.
[6] WANG Y Z, XIAO Y Q, ZHANG C, et al. Study of analgesic and anti-inflammatory effects of lappaconitine gelata[J]. J Tradit Chin Med,2009,29(2):141-145.
[7] 吴延吉.甘肃高乌头有效部位的研究[D].天津:天津大学,2007.
[8] 谢斌,周军辉,石新卫,等.高乌头活性成分提取工艺的优化[J].植物学报,2014,49(2):198-202.
[9] WEN X S, TUN G D, CHUN M D. Crystal structure analysis and antinociceptive property of lappaconitine hydrochloride[J]. Advanced Materials Research,2011,343:1049-1052.
[10] 甘肃省食品药品监督管理局.甘肃省中药材标准[M].兰州:甘肃文化出版社,2009:117-118.
[11] 张志锋,戴领,吴春蕾,等.藏药白花刺参的水分、总灰分、酸不溶性灰分和浸出物的含量测定[J].西南民族大学学报:自然科学版,2011, 37(4):597-602.
[12] 张达正,刘强,曹志强.测定人参水分、总灰分、酸不溶性灰分含量的不确定度评估[J].人参研究,2007,19(2):15-17.
[13] 付敏.乌头碱致心律失常的细胞分子机制的实验研究[D].北京:北京中医药大学,2007.

