苗药朱砂根的HPLC指纹图谱研究Δ
孙绪,姚成芬,付思红,巩仔鹏,刘亭,杨畅,查俊,李勇军#(.贵州省药物制剂重点实验室,贵阳550004;2.贵州医科大学药学院,贵阳550004;.民族药与中药开发应用教育部工程研究中心/国家苗药工程技术研究中心,贵阳550004)
苗药朱砂根的HPLC指纹图谱研究Δ
孙绪1,2*,姚成芬1,3,付思红1,3,巩仔鹏1,刘亭1,杨畅1,查俊3,李勇军3#(1.贵州省药物制剂重点实验室,贵阳550004;2.贵州医科大学药学院,贵阳550004;3.民族药与中药开发应用教育部工程研究中心/国家苗药工程技术研究中心,贵阳550004)
目的:建立苗药朱砂根的高效液相色谱(HPLC)指纹图谱。方法:采用HPLC法。色谱柱为Diamonsil C18,流动相为甲醇-水(梯度洗脱),流速为1.0 mL/min,检测波长为220 nm,柱温为30℃,进样量为10 μL。以11-O-(3,′4,′5′-三羟基没食子酰基)-岩白菜素为参照,测定16批药材样品的HPLC图谱,采用《中药色谱指纹图谱相似度评价系统》(2012版)进行共有峰指认和相似度评价,并就指纹图谱进行聚类分析。结果:16批朱砂根药材的HPLC图谱有6个共有峰,其中8批药材样品的相似度均>0.9;16批朱砂根药材可聚为4类。结论:该研究所建指纹图谱可为朱砂根药材的鉴别和质量评价提供参考。
朱砂根;高效液相色谱法;指纹图谱;聚类分析
朱砂根又名八爪金龙,为紫金牛科植物朱砂根Ardisia crenata Sims.的干燥根及根茎,主要成分为三萜皂苷、鞣质、糖类等[1],具清热解毒、散瘀止痛、祛风除湿之功效,临床多用于咽喉肿痛、扁桃体炎、风湿骨痛等症的治疗[2],收载于2015年版《中国药典》(一部)[3]和2003年版《贵州省中药材、民族药材质量标准》[4]。2015年版《中国药典》(一部)仅收载了朱砂根药材中岩白菜素含量的测定方法,为进一步完善其质量标准,本课题组在前期研究[5]的基础上收集了具有代表性的贵州省不同产地朱砂根药材,采用分析效能高、速度快且应用较广的高效液相色谱法(HPLC)建立了指纹图谱[6-9],并就结果进行了聚类分析。
1 材料
1.1 仪器
1100型HPLC仪,包含二极管阵列检测器、四元梯度泵、脱气机、自动进样器、柱温箱、ChemStation色谱工作站(美国Agilent公司);Me AE240型电子分析天平[梅特勒-托利多仪器(上海)有限公司]。
1.2 试剂
岩白菜素、11-O-(3′,4′,5′-三羟基没食子酰基)-岩白菜素对照品均为贵州省药物制剂重点实验室自制,经核磁共振、红外光谱检测,质谱分析确证其结构,经HPLC法检测纯度均>98%;试验所用试剂均为分析纯,水为纯化水。
1.3 药材
16批朱砂根药材采自贵州省不同产地(见表1),由贵州医科大学生药学教研室龙庆德副教授鉴定为真品。
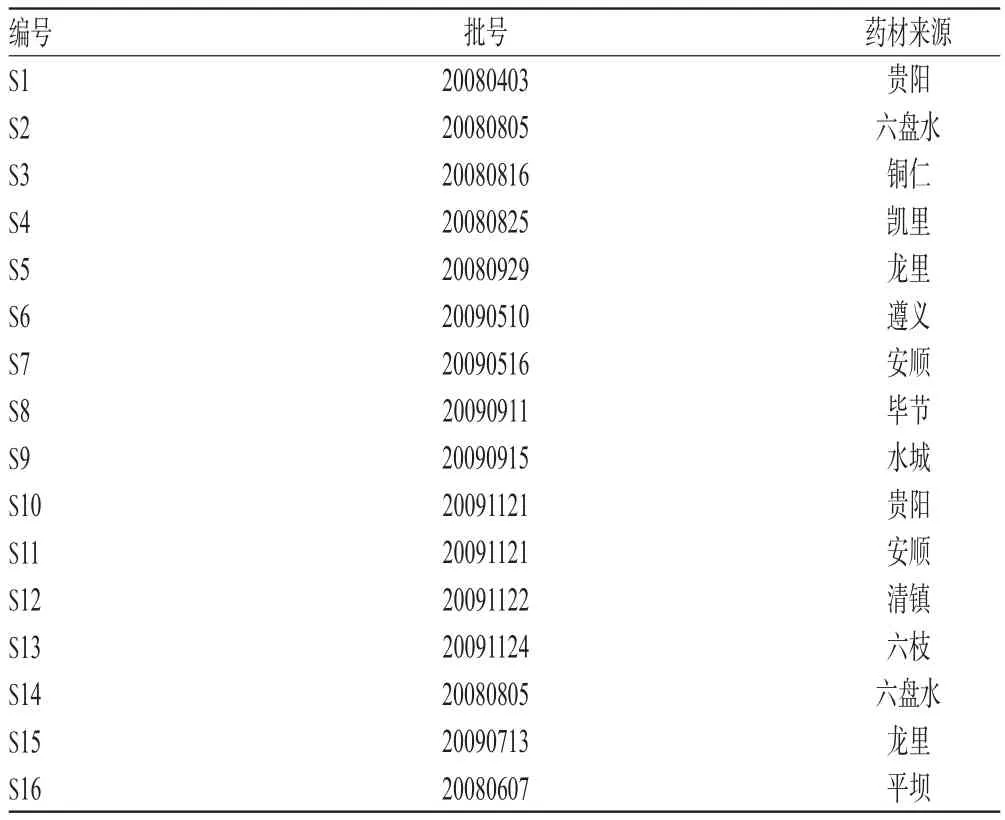
表1 朱砂根药材来源Tab 1 The sources ofA.crenata
2 方法与结果
2.1 色谱条件
色谱柱:Diamonsil C1(8250 mm×4.6 mm,5 μm);流动相:甲醇(A)-水(B),梯度洗脱(0~5 min,5%→15%A;5~10 min,15%→20%A;10~30 min,20%→40%A;30~45 min,40%→60%A);流速:1.0 mL/min;检测波长:220 nm;柱温:30℃;进样量:10 μL。
2.2 溶液的制备
2.2.1 混合对照品溶液分别称取待测成分对照品适
量,加甲醇制成岩白菜素、11-O-(3′,4′,5′-三羟基没食子酰基)-岩白菜素质量浓度分别为0.496 4、1.061 0 mg/mL的混合对照品溶液。
2.2.2 供试品溶液取药材样品粉末(过40目筛)1 g,精密称定,精密加甲醇25 mL,称定质量,加热回流提取2 h,放冷至室温,再次称定质量,用甲醇补足减失的质量,摇匀,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.3 方法学考察
2.3.1 精密度试验取“2.2.2”项下供试品溶液适量,按“2.1”项下色谱条件连续进样测定6次,以11-O-(3′,4′,5′-三羟基没食子酰基)-岩白菜素的保留时间和峰面积为参照,记录各共有峰相对保留时间和相对峰面积。结果,6个共有峰相对保留时间和相对峰面积的RSD<3.0%(n=6),表明方法精密度良好。
2.3.2 稳定性试验取“2.2.2”项下供试品溶液(编号:S1)适量,分别于室温下放置0、1、2、4、8、12、24 h时按“2.1”项下色谱条件进样测定,以11-O-(3′,4′,5′-三羟基没食子酰基)-岩白菜素的保留时间和峰面积为参照,记录各共有峰相对保留时间和相对峰面积。结果,6个共有峰相对保留时间和相对峰面积的RSD<3.0%(n=7),表明供试品溶液室温放置24 h内基本稳定。
2.3.3 重复性试验精密称取同一批药材样品(编号:S1)适量,按“2.2.2”项下方法制备供试品溶液,共6份,再按“2.1”项下色谱条件进样测定,以11-O-(3′,4′,5′-三羟基没食子酰基)-岩白菜素的保留时间和峰面积为参照,记录各共有峰相对保留时间和相对峰面积。结果,6个共有峰相对保留时间和相对峰面积的RSD<3.0%(n=6),表明本方法重复性良好。
2.4 HPLC指纹图谱的生成及相似度、共有峰相关分析
2.4.1 HPLC指纹图谱的生成取16批药材样品各适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,采用《中药色谱指纹图谱相似度评价系统》(2012版)对16批药材样品的HPLC图谱进行分析,得HPLC指纹图谱,详见图1、图2。

图1 16批药材样品HPLC叠加指纹图谱Fig 1 HPLC superposed chromatograms of 16 batches of medicinal materials
2.4.2 相似度分析采用《中药色谱指纹图谱相似度评价系统》(2012版)对16批药材样品的HPLC图谱进行比较分析,详见表2。结果,16批药材样品中有8批差异较小,相似度均>0.9;另外4批药材样品相似度在0.7~0.9之间;还有4批药材样品相似度在0.2~0.4之间。表明不同产地朱砂根药材化学成分差异较大。

图2 药材样品HPLC对照指纹图谱Fig 2 Control HPLC Fingerprint of samples
2.4.3 共有峰相关数据分析采用《中药色谱指纹图谱相似度评价系统》(2012版)对16批药材样品的HPLC图谱进行比较分析。结果,16批药材样品有6个共有峰,通过对照品HPLC图谱确定4号峰为岩白菜素,5号峰为11-O-(3′,4′,5′-三羟基没食子酰基)-岩白菜素。以5号峰为参照峰,计算其他共有峰与5号峰的相对保留时间和相对峰面积,详见表3、表4。
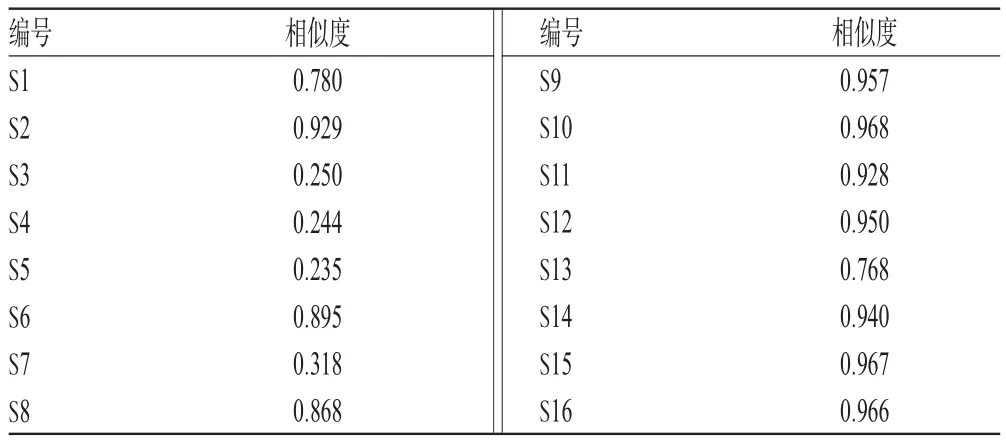
表2 16批药材样品相似度评价结果Tab 2 Similarity evaluation of 16 batches of samples

表3 16批药材样品HPLC图谱共有峰的相对保留时间Tab 3 Relative retention time of common peaks in HPLC fingerprints of 16 batches of samples

表4 16批药材样品HPLC图谱共有峰的相对峰面积Tab 4 Relative peak areas of common peaks in n HPLC fingerprints of 16 batches of samples
2.5 聚类分析
就HPLC指纹图谱中各共有峰峰面积进行标准化处理,采用SPSS 18.0统计软件中系统聚类法(Hierarchical cluster)的Ward法中欧氏距离平方法(Squared euclidean distance)对16批药材样品进行系统聚类分析,绘制树状图,详见图3。

图3 16批药材样品的聚类分析树状图Fig 3 Cluster analysis of 16 batch of medicinal materials samples
由图3可知,16批不同产地药材样品在距离为5的条件下可以分为4类:第1类药材样品7批(S2、S9、S10、S11、S14、S15、S16),其相似度均>0.9,此类药材样品中岩白菜素含量都普遍较高;第2类药材样品4批(S3、S4、S5、S7),相似度在0.2~0.4之间,此类药材样品中岩白菜素含量很低;第3类药材样品4批(S1、S6、S8、S13),相似度在0.7~0.9之间,此类药材样品中岩白菜素含量介于前2类之间;第4类药材样品1批(S12),虽然其相似度在0.9以上,但其2号共有峰含量明显高于其他批药材样品,化学成分信息量也较为全面,因此聚为一类。
3 讨论
本课题组采用HPLC法建立了苗药朱砂根的指纹图谱分析方法。试验中对流动相、洗脱梯度、流速、柱温等色谱条件进行了优化,在优化后的色谱条件下,各待测成分峰达到较好分离且基线平稳;并考察了提取方法、提取溶剂、提取时间等供试品溶液制备方法,得到了最适合的条件。方法学验证结果表明,所建立的朱砂根药材指纹图谱分析方法准确、可靠。
相似度评价法是以两者中若干共有的、具有特征的指标作为统一尺度,运用适当的判定原则来描述两者之间匹配程度的方法[10-12];聚类分析法是根据相似程度大小将样品归类,在中药的真伪鉴别、质量评价及品种分类等方面均有应用[13-16]。本研究就所鉴定的16批朱砂根药材样品的指纹图谱进行了相似度评价及聚类分析,由相似度评价结果可见,其中有4批药材样品相似度较低,差异较大,而造成该差异的主要因素是各共有峰含量的差异;聚类分析结果准确地将各批药材归类,达到了质量评价及品种分类的目的。
综上所述,本研究所建指纹图谱可为朱砂根药材的鉴别和质量评价提供参考。
[1] 陈尚钘,胡文杰,黄艳丽,等.朱砂根化学成分的初步分析[J].江西林业科技,2007,21(6):15-17.
[2] 贵州省中药普查办公室.贵州中药资源[S].北京:中国医药科技出版社,1992:785.
[3] 国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:138.
[4] 贵州省药品监督管理局.贵州省中药材、民族药材质量标准[S].贵阳:贵州科技出版社,2003:164.
[5] 李勇军,夏彬,龙庆德,等.朱砂根主要活性成分的含量测定研究[J].时珍国医国药,2011,22(8):1929-1931.
[6] 贾成友,赵凤平,李微,等.HPLC指纹图谱结合共有模式识别评价重庆市售青蒿饮片质量的一致性[J].中国药房,2015,26(27):3828-3831.
[7] 涂兴明,吴涵,吴康郁.中药指纹图谱的研究与应用[J].海峡药学,2016,28(5):1-4.
[8] 娄涛涛,陀扬凌,金玲,等.黑果枸杞及其伪品白刺果的HPLC指纹图谱研究[J].中国药房,2016,27(9):1245-1248.
[9] 罗文汇,刘布鸣,彭丽诗,等.石柑子药材的HPLC指纹图谱研究[J].中国药房,2016,27(33):4701-4704.
[10] 孙国祥,闫波,侯志飞,等.中药色谱指纹图谱评价方法研究进展[J].中南药学,2015,13(7):673-681.
[11] 关洪月,李林,刘晓,等.中药指纹图谱相似度计算方法探析[J].中国实验方剂学杂志,2011,17(18):282.
[12] 孙国祥,张玉静,孙万阳,等.中药一致性评价关键问题:中药标准制剂制模式和定量指纹图谱检查项[J].中南药学,2015,13(10):1026-1032.
[13] 朱晓勤,尹莲.化学模式识别在中药分类和质量评价中的应用[J].中华中医药学刊,2007,25(10):2111.
[14] 黄琪,黄彩虹,雷鹏,等.地锦草药材HPLC指纹图谱及模式识别研究[J].中国实验方剂学杂志,2013,19(12):95-97.
[15] 潘伟东,杜义龙,赵胜男,等.韩信草的高效液相色谱指纹图谱及化学模式识别[J].药物分析杂志,2015,35(2):250-252.
[16] 吴玲芳,林琛,袁永兵,等.叶下珠指纹图谱及模式识别研究[J].中草药,2015,46(4):572-575.
Study on HPLC Fingerprint of Miao Medicine Ardisia crenata
SUN Xu1,2,YAO Chengfen1,3,FU Sihong1,3,GONG Zaipeng1,LIU Ting1,YANG Chang1,ZHA Jun3,LI Yongjun(31.Guizhou Provincial Key Lab of Pharmaceutic Preparation,Guiyang 550004,China;2.School of Pharmacy,Guizhou Medical University,Guiyang 550004,China;3.Engineering Research Center for the Development and Application of Ethnic Medicine and TCM,Ministry of Education/National Engineering Research Center of Miao Medicines,Guiyang 550004,China)
OBJECTIVE:To establish HPLC fingerprints of Miao medicine Ardisia crenata.METHODS:HPLC method was adopted.The determination was performed on Diamonsil C18column with mobile phase consiste of methanol-water(gradient elution)at the flow rate of 1.0 mL/min.The detection wavelength was 220 nm,and column temperature was maintained at 30℃.The sample size was 10 μL.Using 11-O-(3,′4,′5′-three-o-galloylhyperin)-bergeninum as reference,HPLC fingerprints of 16 batches of samples were determined.Common identification and similarity evaluation were performed by using TCM Chromatographic Fingerprint Similarity Evaluation Software(2012 edition).Cluster analysis of fingerprrints was conducted.RESULTS:There were 6 common peaks in HPLC fingerprints of 16 batches of samples.The similarity among 8 batches was more than 0.9.The 16 batches of samples could be clustered into 4 categories.CONCLUSIONS:Established fingerprints can provide reference for identification and quality evaluation of A.crenata.
Ardisia crenata;HPLC;Fingerprint;Cluster analysis
R284
A
1001-0408(2017)30-4285-04
DOI10.6039/j.issn.1001-0408.2017.30.29
贵州省科技计划项目(No.黔科合平台人才〔2016〕5613、5677);贵州省教育厅项目(No.黔教合协同创新字〔2013〕04、黔科合KY字〔2013〕122、黔教研合ZYRC字〔2014〕012);贵州省优秀青年科技人才培养对象专项(No.黔科合人字〔2015〕11号)
*硕士研究生。研究方向:中药药效物质基础及质量控制。电话:0851-86908468。E-mail:928763710@qq.com
#通信作者:教授。研究方向:天然产物活性。电话:0851-86908468。E-mail:liyongjun026@126.com
2017-01-10
2017-02-18)
(编辑:张静)

