α′-AlH3的制备及形成研究
张 彦,唐 望,秦明娜,石 强,汪 伟,邱少君
(西安近代化学研究所,西安 710065)
2016-04-27;
2016-06-06。
张彦(1981—),女,博士,研究方向为含能材料。E-mailzhangyanenya@aliyun.com
α′-AlH3的制备及形成研究
张 彦,唐 望,秦明娜,石 强,汪 伟,邱少君
(西安近代化学研究所,西安 710065)
以LiAlH4和A1C13为原料,通过乙醚法制备了AlH3,采用扫描电子显微镜(SEM)和X射线粉末颜射(XRD),研究了制备条件对产物形貌、晶型的影响规律。结果表明,氢化铝醚合物高温脱醚时,混合溶剂中乙醚比例是影响AlH3晶型及形貌的主要因素,当结晶时,体系中乙醚不能及时除去,会导致α′-AlH3的形成,且AlH3形貌逐渐由立方体变成绒球状。伴生的α′型对AlH3室温存储稳定性及安全性有较大影响,α′型存在加快AlH3在室温下分解,且使得样品摩擦感度升高。
α′-AlH3;合成;晶型;固体推进剂
0 引言
α-三氢化铝(AlH3)的氢含量很高,质量分数可达10%,体积储氢密度(148 g H2/L)是液态氢的2倍,且放氢过程极为简单(2AlH3→ 2Al+3H2),是一种很有应用前景的储氢材料[1]。AlH3除可做储氢材料外,其相对于铝粉具有燃烧热更高、可产生气体等优点,也是一种很有潜力的高能推进剂添加剂。计算表明[2-3],在固体推进剂中使用AlH3代替铝粉,比冲可提高10 s;在固液推进剂中使用AlH3代替铝粉,比冲可提高32 s;在液体推进剂中添加AlH3,比冲可提高27 s。以AlH3、ADN和GAP组成的固体推进剂,其标准理论比冲可达294 s,比传统推进剂高20%~25%。此外,AlH3还可使固体推进剂的绝热火焰温度降低,对发动机热保护性能要求更小,从而提高装填系数,进一步提高发动机性能[2-3]。
α-AlH3是已知AlH3的7种晶型(α、α′、β、γ、ε、δ、ξ)中热稳定性最好的,而其他晶型热稳定性均比α型差,且室温下易缓慢分解。因此,α-AlH3是唯一在推进剂配方中有应用价值的晶型[1]。AlH3的合成方法众多,如有机金属法[4-5]、机械研磨法[6-7]、电化学法[8]、直接反应法[9-10]等,但目前文献报道,仅乙醚法能获得高纯度的α-AlH3,且产率高。所以,至今为止,α-AlH3仍采用此方法合成。此方法通过LiAlH4和AlCl3在乙醚中反应,然后高温除去络合的乙醚[4-5],得到AlH3。该合成方法简单,但对反应条件,如温度、时间等十分敏感,微小的变化都易导致其他晶型的生成。常见的伴生晶型主要有α′、β和γ型[4]。其中,对于β和γ型的形成研究较多,如添加LiA1H4易结晶形成
γ-AlH3,而同时添加LiA1H4和LiBH4易生成β-AlH3。β、γ这两种晶型均可通过温度升高和时间延长,最终转变成α-AlH3[4]。研究表明,α′型难以转化成α型[4],通常会在转化过程中发生分解。此外,伴生α′-AlH3存在,对于AlH3的性质有较大的影响[11],会导致AlH3的分解温度提前,室温下稳定性降低,还会影响AlH3感度,从而影响其应用安全性及安定性。虽然α′型对AlH3性质影响较大,但对α′型AlH3的形成原因研究较少。因此,有必要对α′型AlH3形成过程进行研究,以便对AlH3结晶过程有更全面认识。
本文以LiAlH4与AlCl3为原料,在乙醚中反应制备出AlH3醚合物,在甲苯中脱醚结晶获得AlH3,采用SEM、XRD对生成的AlH3进行表征,研究脱醚结晶过程中乙醚用量对AlH3晶型影响,并提出形成α′-AlH3晶型的过程。
1 试验
1.1 试剂与仪器
试剂:LiAlH4,分析纯,天津市北斗星精细化工有限公司;AlCl3,分析纯,东营坤宝化工有限责任公司;甲苯,分析纯,成都科龙试剂厂;无水乙醚,分析纯,成都科龙试剂厂。
仪器:日本理学公司Dmax-3A型X射线衍射仪;荷兰FEI公司Quanta 600型场发射扫描电子显微镜。
1.2 实验过程
(1)AlH3醚合物的制备
氩气保护下,将1.1 g LiAlH4与1.08 g AlCl3在70 ml无水乙醚中反应30 min,控制反应温度在-10~-5 ℃。然后,除去LiCl沉淀,得到上层清液,即AlH3醚合物溶液。
(2)AlH3制备
将上述所得AlH3醚合物迅速加入到200 ml的90 ℃甲苯溶液中,继续搅拌2 h后,停止加热,冷却至室温,过滤得白色固体。乙醚(3×30 ml)洗涤固体,再依次用去离子水洗涤,而后在40 ℃下真空干燥1 h,得灰白色粉末。
(3)不同晶型比例AlH3的制备
改变制备AlH3醚合物时溶剂乙醚(100 ml和40 ml)的用量,得到不同浓度AlH3醚合物溶液。AlH3制备条件与步骤(2)中相同,将所得AlH3醚合物加入甲苯溶液中,加热,搅拌,得到不同晶型比例的AlH3。
(4)样品表征
采用荷兰FEI公司Quanta 600型场发射扫描电子显微镜( SEM) ,对样品的表面形貌结构进行表征。XRD数据通过日本理学公司Dmax-3A型X射线衍射仪(Cu靶)进行测试得到。
(5)感度测试
撞击感度测试根据GJB 772A—97 方法601.1 进行,测试条件为落锤重5 kg,药量50 mg,落锤高度50 cm,撞击感度用爆炸概率P(%)表示。摩擦感度测试根据GJB 772A—97 方法602.1 进行,测试条件为表压3.92 MPa,摆角90°,药量20 mg,用爆炸率P(%)表示。
2 结果与讨论
2.1 AlH3的制备
图1(a)是制备得到的AlH3的XRD图。其中,标注实心方块的衍射峰为α-AlH3,空心方块的衍射峰为α′-AlH3。从XRD图上可看到产物晶型含有α和α′型,其中α′-AlH3含量为10.1%,没有出现分解产物Al。
图1(b)是AlH3产物的SEM图,AlH3晶体主要由立方体状的晶体和一些聚束状的晶体组成。许多研究表明,不同AlH3晶型都有独特的形貌,α-AlH3一般为立方体或六面体,γ-AlH3像针状的,α′-AlH3则像针垫或绒球状[4]。结合XRD图分析,块状的晶体是α-AlH3,而那些像绒球状的晶体则符合α′型AlH3的独特形貌。
图1(c)是放大后的立方晶体AlH3的SEM图。从图上可清晰观察到,在立方晶体上,还有一些针状晶体存在,这些针状的晶体可能是残存的γ型AlH3,由于量很少,衍射强度太小,没有在XRD图上观察到。这些针状晶体并不仅是附着在立方晶体上的,而是与立方晶体融合在一体的。因此,立方体α-AlH3可能是由这些针状晶体聚集、生长、转变而来的。
图1(d)是放大后集束状晶体AlH3的SEM图,这类集束状α′-AlH3晶体是由许多针状晶体聚集在一起构成,且它们与立方状的α-AlH3晶体生长在一起。因此,AlH3醚合物在高温下迅速脱醚后,AlH3晶体生长,部分转变成立方体α型AlH3,另一部分则无法转变,最终形成α′-AlH3。
2.2 乙醚含量对AlH3形貌和晶型的影响
当醚合物溶液中溶剂乙醚量增加至100 ml,制备的AlH3的SEM、XRD图分别见图2和图3。图2(a)为AlH3的SEM图,乙醚用量为100 ml;图2(b)为放大后的SEM图。图3(a)~(c)乙醚用量分别为100、70、40 ml。XRD结果表明,获得的AlH3依然为α型和α′型两种晶型,但其中α′-AlH3含量增加至51.3%,而α-AlH3则减少。从获得AlH3的SEM图上可见,随着乙醚含量的改变,AlH3形貌与图1(b)相比发生较大变化,其中立方体型α-AlH3明显减少,与XRD结果相符,且其形貌变为长条状。集束状α′-AlH3也消失,都变成5~20 μm的绒球状AlH3。
当醚合物溶液中溶剂乙醚量较少,制备的AlH3的SEM、XRD图分别见图4和图3。图4(a)为AlH3的SEM图,乙醚用量为40 ml;图4(b)为放大后的SEM图。XRD结果表明,随着乙醚含量减少,获得AlH3晶型基本为α型,而α′-AlH3的含量则很少,约为5.6%。此时,从SEM图上可见,AlH3形貌也大多为立方体型,几乎观察不到明显的α′-AlH3。从放大立方体晶体图(图4(b))上看到,立方体上及周边仍有少量针状晶体,与XRD结构结合分析,这种晶体应是α′-AlH3,可能是由于含量过少,而没有出现聚集生长情况。
2.3 α′-AlH3的形成过程分析
AlH3制备分为两个步骤,反应式如下:
3LiAlH4+AlCl3+4nEt2O→3LiCl+4AlH3·nEt2O
AlH3·nEt2O→AlH3+nEt2O
在醚合物制备时,乙醚虽作为反应物参与,但由于其含量大大过量,因此大量乙醚是作为溶剂溶解醚合物。且AlH3醚合物制备时,所用的原料量一致,可假设生成的AlH3醚合物量也一样。因此,在同样条件下脱醚结晶,是溶剂体系(乙醚-甲苯)的比例不同,导致获得不同α′-AlH3。
在混合溶剂(乙醚-甲苯)体系中,溶剂沸点随着乙醚含量的增加而不断下降。而脱醚过程需要能量才能实现,当乙醚含量增加,相同条件下脱醚时间增加长,相同时间内体系残留的乙醚也随着增加。乙醚作为溶剂影响脱醚速度,残留在脱醚体系中的AlH3乙醚络合物,相当于杂质影响AlH3的结晶,令脱醚后的AlH3无法转变成α型,只能生成相对稳定的α′-AlH3。脱醚慢生成α′-AlH3更稳定的比率可能更高。
结合SEM及XRD表征结果,AlH3的形成过程(如图5所示)为:当醚合物加入甲苯中,在温度作用下,脱去醚,生成AlH3并开始聚集生长,形成针状。但由于杂质乙醚在存在,针状晶体只能聚集生成相对稳定绒球状的α′-AlH3。当体系中乙醚从不断被蒸馏除去,针状晶体AlH3生长逐渐转变为更稳定的α型立方晶体。
2.4 伴生α′型对AlH3的影响
有研究表明[11-12],AlH3在室温下缓慢分解释放氢气。表1是制备的三种AlH3样品在室温下存放45 d分解情况。通过比较放置前后的氢含量变化表明,α′型存在导致AlH3的分解加快,α′型越多分解速度越快。其中,绒球状的AlH3室温下45 d分解率达到1.19%。
表2列出了制备的三种AlH3的撞击感度和摩擦感度测试结果。感度测试结果表明,所有的AlH3对撞击均为钝感,随着α′型AlH3含量增加,其撞击感度变化不明显。但α′型AlH3含量增加,相应的摩擦感度增加明显,与文献[11]观察结果类似。伴生的α′型AlH3绒球状,在受到外来摩擦力作用时,相比立方体的α型容易折断、破碎,从而导致AlH3分解。
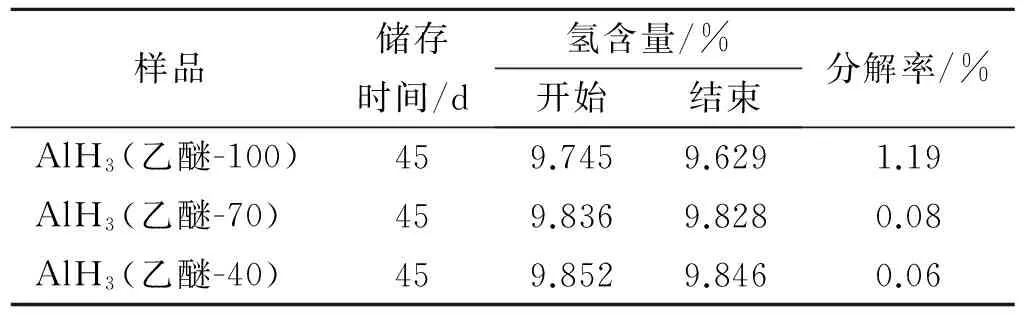
表1 室温储存AlH3中H元素含量变化

表2 AlH3的撞击感度和摩擦感度
3 结论
(1)以LiAlH4与AlCl3为原料在乙醚中反应制备出AlH3醚合物,在甲苯中脱醚结晶获得AlH3,通过改变醚合物溶液中乙醚的量,获得不同形貌及晶型含量比率不同的AlH3。
(2)乙醚是影响α′型AlH3形成的主要因素,当乙醚无法及时除去,其作为体系的杂质导致针状晶体无法转化成α型立方体,生成绒球状α′-AlH3。
(3)伴生α′型对AlH3室温存储稳定性及安全性有明显影响。α′型存在加快AlH3在室温下分解,且使得摩擦感度升高。
[1] Greztz J,Reilly J J,Yartys V A,et al.Aluminum hydride as a hydrogen and energy storage material:Past,present and future[J].J.Alloys Compd.,2011,509(2):517-528.
[2] 刘明星,何金选,曹一林.三氢化铝的合成及性能研究[J].固体火箭技术,2008,31(1):75-78.
[3] 张志国,何伟国,赵传富,等.三氢化铝制备工艺及稳定性研究进展[J].化学推进剂与高分子材料,2010,8(2):11-14.
[4] Brower F M,Matzek N E,Reigler P F,et al.Preparation and properties of aluminum hydride[J].J.Am.Chem.Soc.,1976,98(9):2450-2453.
[5] Bulychev B M,Verbetskii V N,Storozhenko P A.“Direct” synthesis of unsolvated aluminum hydride involving lewis and bronsted acids[J].Russ.J.Inorg.Chem.,2008,53(7):1081-1086.
[6] Sartori S,Istad-lem A,Brinks H W,et al.Mechanochemical synthesis of alane[J].Int.J.Hydrogen Energy,2009,34(15):6350-6356.
[7] Paskevicius M,Aheppard D A,Buckley C E.Characterisation of mechanochemically synthesised alane (AlH3) nanoparticles[J].J.Alloys Compd.,2009,487(1):370-376.
[8] Zidan R,Garcia-diaz B L,Fewox C S,et al.Aluminium hydride:A reversible material for hydrogen storage[J].Chem.Comm.,2009,40(25):3717-3719.
[9] Graetz J,Chaudhuri S,Wegrzyn J,et al.Direct and reversible synthesis of AlH3-triethylenediamine from Al and H2[J].J.Phys.Chem.C,2007,111(51):19148-19152.
[10] Appel M,Frankel J P.Production of aluminum hydride by hydrogen-ion bombardment[J].J.Chem.Phys.,1965,42(11):3984-3988.
[11] 朱朝阳,马煜,张素敏,等.杂质晶型对AlH3样品稳定性和安全性影响的研究[J].含能材料,2011,19(6):637-640.
[12] Graetz J,Reilly J J.Thermodynamics of theα,βandγpolymorphs of AlH3[J].J.Alloys Compd.,2006,424(1-2):262-265.
Preparationofα′-AlH3anditscrystallizationprocess
ZHANG Yan,TANG Wang,QIN Ming-na,SHI Qiang,WANG Wei,QIU Shao jun
(Xi’an Modern Chemistry Research Institute, Xi’an 710065,China)
AlH3was prepared in ether using LiAlH4and A1C13as the starting materials.The crystallization of non-solvated AlH3from the solvent was studied by X-ray diffraction(XRD)and Scanning electron microscopy(SEM).Ether plays an important role in the crystallization and formation ofα′-AlH3in terms of morphology and phase fraction.If ether were not removed from the crystallization system on time,it became an impurity,leading to formation ofα′-AlH3.Furthermore,the effects ofα′-AlH3on the thermal stability and sensitivity of AlH3were studied.The presence ofα′-AlH3could increase the decomposition rate and friction sensitivity of AlH3.
α′-AlH3;synthesis;polymophs;solid propellant
V512
A
1006-2793(2017)05-0605-04
10.7673/j.issn.1006-2793.2017.05.013
(编辑:崔贤彬)

