基于均相氧催化反应的锂空气电池研究进展
朱允广, 王 庆
(新加坡国立大学材料科学与工程系,新家坡 117579)
特约专栏
2017-07-06
新加坡国立研究基金会(NRF-CRP10-2012-06)
朱允广,男,1987年生,博士研究生
王 庆,男,1975年生,副教授,博士生导师,Email: qing.wang@nus.edu.sg
10.7502/j.issn.1674-3962.2017.10.01
基于均相氧催化反应的锂空气电池研究进展
朱允广, 王 庆
(新加坡国立大学材料科学与工程系,新家坡 117579)
由于高的理论能量密度,锂空气电池被看作最有前景的能源存储系统之一。但是,目前仍有许多因素制约着它的发展,比如大的极化电压、电解液和空气电极的不稳定性,以及由此带来的差的循环稳定性等。此前,研究人员重点研究了各种固态电催化剂来解决上述问题。但由于固态催化剂自身的特性,它并不能解决空气电极的表面钝化以及孔隙的堵塞问题,因此人们开始转向均相催化剂。从金属空气电池的结构来看,由于正极的有效空间有限,即使均相催化剂也不能从根本上解决正极的钝化和堵塞问题。因此,本课题组设计了一种新的锂空气电池装置——氧化还原液流锂空气电池,来彻底解决上述的两个问题。在此文最后,将根据目前基础研究和实际应用之间的差距,简要讨论未来锂空气电池的发展。
锂空气电池;均相催化剂;氧化还原靶向反应;高能量密度;高功率密度;锂空气氧化还原液流电池
1 前 言
作为一种先进的化学电源,锂离子电池虽然在便携电子、电动汽车、以及大型储能方面都发挥着重要作用。但是基于锂离子在电极材料中的可逆脱嵌反应这一工作原理,已经难以满足对能量密度的日益增长的需求[1,2]。因此,寻找更优越的电池化学体系变得越来越重要。锂空气电池,由于其能量密度比锂离子电池高5~10倍,在过去几年受到了广泛的关注[3]。
在各种锂空气电池体系中,研究最多的是基于非水电解质的电池体系。如图1所示,非水系的锂空气电池包含金属锂阳极、隔膜、空气电极(阴极)、以及电解液。在放电过程中,金属锂在阳极氧化,同时氧气在空气电极中还原生成Li2O2。Li2O2在多数有机电解液中的溶解度很低,并且是一个绝缘体。随着Li2O2在空气电极上的累积,电极发生钝化;同时氧气和锂离子的传输通道逐渐被堵塞,这导致放电过程的提前结束[4,5]。在充电过程中,Li2O2在电极上氧化,并析出氧气;同时金属锂在对电极沉积出来。

图1 基于非水电解质的锂空气电池结构及工作原理示意图Fig.1 Diagram of aprotic lithium oxygen battery and its working mechanism
作为未来一种高能量密度的电池体系,锂空气电池的发展目前还面临着许多的基础科学问题需要解决。其中由于氧还原反应(ORR)和氧析出反应(OER)的动力学限制,锂空气电池通常表现出较大的极化电压(> 1 V)和较低的能量效率。因此,研究人员利用各种电催化剂,比如碳基材料、贵金属、金属氧化物等,来修饰空气电极以减少极化现象[6]。但这些固体的电催化剂无法阻止电极的表面钝化和孔隙堵塞问题,这在深度放电的状态下尤其严重。因此研究人员开始关注液相催化剂-氧化还原介质,来降低极化电压,同时缓解电极钝化和堵塞的问题[7-9]。但从电池的结构来看,即使使用液相催化剂,锂空气电池的容量仍然受限于空气电极的孔隙体积。因此,本课题组把液相催化剂和液流系统结合在一起,将Li2O2的生成和分解从空气电极转移到气体扩散罐中,从而彻底地解决了电极的钝化和堵塞问题,得到更加稳定的锂空气电池系统[10,11]。
2 固体电催化剂在锂空气电池中的应用
在过去的十年中,锂空气电池的研究主要集中在电催化材料和空气电极结构的发展上,以促进电池的反应动力学从而减少极化电压以及提高电池的循环稳定性。
碳基材料是一种普遍用于空气电极的材料,主要包含一维(如碳纳米管、碳纤维)、二维(如石墨烯)、三维碳材料(多孔碳)[12-14]。除了改善材料的形貌和结构外,人们还通过氮、硼、磷、或硫等的掺杂来提高缺陷和边界位点,以提高碳材料的催化性能[15]。虽然碳材料在锂空气电池的应用中有诸多优点,但其高电压下的不稳定性会产生副产物,导致电池的稳定性变差[16]。与碳基材料相比,贵金属催化剂往往具有更高的催化活性和稳定性,因此一直受到研究人员的关注[17]。以Pt/Au纳米颗粒为例,Au和Pt纳米颗粒可以在ORR和OER过程中分别起到很好的催化效果。电池的放电和充电平台分别可以稳定在2.7 V 和3.6 V。但这种良好的电池性能只限于大约1200 mAh/gcarbon的放电容量。同时由于空气电极碳材料的负载量很小,电池的绝对放电容量其实非常有限。另外,从锂空气电池应用的角度来看,昂贵的贵金属催化剂并不适合大规模的应用。研究人员还发现,虽然贵金属自身比较稳定,但其高的催化活性也造成电解液的分解,从而对锂空气电池造成损害[18]。价格低廉、催化活性良好的金属氧化物,在锂空气电池领域一直受到研究人员的重视。例如,二氧化锰,由于其双向催化活性,被广泛地用于空气电极上[19-22]。除了金属氧化物, 其它一些金属化合物在空气电极上也有比较多的研究,比如TiC、TiN、MoS2、Mo2C等[23-26]。
虽然研究人员发展了很多固态催化剂,但是放电产物在空气电极的累积造成的表面钝化和孔隙堵塞问题仍然无法解决。因此,近年来一些研究小组开始转向液相催化剂—氧化还原介质,来解决上述问题。
3 液相催化剂在锂空气电池中的应用


图2 均相催化剂在锂空气电池中的工作原理示意图Fig.2 Working principle of homogenous catalysts in lithium oxygen battery
2012年,研究人员第一次在专利中提出了将氧化还原介质用在金属空气电池中[7],并报道了一系列有潜力的液相氧析出催化剂,在充电时用于分解电池的放电产物。此后,多种液相氧析出催化剂相继被应用在锂空气电池中,并取得了不错的电池性能,比如TTF、LiI、TEMPO、FePc等[8,27-29]。为了提高锂空气电池的放电容量,氧还原催化剂也逐渐受到人们的关注。Owen研究组[9]最早报道了Ethyl Viologen (EV)在锂空气电池中的应用。他们研究了EV对电池中超氧根离子的影响,并认为其能缩短超氧根离子的寿命而增加电池的稳定性。最近,Bruce研究组[30]在锂空气电池中使用2,5-di-tertbutyl-1,4-benzoquinone(DBBQ),发现电池容量有了80~100倍的提升。该组指出,Li2O2在空气电极一侧的产量可以达到10 mg/cm2,这相当于11.6 mAh/cm2的放电容量。但由于受空气电极有效体积的限制,这个单位面积的容量仍然无法同现有的锂离子电池相比。另外,该组认为DBBQ在溶液中与超氧根形成LiDBBQ-O2中间体,能够稳定超氧根离子从而达到稳定电解液以及电极的效果。这对电池循环稳定性的提高是一个很大的促进。
虽然从固态电催化剂转向液相催化剂能有效地提升锂空气电池的性能,但是相关研究仍存在一定争议。首先,液相催化剂的“穿梭效应”在金属锂电极上发生副反应,会极大地降低电池的库仑效率。为了减少穿梭效应的影响,人们应该使用锂离子固态电解质或者锂离子导电聚合物膜[10,31-34];其次,由于液相催化剂是一种具有电化学活性的分子材料, 其本身同样可以提供一定的电化学容量。因此,在分析液相催化剂的催化性能时,应通过氧消耗和氧析出的数据正确计算由氧气参与反应提供的容量[35]。本课题组注意到,当使用液相催化剂时,多数研究工作仍然以固相催化剂的质量来计算比容量,而这并不能准确地反映液相催化的效果。另外,更细节的电解液信息能够帮助其他研究人员更准确地评估液相催化剂的活性,比如电解液的体积、液相催化剂的浓度等;最后,液相催化剂的稳定性是一个重要指标。很多液相催化剂是有机分子,在苛刻的空气环境下,很难保证其结构的稳定性,电池的性能随着工作时间的增加而衰减。
液相催化剂在锂空气电池中的反应过程是非常复杂的。在不同的电池条件下,锂空气电池的电极反应以及放电产物会有比较大的差别[36,37]。下面以LiI在锂空气电池中的应用为例来说明这个复杂的过程。2014年,LiI就已经在锂空气电池中有了应用[27]。该报道指出对于放电产物Li2O2, I3-是一个非常有效的催化剂。随后,本课题组将LiI用在液流锂空气电池中,却发现了不同的充电现象:在干燥的电解液中,I3-与Li2O2的反应是很慢的;通过第一性原理计算,相比I3-,Li2O2更容易与I2发生反应。2015年,Grey研究组[38]报道了在微量水存在的情况下,I3-在充电时能促使LiOH的分解,并得到了非常优越的电池性能。但一般认为,LiOH属于非常稳定的化合物,在热力学上I3-并不能氧化LiOH, 这个结果因而引起了比较大的争议。本课题组随后进行了系统的研究, 发现有机电解液中的微量水或者质子能促进一个新的化合物—LiOOH的生成。而LiOOH与I3-的反应活性远大于其它锂的化合物(Li2O2, LiOH等)[33]。随后,其他研究小组也报道了关于OOH-以及I2在锂空气电池中的类似研究结果[39-43]。
虽然液相催化剂成为了锂空气电池的一个重要研究方向,但是根据目前的电池结构,空气电极钝化和孔隙堵塞在电池深度放电条件下仍然无法避免。因此,基于上述问题,本课题组结合液相催化剂和液流电池的结构,设计了能彻底解决以上问题的液流锂空气电池装置。
4 氧化还原液流锂空气电池
如图3所示,氧化还原液流锂空气电池(Redox Flow Lithium Oxygen Battery, RFLOB)通过液流系统将氧化还原介质在电池正极和氧气环境的气体扩散罐(GDT)之间循环流动。这个设计可以将Li2O2产生和分解的反应位点与正极分开,从而从根本上解决空气电极钝化和孔隙堵塞的问题。
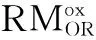
放电过程:

(1)

(2)
充电过程:
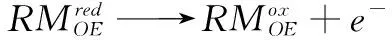
(3)
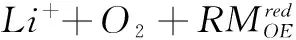
(4)

图3 氧化还原锂空气液流电池的结构和工作原理示意图。右下角为运行中的氧化还原锂空气液流电池的照片[10]Fig.3 Structure and working principle of redox flow lithium oxygen battery (RFLOB). The photo at the bottom right corner is RFLOB[10]
与传统的锂空气电池相比,RFLOB对正极的要求相对较低。在传统锂空气电池中,正极除了要具备较高的电子电导和优化的孔隙结构外,还要有高的催化活性来促进ORR和OER过程,以及好的化学稳定性来抵抗超氧根的氧化。但在RFLOB中,正极与传统的液流电池一样,主要提供电解液中的氧化还原介质发生电化学反应的场所。因此,RFLOB能极大地降低电极成本并得到更高的能量密度。从目前的研究来看,RFLOB的面积比容量不受限于阴极。在充分利用负极金属锂的条件下,其单位面积的放电容量可以达到锂金属在负极担载量的上限[10]。同时,由于电极极化的减小,RFLOB有希望能达到一个较高的放电功率密度,从而进一步加快锂空气电池应用的步伐。
但相比传统锂空气电池,RFLOB对隔膜的要求比较高。如前面所述,当使用液相催化剂时,电池隔膜往往只能选择锂离子固态电解质或者锂离子导电聚合物膜[10,31-34]。从未来发展看,由于这个隔膜能阻止空气中的氧气、二氧化碳以及水蒸气对锂金属负极的腐蚀,高电导的锂离子固态电解质或者锂离子导电聚合物膜对传统锂空气电池也是必要的。
5 结 语
从非水系锂空气电池概念的提出,到现在已有二十多年,但仍然有许多基础的科学问题需要解决。
首先,从锂空气电池的反应以及工作原理来看,目前空气电极的设计仍然无法解决长期循环稳定性,电极钝化和孔隙堵塞的问题。通过引入液相催化剂可以在一定程度上缓解上述问题。但由于电池的放电产物仍然沉积在空气电极中,电池正极的传质以及放电深度最终会受到限制。因此实现高的能量密度仍然需要优化甚至改变正极的结构以提高放电深度。从这个角度来看,在大规模储能的应用上RFLOB是一种可供选择的方案。
其次,锂金属负极的循环稳定性一直以来是锂二次电池需要解决的一个重要问题,这在锂空气电池中尤其突出。一方面,锂金属具有很强的活性,极易被来自空气中的氧气、二氧化碳及水蒸气等腐蚀。因此,设计选择性优越的隔膜是一个重要的解决途径。另一方面,锂金属在多次充放电过程中容易产生枝晶并在表面形成固体电解质界面膜(SEI)。枝晶容易刺破隔膜造成电池短路,从而带来安全问题。而SEI膜则会造成锂金属的不可逆消耗,增加电池内阻,而带来能量损失。
最后,锂空气电池虽然已经研究和发展了20多年,该电池体系的比容量仍然没有统一的标准[44]。用基于脱嵌反应的锂离子电池的方法来计算锂空气电池的比容量是没有实际意义的。因此,对于锂空气电池的评估应该考虑空气电极的整体质量和体积。而对于使用氧化还原媒介的电池还应考虑其添加量以及贡献的容量,这才能更清楚地评估器件的性能以及应用的前景。
虽然锂空气电池仍然存在许多问题,但作为目前理论能量密度最高的储能器件仍然是未来发展的一个重要方向。而作为一种新的锂空气电池的设计方案,本课题组希望氧化还原液流锂空气电池能为研究人员提供一种新的研究思路。
References
[1] Aurbach D, McCloskey B D, Nazar L F,etal.NatureEnergy[J], 2016, 1: 16128.
[2] Grande L, Paillard E, Hassoun J,etal.AdvancedMaterials[J], 2015, 27 (5): 784-800.
[3] Abraham K M.TheJournalofPhysicalChemistryLetters[J], 2015, 6 (5): 830-844.
[4] Radin M D, Monroe C W, Siegel D J.TheJournalofPhysicalChemistryLetters[J], 2015, 6 (15): 3017-3022.
[5] Højberg J, McCloskey B D, Hjelm J,etal.ACSAppliedMaterials&Interfaces[J], 2015, 7 (7): 4039-4047.
[6] Imanishi N, Luntz A C, Bruce P.TheLithiumAirBattery:Fundamentals[M]. New York: Springer, 2014:86-89.
[7] Chase G V, Zecevic S, Wesley W T,etal. US,20,120,028,137: 2012[P].
[8] Chen Y, Freunberger S A, Peng Z,etal.NatureChemistry[J], 2013,5 (6): 489-494.
[9] Lacey M J, Frith J T, Owen J R.ElectrochemistryCommunications[J], 2013, 26: 74-76.
[10] Zhu Y G, Jia C, Yang J,etal.ChemicalCommunications[J], 2015, 51 (46): 9451-9454.
[11] Zhu Y G, Wang X, Jia C,etal.ACSCatalysis[J], 2016, 6(9): 6191-6197.
[12] Mitchell R R, Gallant B M, Thompson C V,etal.Energy&EnvironmentalScience[J], 2011, 4 (8): 2952-2958.
[13] Lim H D, Park K Y, Song H,etal.AdvancedMaterials[J], 2013, 25 (9): 1348-1352.
[14] Li Y, Wang J, Li X,etal.ChemicalCommunications[J], 2011, 47 (33): 9438-9440.
[15] Wang Z L, Xu D, Xu J J,etal.ChemicalSocietyReviews[J], 2014, 43 (22): 7746-7786.
[16] Ottakam Thotiyl M M, Freunberger S A, Peng Z,etal.JournaloftheAmericanChemicalSociety[J], 2012, 135 (1): 494-500.
[17] Lu Y C, Xu Z, Gasteiger H A,etal.JournaloftheAmericanChemicalSociety[J], 2010, 132 (35), 12170-12171.
[18] Freunberger S A, Chen Y, Peng Z,etal.JournaloftheAmericanChemicalSociety[J], 2011, 133 (20): 8040-8047.
[20] Mao L, Sotomura T, Nakatsu K,etal.JournaloftheElectrochemicalSociety[J], 2002, 149 (4): A504-A507.
[21] Cheng F, Shen J, Ji W,etal.ACSAppliedMaterials&Interfaces[J], 2009, 1(2): 460-466.
[22] Pickrahn K L, Park S W, Gorlin Y,etal.AdvancedEnergyMaterials[J], 2012, 2 (10): 1269-1277.
[23] Ottakam Thotiyl M M, Freunberger S A, Peng Z,etal.NatureMaterials[J], 2013, 12 (11): 1050-1056.
[24] Li F, Ohnishi R, Yamada Y,etal.ChemicalCommunications[J], 2013, 49 (12): 1175-1177.
[25] Asadi M, Kumar B, Liu C,etal.ACSNano[J], 2016, 10 (2): 2167-2175.
[26] Kundu D, Black R, Adams B,etal.TheJournalofPhysicalChemistryLetters[J], 2015, 6 (12): 2252-2258.
[27] Lim H D, Song H, Kim J,etal.AngewandteChemieInternationalEdition[J], 2014, 53 (15): 3926-3931.
[28] Bergner B J, Schürmann A, Peppler K,etal.JournaloftheAmericanChemicalSociety[J], 2014, 136 (42): 15054-15064.
[29] Sun D, Shen Y, Zhang W,etal.JournaloftheAmericanChemicalSociety[J], 2014, 136 (25): 8941-8946.
[30] Gao X, Chen Y, Johnson L,etal.NatureMaterials[J], 2016, 15 (8): 882-888.
[31] Jia C, Pan F, Zhu Y G,etal.ScienceAdvances[J], 2015, 1 (10): e1500886.
[32] Bergner B J, Busche M R, Pinedo R,etal.ACSAppliedMaterials&Interfaces[J], 2016, 8 (12): 7756-7765.
[33] Zhu Y G, Liu Q, Rong Y,etal.NatureCommunications[J], 2017, 8: 14308.
[34] Gao X, Chen Y, Johnson L R,etal.NatureEnergy[J], 2017, 2: 17118.
[35] Pande V, Viswanathan V.ACSEnergyLetters[J], 2016, 2(1): 60.
[36] Viswanathan V, Pande V, Abraham K M,etal.Science[J], 2016, 352: 667.
[37] Kwak W J, Hirshberg D, Sharon D,etal.JournalofMaterialsChemistryA[J], 2015, 3: 8855-8864.
[38] Liu T, Kim G, Carretero-González J,etal.Science[J], 2016, 352: 667.
[39] Zhang W, Shen Y, Sun D,etal.NanoEnergy[J], 2016, 30: 43-51.
[40] Qiao Y, Wu S, Yi J,etal.AngewandteChemieInternationalEdition[J], 2017, 56 (18): 4960-4964.
[41] Wu S, Qiao Y, Yang S,etal.NatureCommunications[J], 2017, 8: 15607.
[42] Tulodziecki M, Leverick G M, Amanchukwu C V,etal.Energy&EnvironmentalScience[J], 2017, 10:1828.
[43] Qiao Y, Wu S, Sun Y,etal.ACSEnergyLetters[J], 2017, 2(8): 1869.
[44] Freunberger S A.NatureEnergy[J], 2017, 2: 1709.
Research Progress of Lithium Oxygen Batteries Based on Redox Catalysis
ZHU Yunguang, WANG Qing
(Department of Materials Science and Engineering, Faculty of Engineering, National University of Singapore, 117576, Singapore)
Lithium oxygen battery is considered as one of the most promising energy storage systems due to its high theoretical energy density. However, its development is severely hindered by the large overpotentials and poor cycling stability. Efforts have previously been taken on the development of various types of heterogeneous electrocatalysts to enhance the electrode reactions. However, issues pertaining to surface passivation and pore clogging of the cathode remain. Homogenous catalysis with soluble redox mediators thus comes to the attention. While effective in addressing the surface passivation issue, pore clogging problem remains unsolved due to the limited space in the cathode. Therefore, redox flow lithium oxygen battery was proposed by introducing a gas diffusion tank, which elegantly overcomes these hurdles. Lastly, the gap between present research work and practical applications, as well as future development of lithium oxygen battery is briefly discussed.
lithium oxygen battery; homogeneous catalyst; redox targeting reaction; high energy density; redox flow lithium oxygen battery
TM911.41
A
1674-3962(2017)10-0689-05
(编辑 吴 琛)

