淀粉纳米微粒的分散性研究
吴修利,郭春香,姜雪,段蕾,余俊敏
(长春大学食品科学与工程学院,吉林长春130012)
实验研究
淀粉纳米微粒的分散性研究
吴修利,郭春香,姜雪,段蕾,余俊敏
(长春大学食品科学与工程学院,吉林长春130012)
本文对淀粉纳米微粒的分散性能进行了研究。试验考察了超声时间、溶剂类型、溶液pH值和离子强度四个因素。试验表明:最佳超声分散时间为10min;淀粉纳米微粒分散在DMSO、去离子水和生理盐水中稳定性逐渐降低;在溶液pH值为酸性及弱碱性条件下,纳米粒子更为稳定;低离子强度下,粒径尺寸变化较小,提高NaCl水溶液浓度,淀粉纳米微粒粒径会迅速增加。
淀粉纳米微粒;分散性;稳定性
近年来,纳米微粒的研究备受瞩目。由于其具有小尺寸效应,溶解度高等优势,被广泛应用生物科技领域和污染控制、聚合材料合成等方面[1,2]。但因纳米微粒具有极大的比表面积效应和较高的表面能特点,在实际应用过程中极易形成二次粒子团聚,粒子尺寸增大甚至使纳米微粒失去所具备的功能。同时,纳米微粒的分散性也会对纳米复合材料的性能带来巨大的影响[3]。因此研究纳米微粒在液相介质中的分散性和稳定性显得尤为重要。
本试验对淀粉纳米微粒的分散性和稳定性进行了研究,考察了超声时间、溶剂类型、溶液p H值和离子强度等因素的影响,为纳米微粒在不同领域的进一步应用提供理论基础。
1 材料与方法
1.1 材料试剂与仪器
试验材料与试剂:玉米淀粉(长春大成玉米淀粉有限公司);二甲基亚砜(分析纯,北京化工厂);乙醇(分析纯,北京化工厂)。
主要仪器:高功率数控超声波清洗器(K Q-600K DE昆山市超声仪器有限公司);纳米粒径电位分析仪(N ano-Z S90英国马尔文公司)。
1.2 淀粉纳米微粒制备[4]
浓度10g/L淀粉二甲基亚砜溶液在沸水浴中保温1h,然后用一次性注射器(内径0.30mm×8mm)吸取1m L溶液,在磁力搅拌下,逐滴加入20m L乙醇中,而后离心去上清液,用乙醇洗涤三次,备用。
2 结果与分析
作为动力学稳定性的高分散系统来说,淀粉纳米微粒分散液的稳定性会受p H值和电解质浓度的影响,某些物理条件的改变还可能发生聚沉作用出现沉淀。超声可有效降低介质中由于表面活性产生粒子团聚的现象。本研究探讨超声时间、不同溶剂、p H值和离子强度四个主要影响因素。
2.1 淀粉纳米微粒在溶液中的状态

图1 玉米淀粉水溶液(A),淀粉-DMSO糊液(B)和淀粉纳米粒子水溶液(C)照片
图1为室温条件下玉米淀粉水溶液(A)、玉米淀粉——二甲基亚砜(D M S O)糊液(B)和玉米淀粉纳米微粒水溶液(C)静止不同时间的溶液分散状态。
由图1可以看出原淀粉水溶液静止后极易形成明显的分层,淀粉沉积在底部;淀粉-D M S O糊液变得澄清透明;淀粉纳米微粒水溶液成为带有蓝色乳光的浊液。
原淀粉不溶于冷水且微粒比重大于水,而出现分层。D M S O可扩散到淀粉基质中,破坏淀粉分子间或分子内的氢键,导致淀粉链慢慢伸展,在搅拌作用下形成均匀澄清淀粉糊液。淀粉纳米微粒可以分散在水溶液中形成稳定的胶体粒子,呈现带有蓝色乳光的浊液。
2.2 超声时间对淀粉纳米微粒水溶液分散性的影响
将新制备的淀粉纳米微粒溶于去离子水中制备成0.1%的水溶液,超声时间对粒子分散性的影响,如图2(A,B)所示。
如图2(A)所示,淀粉纳米微粒在水溶液中粒径的尺寸随超声时间的延长逐渐变小,当超声时间超过10m in后,粒径变化不明显;由图2(B)可知,峰宽随着超声时间的增加而变窄,而峰的强度逐渐增高,并且粒径分布曲线逐渐向小尺寸粒子方向移动,显然在超声场的作用下,粒子间软团聚的大微粒被分散成小粒子。

图2 (A)超声时间对淀粉纳米颗粒水溶液粒径和粒度分布的影响图 2(B)中 1-5超声时间分别为 3m in,5m in,8m in,10m in,20m in
2.3 不同溶液中的淀粉纳米微粒的分散性
淀粉纳米微粒在溶液的分散性对实际应用十分重要。在室温条件下,以去离子水、D M S O、生理盐水为溶剂将淀粉纳米微粒分别配制成0.1%的溶液,粒径分布曲线,如图3。
由图3可知,淀粉纳米微粒分散在三种不同溶剂中时,有两个峰出现在40n m和250n m附近,还有一处弱峰出现在5μm处。溶解分散在D M S O中的淀粉纳米微粒具有最小的粒径尺寸(200.4±5.672n m),峰宽相对较窄,PD I指数为 0.403±0.044,其次是生理盐水和去离子水。
由图4可知,将上述三种淀粉纳米微粒悬浮液通过0.45μm孔径的水膜对或有机膜进行进一步过滤处理,并比较过滤前后分布曲线。分析可知,位于5μm处的峰在过滤后消失,证实了聚集的微粒或灰尘等大粒子被滤除。而250n m左右的峰值向左侧出现左移,说明滤后悬浮液的平均粒径变小。相对于250n m位置峰强度的增加,40n m处的峰强基本没有变化。C hak r a b o rt y等[5]认为250n m附近的峰是由于悬浮液中粒子动态聚集所形成的,并通过实验进一步加以证实。而40n m处形成峰则被学者认为是淀粉微观结构中孤立的小体结构(b l o c k l e t s)[6]。

图3 淀粉纳米颗粒在去离子水(A)、生理盐水(B)和DMSO(C)中粒度分布
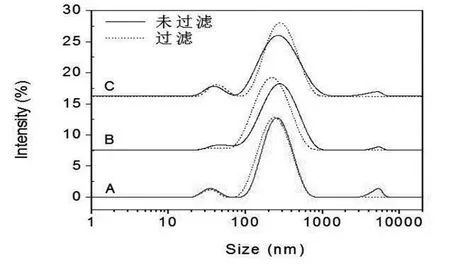
图4 淀粉纳米颗粒在去离子水(A)、生理盐水(B)和DMSO(C)中过滤前后粒度分布

图5 不同pH分散液对淀粉纳米颗粒电位(A)和粒径(B)的影响
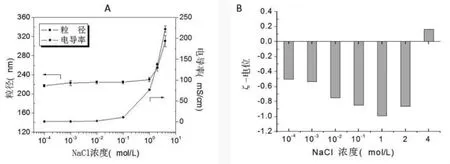
图6 不同浓度NaCl溶液对淀粉纳米颗粒粒径及电位的影响
2.4 pH值对淀粉纳米微粒溶液稳定特性的影响
将新制备的淀粉纳米微粒溶于用0.1M的盐酸或0.1M的N a OH调节出的不同p H值水溶液中,制备粒子浓度为0.1%的不同溶液,采用超声分散,而后比较淀粉纳米微粒水溶液在不同p H值条件下的粒径变化和电位变化,试验结果如图5。
分散液中粒子的稳定性可通过测定溶液的ζ-电位进行分析。一般而言,溶液越稳定,测得的ζ-电位绝对值也越大。如图5(A),调节溶液的p H值从1.42上升到11.12的过程中,ζ-电位从-0.479mv下降至-5.43mv,且在p H值≤7时,ζ-电位变化较平缓,可能因为在酸性及中性条件下,淀粉纳米粒子表面带电荷量较少,粒子外双电层的厚度较小,ζ-电位趋于0。热力学表明,当电位接近于0时,静电排斥力与范德华引力相比较小,粒子分散性差粒子易发生聚集或相分离。当p H>7时,淀粉分子表面的一定羟基解离,吸引更多的异电离子,静电排斥力大于范德华引力,所以纳米粒子分散更好[7]。从图5(B)可知,在酸性及弱碱性条件下,即p H小于7.74的时候,纳米微粒的粒径变化甚小,与图5(A)的结果保持一致。在碱性条件下,即p H值大于9.12的时候,粒径有很明显的改变,同时粒径数据精密度相对较差,可能是在碱性条件的淀粉分子链,因为淀粉纳米微粒氢键的破坏而重新伸展、缠绕或者形成桥联结构,因此粒径有较大的变化。2.5盐溶液浓度对纳米微粒分散性的影响
以不同浓度氯化钠盐溶液为溶剂,将淀粉纳米微粒制备成0.1%浓度的溶液,后经由超声分散,分析讨论纳米微粒粒径和电位受盐溶液的浓度变化的影响程度。纳米颗粒会因为电解质电解产生的离子具有选择性吸附的特性而带上正、负电荷,因此在布朗运动中相互排斥避免聚沉现象产生。如图6(A)曲线变化可知,与无盐溶液相比较(215n m),随氯化钠盐溶液浓度从10-4 M增至1M时,纳米微粒尺寸变化不大,由217 n m至230 n m区间,也只对应7%的增加,因此证明盐溶液中的粒子相对稳定。然而当氯化钠盐溶液的浓度从1M上升到4M时,微粒粒径达到了310n m,变化速度非常快。盐溶液中微粒的聚集现象时微粒尺寸变化的主要原因。可知高浓度盐溶液情况下粒子发生聚集现象,而没有在研究区域看到沉淀,是由于纳米粒子的进一步聚集沉淀由于外围亲水层厚度而被阻止[8],由图6(B)可知,氯化钠盐溶液的浓度对纳米微粒ζ-电位的影响。向去离子水中加入新制备的淀粉纳米微粒测得ζ-电位基本趋近于0,然而,以不同浓度盐溶液为溶剂的样品则都测得为负值(除4M外),证明此时在盐溶液中分散的纳米粒子的表面带负电荷。当氯化钠盐溶液的浓度从10-4M增加到1M时,纳米微粒盐溶液分散液的ζ-电位从-0.504mv较小至-0.991mv。
3 结论
本文研究了超声时间、溶剂类型、溶液p H值和离子强度四个因素对纳米微粒溶液分散性和稳定性的影响。当超声时间达到10m in后,粒子即可达到一个很好的分散状态;当淀粉纳米微粒分散于不同溶剂中,其稳定的次序为D M S O>去离子水>生理盐水;在酸性及弱碱性条件下,颗粒尺寸变化较小,而当碱性条件下,粒子尺寸变化较明显;在高离子强度下粒子会发生一定程度的聚集,颗粒尺寸会迅速增加。
[1]Hui X,Smith J W.Fabrication of PLGA nanoparticles with a fluidic nanoprecipitation system[J].Journal of Nanobiotechnology,2010,8(01):18.
[2]Bukhari A,Idris A,Atta M.Effect of organic and aqueous dispersion medium on the development of polystyrene nanoparticles in nanoprecipitation method[J].2012,10(3-4):28-32.
[3]付翔.定量评价纳米粒子在基体中的分散性[D].浙江理工大学,2014.
[4]Wu,Xiuli,Chang,Yanjiao,Fu,Youjia,et al.Effects of nonsolvent and starch solution on formation of starch nanoparticles by nanoprecipitation[J].Starch-St?rke,2016,68(3-4):258-263.
[5]Kakran M,Sahoo N G,Li L,et al.Fabrication of quercetin nanoparticles by anti-solvent precipitation method for enhanced dissolution[J].Powder Technology,2012,223(06):59-64.
[6]Kim H Y,Ju H L,Kim J Y,et al.Characterization of nanoparticles prepared by acid hydrolysis of various starches[J].Starch-St rke,2012,64(05):367-373.
[7]Stojanovic′Z P,Jeremic′K,Jovanovic′S,et al.Light scattering and viscosity investigation of dilute aqueous solutions of carboxymethylstarch.[J].Starch - St?rke,2010,61(3-4):199-205.
[8]Tan Y,Xu K,Niu C,et al.Triglyceride-water emulsions stabilised by starch-based nanoparticles[J].Food Hydrocolloids,2014,36(02):70-75.
TS236;TB383
A
10.14025/j.cnki.jlny.2017.21.022
吉教科合字〔2016〕第301号;长春大学国家级科研项目培育项目(2016 JBC26L26)
吴修利,博士,副教授,研究方向:淀粉及淀粉衍生物。

