合金元素对铸造Fe-Cr铁素体不锈钢耐浓硫酸腐蚀性能的影响
,,
(浙江省宣达耐腐蚀特种金属材料研究院,永嘉 325105)
合金元素对铸造Fe-Cr铁素体不锈钢耐浓硫酸腐蚀性能的影响
欧阳明辉,刘焕安,叶际宣
(浙江省宣达耐腐蚀特种金属材料研究院,永嘉325105)
采用电化学技术、浸泡腐蚀及能谱分析等研究了合金元素对铸造Fe-Cr铁素体不锈钢耐浓硫酸腐蚀行为的影响。结果表明:随铬含量的增加,Fe-Cr合金的耐浓硫酸腐蚀性能增强,单一的铬合金化不能使Fe-Cr合金在60 ℃,98% H2SO4中自钝化;钼能促进Fe-Cr25-Mo合金的钝化和自钝化,随钼含量的增加,Fe-Cr25-Mo合金的耐浓硫酸腐蚀性能增强;辅助合金元素镍、铜可促进Fe-Cr25Mo2合金的钝化和自钝化,而钛、铌的影响不大。
铁素体不锈钢;浓硫酸;电化学技术;合金元素
Abstract: The effects of alloying elements on the corrosion behavior of foundry Fe-Cr ferritic stainless steels in concentrated sulfuric acid were studied by electrochemical techniques, immersion corrosion and energy dispersive spectroscopy (EDS). The results show that the corrosion resistance of Fe-Cr alloys in concentrated sulfuric acid improved with the increase of Cr content. However, the single Cr alloyed Fe-Cr alloy was unable to reach self-passivation in 98% H2SO4at 60 ℃. Mo addition enhanced the corrosion resistance and promoted the passivation and self-passivaiton of Fe-Cr25-Mo alloys. Elements Ni and Cu can also promoted the passivation and self-passivation of Fe-Cr25Mo2 alloys, whereas Ti and Nb only had a little influence on the passivation.
Keywords: ferritic stainless steel; concentrated sulfuric acid; electrochemical technique; alloying element
铁素体不锈钢具有优良的耐蚀性和力学性能,并且与其他不锈钢钢种比,其镍含量较低(可节约镍资源),被越来越广泛地应用于汽车,建筑,家庭用具及各种化工系统流程中[1-6]。在硫酸制酸系统流程中采用了大量的泵、阀、管件等铸造件,而这些铸造件接触的介质主要为浓硫酸。浓硫酸具有独特的腐蚀性,浓硫酸中的去极化剂有HSO4-,H3O+离子和H2SO4分子,前两种均为H2SO4的解离产物。去极化剂H2SO4分子主要发生阴极还原反应,见式(1)~(3);而去极化剂HSO4-,H3O+离子主要发生析氢腐蚀反应,见式(4)~(5)。因此,不锈钢在浓硫酸中的腐蚀非常复杂,既可发生H2SO4分子去极化腐蚀反应也可发生析氢腐蚀反应[7]。作者所在工作组曾研究了446型和447型铁素体不锈钢在浓硫酸中的耐蚀性及腐蚀电化学特性[8],但目前就合金元素对铸造铁素体不锈钢在浓硫酸中耐蚀性的研究还少见报道。研究合金元素对铸造铁素体不锈钢在浓硫酸中耐蚀性的影响,有利于新型合金的开发和应用。本工作通过电化学技术、浸泡腐蚀及能谱分析等方法研究了合金元素对铸造铁素体不锈钢耐浓硫酸腐蚀性能的影响。
1 试验
试验合金为自制的铸造铁素体不锈钢,其化学成分见表1。先在铁基体中依次添加Cr,Mo,Ni,Cu,Nb,Ti等合金元素,再采用3 kg真空感应电炉进行熔炼。

表1 各试验合金的化学成分(质量分数)Tab. 1 Chemical composition of test alloys (mass) %
将炼制好的合金钢锭分别切割成50 mm×25 mm×5 mm的浸泡腐蚀试样及φ15 mm的电化学试样。采用水磨砂纸逐级打磨试样表面(浸泡腐蚀试样最细采用200号砂纸,电化学试样最细采用600号砂纸),再依次采用无水酒精超声清洗除油,二次蒸馏水清洗,最后用滤纸吸干水分备用。测试溶液为分析纯级浓硫酸,98% H2SO4(质量分数)。
电化学测试采用VersaSTAT4电化学工作站及其耦合的VersaStudio软件进行,试验温度为80 ℃。采用Model K47腐蚀电池系统,待测试样装夹在K105型样品支持体中,暴露面积为1 cm2。试验合金为工作电极,铂丝电极为参比电极,铂片电极为辅助电极。工作电极浸入溶液后立即记录开路电位;测量极化曲线时的电位扫描速率为20 mV/min;测量电化学阻抗谱时,待测试样需在开路电位下稳定1 h,正弦波激励信号幅值为10 mV,扫描频率范围为100 mHz~100 kHz;Mott-Schottky曲线测量使用的交流信号频率为1 kHz。
浸泡腐蚀试验的测试时间为72 h,试验温度为100 ℃,采用失重法计算腐蚀速率。采用能谱仪(EDS)分析腐蚀后试样表面元素含量。
2 结果与讨论
2.1 铬的影响
2.1.1 电化学试验
铬是铁素体不锈钢最主要的合金化元素。表2为不同铬含量(以下均指质量分数)的Fe-Cr合金在60 ℃,98% H2SO4中的电化学参数。
开路电位测试结果表明:不同铬含量的Fe-Cr合金浸入溶液后,均发生了强烈的析氢腐蚀,产生大量的氢气,由于活化极化之后析氢腐蚀受到抑制,开路电位处于一个稳定的平台;但随铬含量的升高,Fe-Cr合金的开路电位总体上呈上升趋势,由13% Cr时-0.979 V升高到30%Cr时的-0.891 V;而铬含量为22%~28%时,合金的开路电位变化不大。可见,即使将铬含量提高到30%仍不能使Fe-Cr合金在所测试的溶液中产生自钝化,合金均发生活化态的腐蚀,这表明单一的铬合金化难以使其产生自钝化。
极化曲线测试结果表明:随铬含量的增加,维钝电流密度逐渐减小,过钝化电位逐渐升高,钝化区间逐渐扩大,而致钝电流密度则无明显规律,这可能是因为Fe-Cr合金的表面状态及腐蚀产物对其活化-钝化过程有一定的影响。

表2 不同铬含量的Fe-Cr合金在60 ℃、98% H2SO4中的电化学参数Tab. 2 Electrochemical parameters of Fe-Cr alloys with different Cr content in 98% H2SO4 at 60 ℃
2.1.2 浸泡腐蚀试验
图1为不同铬含量的Fe-Cr合金在100 ℃,98% H2SO4中的腐蚀速率曲线。由图1可见:铬含量不超过18%时,腐蚀速率变化不大;铬含量为18%~28%时,随铬含量的增加,腐蚀速率快速下降;铬含量为30%时,腐蚀速率又略微上升。
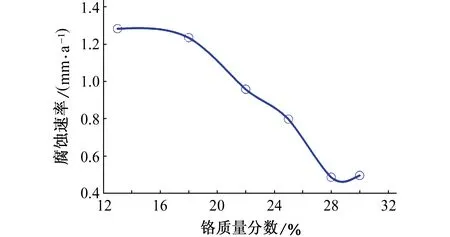
图1 不同铬含量的Fe-Cr合金在100 ℃、98% H2SO4中的腐蚀速率曲线Fig. 1 Corrosion rate curve of Fe-Cr alloys with different Cr content in 98% H2SO4 at 60 ℃
图2为在100 ℃,98% H2SO4中腐蚀后Fe-Cr合金表面铬含量,表面铬含量越高,说明其在合金表面的富集程度越高。由图2可知:Fe-Cr合金中铬含量不超过22%时,随铬含量的增加,铬在合金表面的富集程度变化不大;Fe-Cr合金中铬含量为22%~30%时,铬在合金表面的富集程度较高,能发挥最大的耐蚀效用。

图2 在100 ℃,98% H2SO4中腐蚀后不同铬含量Fe-Cr合金表面的铬含量Fig. 2 Cr content on the surface of Fe-Cr alloys with different Cr content after corrosion in 98% H2SO4at 100 ℃
铬是易钝化元素,能与铁基体合金组成固溶体,且可以通过在合金表面形成Cr2O3氧化膜,使合金的溶解速率大大降低,从而提高合金的耐蚀性。在98% H2SO4中,添加13% Cr就可使合金具有钝化特性[1-2]。综上所述,添加铬能提高Fe-Cr合金在浓硫酸中的耐蚀性,且其最佳含量为22%~28%。
2.2 钼的影响
2.2.1 电化学试验
将铬含量固定在25%,调节Fe-Cr25-Mo合金中的钼含量以研究钼含量对高铬铁素体不锈钢在浓硫酸中耐蚀性的影响。
图3为Fe-Cr25-Mo合金在60 ℃,98% H2SO4中的时间-电位曲线。由图3可知:与Fe-Cr合金一样,Fe-Cr25-Mo合金浸入98% H2SO4后主要发生析氢腐蚀,随后电位进入一个稳定的平台;但当钼含量不超过2%时,随钼含量的增加,Fe-Cr25-Mo合金的电位有所升高,但是合金仍然处于活化腐蚀状态;而当钼含量增加到3%时,电位跃升到一个较高的平台进入了钝化态腐蚀,合金得到钝化膜的保护,耐蚀性提高。

图3 不同钼含量的Fe-Cr25-Mo合金在60 ℃,98% H2SO4中的时间-电位曲线Fig. 3 Potential vs time curves for Fe-Cr25-Mo alloys with different Mo content in 98% H2SO4 at 60 ℃
图4为不同钼含量的Fe-Cr25-Mo合金在60 ℃,98% H2SO4中的致钝电流密度Jpp,维钝电流密度Jp。由图4可知:随钼含量的升高,Fe-Cr25-Mo合金在60 ℃,98% H2SO4中的致钝电流密度降低,且当钼含量在1.0%~1.5%时,致钝电流密度降低最快,钼含量超过1.5%之后,致钝电流密度变化不大;维钝电流密度几乎随钼含量的增加呈线性降低。
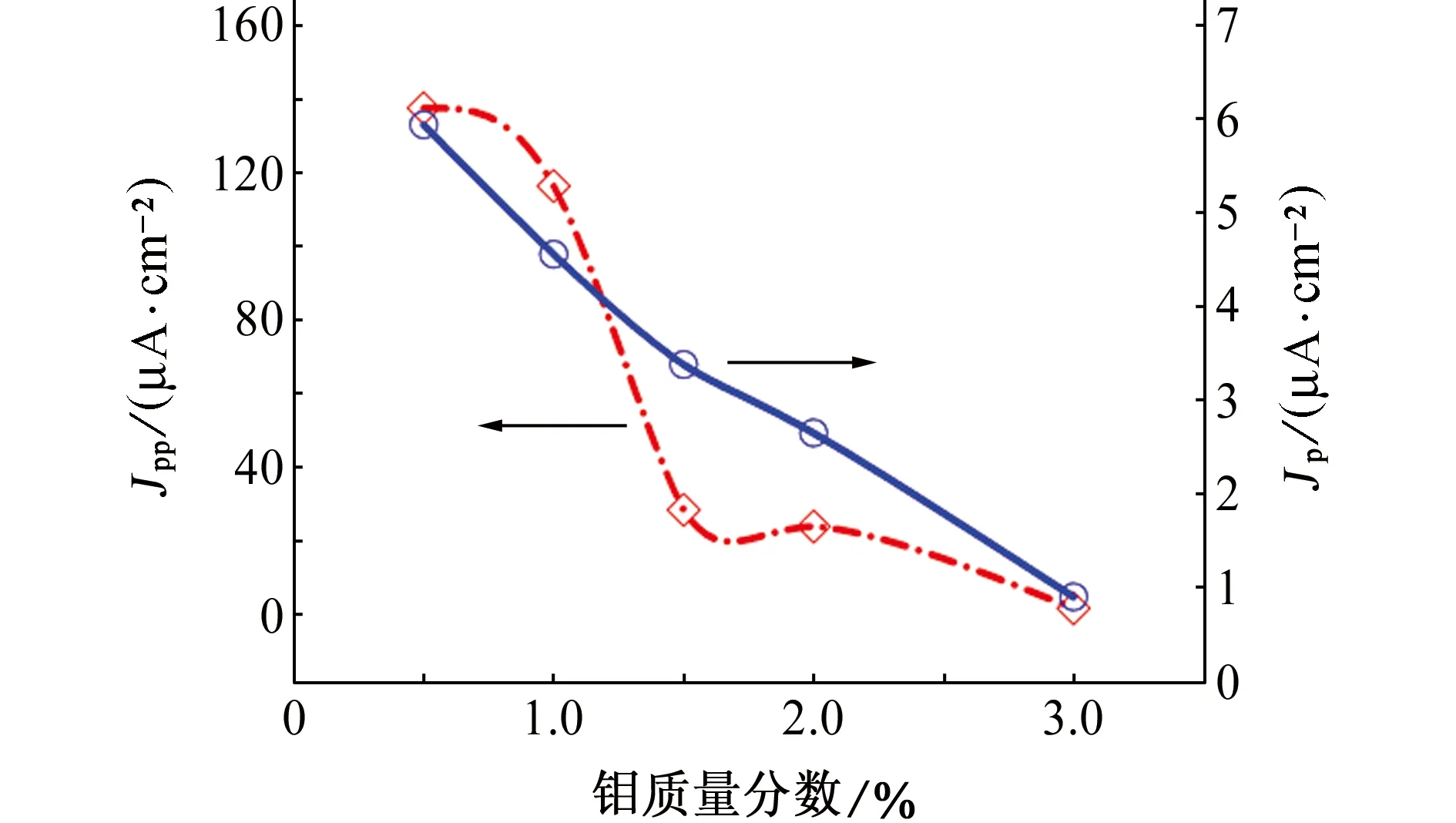
图4 钼含量对Fe-Cr25-Mo合金在60 ℃,98% H2SO4中的钝化电流密度的影响Fig. 4 Effect of Mo content on passivation current density of Fe-Cr25-Mo alloys in 98% H2SO4 at 60 ℃
图5为不同钼含量的Fe-Cr25-Mo合金在60 ℃,98% H2SO4中的Nyquist图。由图5可知:Fe-Cr25-Mo合金在60 ℃,98% H2SO4中的电化学阻抗谱均呈现出容抗弧特性,且容抗弧半径随钼含量增加而增大。钼含量不超过2.0%时,腐蚀主要为活化腐蚀,表现出双电层的容抗特性;而钼含量增加至3.0%时,腐蚀为钝化腐蚀,表现为合金表面钝化膜的容抗特性[9]。

图5 钼含量对Fe-Cr25-Mo合金在60 ℃,98% H2SO4中Nyquist图的影响Fig. 5 Effect of Mo content on the Nyquist diagram of Fe-Cr25-Mo alloys in 98% H2SO4 at 60 ℃
活化腐蚀采用等效电路R(QR)拟合,而钝化腐蚀采用等效电路R{Q[R(QR)]}进行拟合[9],拟合结果见表3。由表3可知,在60 ℃,98% H2SO4中,Fe-Cr25-Mo合金的传递电阻Rt随钼含量的增加而增大,且钼含量不低于1.5%时,传递电阻增大明显,钼含量为3.0%时,传递电阻增大了一个数量级。这主要是因为腐蚀由活化态转为钝化态。

表3 不同钼含量的Fe-Cr25-Mo合金在60 ℃,98% H2SO4中的阻抗谱的等效电路参数Tab. 3 EIS equivalent circuit parameters of Fe-Cr25-Mo alloys with different Mo content in 98% H2SO4 at 60 ℃
2.2.2 浸泡腐蚀试验
钼含量对Fe-Cr25-Mo合金在100 ℃,98% H2SO4中的腐蚀速率影响见图6。由图6可知:随钼含量的增加Fe-Cr25-Mo合金的腐蚀速率降低,当钼含量增加到1%时,合金的腐蚀速率降低较为明显,钼含量在1%~3%时,腐蚀速率变化较为平稳。

图6 钼含量对Fe-Cr25-Mo合金在100 ℃,98% H2SO4中均匀腐蚀速率的影响Fig. 6 Effect of Mo content on the corrosion rate of Fe-Cr25-Mo alloys corroded in 98% H2SO4 at 100 ℃
图7为不同钼含量的Fe-Cr25-Mo合金在100 ℃,98% H2SO4中腐蚀后表面钼含量,表面钼含量越高,说明其在合金表面的富集程度越高。由图7可知:当钼含量增加到1.5%时,钼的富集程度明显增加,之后在1.5%~3.0%的范围内变化较为平稳。钼是不锈钢和各种耐蚀合金常用的合金化元素,能赋予铁素体不锈钢更优异的耐蚀性,特别是改善铁素体不锈钢的钝化能力,提高钢的耐点蚀和耐缝隙腐蚀性能。通过与铬复合合金化作用,钼可以明显抑制铁素体不锈钢在98% H2SO4中的析氢过程,促进其钝化和自钝化,提高钝化膜的自我修复能力[1-2],从而提高基体的耐蚀性。

图7 在100 ℃,98% H2SO4中腐蚀后不同钼含量Fe-Cr25-Mo合金表面的铬含量Fig. 7 Mo content on the surface of Fe-Cr25-Mo alloys with different Mo content after corrosion in 98% H2SO4 at 100 ℃
2.3 辅助合金元素的影响
2.3.1 电化学试验
将铬含量及钼含量分别固定在25%和2%,调节辅助合金元素含量以研究其对铸造高铬铁素体不锈钢在浓硫酸中耐蚀性能的影响。
图8为采用不同辅助合金元素的Fe-Cr25Mo2合金在60 ℃,98% H2SO4中的时间-电位曲线。由图8可知:辅助合金化的Fe-Cr25Mo2合金浸入浓硫酸中后,开始也产生析氢腐蚀,之后产生了电位的波动并最终使Fe-Cr25Mo2合金自钝化。这一自钝化现象可能是因为辅助合金元素对合金腐蚀的表面步骤和电化学反应步骤产生了影响,从而促进了合金的自钝化[10]。由试验结果可知,单独采用铬合金化时,即使将铬含量增加至30%仍不能使合金在60 ℃,98% H2SO4中产生自钝化,采用铬钼复合合金化时,则要将钼含量提升至3%方可使合金产生自钝化。而在Fe-Cr25Mo2合金的基础上进一步采取镍、铜、铌、钛辅助合金化后,无论是单独添加还是复合添加辅助合金元素均可使合金在60 ℃,98% H2SO4中产生自钝化。因此,复合合金化对于提高铸造高铬铁素体不锈钢在浓硫酸中的自钝化能力具有重要的作用。

图8 辅助合金元素对Fe-Cr25Mo2合金在60 ℃,98% H2SO4中的时间-电位曲线的影响Fig. 8 Effects of assistant alloying elements on the curves of potential vs time for Fe-Cr25Mo2 alloys in 98% H2SO4 at 60 ℃
图9为Fe-Cr25Mo3合金及辅助合金化的Fe-Cr25Mo2合金在60 ℃,98% H2SO4中自钝化后测得钝化膜的Mott-Schottky图。由图9可知:Fe-Cr25Mo3合金在自钝化后所获得的钝化膜呈P型半导体特性,钝化膜主要由较低价态的金属氧化物或氢氧化物如Cr2O3、FeO、MoO2、Fe(OH)2组成,当电位升高至平带电位以上,则钝化膜呈n型半导体特性,此时钝化膜主要由高价态的Fe2O3、CrO3、MoO3、Cr(OH)3组成。辅助合金化的Fe-Cr25Mo2合金钝化膜的电容特性与Fe-Cr25Mo3合金钝化膜的较为相似,在平带电位以下表现为P型半导体特性,平带电位以上表现为n型半导体特性。这表明镍,铜,铌,钛可能并不参与构成钝化膜,而仅仅是改变钝化膜的掺杂浓度和有序性,促进合金的钝化,提高合金的钝化能力。

图9 Fe-Cr25Mo3合金和辅助合金化的Fe-Cr25Mo2合金在60 ℃,98% H2SO4中的Mott-Schottky曲线Fig. 9 Mott-Schottky curves of Fe-Cr25Mo3 alloy and Fe-Cr25Mo2 alloys with assistant alloying elements in 98% H2SO4 at 60 ℃
2.3.2 浸泡腐蚀试验
图10为辅助合金元素对Fe-Cr25Mo2合金在100 ℃,98% H2SO4中的均匀腐蚀速率的影响。由图10可知:加入少量镍的Fe-Cr25Mo2合金腐蚀速率最大,与电化学测试结果不一致,这可能是因为测量时间不同所造成的。也有研究表明,镍对不锈钢耐浓硫酸腐蚀有害,因为镍能使不锈钢产生活化-钝化的周期性波动腐蚀[10-11]。铜可提高不锈钢耐浓硫酸腐蚀的性能,采用铜辅助合金化的合金的腐蚀速率比采用镍的要低很多,而采用镍,铜复合合金化的合金的腐蚀速率最低,这充分体现了复合合金化对提高合金耐浓硫酸腐蚀的重要作用[12]。在此基础上采用铌,钛辅助合金化的合金的腐蚀速率相对有轻微的增加,表明钛和铌对铁素体不锈钢耐高温浓硫酸腐蚀性能无明显影响,甚至略有不利作用。钛,铌在铁素体不锈钢中主要作用是稳定碳、氮化物以提高工艺成型性能[1-2]。EDS分析表明(图略):不同辅助合金化的Fe-Cr25Mo2合金在100 ℃,98% H2SO4中腐蚀后,镍、铜、钛的含量相对于腐蚀前降低,而铌的含量腐蚀前后变化不大。这与电化学测量的结果一致。综上所述,铸造铁素体不锈钢应以铬、钼为主合金化元素,且加入适量的辅助合金元素,才能使合金获得优良的耐浓硫酸腐蚀性能。

图10 辅助合金元素对Fe-Cr25Mo2合金在100 ℃,98% H2SO4中的均匀腐蚀的影响Fig. 10 The effect of assistant alloying elements on Fe-Cr25Mo2 alloys in 98% H2SO4 at 100 ℃
3 结论
(1) 铸造高铬铁素体不锈钢在100 ℃,98% H2SO4中的耐蚀性随铬含量的增加而降低,但铬含量应不高于28%;而在60 ℃,98% H2SO4中,即使将铬含量增加至30%仍不能使其自钝化。
(2) 铸造高铬铁素体不锈钢在100 ℃,98% H2SO4中的耐蚀性随钼含量增加而提高,钼可有效抑制析氢腐蚀,促进铁素体不锈钢钝化,当钼含量增加至3%时可使Fe-Cr25Mo3合金在60 ℃,98% H2SO4中产生自钝化。
(3) 辅助合金元素镍、铜与铬钼复合合金化可显著提高铸造高铬铁素体不锈钢在浓硫酸中的钝化及自钝化能力,进而提高合金的耐浓硫酸腐蚀性能,而钛、铌的影响不大。
[1] 陆世英,张凯廷,杨长强,等. 不锈钢[M]. 北京:原子能出版社,1995.
[2] 康喜范. 铁素体不锈钢[M]. 北京:冶金工业出版社,2012.
[3] 杨献金,姜志祥. 445铁素体不锈钢内胆水箱的加工性能和耐蚀性[J]. 腐蚀与防护,2012,33(7):630-633.
[4] 杨欣妍,陈旭,丁毅,等. 热处理工艺对430铁素体不锈钢耐蚀性的影响[J]. 腐蚀与防护,2013,34(1):49-51.
[5] 邱德良,刘焕安,赵成永. 高铬铁素体不锈钢制造硫磺制酸干吸设备探讨[J]. 硫磷设计与粉体工程,2007(4):22-25.
[6] 刘焕安,叶际宣. 高铬铁素体不锈钢在硫酸和湿法磷酸生产中的应用[J]. 硫磷设计与粉体工程,2006(5):32-36.
[7] 欧阳明辉,刘焕安,叶际宣. 不锈钢在浓硫酸中的腐蚀探讨[J]. 全面腐蚀控制,2015(8):39-44.
[8] 欧阳明辉,刘焕安,叶际宣. 铁素体不锈钢446在高温浓硫酸中耐蚀性研究与应用探讨[J]. 硫酸工业,2015(5):62-65.
[9] 曹楚南,张鉴清. 电化学阻抗谱导论[M]. 北京:科学出版社,2002.
[10] LI Y,IVES M B,COLEY K,et al. Corrosion of nickel-containing stainless steel in concentrated sulphuric acid[J]. Corrosion science,2004,46(8):1969-1979.
[11] MATSUHASHI R. The effect of Ni content on the corrosion behavior of stainless steels in highly concentrated sulfuric acid[J]. Corrosion Engineering,1990,39:89-100.
[12] 欧阳明辉,刘焕安,叶际宣. 双相不锈钢在硫酸介质中的应用探讨[J]. 硫酸工业,2011(5):36-41.
Effect of Alloying Elements on Corrosion Resistance of Foundry Fe-Cr Ferritic Stainless Steels in Concentrated Sulfuric Acid
OUYANG Minghui, LIU Huanan, YE jixuan
(The Institute of Xuanda Corrosion-Resistant Special Metals of Zhejiang Province, Yongjia 325105, China)
10.11973/fsyfh-201710005
TG174
A
1005-748X(2017)10-0761-06
2016-03-20
欧阳明辉(1982-),工程师,硕士,主要从事特种金属材料研发及腐蚀电化学研究工作,0577-57762279,ouyang_minghui@xuanda.com

