HPLC法同时测定牛黄宁宫片中6种成分的含量
孙艳涛,宋玉红,赵磊,于浪天,王良(1.吉林师范大学化学学院,吉林四平16000;2.吉林师范大学环境友好材料制备与应用省部共建教育部重点实验室,吉林四平 1010;.吉林省四平市食品药品检验所,吉林四平 16099;.中国药科大学中药学院,南京 211198)
HPLC法同时测定牛黄宁宫片中6种成分的含量
孙艳涛1,2*,宋玉红1,2,赵磊3,于浪天4,王良1#(1.吉林师范大学化学学院,吉林四平136000;2.吉林师范大学环境友好材料制备与应用省部共建教育部重点实验室,吉林四平 130103;3.吉林省四平市食品药品检验所,吉林四平 136099;4.中国药科大学中药学院,南京 211198)
目的:建立同时测定牛黄宁宫片中6种成分含量的方法。方法:采用高效液相色谱法。色谱柱为TC-C18,流动相为甲醇-0.05%磷酸(梯度洗脱),流速为1.0 mL/min,检测波长为280 nm,柱温为25℃,进样量为10µL。结果:甘草苷、盐酸小檗碱、连翘苷、黄芩苷、大黄素和大黄酚检测质量浓度线性范围分别为3.2~320 µg/mL(r=0.999 9)、8.8~880 µg/mL(r=0.999 8)、5.6~560µg/mL(r=0.999 5)、2.0~200 µg/mL(r=0.999 9)、4.4~440 µg/mL(r=0.999 9)、2.0~200 µg/mL(r=0.999 7);精密度、稳定性、重复性试验的RSD<6.0%;加样回收率分别为96.34%~97.25%(RSD=0.33%,n=6)、96.12%~98.06%(RSD=0.82%,n=6)、96.36%~99.09%(RSD=1.02%,n=6)、95.84%~97.32%(RSD=0.65%,n=6)、95.83%~97.92%(RSD=0.88%,n=6)、98.60%~99.65%(RSD=0.42%,n=6)。结论:该方法操作简便,精密度、稳定性、重复性好,可用于牛黄宁宫片中6种成分含量的测定。
牛黄宁宫片;高效液相色谱法;含量测定
ABSTRACTOBJECTIVE:To establish a method for simultaneous determination of 6 components in Niuhuang ninggong tablets.METHODS:HPLC method was adopted.The determination was performed on TC-C18column with mobile phase consisted of methanol-0.05%phosphate acid(gradient elution)at the flow rate of 1.0 mL/min.The detection wavelength was set at 280 nm,and the column temperature was 25℃.The sample size was 10µL.RESULTS:The linear ranges of glycyrrhizin,berberine hydrochloride,baicalin,baicalin,emodin and chrysophanol were 3.2-320 µg/mL(r=0.999 9),8.8-880 µg/mL(r=0.999 8),5.6-560 µg/mL(r=0.999 5),2.0-200 µg/mL(r=0.999 9),4.4-440 µg/mL(r=0.999 9),2.0-200 µg/mL(r=0.999 7),respectively.RSDs of precision,stability and reproducibility tests were all lower than 6.0%.The recoveries were 96.34%-97.25%(RSD=0.33%,n=6),96.12%-98.06%(RSD=0.82%,n=6),96.36%-99.09%(RSD=1.02%,n=6),95.84%-97.32%(RSD=0.65%,n=6),95.83%-97.92%(RSD=0.88%,n=6),98.60%-99.65%(RSD=0.42%,n=6),respectively.CONCLUSIONS:The method is simple,accurate,stable and reproducible,and can be used for content determination of 6 components in Niuhuang ninggong tablets.
KEYWORDSNiuhuang ninggong tablets;HPLC;Content determination
中成药作为一个完整的制剂,强调的是各味药材的协同作用。目前,以单一有效成分或指标成分难以真正控制中成药质量。有些中成药生产企业为了降低成本,利用药检质量标准不能完全控制所有药材的漏洞,漏加、少加药材。因此,必需建立一种快速、准确、全面分离、检测中成药中多种活性成分的方法,以便更好地监控中成药质量和用药安全[1-4]。
精神分裂症是最常见和最严重的精神疾病之一[5]。牛黄宁宫片可用于外感热病、高热神昏、惊风抽搐、肝阳眩晕、耳鸣头痛、心烦不寐及癫痫狂燥的治疗,对精神分裂症有一定的抗复发作用[6-12]。牛黄宁宫片由牛黄、蒲公英、雄黄、连翘、大黄、冰片、金银花、甘草、黄连、黄芩、钩藤、大黄磁石(煅)、玄参、葛根等27味中药材经提取加工制成,该制剂收录于《中国卫生部药品标准中药成方制剂》(WS3-B-2852-98)。原质量标准中仅有简单的显微鉴别、砷量检测和胆酸含量检测[13]。专利“一种控制牛黄宁宫片质量的方法”也仅对性状鉴别、显微及薄层色谱鉴别、三氧化二砷检验和黄芩含量测定进行了控制[14]。上述方法检测指标少,有可能导致其他组分不稳定或缺乏,难以全面准确控制药品质量。目前,有关牛黄宁宫片中多个活性成分含量的测定未见报道。本试验采用高效液相色谱法(HPLC)同时测定牛黄宁宫片中6种成分的含量,为全面控制该制剂的质量提供理论基础。
1 材料
1.1 仪器
1100型HPLC仪,包括VWD检测器(美国Agilent公司);UV-2550型紫外分光光度计(日本Shimadzu公司);FA1104N型万分之一电子分析天平(上海精密科学仪器有限公司);SK5200H型超声波清洗器(上海科导超声仪器有限公司)。
1.2 药品与试剂
牛黄宁宫片(沈阳红药制药有限公司,批号:Z21021460,规格:0.34 g/片);大黄素对照品(批号:110756-200110,纯度:100%)、大黄酚对照品(批号:110796-201017,纯度:100%)、连翘苷对照品(批号:110821-201112,纯度:96.8%)、甘草苷对照品(批号:111610-201106,纯度:93.7%)、黄芩苷对照品(批号:110715-201318,纯度:93.3%)、盐酸小檗碱对照品(批号:110713-201212,纯度:86.7%)均购自中国食品药品检定研究院;甲醇为色谱纯,其余试剂均为分析纯,水为纯化水。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:TC-C18(250 mm×4.6 mm,5µm);流动相:甲醇(A)-0.05%磷酸(B),梯度洗脱(0~35 min,10%→80%A;35~55 min,80%A;55~60 min,80%→10%A);流速:1.0 mL/min;检测波长:280 nm;柱温:25 ℃;进样量:10µL。在上述色谱条件下,理论板数以甘草苷、盐酸小檗碱、黄芩苷、连翘苷、大黄素和大黄酚峰计均>3 000;保留时间分别为21.73、23.05、25.96、27.74、43.20和44.28 min,各成分基线分离良好,详见图1。
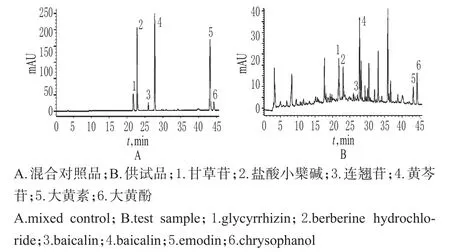
图1 高效液相色谱图Fig 1 HPLC chromatograms
2.2 溶液的制备
2.2.1 混合对照品溶液 精密称取待测成分对照品各适量,分别置于5 mL量瓶中,加甲醇溶解并定容,称定质量,超声(功率:200 W,频率:59 kHz,下同)处理30 min,再次称定质量,用甲醇补足减失的质量,制成甘草苷、盐酸小檗碱、黄芩苷、连翘苷、大黄素、大黄酚质量浓度分别为200、800、560、320、200、440 µg/mL的单一对照品溶液。分别精密量取上述单一对照品溶液适量,置于5 mL量瓶中,加甲醇定容,即得。
2.2.2 供试品溶液 取样品若干,除去糖衣,用玻璃研钵研细,精密称取0.038 14 g,置于5 mL量瓶中,加甲醇溶解并定容,称定质量,超声处理45 min,再次称定质量,用甲醇补足减失的质量,摇匀,静置24 h,滤过,即得。
2.3 线性关系考察
精密量取“2.2.1”项下混合对照品溶液0.1、0.5、1、2、4、5、6、7、8、9、10 μL,按“2.1”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(x,μg/mL)为横坐标、峰面积(y)为纵坐标进行线性回归,回归方程与线性范围见表1。

表1 回归方程与线性范围Tab 1 Linear equations and linear ranges
2.4 精密度试验
取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,甘草苷、盐酸小檗碱、黄芩苷、连翘苷、大黄素、大黄酚峰面积的RSD分别为1.41%、2.80%、2.87%、2.11%、1.02%、1.45%(n=6),表明仪器精密度良好。
2.5 稳定性试验
取“2.2.2”项下供试品溶液(批号:Z21021460)适量,分别于室温下放置0、2、4、8、12 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,甘草苷、盐酸小檗碱、黄芩苷、连翘苷、大黄素、大黄酚峰面积的RSD分别为0.76%、1.56%、2.56%、2.09%、4.96%、5.68%(n=5),表明供试品溶液室温放置12 h内基本稳定。
2.6 重复性试验
精密称取同一批样品(批号:Z21021460)适量,按“2.2.2”项下方法制备供试品溶液,共6份,再按“2.1”项下色谱条件进样测定,记录峰面积。结果,甘草苷、盐酸小檗碱、黄芩苷、连翘苷、大黄素、大黄酚峰面积的RSD分别为1.51%、1.46%、6.44%、2.46%、1.54%、1.98%(n=6),表明本方法重复性良好。
2.7 加样回收率试验
取已知含量样品(批号:Z21021460)适量,共6份,分别加入一定质量的待测成分对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表2。
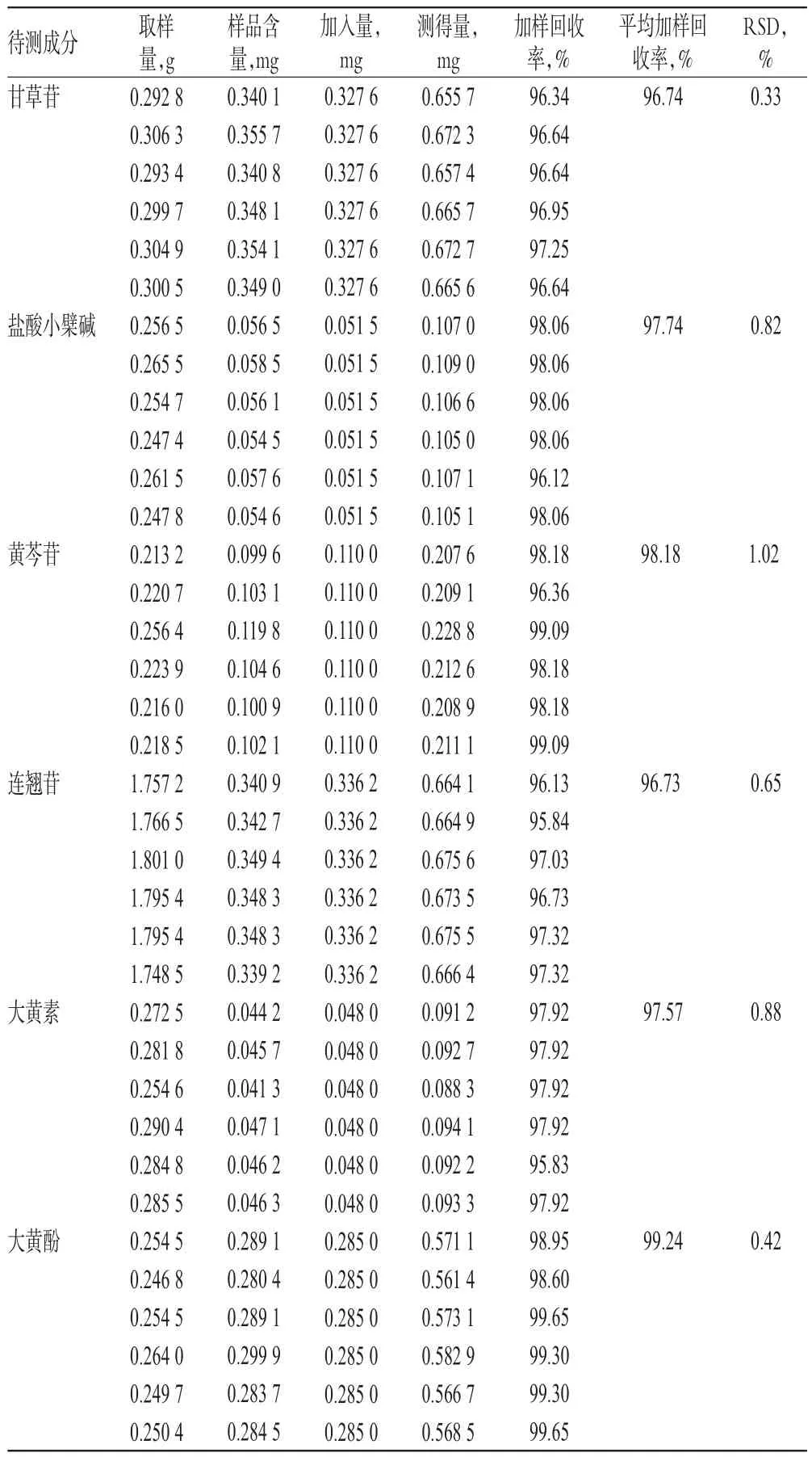
表2 加样回收率试验结果(n=6)Tab 2 Results of recovery tests(n=6)
2.8 样品含量测定
取样品适量,分别按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算样品含量。结果,样品中甘草苷、盐酸小檗碱、黄芩苷、连翘苷、大黄素、大黄酚含量平均值分别为1.161 4、0.220 3、0.467 2、0.194 0、0.162 2、1.136 0 mg/g(n=3)。
3 讨论
3.1 检测波长的选择
通过紫外分光光度计对大黄酚、大黄素、甘草苷、连翘苷、黄芩苷和盐酸小檗碱进行测定,发现上述几种成分在280 nm波长处均有较好的紫外吸收,故采用280 nm作为检测波长。
3.2 流动相的选择
预试验中笔者分别选用甲醇-水(70∶30,V/V,等度洗脱)、甲醇-水(梯度洗脱)、甲醇-0.05%磷酸溶液(梯度洗脱)、乙腈-水(80∶20,V/V,等度洗脱)、甲醇-0.05%磷酸溶液(梯度洗脱)作流动相。结果显示,流动相为甲醇-0.05%磷酸溶液(梯度洗脱)时,色谱峰能够很好地分离,且峰形较好,可有效地缩短分析时间,满足分析要求。
综上所述,本方法操作简便,精密度、稳定性、重复性好,可用于牛黄宁宫片中6种成分含量的测定。
[1]郑翔,尹松鹤.药品检验的质量控制以及措施[J].生物技术世界,2015,12(6):275-276.
[2]陈艳.浅析药品质量检验方法及其评价[J].药物与人,2015,28(1):379-381.
[3]文永盛.中成药质量监管探讨[J].中国药品标准,2010,11(4):250.
[4]张弛,朱嘉亮,郭志鑫,等.我国药品质量分析研究的方法和策略[J].中国药事,2011,25(1):63-64.
[5]蒋立新,褚留杰,张瑞岭.4种抗精神病药治疗精神分裂症急性期的最小成本分析[J].中国药房,2015,26(11):1445-1447.
[6]杨秀双,张平鑫,张春霞,等.牛黄宁宫片联合西药治疗精神分裂症临床观察[J].中国中医药信息杂志,2008,15(4):80-81.
[7]巩秀芹.利培酮片联合牛黄宁宫片治疗精神分裂症临床观察[J].海南医学院学报,2012,18(11):1672-1674.
[8]杨伟芳,陈统献,褚文浩,等.牛黄宁宫片治疗精神分裂症65例[J].中国药业,2012,21(8):88-89.
[9]段德香,王萍,平军辉.牛黄宁宫片治疗躁狂发作的临床研究[J].中国中医药咨讯,2011,3(8):187-188.
[10]郝宝利,邱慧敏.奎硫平联合牛黄宁宫片治疗精神分裂症比较分析[J].临床心身疾病杂志,2005,11(4):317-318.
[11]宋昊,马建东,陈永新,等.奥氮平联合牛黄宁宫片治疗难治性精神分裂症[J].中国实验方剂学杂志,2013,19(21):306-310.
[12]李文国.利培酮联合牛黄宁宫片治疗精神分裂症的可行性[J].医学理论与实践,2016,29(7):886-888.
[13]卫生部.卫生部药品标准:中药成方制剂:第十五册[S].北京:人民卫生出版社,2002:36.
[14]张成海,周文波,陈心,等.一种牛黄宁宫片的质量控制方法:中国,200810179211.0[P].2008-12-01.
(编辑:张 静)
Simultaneous Determination of 6 Components in Niuhuang Ninggong Tablets by HPLC
SUN Yantao1,2,SONG Yuhong1,2,ZHAO Lei3,YU Langtian4,WANG Liang1(1.College of Chemistry,Jilin Normal University,Jilin Siping 136000,China;2.Key Laboratory of Preparation and Application of Environmental Friendly Materials,Ministry of Education,Jilin Normal University,Jilin Siping 130103,China;3.Siping Institute for Food and Drug Control,Jilin Siping 136099,China;4.College of TCM,China Pharmaceutical University,Nanjing 211198,China)
R286;R927
A
1001-0408(2017)27-3862-03
2016-10-12
2016-12-08)
*副教授。研究方向:光谱分析和色谱分析。E-mail:1979yanzi@163.com
#通信作者:教授。研究方向:分析化学。E-mail:16421800@qq.com
DOI 10.6039/j.issn.1001-0408.2017.27.33

