土壤辛硫磷污染对蚯蚓的生态毒理效应研究*
贾 茹 王梦远 黄 擎
(北京理工大学材料学院,北京 100081)
土壤辛硫磷污染对蚯蚓的生态毒理效应研究*
贾 茹 王梦远 黄 擎#
(北京理工大学材料学院,北京 100081)
采用经济合作与发展组织(OECD)标准法配置的人工土壤研究了不同初始质量浓度(25、50、100mg/kg)辛硫磷对蚯蚓的生态毒理效应,测定了不同老化时间(7、14、21、28d)下蚯蚓体内及土壤中辛硫磷含量及各项生态毒理指标。结果表明:28d内辛硫磷在蚯蚓体内及土壤中的含量持续降低;蚯蚓体内蛋白质随老化时间的延长逐渐降低;超氧化物歧化酶(SOD)、过氧化氢酶(CAT)活性随辛硫磷初始浓度增加总体呈先升后降的趋势,随老化时间的延长,SOD活性总体降低,而CAT活性先降后升;28d时丙二醛(MDA)含量达到最高,且随辛硫磷初始浓度增加而总体显著提高(P<0.05);土壤酸性磷酸酶(ACP)活性随辛硫磷初始浓度增加而总体提高,而土壤脲酶(UE)活性随老化时间的延长总体增加。综合而言,SOD活性、CAT活性、MDA含量及土壤ACP活性可作为评价辛硫磷生态毒理效应的生物标志物,在有机磷农药的环境安全性评价过程中应给予考虑。
土壤污染 辛硫磷 蚯蚓 生态毒理效应
Abstract: The subacute toxicity of the phoxim at different concentrations (25,50,100 mg/kg) to earthworm was studied by OECD artificial soil method. The phoxim concentrations in the soil and earthworms and ecotoxicological indexes were measured at the 7th,14th,21stand 28thaging day,respectively. Results were as follows:the phoxim concentrations in earthworms and soil kept decreasing within 28 days. The protein concentrations in earthworms decreased with time prolonged. Superoxide dismutase (SOD),catalase (CAT) activity in earthworms increased first and then decreased with initial concentrations of phoxim increasing. With the aging time increasing,the former activity kept decreasing,while the later tended to decrease first and then rise again. Malondialdehyde (MDA) concentration in earthworms reached the maximum on the 28thday,which increased significantly with initial phoxim concentration increasing in soil (P<0.05). The activity of alkaline phosphatase (ACP) in soil increased with initial phoxim concentration increasing,while that of urease (UE) rose with aging time. In conclusion,SOD activity,CAT activity,MDA concentration and soil ACP activity could be used as biomarkers for evaluation of ecotoxicological effect of phoxim,which should be considered in the environmental security assessment of organophosphorus pesticide.
Keywords: soil pollution; phoxim; earthworm; ecotoxicological effects
我国是一个农业大国,农药使用品种多,用量大,其中70%(质量分数,下同)~80%的农药直接散落到环境中,对土壤、地表水、地下水和农产品造成污染,并进一步通过食物链对人类健康造成影响。有机磷农药因其高效性且在环境中具有较低的持久性而取代有机氯农药并得到广泛应用[1-2]。辛硫磷是一种以触杀、胃毒为主的高效低毒有机磷杀虫剂,主要是通过抑制神经系统乙酰胆碱酯酶活性,使突触后膜乙酰胆碱累积导致昆虫死亡[3],是农业生产中常用的农药之一。
蚯蚓是陆地食物链底部的一种重要生物,在土壤污染生态毒理测试中可作为敏感生物受试物[4-6],在正常情况下其体内自由基的产生与消除处于动态平衡,当受到外源物质胁迫时,自由基的产生大于分解而发生累积,此时其体内的抗氧化系统发挥作用维持氧化-抗氧化平衡[7-8]。研究表明,蚯蚓体内抗氧化酶活性可作为研究有机农药生态风险的生物标志物使用[9-11],但辛硫磷对蚯蚓体内抗氧化体系的研究还鲜有报道。
本研究通过在人工土壤中施加辛硫磷,分析不同老化时间蚯蚓体内及土壤中辛硫磷含量,蚯蚓体内超氧化物歧化酶(SOD)活性、过氧化氢酶(CAT)活性、丙二醛(MDA)含量、蛋白质含量、土壤脲酶(UE)活性及酸性磷酸酶(ACP)活性,探讨蚯蚓体内及土壤中辛硫磷含量与相应酶活性的剂量效应关系,旨在为有机磷农药的环境安全性评价以及揭示该类化合物的生物毒性机制提供有效的科学依据。
1 材料与方法
1.1 试剂与材料
辛硫磷为有效成分40%(质量分数)的乳油。选用赤子爱胜蚓(Eiseniafetida),以发酵牛粪作为饲料,于室温(20~25 ℃)、自然光条件下饲养与繁殖,挑选生殖环明显且无损伤、体重300~500 mg的健康成熟蚯蚓作为受试生物,实验前将蚯蚓放在湿润的滤纸上清肠24 h。
实验用土壤为依据经济合作与发展组织(OECD)标准法[12]配置的人工土壤,其成分为10%(质量分数,下同)泥炭藓、20%高岭土、69%工业石英砂(粒径为0.1~0.3 mm),添加1%的碳酸钙将pH调整为6.5±0.5,配制完成后风干、研磨并过1 mm筛备用。
1.2 实验方法
取适当体积的辛硫磷乳油用丙酮溶解定容为辛硫磷母液备用。分为4个处理组,包括辛硫磷初始质量浓度为0 mg/kg的对照组以及辛硫磷初始质量浓度为25、50、100 mg/kg的实验组,每个处理组将400 g风干土壤置于500 mL烧杯中,定量加入辛硫磷母液,用去离子水调节土壤湿度为25%后平衡5 h。预处理后的蚯蚓冲洗干净,用滤纸吸干体表水分并称量,每个处理组加入20条蚯蚓。均设3组平行处理。实验控制条件为:温度(20±1) ℃,相对湿度80%,光照条件为光照18 h黑暗6 h循环。分别老化7、14、21、28 d后对全部蚯蚓和土壤进行取样。所取土壤样品分为两部分,一部分风干2 d后研磨并过1 mm筛后进行土壤UE和ACP活性分析,另一部分冷冻干燥后测定辛硫磷含量;新鲜蚯蚓样品测定SOD活性、CAT活性、MDA含量和蛋白质含量,冷冻干燥后进行辛硫磷含量分析。
1.3 指标分析方法
土壤中(或蚯蚓体内)辛硫磷含量分析采用高效液相色谱法。称取20 g冷冻干燥的土壤(或5 g蚯蚓)加入25(或5) mL丙酮溶液,振荡1 min后超声处理20 min。上清液用分液漏斗过滤,滤液经旋转蒸发处理后定容至10 mL,取1 mL装入液相色谱仪专用取样瓶,进行定量分析。
蚯蚓体内CAT活性、SOD活性、MDA含量、蛋白质含量以及土壤ACP、UE活性分析均采用相应试剂盒进行。CAT活性依据H2O2在240 nm处有特征吸收峰,测定酶促反应前后H2O2含量差值计算得出,即每克组织每分钟催化1 nmol H2O2降解的酶活力,单位U/g。SOD活性测定采用黄嘌呤氧化酶法,在560 nm处比色测定超氧阴离子还原氮蓝四唑生成蓝色甲臜的含量,即黄嘌呤氧化酶偶连反应体系中抑制率为50%时的酶活力,单位U/g。MDA含量依据其与硫代巴比妥酸缩合生成红色产物在波长532、600 nm处的吸光度差值进行测定,单位nmol/g。蛋白质含量采用考马斯亮蓝法测定,单位μg/mL。土壤ACP活性依据其在酸性环境中催化磷酸苯二钠水解,进而在660 nm处测得水解产物(苯酚)的生成量进行表征,即37 ℃下每克土壤24 h释放的苯酚含量,单位U/g。土壤UE活性利用靛酚蓝比色法在578 nm处比色测得,即37 ℃下每克土壤24 h产生的氨氮含量,单位U/g。
1.4 数据处理
测定结果均以平均值±标准偏差表示,采用Origin 9.1和SPSS Statistics 20.0软件进行分析。
2 结果与讨论
2.1 蚯蚓体内与土壤中辛硫磷含量
如图1所示,相同老化时间下,随辛硫磷初始浓度的增加,蚯蚓体内辛硫磷显著增加(P<0.05),100 mg/kg实验组蚯蚓体内辛硫磷是25 mg/kg实验组的2.26~7.05倍。各实验组蚯蚓体内辛硫磷大体随老化时间的延长而逐渐降低,28 d比7 d降低了87.7%~94.6%。如图2所示,相同老化时间下,土壤中辛硫磷随初始浓度的增加显著升高(P<0.05),100 mg/kg实验组土壤中辛硫磷是25 mg/kg实验组的2.99~10.34倍。各实验组土壤中辛硫磷均会随老化时间延长逐渐下降,28 d比7 d降低了65.9%~90.1%。
2.2 蚯蚓体内生理指标变化
如图3所示,蚯蚓体内蛋白质随老化时间的延长逐渐降低,28 d比7 d降低了66.8%~69.3%;蚯蚓体内蛋白质随辛硫磷初始浓度增加无显著变化。如图4所示,7、21、28 d时,蚯蚓体内SOD活性随辛硫磷初始浓度的增加先升后降,25、50 mg/kg实验组中蚯蚓体内SOD活性达到最大,分别是对照组的1.11~2.10倍;14 d实验组SOD活性均显著低于对照组(P<0.05)。SOD活性随老化时间的延长有总体降低的趋势。如图5所示,7 d时,实验组蚯蚓体内CAT活性比对照组显著降低13%~42%(P<0.05);14、21、28 d时,随着辛硫磷初始浓度增加,CAT活性总体先升后降,25 mg/kg实验组最高,是对照组的1.10~2.13倍。CAT活性随老化时间的延长总体呈先降后升的趋势,21 d时达到最小值。如图6所示,蚯蚓体内MDA大体随老化时间的延长而提高,28 d时达到最高。7、14、21 d时,各实验组MDA与对照组差异总体不显著;28 d时,50、100 mg/kg实验组中蚯蚓体内MDA显著升高(P<0.05),分别是对照组的1.53、1.52倍。

注:小写字母相同表示差异不显著;不同表示差异显著。图2至图8同。
图1不同老化时间下的蚯蚓体内辛硫磷
Fig.1 Phoxim concentration in earthworms at different aging time

图2 不同老化时间下土壤中辛硫磷Fig.2 Phoxim concentration in soil at different aging time

图3 不同老化时间下蚯蚓体内蛋白质Fig.3 Protein concentration in earthworms at different aging time

图4 不同老化时间下蚯蚓体内SOD活性Fig.4 SOD activity in earthworms at different aging time

图5 不同老化时间下蚯蚓体内CAT活性Fig.5 CAT activity in earthworms at different aging time

图6 不同老化时间下蚯蚓体内MDAFig.6 MDA concentration in earthworms at different aging time
2.3 土壤ACP、UE活性变化
如图7所示,土壤ACP活性随辛硫磷初始浓度增加而总体提高。21 d内各实验组土壤ACP活性均总体显著高于对照组(P<0.05),7 d时实验组是对照组的1.53~5.78倍,14 d时为1.06~2.23倍,21 d时为1.36~1.85倍;28 d时,25、100 mg/kg实验组与对照组差异显著(P<0.05),分别是对照组的0.88、1.69倍,而50 mg/kg实验组与对照组无显著差异。如图8所示,土壤UE活性随老化时间的延长总体增加,28 d时是7 d的1.28~3.79倍。7、21 d时100 mg/kg实验组中土壤UE活性最高;14 d时25 mg/kg实验组最高;28 d各实验组土壤UE活性显著低于对照组(P<0.05)。由此可见,在辛硫磷暴露条件下,土壤ACP活性对辛硫磷浓度较敏感,而土壤UE活性则对老化时间更敏感。

图7 不同老化时间下土壤ACP活性Fig.7 Soil ACP activity at different aging time

图8 不同老化时间下土壤UE活性Fig.8 Soil UE activity at different aging time
2.4 讨 论
由表1可知,蚯蚓体内辛硫磷含量与CAT活性呈显著负相关,而SOD活性、蛋白质含量、MDA含量则与辛硫磷含量无显著相关性。
辛硫磷在老化28 d内对蚯蚓体内抗氧化酶系统产生了影响,对不同酶呈现出不同程度的刺激或抑制作用。当蚯蚓受到辛硫磷胁迫时,体内CAT、SOD活性变化趋势基本一致,随着辛硫磷初始浓度的增加总体呈先升后降的趋势。对于清除活性氧自由基,CAT与SOD有着不同的作用机制,CAT可有效将SOD歧化活性氧自由基的产物H2O2转化为H2O和O2[13-14]。与对照组比,7 d时,25、50 mg/kg实验组的SOD活性升高,而CAT活性降低,这可能是因为当蚯蚓受到辛硫磷氧化胁迫时,体内自由基数量增多诱导SOD合成量增加,CAT尚未被诱导同时酶蛋白被破坏或消耗导致CAT活性下降[15],表明生物体内活性氧的清除SOD发挥作用在前、CAT作用在后。14 d时,各实验组SOD活性降低、CAT活性总体升高,表明辛硫磷胁迫下蚯蚓体内的活性氧自由基大量积累,使SOD活性受到抑制,而H2O2刺激了CAT合成使实验组CAT活性升高。21、28 d时,总体上SOD、CAT活性在低浓度实验组受到刺激,而在高浓度实验组受到不同程度的抑制,表明在实验后期,当外源污染物对蚯蚓产生的损伤在一定程度内,体内SOD、CAT等抗氧化酶系统能相互协作保护细胞免受活性氧自由基的损伤。
MDA含量是有机体组织或细胞脂质过氧化的产物,其增加是机体细胞膜损伤的标志。在实验初期,有机污染物刺激蚯蚓体内抗氧化酶活力增加减轻了活性氧对机体细胞的损伤程度,因而实验组蚯蚓体内MDA含量与对照组总体无显著变化;28 d时实验组MDA含量与对照组差异显著,随辛硫磷初始浓度升高与老化时间延长,体内大量自由基的产生超出了机体抗氧化系统的清除能力而积累,细胞膜发生脂质过氧化使蚯蚓体内MDA含量总体显著增加。由此可见,MDA含量变化可作为反映辛硫磷对蚯蚓毒性效应的指标之一。
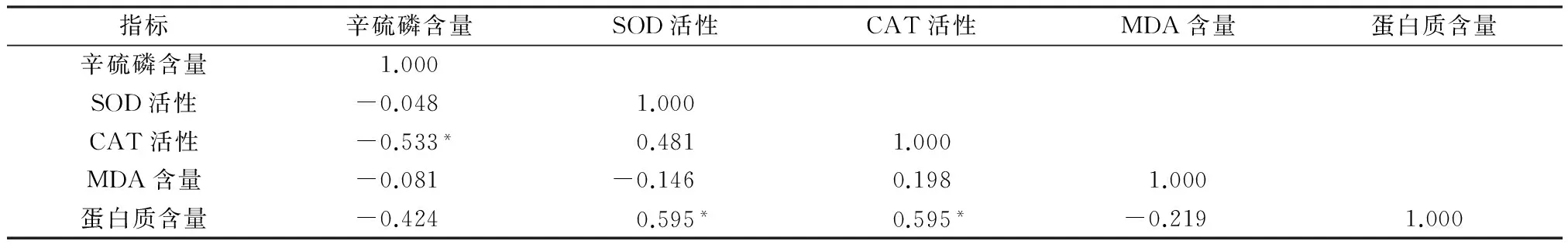
表1 蚯蚓生态毒理指标相关系数矩阵1)
注:1)*表示具有显著相关性。
由表2可知,土壤中辛硫磷含量、土壤UE活性和土壤ACP活性间无显著相关性。

表2 土壤生态毒理指标相关系数矩阵
3 结 语
有机磷农药辛硫磷对蚯蚓具有毒性效应,使蚯蚓体内各项生态毒理指标产生变化。短期暴露条件下,SOD比CAT先发挥抗氧化作用,而MDA含量无明显变化。长期暴露条件下,SOD、CAT活性随着辛硫磷初始浓度增加总体呈先升后降的趋势,而MDA含量总体显著增加。辛硫磷暴露会造成土壤ACP活性增加,而土壤UE活性随老化时间的延长有增加趋势。综合而言,SOD活性、CAT活性、MDA含量与土壤ACP活性随辛硫磷初始浓度不同均会发生变化,这4种指标可作为评价辛硫磷生态毒理效应的生物标志物,在辛硫磷的使用以及环境安全性评价过程中应给予考虑。
[1] SEEBUNRUENG K,SANTALADCHAIYAKIT Y,SRIJARANAI S.Vortex-assisted low density solvent liquid-liquid microextraction and salt-induced demulsification coupled to high performance liquid chromatography for the determination of five organophosphorus pesticide residues in fruits[J].Talanta,2015,132:769-774.
[2] 李辉龙.1,2,4-TCB对蚯蚓(Eiseniafetida)的细胞和分子毒理机制研究[D].杭州:浙江工业大学,2011.
[3] SHANG J Y,SHAO Y M,LANG G J,et al.Expression of two types of acetylcholinesterase gene from the silkworm,Bombyxmori,in insect cells[J].Insect Science,2007,14(6):443-449.
[4] CHEN C,ZHOU Q X,LIU S,et al.Acute toxicity,biochemical and gene expression responses of the earthwormEiseniafetidaexposed to polycyclic musks[J].Chemosphere,2011,83(8):1147-1154.
[5] WU S J,ZHANG H X,ZHAO S L,et al.Biomarker responses of earthworms (Eiseniafetida) exposured to phenanthrene and pyrene both singly and combined in microcosms[J].Chemosphere,2012,87(4):285-293.
[6] MAITY S,ROY S,CHAUDHURY S,et al.Antioxidant responses of the earthwormLampitomauritiiexposed to Pb and Zn contaminated soil[J]. Environmental Pollution,2008,151(1):1-7.
[7] DU L,LI G D,LIU M M,et al.Evaluation of DNA damage and antioxidant system induced by di-n-butyl phthalates exposure in earthworms (Eiseniafetida)[J].Ecotoxicology and Environmental Safety,2015,115:75-82.
[8] ZHANG W,LIU K,CHEN L,et al.A multi-biomarker risk assessment of the impact of brominated flame retardant-decabromodiphenyl ether (BDE209) on the antioxidant system of earthwormEiseniafetida[J].Environmental Toxicology and Pharmacology,2014,38(1):297-304.
[9] ZHANG Q M,ZHANG B H,WANG C X.Ecotoxicological effects on the earthwormEiseniafetidafollowing exposure to soil contaminated with imidacloprid[J].Environmental Science and Pollution Research,2014,21(21):12345-12353.
[10] WANG Y H,CHEN C,QIAN Y Z,et al.Ternary toxicological interactions of insecticides,herbicides,and a heavy metal on the earthwormEiseniafetida[J].Journal of Hazardous Materials,2015,284:233-240.
[11] ZHANG Q M,ZHANG G L,YIN P J,et al.Toxicological effects of soil contaminated with spirotetramat to the earthwormEiseniafetida[J].Chemosphere,2015,139:138-145.
[12] Organization for Economic Cooperation and Development.OECD guideline for testing chemicals,section 2:effects on biotic systems[M].Paris:OECD,1984.
[13] 朱新产,叶宝兴.生物科学基础实验:植物类[M].北京:高等教育出版社,2007.
[14] YAO X H,MIN H,LÜ Z H.Influence of acetamiprid on soil enzymatic activities and respiration[J].European Journal of Soil Biology,2006,42(2):120-126.
[15] 王艳,马泽民,吴石金.3种PAEs对蚯蚓的毒性作用和组织酶活性影响的研究[J].环境科学,2014,35(2):770-779.
Ecotoxicologicaleffectofphoximpollutioninsoilonearthworms
JIARu,WANGMengyuan,HUANGQing.
(SchoolofMaterialsScienceandEngineering,BeijingInstituteofTechnology,Beijing100081)
贾 茹,女,1992年生,硕士研究生,研究方向为土壤环境化学。#
。
*“十二五”农村领域国家科技计划课题(No.2013BAD16B01);北京理工大学基础研究基金资助项目(No.20141042004);北京理工大学科技创新计划项目(No.2015CX02027)。
10.15985/j.cnki.1001-3865.2017.09.003
2016-04-29)

