工业铁渣硫酸浸出-除铜实验研究
苏瑞娟
(甘肃有色冶金职业技术学院, 甘肃 金昌 737100)
工业铁渣硫酸浸出-除铜实验研究
苏瑞娟
(甘肃有色冶金职业技术学院, 甘肃 金昌 737100)
应用还原浸出机理以及置换除铜机理,通过单因素条件实验和综合因素条件实验研究把硫酸作为浸出剂还原浸出工业铁渣。研究结果表明:随硫酸浓度的增加,渣率逐渐降低,镍浸出率逐渐升高,当硫酸浓度达到一定值后渣率和镍浸出率均趋于稳定,硫酸浓度过高会使浸出液pH太低,不利于浸出液净化处理;当浆化液固比为5∶1,浸出时间3 h,浸出温度75~85℃,硫酸的含量为80 g/L,铁粉加入过量倍数为1.2时,镍浸出率可达98.86%,渣率为11.48%,该条件为硫酸浸出铁渣的最佳工艺条件。
工业铁渣 浸出 除铜
随着现代工业的发展,金属原矿资源日益紧张,而采用新方法、新技术、新工艺,充分利用工业废渣中的金属,开发高附加值的功能材料,已成为工业废渣资源化利用的主要研究方向[1-3]。本文主要以金川公司所堆存的镍钴湿法冶金过程中产生的渣,铜冶炼厂回转窑焙烧产出的综合铁渣和公司内部生产过程中所产生的污泥渣为原料,从中浸出镍、铁等其他有价金属,从而为提取渣中的铁奠定理论基础。
1 实验原料
本课题研究的原料(综合铁渣)均来自于金川公司,其主要成分见表1所示。

表1 原料(综合铁渣)主要成分 %
2 实验机理
2.1 还原浸出机理
浸出是指利用适当的溶剂使矿石、精矿和半成品中的一种或几种有价成分优先溶出,使之与脉石相分离。
硫酸浸出的实质是利用稀硫酸的酸性,将铁渣中的金属元素转化成盐溶液[4-6]。黄钠铁矾渣含有高价金属Fe(Ⅲ),在酸性溶液中Fe3+是中强氧化剂,它可以把铁、镍、铜等氧化,降低了金属的浸出率,为此在硫酸浸出后,需加入亚硫酸钠还原浸出。可能发生的主要反应为:


式(4)中 Me为 Ni、Co、Cu、Zn、Mn、Ca、Mg等。
2.2 置换除铜机理
因铁渣酸浸液中铜元素主要以Cu2+的形式存在,为与后续工艺衔接,需用铁粉将其还原[7-8],可能发生的主要反应为:

3 实验结果与讨论
3.1 单因素条件实验
3.1.1实验条件
1)铁渣浆化液固质量比5∶1,温度75~85℃,硫酸质量浓度依次为 50g/L、60g/L、70g/L、80g/L、90g/L、100g/L、110g/L和120g/L;
2)硫酸浸出0.5 h后加入亚硫酸钠,还原2 h后加入铁粉,总反应时间3 h;
3)亚硫酸钠、铁粉的加入量分别为浸出液Fe3+、Cu2+质量浓度的1.2倍。
3.1.2 硫酸浸出-除铜实验结果(见表2)
由表2可看出,随硫酸浓度的增加,渣率逐渐降低,镍浸出率逐渐升高,当硫酸浓度达到一定值后渣率和镍浸出率均趋于稳定,硫酸浓度过高会使浸出液pH太低,不利于浸出液净化处理。
实验结果表明:当硫酸质量浓度为80 g/L时,镍浸出率可达98.86%,渣率为11.48%,该浓度为硫酸浸出铁渣的最佳工艺条件。

表2 硫酸浸出-置换除铜实验结果
3.2 综合条件实验
3.2.1 实验条件
1)铁渣浆化液固质量比5∶1,温度75~85℃,硫酸质量浓度为80 g/L;
2)硫酸浸出0.5 h后加入亚硫酸钠,还原2 h后加入铁粉,总反应时间3 h;
3)亚硫酸钠、铁粉的加入量分别为浸出液Fe3+、Cu2+质量浓度的1.2倍。
3.2.2 综合条件实验结果
由表3可看出,综合条件实验结果比较理想,达到了铁渣浸出和除铜的预期目标。
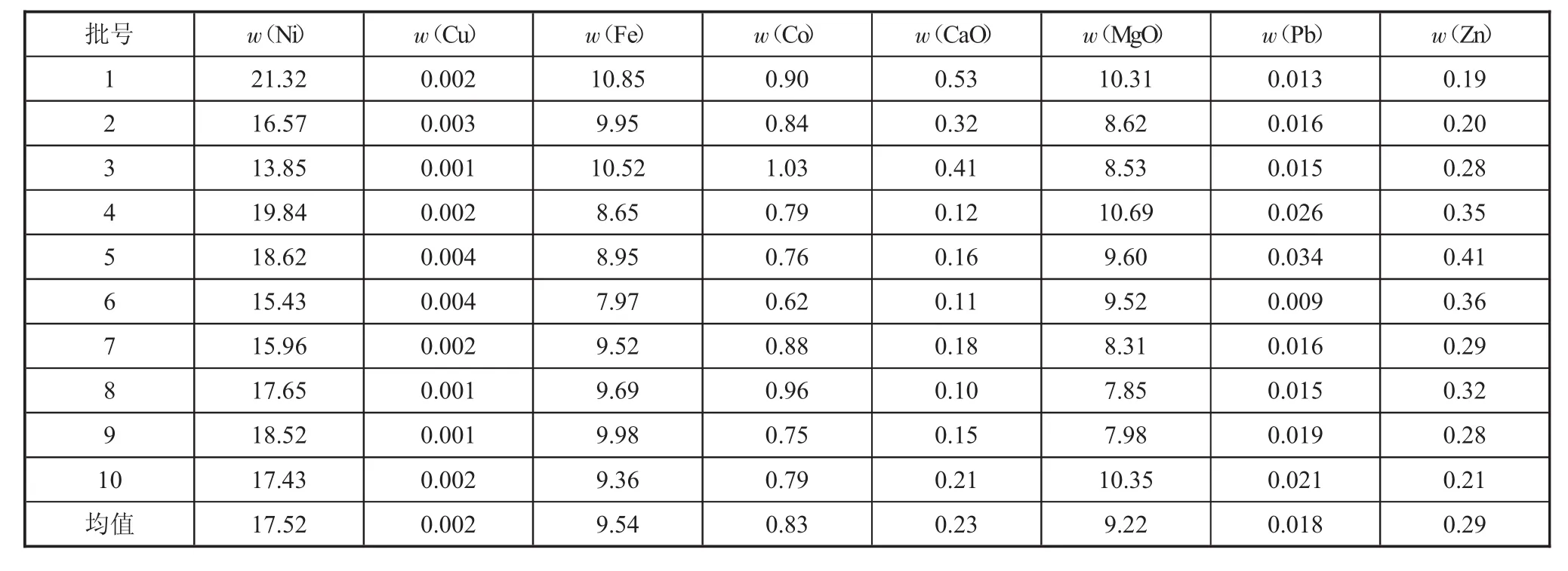
表3 浸出-除铜后液成分%
4 实验结论
通过考察硫酸质量浓度对铁分离效果的影响,得到如下结论。
1)还原浸出-除铜工艺条件为:铁渣浆化液固比5:1,温度75~85℃,硫酸质量浓度为80 g/L;硫酸浸出0.5 h后加入亚硫酸钠,还原2 h后加入铁粉,总反应时间3 h;亚硫酸钠、铁粉的加入量分别为浸出液Fe3+、Cu2+浓度的1.2倍。
2)随硫酸质量浓度的增加,渣率逐渐降低,镍浸出率逐渐升高,当硫酸质量浓度达到一定值后渣率和镍浸出率均趋于稳定,硫酸质量浓度过高会使浸出液pH太低,不利于浸出液净化处理。实验结果表明:当硫酸质量浓度为80 g/L时,镍浸出率可达98.86%,渣率为11.48%。
[1] 曹异生.国内外镍工业现状及前景展望[J].世界有色金属,2005(10):67-71.
[2] 江源,侯梦溪.全球镍资源供需研究[J].有色矿冶,2008,24(2):55-57.
[3] 朱屯.萃取与离子交换[M].北京:冶金工业出版社,2005:85-88.
[4] Saji J,Reddy M L P.Liquid-liquid Extraction Separation of IronIII from Titania Wastesusing TBP-MIBK Mixedsolvent System[J].Hydrometallurgy,2001,61(2):81-87.
[5] Chen Jiayong,Yu Shuqiu,Liu Huizhou,et al.New Mixed Solvent Systems for the Extraction and Separation Offerric Ironin Solutions[J].Hydrometallurgy,1992,30(1-3):401.
[6] AsanoH,Itabashi H,Kawamoto H.Separation of ironⅢby di22ethylh Exyl Phosphate/42 Methy 1222 Pentanone Extraction[J].Journal of the Iron and Steel Institute ofJapan,2001,87(9):623-625.
[7] Suarez C,Ahumada E,Orellana F.Extraction of Iron III from Acidic Sulfate Solutions with bis 22ethylhexyl Phosphoric Acid inPENRECO170ES,Anew Friendly Diluent[J].Journal of Chemical Technologyand Biotechnology2002,77(2):183-189.
[8] Preston JS.Solvent Extraction of Metals Acids[J].Hydrometallurgy,1985,14(2):171-188.
(编辑:王瑾)
Experimental Study of Removing Copper from Sulfuric Acid Leaching of Iron Slag
Su Ruijuan
(Gansu Vocational&Technical College of Nonferrous Metallurgy,Jinchang Gansu 737100)
By mechanism of reducing leaching and copper removal by displacement,through single factor experiment and comprehensive factor experiment,the industrial iron slag was lixviated,by vitriol as leaching agent.The experimental results showed that with the increase of the concentration of sulfuric acid,the slag rate gradually decreased,the nickel leaching rate is increased.When the concentration of sulfuric acid attains to certain value,the slag rate and the nickel leaching rate are tending towards stability.When the concentration of sulfuric acid is too high,the leaching solution pH value is too low,which is unfavorable to purification treatment of leach liquor.When the slurrying liquid-solid ratio is 5:1,the reaction time is 3h,thereaction temperature is 75~85 ℃,the vitriol content is 80 g/L and the dosage of iron powder is 1.2 times of theoretical value.The nickel leaching rate is 98.86%,the slag rate is 11.48%.These are optimum conditions for sulfuric acid leaching slag.
industrial iron slag,leaching,removing copper
TF811;TF803.21
A
1672-1152(2017)04-0031-02
10.16525/j.cnki.cn14-1167/tf.2017.04.12
2017-06-14
苏瑞娟(1985—),女,硕士研究生,毕业于兰州理工大学,讲师,主要研究二次资源回收利用。

