去甲基金霉素高产菌株筛选
魏 娟 ,吴文娟,孙玉杰,祝光耀,赵 臻
(1.天方药业 生物技术研究所,河南驻马店 463000;2. 天方药业 第二化验室河南驻马店 463000;3. 华东理工大学 生物工程学院 上海 200237;4.天方药业技术管理部,河南 驻马店 463000)
去甲基金霉素高产菌株筛选
魏 娟1,吴文娟2,孙玉杰1,祝光耀3,赵 臻4*
(1.天方药业 生物技术研究所,河南驻马店 463000;2. 天方药业 第二化验室河南驻马店 463000;3. 华东理工大学 生物工程学院 上海 200237;4.天方药业技术管理部,河南 驻马店 463000)
本课题对金色链霉菌进行四种处理:自然分离、紫外诱变、EMS诱变、菌种驯化。其中自然分离得到的CM-23菌株效价达到2730u/mL,提高了11.42%;紫外诱变得到的UC-11菌株效价达到3127u/mL,提高了27.63%;EMS诱变得到的EC-18菌株效价达到2789u/mL,提高13.84%;菌种驯化得到的CM3000-3菌株效价达到3839u/mL,提高了56.69%。通过比较这四种处理方法,发现菌种驯筛选到CM3000-3提高最多,而且远远超过其他诱变方法所筛选到的最高菌株。这实验结果可为其他有特定靶位点的抗生素的高产菌株的诱变筛选提供参考。
去甲基金霉素; 筛选; 菌株 ; 金色链霉菌
去甲基金霉素(Demethylchlortetracycline,简称DMCTC),是一种广谱的抗生素。属于四环素类抗生素,与金霉素结构相似。在临床上,去甲基金霉素可用于治疗革兰氏阳性菌和阴性菌引发的疾病,如肺炎、尿路感染、细菌性痢疾、布氏杆菌病及小儿獲红热等疾病。且其具有易被人体吸收、且排泄慢、高效性、长效性等特点,因此去甲基金霉素在医药行业中一种运用十分广泛的抗生素[1-2]。目前,去甲基金霉素市场需求量大,而来源比较单一。主要从生物发酵中获得,因此如何选育出高产的去甲基金霉素生产菌具有较大的经济意义。
得到去甲基金霉素生产菌高产菌株主要通过两种途径:一、自然分离;二、诱变育种。通过自然分离选育出的高产菌株,产量比较稳定,且不易退化。但是自然分离的突变率低、过程慢且不定向性较大。而菌种诱变是筛选高产菌株的简单实用的方法。可以大幅度提高突变率,从而可以筛选到状优良的菌株。目前,常用有物理诱变、化学诱变等,同时,以具有特定靶位点的抗生素为诱变剂进行菌种诱变时,能够得到较多的正向突变菌株。因为微生物可以通过反馈抑制和反馈阻遏调节代谢产物的过量积累,所以筛选抗高浓度自身代谢产物或其结构类似物的抗反馈或抗阻遏突变株,也是获得高产突变菌株的一种有效途径[3]。
1 材料与方法
1.1 菌种
金色链霉菌(Streptomyces aureofaciens)cmctc-H,华东理工大学实验室保藏。
1.2 培养基
1.2.1 固体培养基(g/L)
葡萄糖 10、磷酸二氢钾 0.4、天冬酰胺 0.25、牛肉浸膏 2、琼脂条20、去离子水配制,调pH为6.8~7.0,28±0.5℃,培养12~16天。
1.2.2 种子培养基(g/L)
玉米淀粉 30、黄豆饼粉 30、酵母粉 2、大豆蛋白胨 5、磷酸二氢钾 1.5、硫酸铵 2、碳酸钙 10 、pH自然,豆油0.5mL/250 mL三角瓶,28±0.5℃,220r/min,培养2天。
1.2.3 发酵培养基(g/L)
黄豆饼粉30、玉米浆 3、L-赖氨酸盐 8、氯化钠 3、磷酸二氢钾 0.6、硫酸铵 2、玉米淀粉 80、α-淀粉酶 0.08、碳酸钙 10,pH自然,豆油0.3mL/250 mL三角瓶,28±0.5℃,220r/min,培养7天。
1.3 诱变育种方法
1.3.1 自然分离
由于菌株容易发生退化,因此在使用该出发菌株前进行复壮,以便得到性状优良的出发菌株。
本实验来之实验室保藏的甘油管。打开保藏金色链霉菌甘油管,加无菌水稀释后,分别涂布于平板培养基上,28±0.5℃培养14~16d,将孢子长势较好的单菌落划线于到斜面上,再在28±0.5℃培养14~16d。将长好旳斜面接种于种子培养基中,28±0.5℃,220r/min培养48h,将培养好的种子液以10%接种量转入发酵培养基中,28±0.5℃,220r/min培养7d。通过测定效价挑选出效价较高的菌株备用。
1.3.2 紫外诱变[4-5]
1.3.2.1 金色链霉菌单孢子悬液的制备
取孢子长势较好的金色链霉菌斜面,加入5mL无菌水,用已灭菌的铁铲将金色链霉菌孢子轻轻地刮下来,将刮下的金色链霉菌孢子悬液用移液管转入装有玻璃珠的50mL的三角瓶中,28±0.5℃,100r/min震荡20min,用已灭菌棉花漏斗过滤备用。
1.3.2.2 无菌条件下,分别吸取3mL金色链霉菌单孢子悬液于无菌带磁力搅拌器的平皿中,放在紫外灯(紫外灯功率为50W,照射距离30cm)下分别进行照射30 ,60 ,90 ,120,150 s,将处理后的金色链霉菌孢子悬液以10-1,10-2,10-3,10-4,10-5依次稀释并涂布于平板上。28±0.5℃培养14-16d。并以处理前的菌株作为对照。
1.3.3 EMS诱变[6]
1.3.3.1 金色链霉菌单孢子悬液的制备:取金色链霉菌孢子长势较好的斜面,加入5mL无菌水,用已灭菌的铁铲将金色链霉菌孢子轻轻地刮下来,将刮下的金色链霉菌孢子液用移液管转入装有玻璃珠的100mL的三角瓶中,28±0.5℃,100r/min震荡20min,用已灭菌棉花漏斗过滤备用。
1.3.3.2 分别取5mL金色链霉菌单孢子悬液于50mL三角瓶中,各加入5μl的EMS,28±0.5℃,220r/min分别震荡培养1 ,2,3 ,4,5 h,将处理后的金色链霉孢子悬液以10-1,10--210-3,10-4,10-5依次稀释并涂布于平板上。28±0.5℃培养14-16d。并以处理前的菌株作为对照。
1.3.4 菌种驯化[7]
金色链霉菌先在种子培养基中活化,然后依次2000,3000,4000,5000,6000,7000,8000U增加去甲基金霉素在种子培养基的含量,将处理后的种子液以10-1,10-2,10-3,10-4,10-5依次稀释,并涂布于相应抗性平板上。28±0.5℃培养14~16d。并以处理前的菌株作为对照。
1.4 检测方法
高效液相色谱法
色谱柱的型号:Extend-C18(4.6 mm×150 mm 5μm),流动相:准确称取草酸0.9 g和草酸铵10 g并用dd水定容至1000 mL,然后依次加入300 mL乙腈、200 mL甲醇,混匀,超声波脱气30 min备用。柱温:25℃。等梯度洗脱,流速:0.4 mL/min进样量:3μL,紫外检测波长:350 nm。
2 结果与分析
2.1 自然分离
通过自然分离纯化,挑取孢子丰满且菌落较大的单菌落,分别进行摇瓶发酵实验。在考察的单菌落中,最终获得CM-23菌株效价最高(如图1所示)。

图1 自然分离高产菌株CM-23结果
由图1可知:自然分离出发菌株效价为2450 u/mL左右,经自然分离得到的CM-23菌株F3代效价为2730u/mL,提高11.42%。且F1、F2、F3代相对比较稳定,与初筛结果相比,其效价稳定。自然分离得到的高产菌株一般效价比较稳定且不易退化,但是得到高产菌株的工作量比较大且提高幅度小。
2.2 紫外诱变
2.2.1 紫外诱变条件确定
通过上述不同紫外照射时间孢子悬液与未处理的孢子悬液不同稀释度的平板菌落数可得:紫外照射时间与金色链霉菌致死率关系(如图2所示)。

图2 紫外诱变致死曲线
由图2可知:随着紫外照射时间越长,其致死率越高。一般情况下,正变率随着紫外照射时间越长,其正突变率越小。综合这两种情况,我们选取紫外照射90s为最佳照射时长。
2.2.2 紫外诱变高产菌株筛选
选取紫外照射90s孢子悬液涂布的平板,挑取孢子丰满且菌落较大的单菌落,分别进行摇瓶发酵实验。在考察的单菌落中,UC-11菌株效价最高(如图3所示)。
由图3可知:紫外诱变出发菌株效价为2450 u/mL左右,经紫外诱变得到的UC-11菌株F3代效价为3127u/mL,提高27.63%。且F1、F2、F3代相对比较稳定,与初筛结果3315 u/mL相比,其效价降低较多。紫外诱变得到的高产菌株概率较大且提高较多,但是紫外诱变得到高产菌株易发生回复突变。
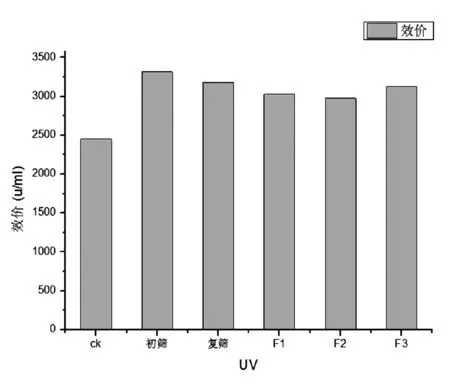
图3 紫外诱变高产菌株UC-11结果
2.3 EMS诱变
2.3.1 EMS诱变条件确定
通过上述不同EMS孢子悬液与未处理的孢子悬液不同稀释度的平板菌落数可得:EMS剂量与金色链霉菌致死率关系(如图4所示)。

图4 EMS诱变致死曲线
由图4可知:随着EMS处理时间的延长,其致死率越高。当EMS处理时间为2h时,菌体致死率达到90%以上。考虑到一般情况下,致死率越高,其正突变率越小。综合这两种情况,我们选取EMS处理2h为最佳时长。
2.3.2 EMS高产菌株的筛选
选取EMS处理时间为2h的孢子悬液涂布的平板,挑取孢子丰满且菌落较大的单菌落,分别进行摇瓶发酵实验。在考察的单菌落中,EC-18菌株最终提高13.84%(如图5所示)。
由图5可知:EMS诱变出发菌株效价为2450 u/mL左右,经EMS诱变得到的EC-18菌株F3代效价为2789u/mL,提高13.86%。且F1、F2、F3代相对比较稳定,与初筛结果相比,其效价稳定。但是EMS诱变后,菌株提高并不明显,与自然分离的CM-23菌株效价一致,因此我们认为EMS诱变结果并不理想。
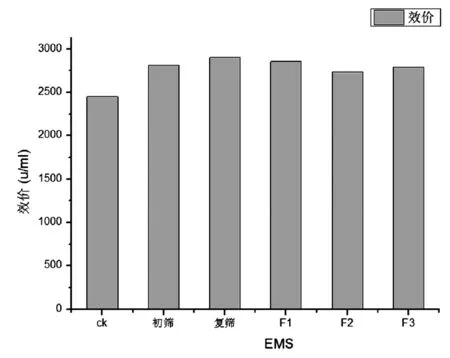
图5 EMS诱变高产菌株EC-18结果
2.4 驯化
在去甲基金霉素添加量为2000,3000,4000U时,平板上单菌落相对较多,但是当去甲基金霉素添加量再增加时,平板上几乎不能长出菌落。在考察的单菌落中,CM3000-3菌株提高最多(如图6所示)。
由图6可知:驯化出发菌株效价为2450 u/mL左右,经驯化后得到的CM3000-3菌株F3代效价为3839u/mL,提高56.69%。且F1、F2、F3代相对比较稳定。与初筛结果3974u/mL相比,其效价相对稳定。去甲基金霉素对金色链霉菌有反馈抑制作用,通过驯化来筛选出抗自身代谢物反馈的高产菌株是一个筛选去甲基金霉素高产菌株的理想方法。
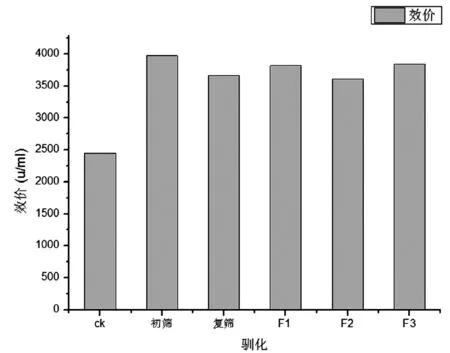
图6 驯化高产菌株CM3000-3结果
2.5 方法比较
本实验对去甲基霉素生产菌同时以自然分离、紫外诱变、EMS诱变、菌种驯化四种方法进行高产菌株的筛选,达到理想效果(如图7所示)。
由图7可知:对去甲基霉素生产菌进行诱变后,其中驯化效果最为突出提高了56.69%,紫外诱变效果次之提高了27.63%,但EMS诱变的得到的最高菌株生产能力与自然筛选相当,因此本实验认为EMS诱变对去甲基霉素高产菌株筛选作用不是太强。通过四种处理方法的比较,我们可以认为微生物可以通过反馈抑制和反馈阻遏调节代谢产物的过量积累,所以筛选抗高浓度自身代谢产物或其结构类似物的抗反馈或抗阻遏突变株,也是获得高产突变菌株的一种有效途径。

图7 不同诱变方法对比
3 展望查
目前去甲金霉素,国内外对其研究的文献较少,且产量也不高。但由于去甲金霉素是及其重要的抗生素,且本身也是合成其他新型抗生素的重要中间体,因此国内外市场的应用十分巨大。随着其在国内外市场的应用越来越大,选育出其高产菌株成为亟待解决的问题。
金色链霉菌生产去甲基金霉素是一个复杂的次级代谢过程,在其遗传背景仍不十分明确的前提下,诱变育种仍是目前获得抗生素高产菌的主要手段。无论是其自发还是诱发的突变株,突变的随机性都非常大,正突变株的出现频率往往较低,传统的育种方法需要进行大量的筛选工作。大量的实践证明,利用自身代谢物的反馈抑制和反馈阻遏调节的特性,将抗生素抗性筛选法与诱变育种方法相结合,可以克服微生物选育过程中传统筛选方法盲目性大、工作量多等缺点。可快速、有效地获得理想的抗生素高产突变株,大大地提高菌种选育工作效。
[1] 贺筱蓉, 李永泉. 原生质体诱变选育去甲基金霉素高产菌[J].浙江大学学报理学版 1997(2):170-177.
[2] 林桂真. 去甲金霉素高产菌株的选育及代谢过程的调控[J].上海:华东理工大学,2014.
[3] 孙玉雯, 崔承彬.抗生素抗性筛选在微生物菌株选育中的作用[J]. 国际药学研究杂志 2008, 35(3):213-217.
[4] 李忠英, 肖杨娟, 罗跃中,等.UV与DES复合诱变选育高产脂肪酶菌株[J]. 氨基酸和生物资源 2011, 33(3):6-9.
[5] 贾永飞.紫外线诱变在青霉素G生产菌种中的应用[J].科技创新导报, 2015(19):105-105.
[6] 涂国全, 刘 姝,黎循航. 通过获得链霉素抗性基因(str)突变株筛选梅岭霉素高产菌株[J].中国抗生素杂志 2002, 27(6):321-325.
[7] Huang D, Wang R, Du W, et al.Activation of glycerol metabolic pathway by evolutionary engineering of Rhizopus oryzae to strengthen the fumaric acid biosynthesis from crude glycerol[J].Bioresource technology 2015, 196(NOV):263.
(本文文献格式:魏 娟,吴文娟,孙玉杰,等.去甲基金霉素高产菌株筛选[J].山东化工,2017,46(14):114-116,118.)
2017-05-09
魏 娟(1987—),女,天方药业生物技术研究所研究员,获得硕士学位,主要从事微生物学研究;通信作者:赵 臻(1989—),项目管理员,学士,主要从事研发项目及成果管理。
Q93
A
1008-021X(2017)14-0114-03

