低温水热纳米二氧化钛分散液制备工艺探索研究
李建业,杨建伟,姜绍龙,甄冠胜
(1.潍坊科技学院,山东 潍坊 262700;2.山东默锐环境产业股份有限公司,山东 潍坊 262714)
低温水热纳米二氧化钛分散液制备工艺探索研究
李建业1,2,杨建伟2,姜绍龙2,甄冠胜2
(1.潍坊科技学院,山东 潍坊 262700;2.山东默锐环境产业股份有限公司,山东 潍坊 262714)
通过采用低温水热法制备了锐钛矿型纳米二氧化钛分散液,研究了钛源与尿素比例、水热反应温度、水热反应时间对纳米催化剂性能的影响,同时通过光还原法对纳米分散液中的纳米二氧化钛进行了铂(Pt)纳米沉积,探索了Pt掺杂量对催化剂性能的影响,罗丹明B(RhB)脱色降解实验,结果表明,最佳反应条件为:硫酸钛与尿素的比例1:1.5,水热温度85℃,反应时间18h,纳米Pt沉积载量为1.5%。
低温水热;纳米二氧化钛;罗丹明B;纳米Pt沉积
环境污染的控制与治理一直是全世界关注的焦点,因此寻求高效的降解环境污染物方法具有重要意义。自从1972年日本科学家Fujishima和Honda[1]首次发现在近紫外光的作用下,金红石型TiO2单晶电极能使水在常温常压下发生分解反应,这一轰动性的发现标志着对金属氧化物半导体异相光催化研究新时期的开始,也掀起了半导体光催化的研究热潮。众多研究人员、科学家在努力探索研究半导体光催化的基本过程,提高TiO2的光量子产率,扩展其响应光谱范围,以及在工业化应用方面都进行了广泛而深入的研究。这些研究与寻找新能源密切相关,主要包括光解水制氢[2]、光化学电池[3]、光化学固氮、有机合成[4],二氧化碳的还原等, 尤其是光催化降解环境污染物[5-7]。然而, TiO2光催化的研究到目前为止已经进行了几十年,但仍然方兴未艾,如火如荼,其原因是(1)由于当今世界的能源危机和环境恶化,迫使人们寻找更清洁,可再生的新能源,而TiO2几乎是目前所发现的效率最高的光催化剂;(2)TiO2在环境治理上的应用前景是极其诱人的,其优势是其他处理方法所无法比拟是。它不但稳定、无毒、活性高,而且能利用廉价、清洁、无穷尽的太阳能,能无选择性矿化几乎所有的有机污染物和还原祛除许多过渡金属离子。
国内对于纳米光催化剂的工业化生产起步较晚,大部分研究还局限于实验室的操作,本文使用廉价的硫酸钛与尿素作为基本原料,采用安全高效的低温水热合成法制备了纳米二氧化钛分散液,并且探索得到了最佳的催化剂制备工艺,同时为了进一步提升催化剂的效率与稳定性,对纳米二氧化钛进行了纳米Pt沉积,通过探索实验得到了最佳的沉积载量。
1 实验部分
1.1 实验试剂与仪器
硫酸钛(Ti(SO4)2),尿素,蒸馏水(自制),氯铂酸(H2PtCl6),异丙醇,氩气;机械搅拌器,高压反应釜(200mL),氙灯(CEL-HXUV300,中教金源),超声分散仪,光反应器(CEL-LB70,中教金源),分光光度计(哈希DR3900),电子分析天平(ME204E,Mettler Toledo),电热鼓风干燥箱(WGL-125B,天津市泰斯特仪器有限公司)。
1.2 纳米二氧化钛分散液的制备
将3.6g Ti(SO4)2溶于150mL蒸馏水中,迅速机械搅拌直至完全溶解,将Ti(SO4)2水溶液转移至三口烧瓶中;将1.35g尿素溶解于50mL蒸馏水中,搅拌至完全溶解,然后将尿素的水溶液转移至分液漏斗中,在连续机械搅拌下缓慢滴入乘有Ti(SO4)2水溶液的三口烧瓶中,尿素溶液滴加完毕后继续搅拌1h,然后将混合溶液转移至高压反应釜中,将反应釜转移至电热鼓风干燥箱中,85℃水热反应24h,反应完毕,将反应釜取出冷却至室温将溶液倒出,离心分离10min,然后将离心管中的清液倒出再重新加入等量的蒸馏水震荡搅拌至分散均匀,再次离心处理,如此重复3~4次直至清液电导率恒定不变后,将催化剂的分散液超声分散处理30min直至分散均匀,室温下保存备用。
1.3 纳米Pt沉积二氧化钛分散液的制备
首先,将水与异丙醇以 1:1 的比例混合置于反应瓶中,反应液总体积为 100 mL,然后将 上述制备纳米 TiO2分散液加入到混合液中。反应瓶密封,通入氩气除氧 1h。 然后在 300 W 的氙灯(CEL-HXUV300,中教金源)下光照。 在光照过程中,将0.5mol/L的 H2PtCl6溶液逐滴缓慢加入到纳米TiO2的悬浮液中,光照2h后,将制备好的样品离心,多次水洗,超声分散至等量的蒸馏水中备用。
1.4 实验方法
采用 CEL-HXUV300氙灯作为光源,分别取在不同实验条件下制备的纳米分散液8mL加入到 100mL 9mg/L的罗丹明B溶液中。反应前将样品置于暗室内搅拌1h,以达到吸附平衡,然后将反应器于氙灯下进行照射,每隔5min取样检测,将所取样品离心处理5min取上清液移至比色皿中,用分光光度计对样品溶液进行吸光度测试,可知罗丹明B最大吸收波长为 554 nm。通过计算罗丹明B溶液的吸光度来测其降解率η,η=,C0-罗丹明B光照前的浓度,C-光照一定时间后的浓度。
2 结果讨论
2.1 硫酸钛与尿素的比例对纳米二氧化钛光催化性能的影响
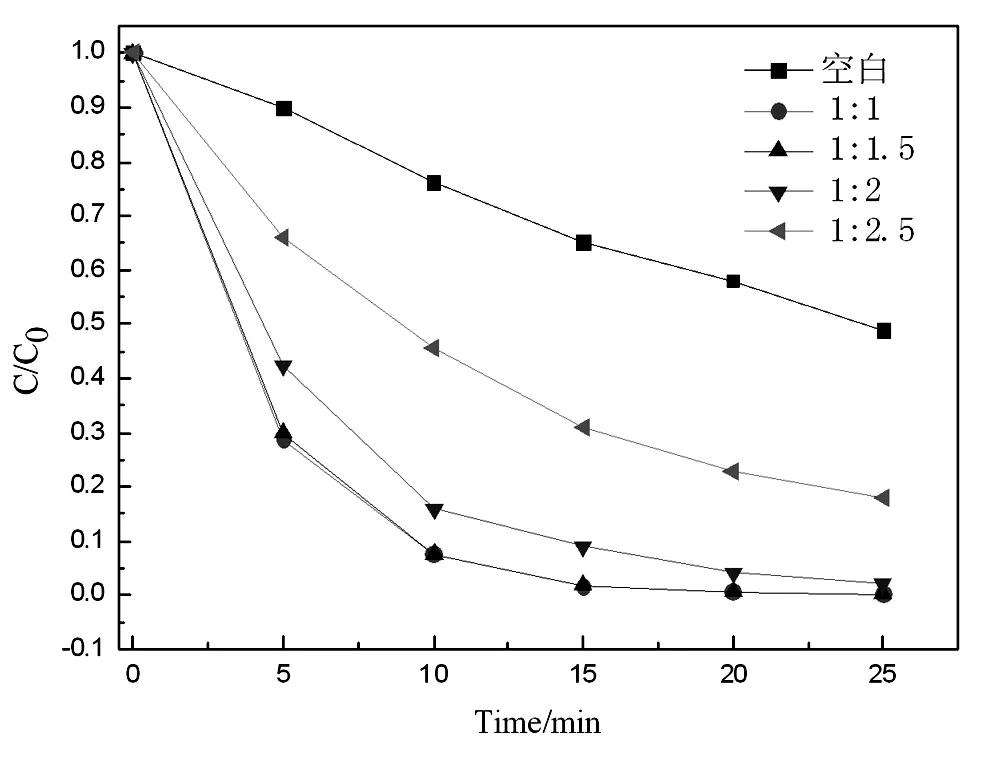
图1 不同硫酸钛与尿素的物质的量比例制备 纳米分散液RhB脱色降解实验
保持其他的实验条件不变,分别调整硫酸钛与尿素的物质的量比例为1:1,1:1.5,1:2,1:2.5制备催化剂分散液,进行光催化RhB脱色降解实验,实验结果如图1所示,硫酸钛与尿素的物质的量比例为1:1时,RhB降解效果最差,试验中发现相比较其他的比例,该反应在相同的反应时间下催化剂的产率偏低,分析为由于尿素的量不足够硫酸钛充分进行水解反应,不仅仅反应不充分,而且反应速度相应减慢,造成最终产物分散液中含有的催化剂量较少,因此降解效果差;同时在图1中发现,当其比例依次改变为1:2与1:2.5时,降解效果逐渐变差,而从最终分散液来看,催化剂分散效果不好,粒径偏大,是由于当尿素比例增大时,伴随反应速度大大提升,因此二氧化钛生长速度较快不能有效的控制催化剂的粒径导致粒径过大,光催化效率相应的降低。因此,从图1结果分析得硫酸钛与尿素的最佳的物质的量比例为1:1.5,在此比例条件下,能保证硫酸钛充分参与水解反应的同时实验反应速度的有效控制,保证纳米催化剂的粒径。
2.2 反应温度对纳米二氧化钛光催化性能的影响
保持其他反应条件不变,分别改变水热温度为65,75,85,95℃制备纳米催化剂分散液,进行RhB光催化脱色降解实验,实验结果如图2所示,如图2中可以明显看出,当反应温度为65℃、75℃时,降解效果与85,95℃相比明显差很多,因为温度较低时催化剂晶型无法转变为锐钛矿相,而无定形态与金红石型催化剂光催化效果与锐钛矿型相比差很多,因此表现为RhB脱色降解效果差,而当反应温度升至85,95℃时RhB降解效果有明显提升,但是85,95℃条件下制备的催化剂效果相差不大,综合经济性考虑选用的最佳反应温度为85℃。
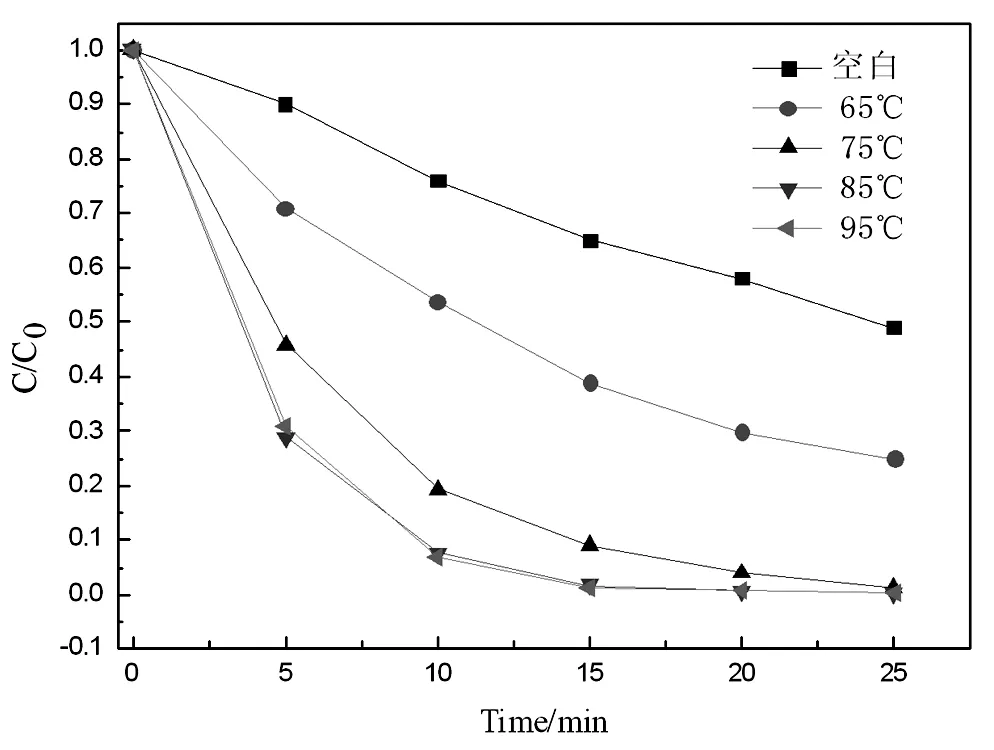
图2 不同水热温度下制备纳米 分散液RhB脱色降解实验
2.3 反应时间对纳米二氧化钛光催化性能的影响
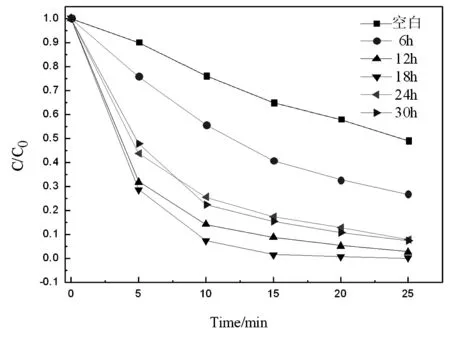
图3 不同反应时间下制备纳米 分散液RhB脱色降解实验
保持其他反应条件不变,改变反应时间分别为6,12,18,24,30h制备纳米分散液,分别将不同条件下制备的分散液进行光催化脱色降解实验,结果如图3所示,结果显示在反应时间为18h时制备的纳米分散液性能最佳,时间太短则纳米催化剂晶型为完成成型,时间太长则会造成晶粒生长过大,导致光催化效率降低。
综上,纳米TiO2分散液最佳的制备工艺条件为:硫酸钛与尿素的最佳比例为1:1.5,水热温度85℃,反应时间18h,其降解RhB的吸光度曲线如图4所示,由图中可以看出,554nm处的波峰并没有发生偏移,证明RhB降解并没有经过脱乙基过程而是直接开环降解。
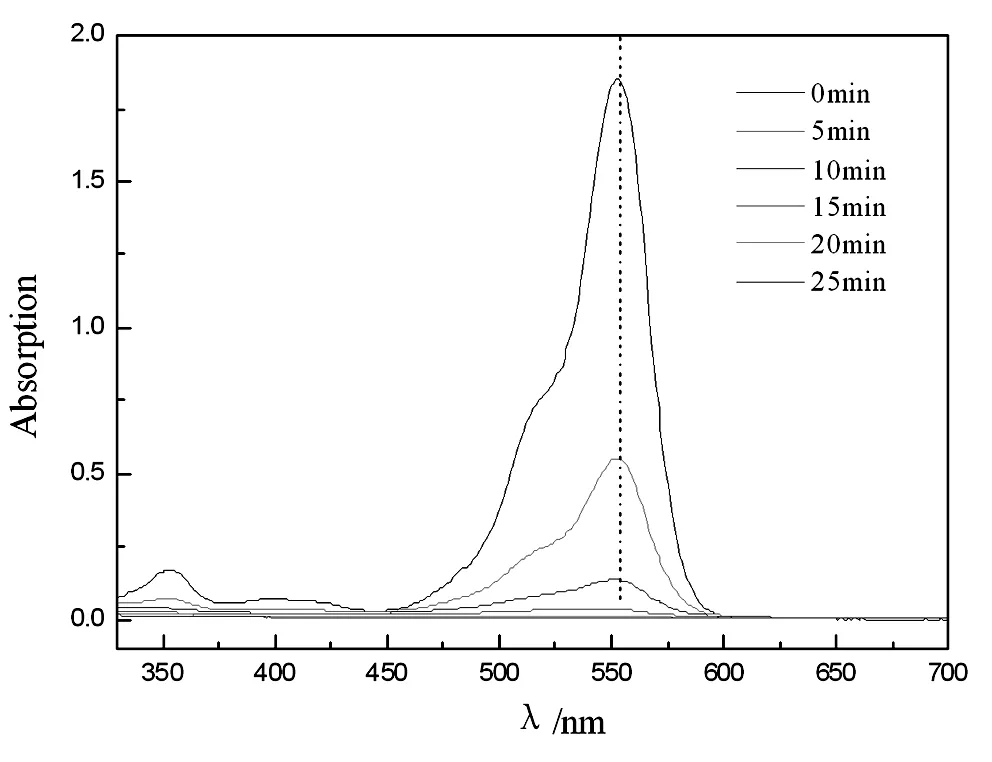
图4 纳米分散液RhB脱色降解吸光度曲线
2.4 纳米二氧化钛光催化性能耐久性测试
众所周知,TiO2作为光催化剂被广泛应用原因之一是源于它出色的稳定性,在本研究中我们通过连续的向反应体系中加入RhB,观察染料的降解速率,来考察了催化剂的稳定性。体系中催化剂分散液用量为8mL(分散液中催化剂浓度为8g/L),初始的罗丹明B染料(浓度9mg/L)降解完毕后,再重新加入浓的染料使它的浓度与当初相同。染料在第二个循环中的降解速度几乎与第一个循环相同(图5) 如此重复11次,染料的降解速率并没有明显地下降,充分证明本试验制备的纳米二氧化钛分散液作为光催化剂在反应条件下是相当稳定的。

图5 纳米分散液RhB脱色降解实验耐久性测试
2.5 纳米Pt沉积二氧化钛分散液性能及沉积量对其光催化性能的影响
由于TiO2能隙较宽 ( Eg=3.2eV),只能够吸收波长在320-420nm的紫外光,因此只能利用不足5% 的太阳光,并且半导体载流子的复合率很高,量子产率较低,这也成为了制约该技术进一步发展的瓶颈,我们通过对TiO2进行改性扩大其响应光谱区间,降低光生载流子的复合率,提高光催化的量子效率,目前常见的改性的方法主要有贵金属沉积、过渡金属离子掺杂、非金属粒子掺杂、光敏化以及半导体间的复合等,其中Pt、Pd等贵金属可有效地拓宽光催化剂的光谱响应范围,提高光催化性能。
当贵金属Pt沉积在 TiO2表面时,载流子会重新分布,电子从费米能级较高的半导体 TiO2转移至费米能级较低的贵金属,直到它们的费米能级相匹配。二者接触后形成的空间电荷层中,贵金属表面获得过量的负电荷,半导体表面显示出过量的正电荷,于是导致能带向上弯曲形成肖特基势垒,而肖特基势垒能有效地捕获光生电子,阻止了光生电子与空穴的复合。同时,在贵金属沉积改性 TiO2的过程中,需将金属的沉积量需控制在一个合适的范围内[8-9]。本文首先研究了纳米TiO2表面沉积纳米Pt后的催化剂光催化活性改变,并探索了贵金属Pt的最佳沉积量。

图6 不同Pt沉积量条件下制备纳米 分散液RhB脱色降解实验

图7 不同Pt沉积量条件下制备纳米分散 液RhB脱色降解实验局部放大
保持其他的反应条件不变,改变氯铂酸的加入量分别调控纳米Pt的沉积量为1%,1.5%,2%,2.5%,进行RhB光催化脱色降解实验,实验结果如图6、图7所示,结果显示,当沉积量为1%与2.5 %时,结果较差,原因是由于当沉积量为1%沉积量较少,还不足以有效的促进光生载流子的分离来提高量子产率,而当沉积量为2.5 %,Pt沉积量过大,其对电子有较强的吸附作用,会减小电子密度,导致复杂场结构的出现,成为电子-空穴对重新复合的中心,最终使催化剂的光催化活性降低同时,贵金属沉积量过多时,TiO2催化剂表面会被覆盖,当光照射时会被阻止,从而减少了光生电子空穴的数目,同样会降低 TiO2光催化反应的速率。从结果可以看出,沉积量为1.5 %,2 %时,光催化降解效果十分接近,从经济性方面考虑,本试验确定最佳的纳米Pt沉积量为1.5%。
3 结论
采用低温水热法制备纳米TiO2分散液,并通过探索实验得到了最佳的催化剂制备条件;同时对所制备的纳米TiO2进行了贵金属纳米Pt沉积,具有良好的光催化性能,通过对RhB的脱色降解实验得到了最佳的沉积载量。
[1] Fujishima A, Honda K. Electrochemical photolysis of water at semiconductor electrode[J], Nature, 1972, 238(5358): 37.
[2] Pérez Larios A, Hernández Gordillo A, Morales Mendoza G,et al. Enhancing the H2Evolution from Water-Methanol Solution Using Mn2+-Mn3+-Mn4+Redox Species of Mn-Doped TiO2Sol-Gel Photocatalysts[J]. Catalysis Today, 2016, 266:9-16.
[3] Peter L M. The Gratzel Cell: Where Next[J]. J Phyl Chem Lett, 2011, 2: 1861-1867.
[4] Ratcliff E L,Zacher B,Armstrong N R. Selective interlayers and contacts in organic photovoltaic cells[J]. J Phys Chem Lett, 2011, 1: 1337-1350.
[5] Dunnill C W, Parkin I P. Nitrogen-doped TiO2thin films: photocatalytic applications for healthcare environments[J]. Dalton Transaction, 2011, 40: 1635-1640.
[6] Wang M, Ioccozia J, Sun L, et al. Inorganic-modified semiconductor TiO2nanotube arrays for photocatalysis[J]. Energy & Environmental Science, 2014, 7: 2182-2202;
[7] Chen X, Mao S S. Titanium dioxide nanomaterials, synthesis, properties, modifications, and applications[J]. Chemical Reviews, 2007, 107: 2891-2959.
[8] Aiabatzis I M, Stergiopoulos T, Bemard M C, et al. Silver modified titanium dioxide thin films for efficient photodegradation of methyl orange[J]. Appl Catal B: Environ, 2003, 42: 187-201.
[9] Vorontsov A V, Savinov E N, Zhen S J. Influence of the form of photodeposited platinum on titania upon its photocatalytic activity in CO and acetone oxidation[J]. J Photochem Photobiol A: Chem, 1999, 125: 113-117.
(本文文献格式:李建业,杨建伟,姜绍龙,等.低温水热纳米二氧化钛分散液制备工艺探索研究[J].山东化工,2017,46(14):24-27.)
Study on Preparation Processes of Nano-TiO2Dispersions by Low-temperature Hydrothermal Method
LiJianye1,2,YangJianwei2,JiangShaolong2,ZhenGuansheng2
(1.Wei Fang University of Science and Technology, Weifang 262714,China;2.Shan Dong Moris Environmental Industry Co., Ltd., WeiFang 262714,China)
Anatase Nano-TiO2dispersions were prepared by Low-temperature Hydrothermal Method. This paper studied thepreparation processes of nano-TiO2dispersions in detail and settled down the optimum conditions through experiments including the molar ratio of Ti(SO4)2and urea,hydrothermal temperature and hydrothermal time. At the same time,the as-prepared were loaded nano-Pt by photo-reduction method, and the optimum Pt deposition weight were obtained by the decolorization and degradation experiment of RhB. The result indicates that the optimum molar ratio of Ti(SO4)2and urea is 1:1.5; the optimum hydrothermal temperature is 85℃,the optimum hydrothermal time is18h and the optimum Pt deposition weight is 1.5wt.%.
low-temperature hydrothermal method;nano-TiO2;RhB; nano-Pt deposition
2017-05-15
李建业(1971—),山东寿光人,博士学位,主要研究方向:工业废水废气治理、饮用水净化。
TB383
A
1008-021X(2017)14-0024-04

