羚羊感冒片的GC指纹图谱研究Δ
林 林,郭东晓,汪 冰,刘广桢(山东省食品药品检验研究院,济南 250101)
·药物分析与检定·
羚羊感冒片的GC指纹图谱研究Δ
林 林*,郭东晓,汪 冰,刘广桢#(山东省食品药品检验研究院,济南 250101)
目的:建立羚羊感冒片的气相色谱(GC)指纹图谱。方法:毛细管柱为DB-5 ms毛细管柱,检测器为氢火焰离子化检测器,进样口温度为240℃,检测器温度为250℃,程序升温,载气为氮气,流速为1.0 mL/min,进样量为1 μL,进样方式为分流进样,分流比为20∶1。以薄荷酮为参照物,测定10批羚羊感冒片的GC图谱,采用《中药色谱指纹图谱相似度评价系统》(2012版)进行共有峰指认和相似度评价。结果:10批羚羊感冒片的GC图谱有14个共有峰,相似度均>0.98。经验证,10批样品GC图谱与对照指纹图谱具有较好的一致性。结论:该研究所建指纹图谱可为羚羊感冒片的鉴别和质量评价提供参考。
羚羊感冒片;气相色谱法;挥发油;特征图谱
羚羊感冒片作为临床常用中成药,具有清热解表的功效,用于治疗流行性感冒,症见发热恶风、头痛头晕、咳嗽、胸闷、咽喉肿痛[1];处方由羚羊角、金银花、连翘、荆芥等中药组合而成[2]。结合生产工艺,荆芥、连翘挥发油以及薄荷素油为该制剂发挥药效的主要成分,而2015年版《中国药典》(一部)未对处方中的挥发油进行质量控制。笔者参考相关文献[3-8],建立了羚羊感冒片挥发油的气相色谱(GC)指纹图谱,可用于羚羊感冒片的质量控制和评价。
1 材料
1.1 仪器
7890A型GC仪,包括氢火焰离子化检测器(美国Agilent公司);CP225D型电子分析天平(德国Satorius公司)。
1.2 药品与试剂
羚羊感冒片[委托山东宏济堂制药集团有限公司代加工,批号:ZZY001~ZZY010(S1~S10),规格:0.32 g/片];薄荷酮对照品(批号:111705-201105)、柠檬烯对照品(批号:100470-201302)、胡薄荷酮对照品(批号:111706-201205)、薄荷脑对照品(批号:110728-200506)均购自中国食品药品检定研究院,α-蒎烯对照品(批号:80605)、乙酸薄荷酯对照品(批号:45987)、β-蒎烯对照品(批号:80609)均购自美国Sigma公司,以上对照品纯度均>98.0%;乙酸乙酯为色谱纯,其余试剂均为分析纯,水为去离子水。
1.3 药材及挥发油
羚羊角、牛蒡子、淡豆豉、金银花、荆芥、连翘、淡竹叶、桔梗、甘草药材和薄荷素油均由北京同仁堂科技股份有限公司提供,经山东中医药大学周凤勤教授鉴定均为真品。
2 方法与结果
2.1 色谱条件
毛细管柱:DB-5 ms毛细管柱(30 m×250 mm,0.10 µm);检测器:氢火焰离子化检测器;进样口温度:240℃;检测器温度:250℃;升温程序:初始温度50℃,保持2 min,以12℃/min升温至90℃,再以6℃/min升温至220℃;载气:氮气;流速:1.0 mL/min;进样量:1 μL;进样方式:分流进样;分流比:20∶1。
2.2 溶液的制备
2.2.1 混合对照品溶液 精密称取待测成分对照品各适量,加乙酸乙酯制成α-蒎烯、β-蒎烯、柠檬烯、薄荷酮、薄荷脑、胡薄荷酮、乙酸薄荷酯质量浓度分别为0.100 8、0.117 3、0.189 4、0.219 3、0.514 2、0.299 8、0.173 6 mg/mL的混合对照品溶液。
2.2.2 供试品溶液 取样品12片,研细,精密称定,置于圆底烧瓶中,自挥发油提取器上端加入乙酸乙酯1 mL,加热提取4 h,分取乙酸乙酯液,用无水硫酸钠脱水后,加乙酸乙酯稀释至2 mL,混匀,即得。
2.2.3 药材挥发油对照溶液 按羚羊感冒片比例取荆芥、连翘各适量,按“2.2.2”项下供试品溶液制备方法制成荆芥挥发油对照溶液、连翘挥发油对照溶液;薄荷素油直接按处方量折算,制成相应质量浓度的对照溶液。
2.3 方法学考察
2.3.1 精密度试验 取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件连续进样测定6次,以薄荷酮的保留时间和峰面积为参照,记录各共有峰相对保留时间和相对峰面积。结果,14个共有峰相对保留时间的RSD<0.01%,相对峰面积的RSD<1.2%(n=6),表明仪器精密度良好。
2.3.2 稳定性试验 取“2.2.2”项下供试品溶液(批号:ZZY001)适量,分别于室温下放置0、2、4、8、16、24 h时按“2.1”项下色谱条件进样测定,以薄荷酮的保留时间和峰面积为参照,记录各共有峰相对保留时间和相对峰面积。结果,14个共有峰相对保留时间的RSD<0.02%,相对峰面积的RSD<1.5%(n=6),表明供试品溶液室温放置24 h内基本稳定。
2.3.3 重复性试验 精密称取同一批样品(批号:ZZY001)适量,按“2.2.2”项下方法制备供试品溶液,共6份,再按“2.1”项下色谱条件进样测定,以薄荷酮的保留时间和峰面积为参照,记录各共有峰相对保留时间和相对峰面积。结果,14个共有峰相对保留时间的RSD<0.02%,相对峰面积的RSD<1.8%(n=6),表明本方法重复性良好。
2.4 GC指纹图谱的生成、指认及相似度分析
2.4.1 GC指纹图谱的生成 取10批样品各适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,采用《中药色谱指纹图谱相似度评价系统》(2012版)对10批样品的GC图谱进行分析,得GC指纹图谱,详见图1、图2。

图110 批样品GC叠加指纹图谱Fig 1 GC overlay fingerprints chromatograms of 10 batches of samples
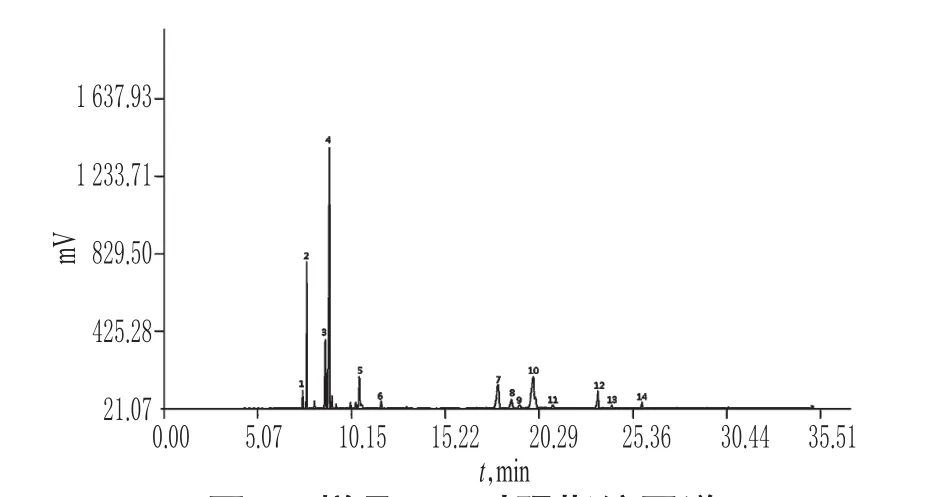
图2 样品GC对照指纹图谱Fig 2 GC fingerprint chromatograms of sample
2.4.2 共有峰的归属和指认 分别取“2.2.1”项下混合对照品溶液和“2.2.3”项下连翘挥发油对照溶液、荆芥挥发油对照溶液、薄荷素油对照溶液适量,按“2.1”项下色谱条件进样测定,通过比较色谱图并查找相关文献[3-12],对图2中主要色谱峰进行归属。结果显示,1、2、3、4、7、8、9、10、11、12、13、14号色谱峰来源于薄荷素油;5、6、7、12号色谱峰来源于荆芥挥发油;1、2、3、4、10号色谱峰来源于连翘挥发油。共有峰中,2、3、4、5、7、10、12号色谱峰分别被指认为α-蒎烯、β-蒎烯、柠檬烯、薄荷酮、薄荷脑、胡薄荷酮、乙酸薄荷酯。经统计,上述7个色谱峰面积之和约占共有峰总面积的85%以上。
2.4.3 相似度与各共有峰相关数据分析 采用《中药色谱指纹图谱相似度评价系统》(2012版)对10批样品的图谱进行比较分析。结果,10批样品的GC图谱相似度均>0.98,详见表1;各共有峰的相对保留时间和相对峰面积见表2、表3。

表1 10批样品相似度评价结果Tab 1 Results of similarity evaluation of 10 batches of samples
2.5 部分市售样品相似度评价
本品种为我院承担的2014年国家评价性抽验品种,来自全国范围内17家企业的多批次样品。取17批样品各适量,分别按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积,并与样品对照指纹图谱比较,采用《中药色谱指纹图谱相似度评价系统》(2012版)进行相似度分析,结果见表4。结果,不同企业产品相似度测定结果差异较大,多数企业产品结果较好,部分企业产品相似度结果较低。

表2 10批样品GC图谱共有峰的相对保留时间Tab 2 Relative retention time of the common peaks of 10 batches of samples in GC chromatograms

表3 10批样品GC图谱共有峰的相对峰面积Tab 3 Relative peak areas of the common peaks of 10 batches of samples in GC chromatograms

表4 部分市售样品的相似度评价结果Tab 4 Results of similarity evalualition of part of the commercially available samples
3 讨论
挥发性成分的提取方式一般包括挥发油提取法和脂溶性溶剂直接提取法,本品为片剂,辅料较多,若采用脂溶性溶剂如乙酸乙酯等直接提取,提取效果较差,故选择用挥发油提取法对待测成分进行提取,而且该方法取样量较大,可以达到富集待测成分的目的。笔者曾考察过乙酸乙酯、环己烷、正己烷、石油醚等溶剂,结果提取效果相当,故选择以毒性较低的乙酸乙酯作为溶剂。由于待测成分较多,且包括部分未知成分,笔者曾经尝试过不同极性的色谱柱进行试验,结果以DB-5 ms毛细管柱的色谱结果最为理想。
本研究中,不同企业样品相似度的测定结果差异很大,其原因可能是在投料和工艺制备过程中存在问题,或是药材来源不同所致。本品中挥发油未进行包合[9-11],直接喷入,可能导致损失较大,而且挥发油易受外界温度的影响,这两方面的原因可能导致样品中挥发性成分含量较低。另外,处方中的连翘药材存在青翘与老翘的区别,两者挥发油差异也较大[12]。
本试验建立的指纹图谱可从整体上对羚羊感冒片中的挥发油进行控制,14个特征峰基本可以定性反映出荆芥、连翘、薄荷素油的投料情况,可为羚羊感冒片的质量控制提供依据。
[1] 国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:1521.
[2] 林林,林永强,汪冰,等.羚羊感冒片质量分析[J].药学研究,2014,33(9):514-517.
[3] 方明月,康文艺,姬志强,等.荆芥挥发油化学成分研究[J].时珍国医国药,2007,18(7):1551-1553.
[4] 杨文武,郭娅,张德伟,等.GC法测定清眩片中薄荷脑的含量[J].药学研究,2014,33(8):444-447.
[5] 裴晓丽,张淑蓉,王秀文,等.不同产地连翘中挥发油及其β-蒎烯含量的比较研究[J].药物分析杂志,2010,30(1):127-129.
[6] 关晓娟,吴查青.顶空气相色谱法测定强力枇杷露中薄荷脑的含量[J].中国药房,2016,27(12):1708-1710.
[7] 沈慈丹,陈斌,姜琳琳,等.气相色谱法测定候选新药SM934原料中有机溶剂残留量[J].中国新药与临床杂志,2010,29(9):688-690.
[8] 张淑蓉,裴晓丽,裴香萍,等.山西道地连翘挥发油GC指纹图谱研究[J].时珍国医国药,2011,22(11):2729-2731.
[9] 陈在敏.薄荷素油特征图谱的研究及多组分含量测定[J].药物分析杂志,2011,31(10):1957-1960.
[10] 贾晓斌,高成林,陈彦,等.小儿腹泻暖脐散中挥发油的提取及其β-环糊精包合物的制备研究[J].中成药,2009,31(12):1852-1854.
[11] 钟玲,尹蓉莉,桂素娟,等.五苓散颗粒中挥发油的β-环糊精包合物的制备工艺研究[J].中成药,2006,28(11):1656-1658.
[12] 董梅娟,李媛媛,王瑞明,等.山西连翘挥发油气相色谱-质谱特征图谱研究[J].中国医院药学杂志,2011,31(5):355-358.
Study on GC Fingerprint of Lingyang Ganmao Tablets
LIN Lin,GUO Dongxiao,WANG Bing,LIU Guangzhen(Shandong Provincial Institute for Food and Drug Control,Jinan 250101,China)
OBJECTIVE:To establish the GC fingerpriont for Lingyang ganmao tablets.METHODS:The determination was performed on DB-5 ms capillary column.Flame ionization detector was adopted with temperature of 250℃(temperature programming).The temperature of injector was 240℃.Carrier gas was nitrogen with flow rate of 1.0 mL/min;the sample size was 1 μL by split sampling with split ratio of 20∶1.Using peppermint ketone as reference,Similarity Evaluation Software for Chromatographic Fingerprint of Traditional Chinese Medicine(2012 edition)was used for the similarity analysis of 10 batches of Lingyang ganmao tablets.RESULTS:There were 14 common peaks in the batches of Lingyang ganmao tablets,similarity degrees were higher than 0.98.It was proved that the GC profiles and control fingerprint of 10 batches of samples had good consistency.CONCLUSIONS:The established fingerprint can provide reference for the identification and quality evaluation of Lingyang ganmao tablets.
Lingyang ganmao tablet;GC;Volatile oil;Characteristic chromatogram
R917
A
1001-0408(2017)24-3397-03
2016-09-13
2017-04-26)
(编辑:张 静)
国家科技重大专项课题(No.2014ZX09304307);山东省自然科学基金资助项目(No.ZR2013HM074)
*副主任药师。研究方向:药物分析。电话:0531-81216523。E-mail:linlinsfda@163.com。
#通信作者:副主任药师。研究方向:药物分析。电话:0531-81216552。E-mail:l_guangzhen@sina.com。
DOI10.6039/j.issn.1001-0408.2017.24.24

